文档内容
第二章 海水中的重要元素—钠和氯
第一节 钠及其化合物 课时作业
专题 钠及钠的氧化物拓展
基础达标
1.下列叙述正确的是( )
A.切开的金属Na暴露在空气中,光亮表面逐渐变暗:2Na+O===Na O
2 2 2
B.一定条件下,2.3 g Na完全与O 反应生成产物的质量一定为3.6 g
2
C.钠在空气中受热时,熔化为银白色的小球,产生黄色的火焰,生成白色粉末
D.钠在空气中长期放置,最终主要生成物为碳酸钠
2. “神舟”号载人航天器中,宇航员所在的返回舱都是密封的,宇航员吸入氧气,呼出
二氧化碳,如果二氧化碳浓度过大,会使宇航员困乏,呼吸频率加快,严重的会窒息,为
使二氧化碳浓度降低而保持舱内氧气的适当比例,可以在返回舱内放入( )
A.NaO B.NaCO
2 2 2 3
C.NaOH D.氧气瓶
3.将金属钠放入盛有下列溶液的小烧杯中,既有气体产生,又有沉淀产生的是
( )
①MgSO 溶液 ②NaHCO 溶液 ③CuSO 溶液
4 3 4
④饱和澄清石灰水 ⑤NH Cl溶液
4
A.①③④ B.②③⑤ C.①④⑤ D.全部
4.向NaO 与HO反应后所得溶液中滴加酚酞溶液,酚酞先变红后褪色。某小组欲探
2 2 2
究其原因,进行如图所示实验:①取反应后的溶液加入MnO ,后迅速产生大量气体且该
2
气体能使带火星的木条复燃;实验②③中红色均不褪去。下列分析不正确的是( )
A.NaO 与HO反应产生的气体为O
2 2 2 2
B.NaO 与HO反应需要MnO 作催化剂
2 2 2 2
C.实验②③证明使酚酞褪色的不是NaOH和O
2
D.NaO 与HO反应可能生成了具有强氧化性的HO
2 2 2 2 25.如图装置,试管中盛有水,气球a中盛有干燥的NaO 粉末,U形管中注有红色的
2 2
墨水。将气球用橡皮筋紧缚在试管口。实验时将气球中的NaO
2 2
粉末抖落到试管b中的水中,将发生的现象是( )
A.U形管内红色墨水褪色 B.试管内溶液变红
C.气球a被吹大 D.U 形管水位:c>d
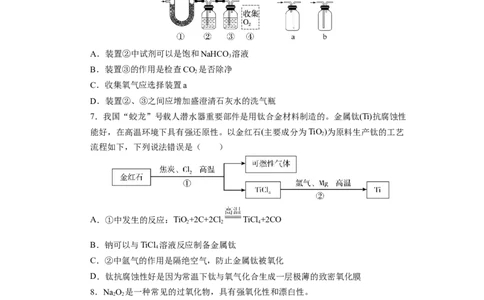
6.以CO 和NaO 为原料,制取纯净干燥的O ,实验装置如图。下列说法正确的是(
2 2 2 2
)
A.装置②中试剂可以是饱和NaHCO 溶液
3
B.装置③的作用是检查CO 是否除净
2
C.收集氧气应选择装置a
D.装置②、③之间应增加盛澄清石灰水的洗气瓶
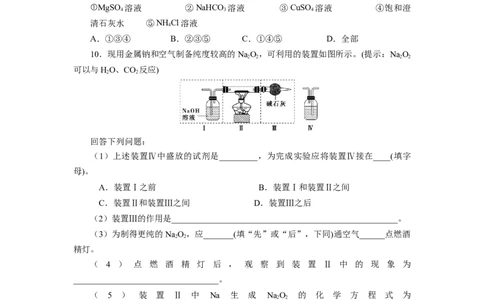
7.我国“蛟龙”号载人潜水器重要部件是用钛合金材料制造的。金属钛(Ti)抗腐蚀性
能好,在高温环境下具有强还原性。以金红石(主要成分为TiO)为原料生产钛的工艺
2
流程如下,下列说法错误是( )
A.①中发生的反应:TiO+2C+2Cl TiCl +2CO
2 2 4
B.钠可以与TiCl 溶液反应制备金属钛
4
C.②中氩气的作用是隔绝空气,防止金属钛被氧化
D.钛抗腐蚀性好是因为常温下钛与氧气化合生成一层极薄的致密氧化膜
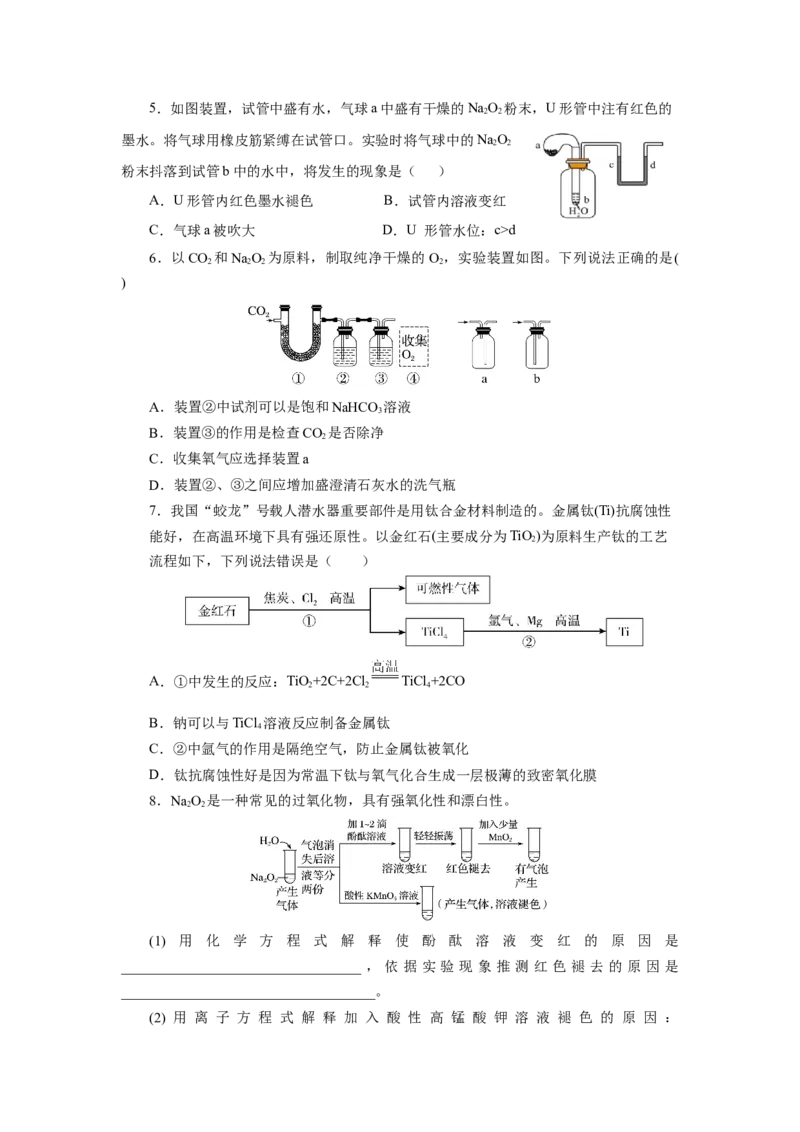
8.NaO 是一种常见的过氧化物,具有强氧化性和漂白性。
2 2
(1) 用 化 学 方 程 式 解 释 使 酚 酞 溶 液 变 红 的 原 因 是
__________________________________ , 依 据 实 验 现 象 推 测 红 色 褪 去 的 原 因 是
____________________________________。
(2) 用 离 子 方 程 式 解 释 加 入 酸 性 高 锰 酸 钾 溶 液 褪 色 的 原 因 :________________________。
(3)根据实验分析,过氧化钠与水反应除了生成氢氧化钠和氧气外,还存在另一反应,
则另一反应的化学方程式为______________________________________________,其反应
类型为__________________。
能力提升
9.将金属钠放入盛有下列溶液的小烧杯中,既有气体产生,又有沉淀产生的是(
)
①MgSO 溶液 ②NaHCO 溶液 ③CuSO 溶液 ④饱和澄
4 3 4
清石灰水 ⑤NH Cl溶液
4
A.①③④ B.②③⑤ C.①④⑤ D.全部
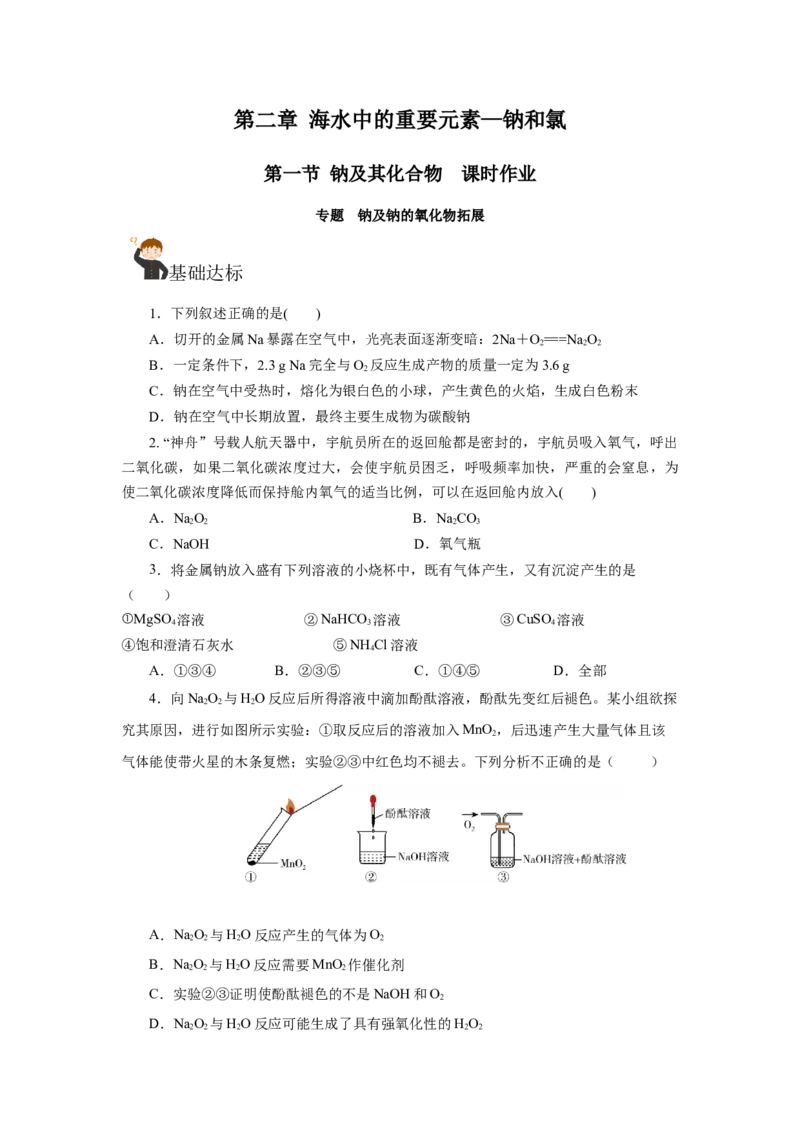
10.现用金属钠和空气制备纯度较高的NaO,可利用的装置如图所示。(提示:NaO
2 2 2 2
可以与HO、CO 反应)
2 2
回答下列问题:
(1)上述装置Ⅳ中盛放的试剂是_________,为完成实验应将装置Ⅳ接在____(填字
母)。
A.装置Ⅰ之前 B.装置Ⅰ和装置Ⅱ之间
C.装置Ⅱ和装置Ⅲ之间 D.装置Ⅲ之后
(2)装置Ⅲ的作用是_____________________________________________________。
(3)为制得更纯的NaO ,应_______(填“先”或“后”,下同)通空气______点燃酒
2 2
精灯。
( 4 ) 点 燃 酒 精 灯 后 , 观 察 到 装 置 Ⅱ 中 的 现 象 为
__________________________________。
( 5 ) 装 置 Ⅱ 中 Na 生 成 NaO 的 化 学 方 程 式 为
2 2
___________________________________。
11.有4种钠的化合物W、X、Y、Z,它们之间存在如下关系:
①W X+HO+CO↑ ②Z+CO―→X+O
2 2 2 2
③Z+HO―→Y+O↑ ④X+Ca(OH) ―→Y+CaCO ↓
2 2 2 3
试回答下列问题:
(1)W、X、Y、Z 的化学式分别是:W________,X________,Y________,
Z________。
(2)以上4个化学反应,属于氧化还原反应的是________(填反应序号),反应中氧化剂是__________(写化学式),还原剂是__________(写化学式)。
(3)若反应④在溶液中进行,写出其离子方程式以及能用该离子方程式表示的另一个化
学反应的化学方程式:
①离子方程式:_______________________________________________________。
②化学方程式:______________________________________________________。
直击高考
12.下列叙述正确的是( )
①Na O与NaO 都能和水反应生成碱,它们都是碱性氧化物 ②钠在常温下不容易被
2 2 2
氧化 ③NaO 可作供氧剂,而NaO不行 ④石蕊溶液中加入NaO 粉末,先变蓝后褪
2 2 2 2 2
色,并有气泡生成 ⑤钠与浓NH Cl溶液反应,放出的气体中含H 和NH
4 2 3
A.都正确 B.①②③④ C.③④⑤ D.②④⑤
13.某研究小组在网上收集到如下信息:钾、钙、钠、镁等活泼金属都能在CO 气体
2
中燃烧。他们对钠在CO 气体中燃烧后的产物中的白色固体进行了如下研究:
2
【实验】将燃烧的钠迅速伸入盛满 CO 的集气瓶中,钠在其中继续燃烧,反应后冷
2
却,瓶底附着黑色颗粒,瓶壁上粘附着白色物质。
【提出假设】
假设1:白色物质是NaO
2
假设2:白色物质是NaCO
2 3
假设3:白色物质是NaO和NaCO 的混合物
2 2 3
该小组对燃烧后的白色产物进行如下探究:
方案1:取少量白色物质于试管中。加入适量水,振荡,样品全部溶于水,向其中加
入无色酚酞试液,溶液变成红色,则白色固体为NaO。
2
方案2:①取少量白色固体于试管中,加入适量水,振荡,样品全部溶于水,向其中
加入过量的CaCl 沝出现白色沉淀;②静置片刻,取上层清液于试管中,滴加无色酚酞试
2
液,无明显现象。
( 1 ) 甲 同 学 认 为 方 案 1 得 到 的 结 论 不 正 确 , 其 理 由 是
_____________________________。
(2)乙同学认为方案2得到的结论正确,白色物质为___________________。
(3)通过方案1和方案2的实验,你认为上述三个假设中,__________成立,你的理
由是__________________________________________________________。(4)写出钠在二氧化碳燃烧中的化学方程式并用双线桥表示电子转移:
___________________________________________________________。