文档内容
第二单元 我们周围的空气
知能优化训练
中考回顾
1.(2017四川广安中考)下列物质属于纯净物的是( )
A.食盐水
B.不锈钢
C.蒸馏水
D.洁净的空气
答案:C
2.(2017呼和浩特中考)空气是人类宝贵的自然资源。下列有关说法不正确的是( )
A.氧气可用作火箭发射的燃料
B.空气可用于工业制备氮气和氧气
C.氦气可用来填充探空气球
D.二氧化碳是植物进行光合作用的基本原料
答案:A
3.(2017天津中考)下列物质中,目前计入“空气污染指数”项目的是( )
A.氮气 B.氧气
C.稀有气体 D.可吸入颗粒物
答案:D
4.(2017西宁中考)下列实验现象的描述错误的是( )
A.红磷在空气中燃烧,产生大量白烟
B.氢气在空气中燃烧,产生淡蓝色火焰
C.碳在氧气中燃烧发出白光,生成黑色固体
D.硫在氧气中燃烧,发出蓝紫色火焰
答案:C
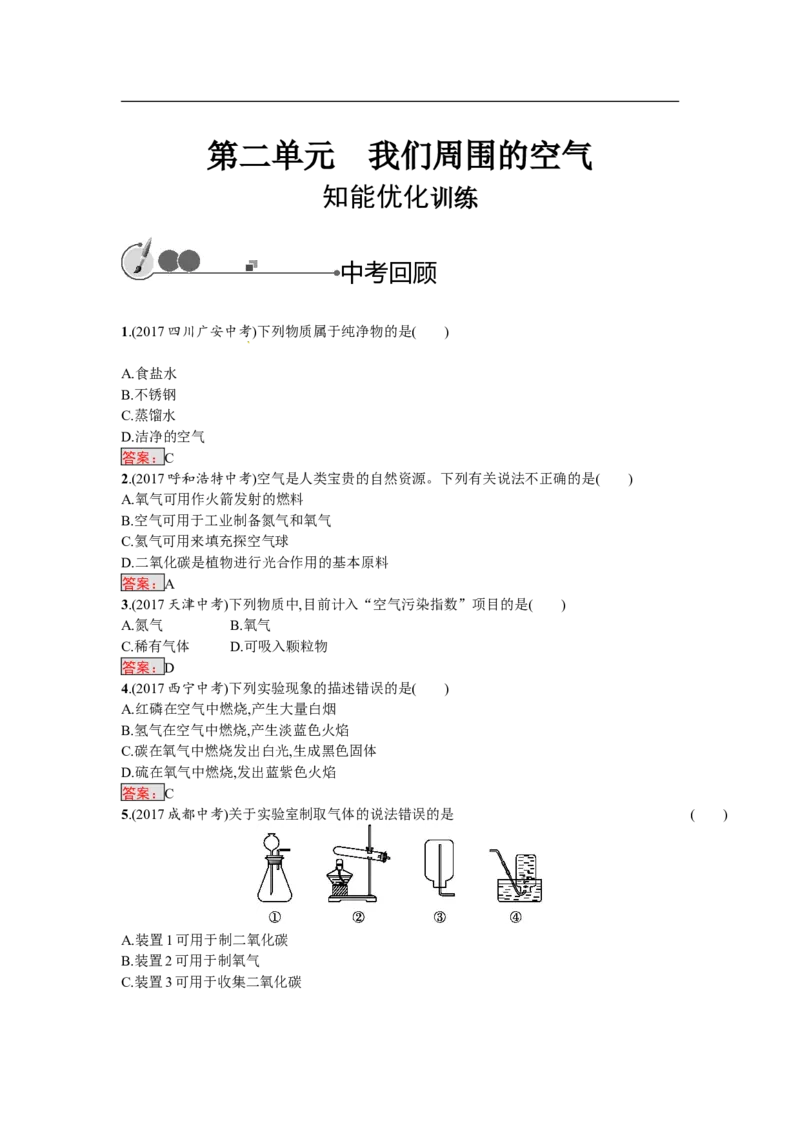
5.(2017成都中考)关于实验室制取气体的说法错误的是 ( )
A.装置1可用于制二氧化碳
B.装置2可用于制氧气
C.装置3可用于收集二氧化碳D.装置4可用于收集氢气
答案:C
6.(2016天津中考)下列说法中正确的是( )
A.红磷在氧气中能燃烧,在空气中不能燃烧
[来源:学。科。网]
B.硫在氧气中燃烧后生成有刺激性气味的气体
C.镁条在氧气中燃烧时,火星四射,生成黑色固体
D.木炭伸入盛有氧气的集气瓶中剧烈燃烧,发出白光
答案:B
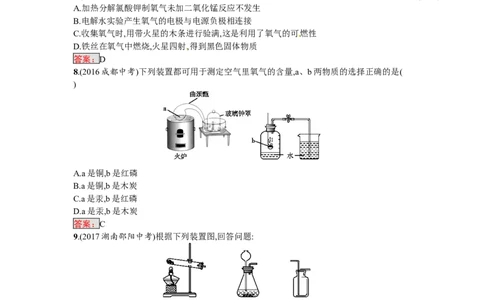
7.(2016四川资阳中考)下列关于氧气实验的说法正确的是 ( )
A.加热分解氯酸钾制氧气未加二氧化锰反应不发生
B.电解水实验产生氧气的电极与电源负极相连接
C.收集氧气时,用带火星的木条进行验满,这是利用了氧气的可燃性
D.铁丝在氧气中燃烧,火星四射,得到黑色固体物质
答案:D
8.(2016成都中考)下列装置都可用于测定空气里氧气的含量,a、b两物质的选择正确的是(
)
A.a是铜,b是红磷
[来源:学&科&网]
B.a是铜,b是木炭
C.a是汞,b是红磷
D.a是汞,b是木炭
答案:C
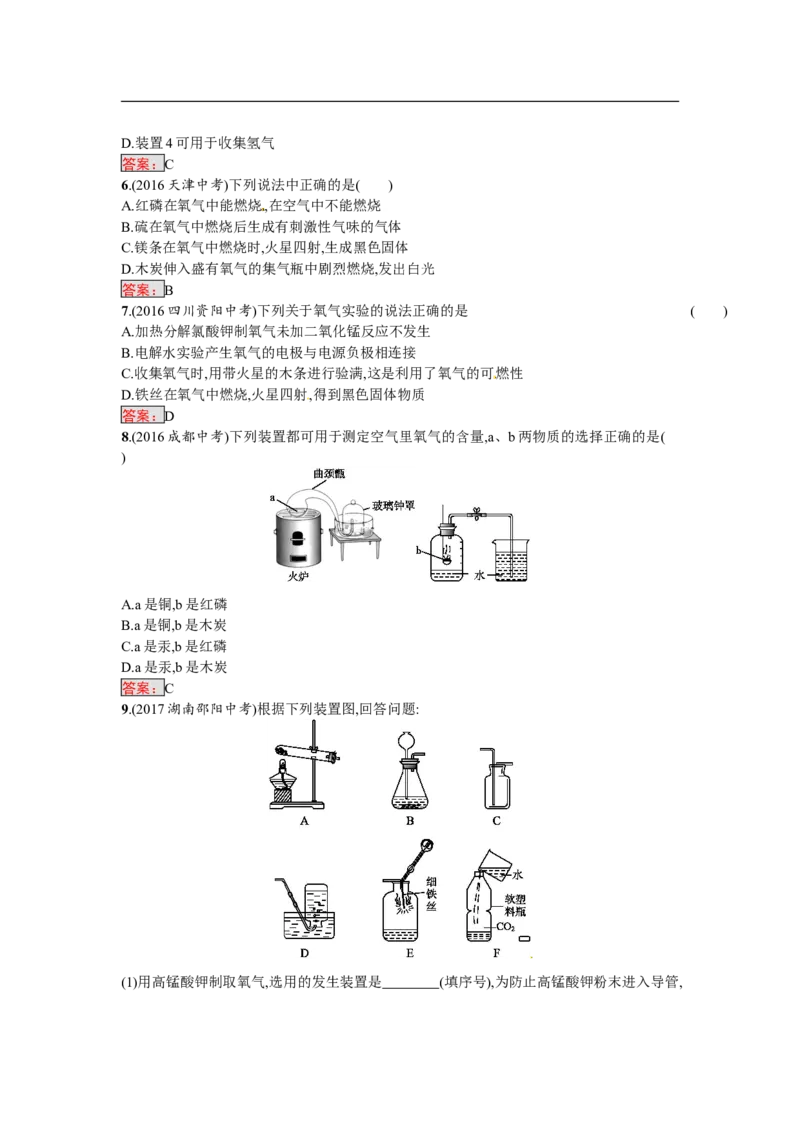
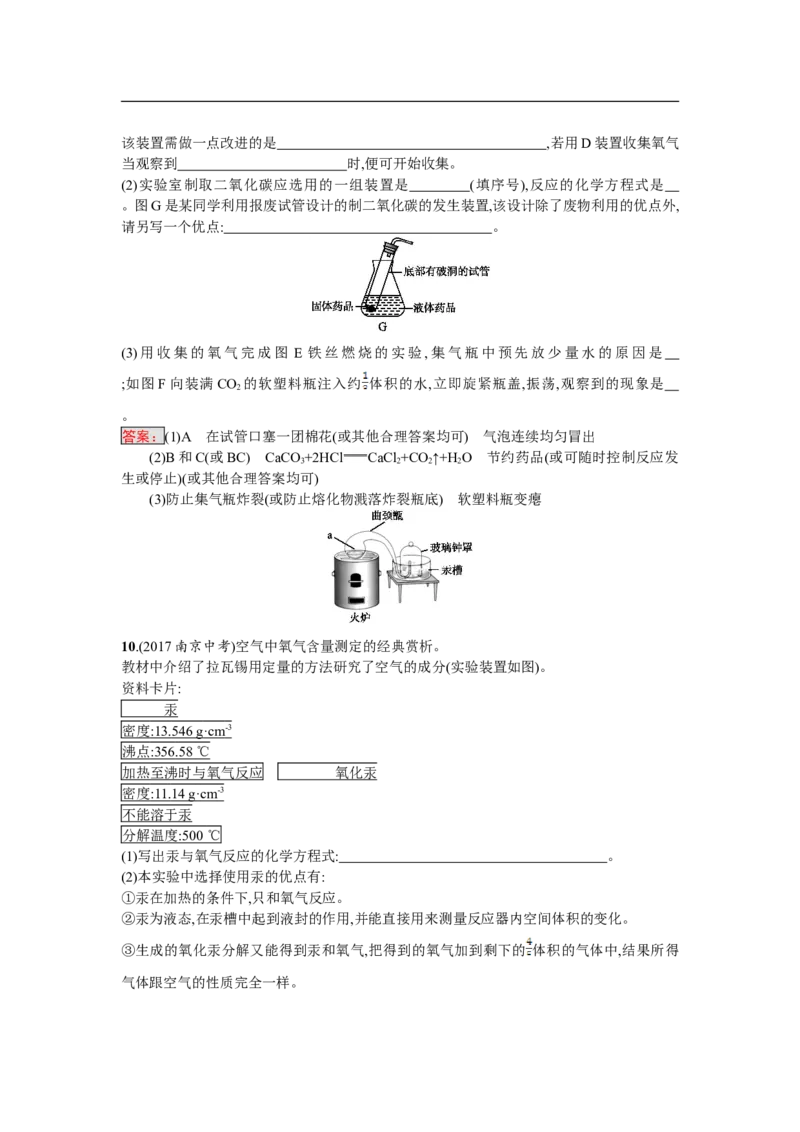
9.(2017湖南邵阳中考)根据下列装置图,回答问题:
(1)用高锰酸钾制取氧气,选用的发生装置是 (填序号),为防止高锰酸钾粉末进入导管,该装置需做一点改进的是 ,若用D装置收集氧气
当观察到 时,便可开始收集。
(2)实验室制取二氧化碳应选用的一组装置是 (填序号),反应的化学方程式是
。图G是某同学利用报废试管设计的制二氧化碳的发生装置,该设计除了废物利用的优点外,
请另写一个优点: 。
(3)用收集的氧气完成图 E 铁丝燃烧的实验,集气瓶中预先放少量水的原因是
;如图F向装满CO 的软塑料瓶注入约 体积的水,立即旋紧瓶盖,振荡,观察到的现象是
2
。
答案:(1)A 在试管口塞一团棉花(或其他合理答案均可) 气泡连续均匀冒出
(2)B和C(或BC) CaCO +2HCl CaCl +CO ↑+H O 节约药品(或可随时控制反应发
3 2 2 2
生或停止)(或其他合理答案均可)
(3)防止集气瓶炸裂(或防止熔化物溅落炸裂瓶底) 软塑料瓶变瘪
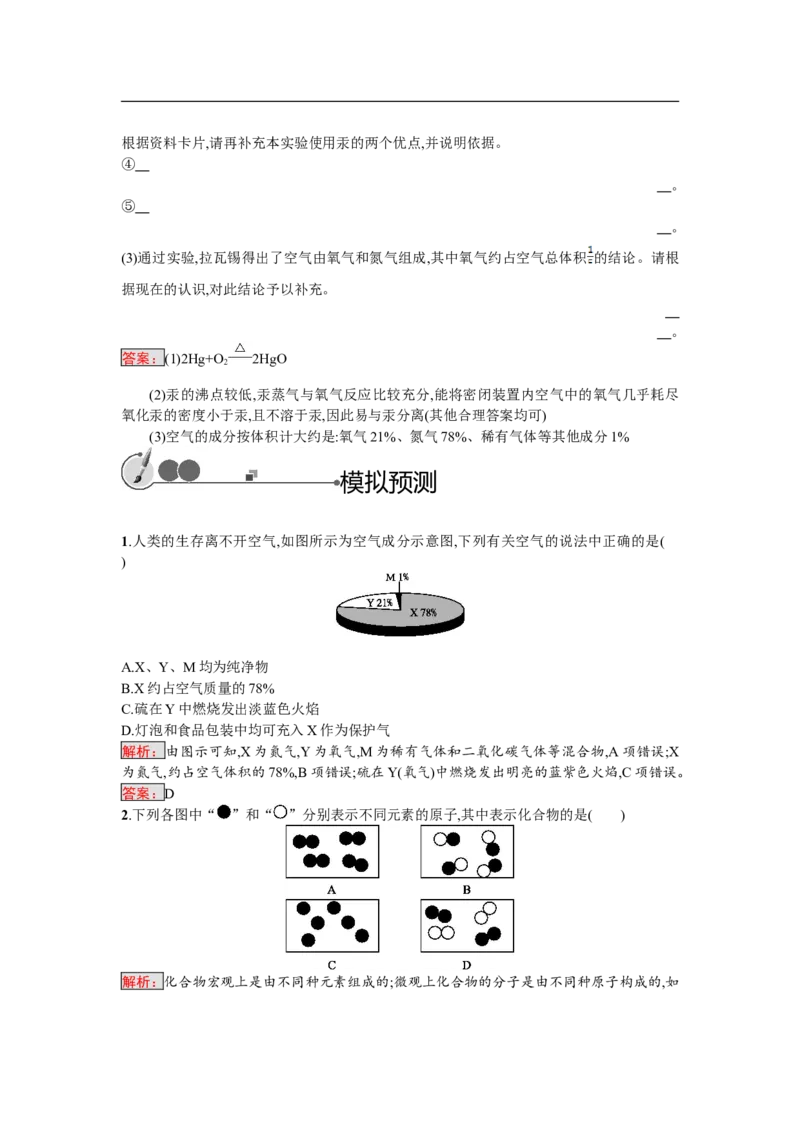
10.(2017南京中考)空气中氧气含量测定的经典赏析。
教材中介绍了拉瓦锡用定量的方法研究了空气的成分(实验装置如图)。
资料卡片:
汞
密度:13.546 g·cm-3
沸点:356.58 ℃
加热至沸时与氧气反应 氧化汞
密度:11.14 g·cm-3
不能溶于汞
分解温度:500 ℃
(1)写出汞与氧气反应的化学方程式: 。
(2)本实验中选择使用汞的优点有:
①汞在加热的条件下,只和氧气反应。
②汞为液态,在汞槽中起到液封的作用,并能直接用来测量反应器内空间体积的变化。
③生成的氧化汞分解又能得到汞和氧气,把得到的氧气加到剩下的 体积的气体中,结果所得
气体跟空气的性质完全一样。根据资料卡片,请再补充本实验使用汞的两个优点,并说明依据。
④
。
⑤
。
(3)通过实验,拉瓦锡得出了空气由氧气和氮气组成,其中氧气约占空气总体积 的结论。请根
据现在的认识,对此结论予以补充。
。
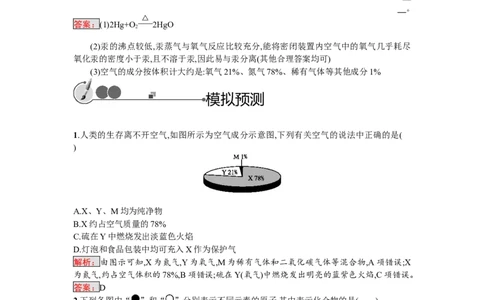
答案:(1)2Hg+O 2HgO
2
(2)汞的沸点较低,汞蒸气与氧气反应比较充分,能将密闭装置内空气中的氧气几乎耗尽
氧化汞的密度小于汞,且不溶于汞,因此易与汞分离(其他合理答案均可)
(3)空气的成分按体积计大约是:氧气21%、氮气78%、稀有气体等其他成分1%
模拟预测
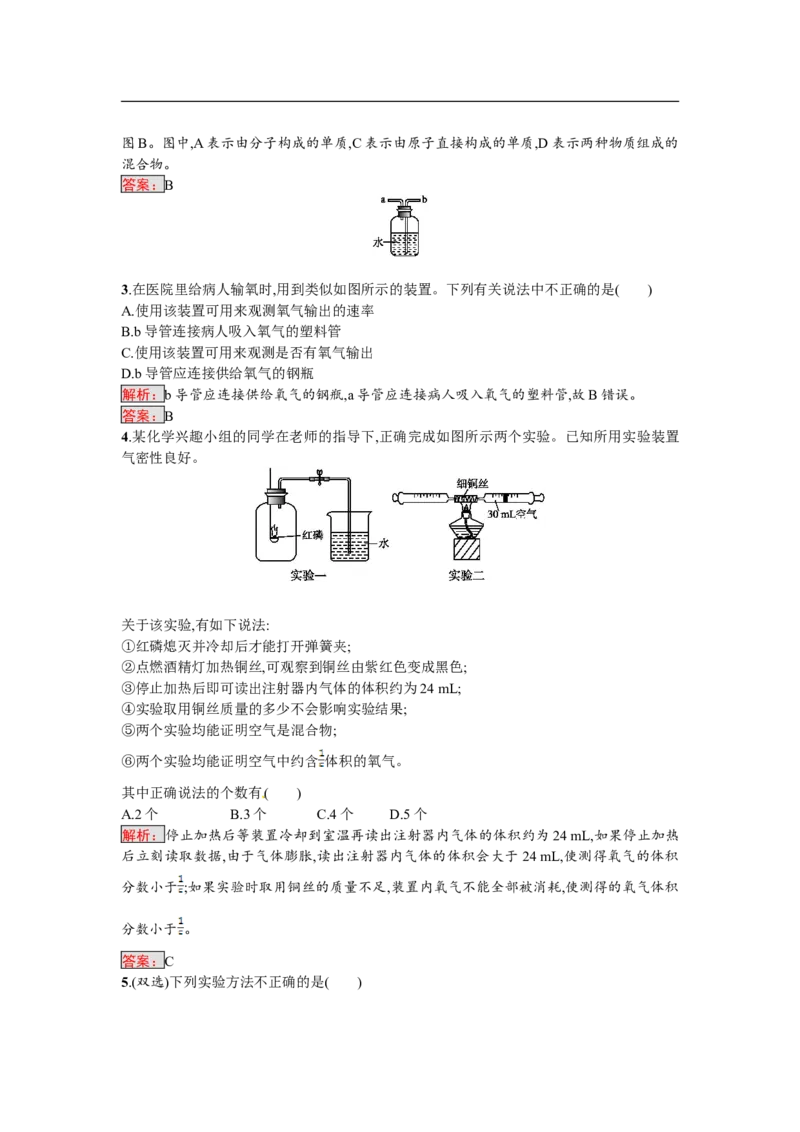
1.人类的生存离不开空气,如图所示为空气成分示意图,下列有关空气的说法中正确的是(
)
A.X、Y、M均为纯净物
B.X约占空气质量的78%
C.硫在Y中燃烧发出淡蓝色火焰
D.灯泡和食品包装中均可充入X作为保护气
解析:由图示可知,X为氮气,Y为氧气,M为稀有气体和二氧化碳气体等混合物,A项错误;X
为氮气,约占空气体积的78%,B项错误;硫在Y(氧气)中燃烧发出明亮的蓝紫色火焰,C项错误。
答案:D
[来源:Z+xx+k.Com]
2.下列各图中“ ”和“ ”分别表示不同元素的原子,其中表示化合物的是( )
解析:化合物宏观上是由不同种元素组成的;微观上化合物的分子是由不同种原子构成的,如图B。图中,A表示由分子构成的单质,C表示由原子直接构成的单质,D表示两种物质组成的
混合物。
答案:B
3.在医院里给病人输氧时,用到类似如图所示的装置。下列有关说法中不正确的是( )
A.使用该装置可用来观测氧气输出的速率
B.b导管连接病人吸入氧气的塑料管
C.使用该装置可用来观测是否有氧气输出
D.b导管应连接供给氧气的钢瓶
解析:b导管应连接供给氧气的钢瓶,a导管应连接病人吸入氧气的塑料管,故B错误。
答案:B
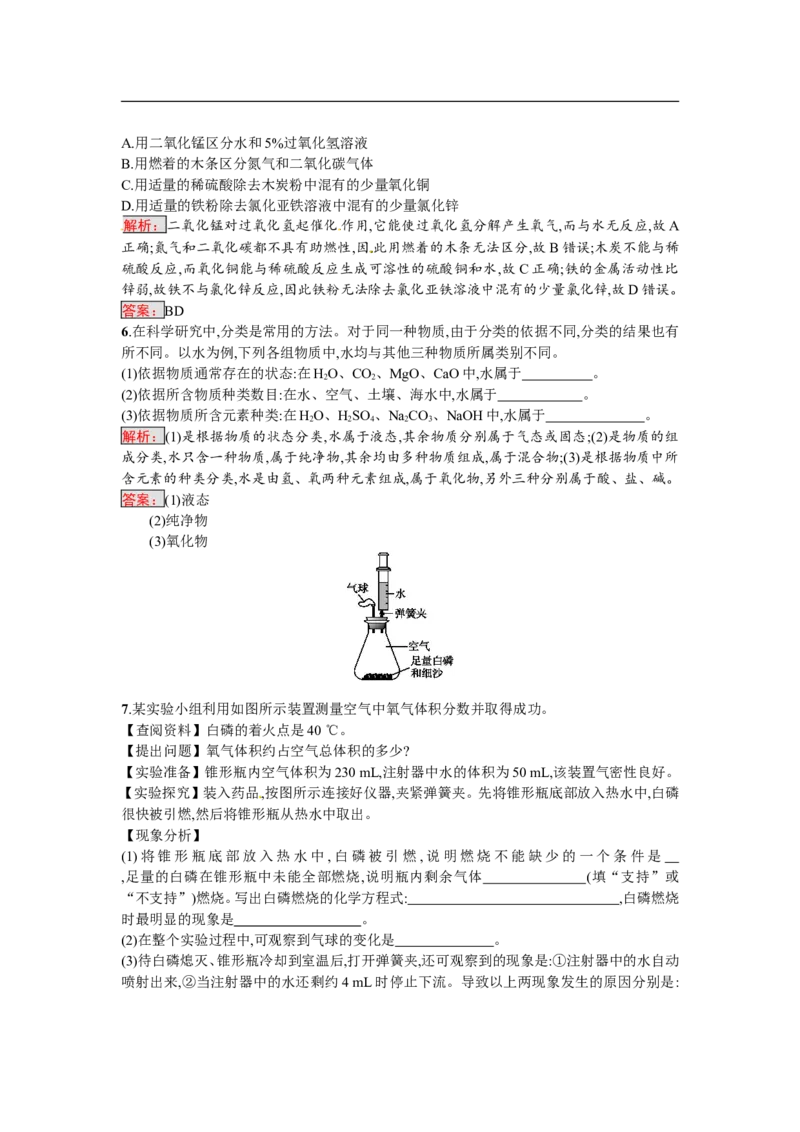
4.某化学兴趣小组的同学在老师的指导下,正确完成如图所示两个实验。已知所用实验装置
气密性良好。
关于该实验,有如下说法:
①红磷熄灭并冷却后才能打开弹簧夹;
②点燃酒精灯加热铜丝,可观察到铜丝由紫红色变成黑色;
③停止加热后即可读出注射器内气体的体积约为24 mL;
④实验取用铜丝质量的多少不会影响实验结果;
⑤两个实验均能证明空气是混合物;
⑥两个实验均能证明空气中约含 体积的氧气。
其中正确说法的个数有( )
A.2个 B.3个 C.4个 D.5个
解析:停止加热后等装置冷却到室温再读出注射器内气体的体积约为24 mL,如果停止加热
后立刻读取数据,由于气体膨胀,读出注射器内气体的体积会大于24 mL,使测得氧气的体积
分数小于 ;如果实验时取用铜丝的质量不足,装置内氧气不能全部被消耗,使测得的氧气体积
分数小于 。
答案:C
5.(双选)下列实验方法不正确的是( )A.用二氧化锰区分水和5%过氧化氢溶液
B.用燃着的木条区分氮气和二氧化碳气体
C.用适量的稀硫酸除去木炭粉中混有的少量氧化铜
D.用适量的铁粉除去氯化亚铁溶液中混有的少量氯化锌
解析:二氧化锰对过氧化氢起催化作用,它能使过氧化氢分解产生氧气,而与水无反应,故A
正确;氮气和二氧化碳都不具有助燃性,因此用燃着的木条无法区分,故B错误;木炭不能与稀
硫酸反应,而氧化铜能与稀硫酸反应生成可溶性的硫酸铜和水,故C正确;铁的金属活动性比
锌弱,故铁不与氯化锌反应,因此铁粉无法除去氯化亚铁溶液中混有的少量氯化锌,故D错误。
答案:BD
6.在科学研究中,分类是常用的方法。对于同一种物质,由于分类的依据不同,分类的结果也有
所不同。以水为例,下列各组物质中,水均与其他三种物质所属类别不同。
(1)依据物质通常存在的状态:在HO、CO、MgO、CaO中,水属于 。
2 2
(2)依据所含物质种类数目:在水、空气、土壤、海水中,水属于 。
(3)依据物质所含元素种类:在HO、HSO 、NaCO、NaOH中,水属于 。
2 2 4 2 3
解析:(1)是根据物质的状态分类,水属于液态,其余物质分别属于气态或固态;(2)是物质的组
成分类,水只含一种物质,属于纯净物,其余均由多种物质组成,属于混合物;(3)是根据物质中所
含元素的种类分类,水是由氢、氧两种元素组成,属于氧化物,另外三种分别属于酸、盐、碱。
答案:(1)液态
(2)纯净物
(3)氧化物
7.某实验小组利用如图所示装置测量空气中氧气体积分数并取得成功。
【查阅资料】白磷的着火点是40 ℃。
【提出问题】氧气体积约占空气总体积的多少?
【实验准备】锥形瓶内空气体积为230 mL,注射器中水的体积为50 mL,该装置气密性良好。
【实验探究】装入药品,按图所示连接好仪器,夹紧弹簧夹。先将锥形瓶底部放入热水中,白磷
很快被引燃,然后将锥形瓶从热水中取出。
【现象分析】
(1)将锥形瓶底部放入热水中,白磷被引燃,说明燃烧不能缺少的一个条件是
,足量的白磷在锥形瓶中未能全部燃烧,说明瓶内剩余气体 (填“支持”或
“不支持”)燃烧。写出白磷燃烧的化学方程式: ,白磷燃烧
时最明显的现象是 。
(2)在整个实验过程中,可观察到气球的变化是 。
(3)待白磷熄灭、锥形瓶冷却到室温后,打开弹簧夹,还可观察到的现象是:①注射器中的水自动
喷射出来,②当注射器中的水还剩约4 mL时停止下流。导致以上两现象发生的原因分别是:①
;
②
。
【得出结论】氧气约占空气总体积的 。
解析:(1)将锥形瓶底部放入热水中,由于温度达到白磷的着火点,因此白磷很快被引燃,说明
燃烧不能缺少的一个条件是温度达到可燃物的着火点;由于氮气不能支持燃烧,因此足量的白
磷在锥形瓶中未能全部燃烧;白磷燃烧生成了五氧化二磷,反应的化学方程式为4P+5O
2
2PO,白磷燃烧时最明显的现象是产生大量白烟;(2)白磷燃烧时放出大量的热,使瓶内压强增
2 5
大,由于白磷燃烧消耗了氧气,冷却到室温,瓶内压强减小,所以,可观察到气球的变化是先变大,
后缩小;(3)由于白磷燃烧消耗了氧气,瓶内压强减小,所以,注射器中的水自动喷出来,又由于空
气中氧气的体积分数约为 ,所以,当注射器中的水还剩下约4 mL时停止下流。
答案:(1)温度要达到可燃物的着火点 不支持 4P+5O 2PO 产生大量白烟
2 2 5
(2)先鼓后瘪(其他合理描述也可)
(3)①白磷燃烧消耗了锥形瓶中的氧气,使瓶中气压降低 ②锥形瓶中氧气约占46 mL,当
注射器中的水进入锥形瓶约46 mL后,瓶中气压与外界相当
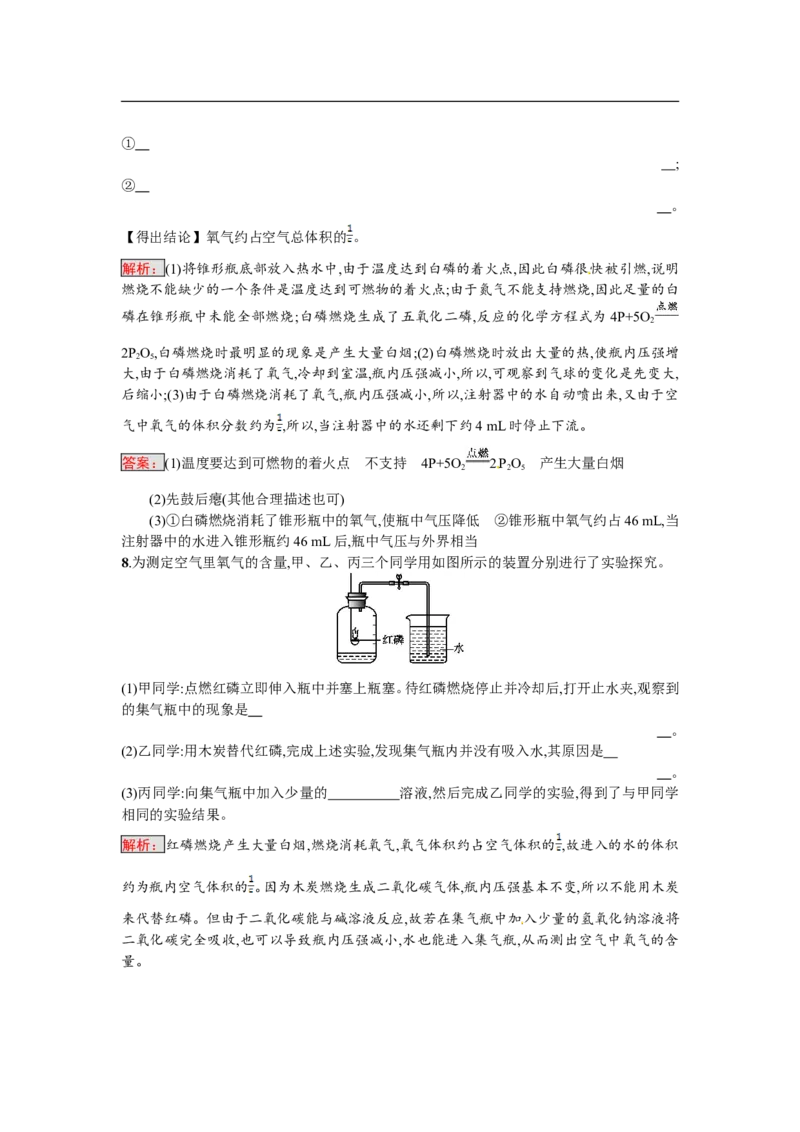
8.为测定空气里氧气的含量,甲、乙、丙三个同学用如图所示的装置分别进行了实验探究。
(1)甲同学:点燃红磷立即伸入瓶中并塞上瓶塞。待红磷燃烧停止并冷却后,打开止水夹,观察到
的集气瓶中的现象是
。
(2)乙同学:用木炭替代红磷,完成上述实验,发现集气瓶内并没有吸入水,其原因是
。
(3)丙同学:向集气瓶中加入少量的 溶液,然后完成乙同学的实验,得到了与甲同学
相同的实验结果。
解析:红磷燃烧产生大量白烟,燃烧消耗氧气,氧气体积约占空气体积的 ,故进入的水的体积
约为瓶内空气体积的 。因为木炭燃烧生成二氧化碳气体,瓶内压强基本不变,所以不能用木炭
来代替红磷。但由于二氧化碳能与碱溶液反应,故若在集气瓶中加入少量的氢氧化钠溶液将
二氧化碳完全吸收,也可以导致瓶内压强减小,水也能进入集气瓶,从而测出空气中氧气的含
量。答案:(1)瓶内产生大量白烟,进入瓶中水的体积约占原空气体积的
(2)木炭燃烧的生成物是二氧化碳气体,瓶内气压基本不变
(3)NaOH
9.做完“铁在氧气里燃烧”实验后,小冬同学有两个疑惑不解的问题,于是他进行了以下探究
活动,请你一同参与。
【问题1】铁燃烧时溅落下来的黑色物质中还有没有铁呢?
【查阅资料1】
(1)自然界中铁的氧化物主要是Fe O 和Fe O 两种(FeO极易被氧化为Fe O);
3 4 2 3 2 3
(2)铁的氧化物能溶于酸的溶液。
【实验探究】
将冷却后的黑色物质碾碎,装入试管,加入 溶液,观察到的现象是
,说明铁燃烧时溅落下来的黑色物质中还含有铁。
【问题2】铁燃烧的产物为什么不是Fe O 呢?
2 3
【查阅资料2】
(1)Fe O 和Fe O 的分解温度、铁的熔点见下表:
3 4 2 3
Fe O Fe O 铁
3 4 2 3
分 解
温 1 5381 400—
度/℃
熔 1
— —
点/℃ 535
[来源:Z.xx.k.Com]
(2)Fe O 高温时分解成Fe O。
2 3 3 4
【理论探讨】
根据实验现象,并结合表中数据,可推知铁在氧气里燃烧时产生的高温可能在
之间,在此温度范围内Fe O 已分解,所以铁在氧气里燃烧的产物是Fe O。
2 3 3 4
【拓展延伸】
(1)实验中为了防止集气瓶炸裂,必须
。
(2)Fe O 高温时会分解成Fe O 和一种气体,请写出此反应的化学方程式: 。
2 3 3 4
(3)有些超市的食品密封包装盒的透明盖内放有黑色的 FeO 粉末,若粉末的颜色
,就说明包装盒破损进气,这样售货员就能及时发现并处理。
解析:利用酸(如盐酸)或者比铁活动性弱的金属的盐溶液(如硫酸铜溶液),根据产生气泡或者
出现紫红色固体来确定黑色固体中有铁。
答案:【实验探究】稀盐酸(或硫酸铜等) 冒气泡(或出现紫红色固体等)
【理论探讨】1 535~1 538 ℃
【拓展延伸】(1)在集气瓶底部放少量的水(或在集气瓶底部铺一层细沙)
(2)6Fe O 4Fe O+O ↑
2 3 3 4 2
(3)由黑色变成红棕色
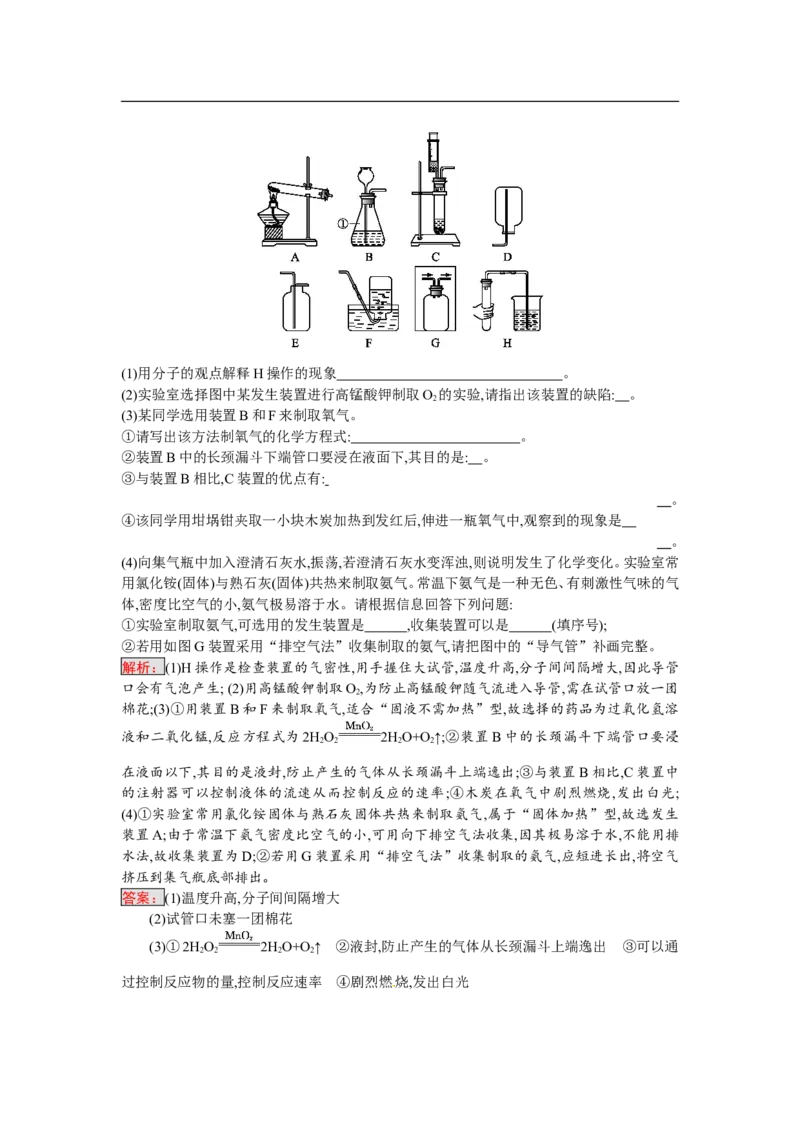
10.在实验室选用图中A~G的装置可以制取氧气。(1)用分子的观点解释H操作的现象 。
[来源:学科网ZXXK]
(2)实验室选择图中某发生装置进行高锰酸钾制取O 的实验,请指出该装置的缺陷: 。
2
(3)某同学选用装置B和F来制取氧气。
①请写出该方法制氧气的化学方程式: 。
②装置B中的长颈漏斗下端管口要浸在液面下,其目的是: 。
③与装置B相比,C装置的优点有:
。
④该同学用坩埚钳夹取一小块木炭加热到发红后,伸进一瓶氧气中,观察到的现象是
。
(4)向集气瓶中加入澄清石灰水,振荡,若澄清石灰水变浑浊,则说明发生了化学变化。实验室常
用氯化铵(固体)与熟石灰(固体)共热来制取氨气。常温下氨气是一种无色、有刺激性气味的气
体,密度比空气的小,氨气极易溶于水。请根据信息回答下列问题:
①实验室制取氨气,可选用的发生装置是 ,收集装置可以是 (填序号);
②若用如图G装置采用“排空气法”收集制取的氨气,请把图中的“导气管”补画完整。
解析:(1)H操作是检查装置的气密性,用手握住大试管,温度升高,分子间间隔增大,因此导管
口会有气泡产生; (2)用高锰酸钾制取O,为防止高锰酸钾随气流进入导管,需在试管口放一团
2
棉花;(3)①用装置B和F来制取氧气,适合“固液不需加热”型,故选择的药品为过氧化氢溶
液和二氧化锰,反应方程式为2HO 2HO+O↑;②装置B中的长颈漏斗下端管口要浸
2 2 2 2
在液面以下,其目的是液封,防止产生的气体从长颈漏斗上端逸出;③与装置B相比,C装置中
的注射器可以控制液体的流速从而控制反应的速率;④木炭在氧气中剧烈燃烧,发出白光;
(4)①实验室常用氯化铵固体与熟石灰固体共热来制取氨气,属于“固体加热”型,故选发生
装置A;由于常温下氨气密度比空气的小,可用向下排空气法收集,因其极易溶于水,不能用排
水法,故收集装置为D;②若用G装置采用“排空气法”收集制取的氨气,应短进长出,将空气
挤压到集气瓶底部排出。
答案:(1)温度升高,分子间间隔增大
(2)试管口未塞一团棉花
(3)①2HO 2HO+O↑ ②液封,防止产生的气体从长颈漏斗上端逸出 ③可以通
2 2 2 2
过控制反应物的量,控制反应速率 ④剧烈燃烧,发出白光(4)①A D ②