文档内容
第六单元 碳和碳的氧化物 检测卷
班级:__________ 姓名:__________
考生注意:1.本试卷共四个大题,满分60分,考试时间45分钟。
2.可能用到的相对原子质量:H—1 C—12 O—16 Cl—35.5 Ca—40
题号 一 二 三 四 总分
得分
一、选择题(本题包括12个小题,每小题2分,共24分。每小题只有一个选项符合题意)
1.下列有关碳单质所发生的变化中,属于化学变化的是( )
A.以石墨为原料制造人造金刚石
B.用铅笔芯在纸上写字,铅笔芯变短了
C.将金刚石加工琢磨成钻石
D.将活性炭投入紫色石蕊溶液中,最终溶液变为无色
2.古代一些书法家、画家用墨书写或绘制的字画能够保存很长时间而不变色,这主要是
因为( )
A.纸的质量好
B.碳的化学性质在常温下比较稳定
C.保存方法得当
D.碳在任何条件下都不与其他物质反应
3.有关碳元素组成的几种物质,以下说法错误的是( )
A.C 是一种新型化合物
60
B.金刚石是天然最硬的物质
C.石墨具有优良的导电性
D.活性炭可以除去冰箱中的异味
4.下列物质的用途与其性质的对应关系不正确的是( )
A.金刚石常用来裁玻璃——金刚石坚硬无比
B.焦炭用来冶炼金属——焦炭具有还原性
C.石墨常用作电极材料——石墨具有导电性
D.木炭可燃烧——木炭具有吸附性
5.鉴别O、CO、CO 三种气体,简便可行的方法是( )
2 2
A.将气体分别通入澄清石灰水
B.将气体分别通入石蕊溶液
C.试验三种气体在水中的溶解性
D.用燃着的木条分别伸入瓶内
6.碳的耗用量称为“碳足迹”(如图所示)。一般情况下,排放的二氧化碳越多,碳足迹
就越大。碳足迹的计算包括一切用于电力、建设、运输等方面的能源以及我们所使用的消耗
品。以下做法可以减小“碳足迹”的是( )
A.减少一次性筷子的使用
B.大量使用煤、石油等燃料
C.将生活垃圾进行焚烧处理D.以私家车出行代替公共交通工具
7.关于一氧化碳和二氧化碳的说法中,正确的是( )
A.CO的含量增加会导致温室效应
B.室内放一盆澄清石灰水可防止CO中毒
C.CO和CO 组成元素相同,所以它们的化学性质相同
2
D.大气中CO 的消耗途径主要是绿色植物的光合作用
2
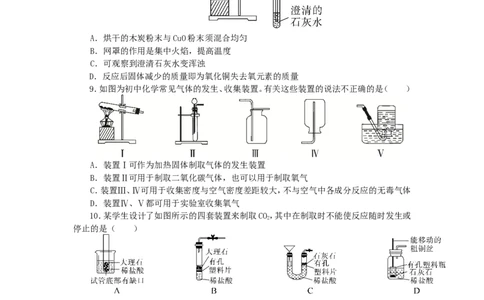
8.按如图进行实验,有关说法及分析不正确的是( )
A.烘干的木炭粉末与CuO粉末须混合均匀
B.网罩的作用是集中火焰,提高温度
C.可观察到澄清石灰水变浑浊
D.反应后固体减少的质量即为氧化铜失去氧元素的质量
9.如图为初中化学常见气体的发生、收集装置。有关这些装置的说法不正确的是( )
A.装置Ⅰ可作为加热固体制取气体的发生装置
B.装置Ⅱ可用于制取二氧化碳气体,也可以用于制取氧气
C.装置Ⅲ、Ⅳ可用于收集密度与空气密度差距较大,不与空气中各成分反应的无毒气体
D.装置Ⅳ、Ⅴ都可用于实验室收集氧气
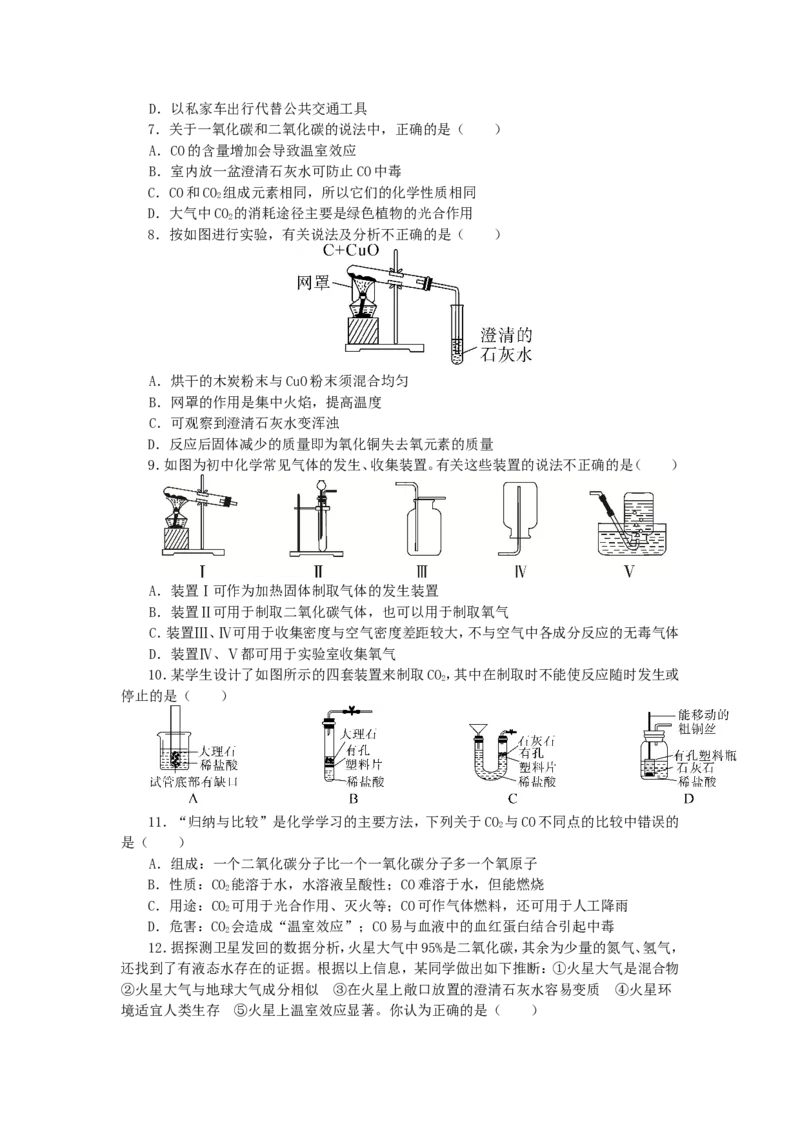
10.某学生设计了如图所示的四套装置来制取CO,其中在制取时不能使反应随时发生或
2
停止的是( )
11.“归纳与比较”是化学学习的主要方法,下列关于CO 与CO不同点的比较中错误的
2
是( )
A.组成:一个二氧化碳分子比一个一氧化碳分子多一个氧原子
B.性质:CO 能溶于水,水溶液呈酸性;CO难溶于水,但能燃烧
2
C.用途:CO 可用于光合作用、灭火等;CO可作气体燃料,还可用于人工降雨
2
D.危害:CO 会造成“温室效应”;CO易与血液中的血红蛋白结合引起中毒
2
12.据探测卫星发回的数据分析,火星大气中95%是二氧化碳,其余为少量的氮气、氢气,
还找到了有液态水存在的证据。根据以上信息,某同学做出如下推断:①火星大气是混合物
②火星大气与地球大气成分相似 ③在火星上敞口放置的澄清石灰水容易变质 ④火星环
境适宜人类生存 ⑤火星上温室效应显著。你认为正确的是( )A.①③⑤
B.②③⑤
C.②③④
D.①④⑤
二、填空与简答题(本题包括4个小题,共22分)
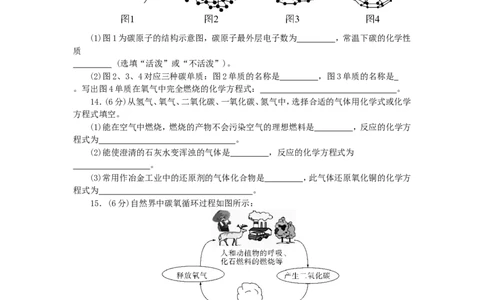
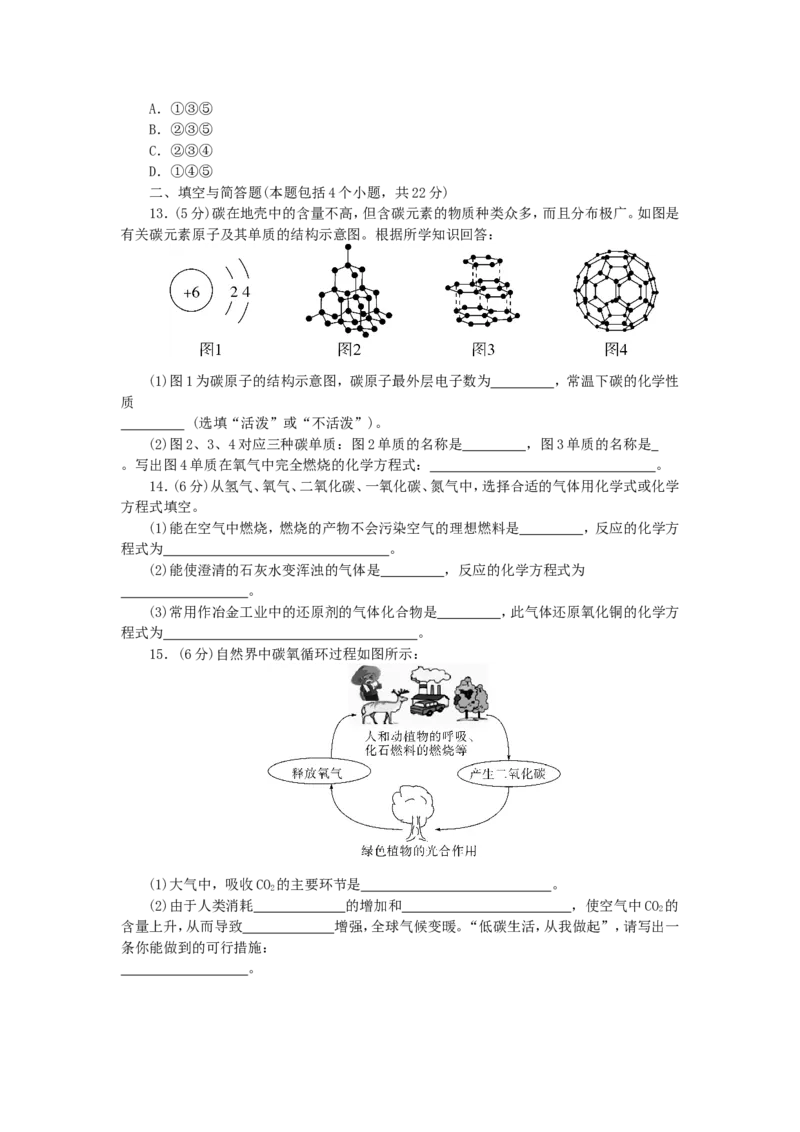
13.(5分)碳在地壳中的含量不高,但含碳元素的物质种类众多,而且分布极广。如图是
有关碳元素原子及其单质的结构示意图。根据所学知识回答:
(1)图1为碳原子的结构示意图,碳原子最外层电子数为 ,常温下碳的化学性
质
(选填“活泼”或“不活泼”)。
(2)图2、3、4对应三种碳单质:图2单质的名称是 ,图3单质的名称是
。写出图4单质在氧气中完全燃烧的化学方程式: 。
14.(6分)从氢气、氧气、二氧化碳、一氧化碳、氮气中,选择合适的气体用化学式或化学
方程式填空。
(1)能在空气中燃烧,燃烧的产物不会污染空气的理想燃料是 ,反应的化学方
程式为 。
(2)能使澄清的石灰水变浑浊的气体是 ,反应的化学方程式为
。
(3)常用作冶金工业中的还原剂的气体化合物是 ,此气体还原氧化铜的化学方
程式为 。
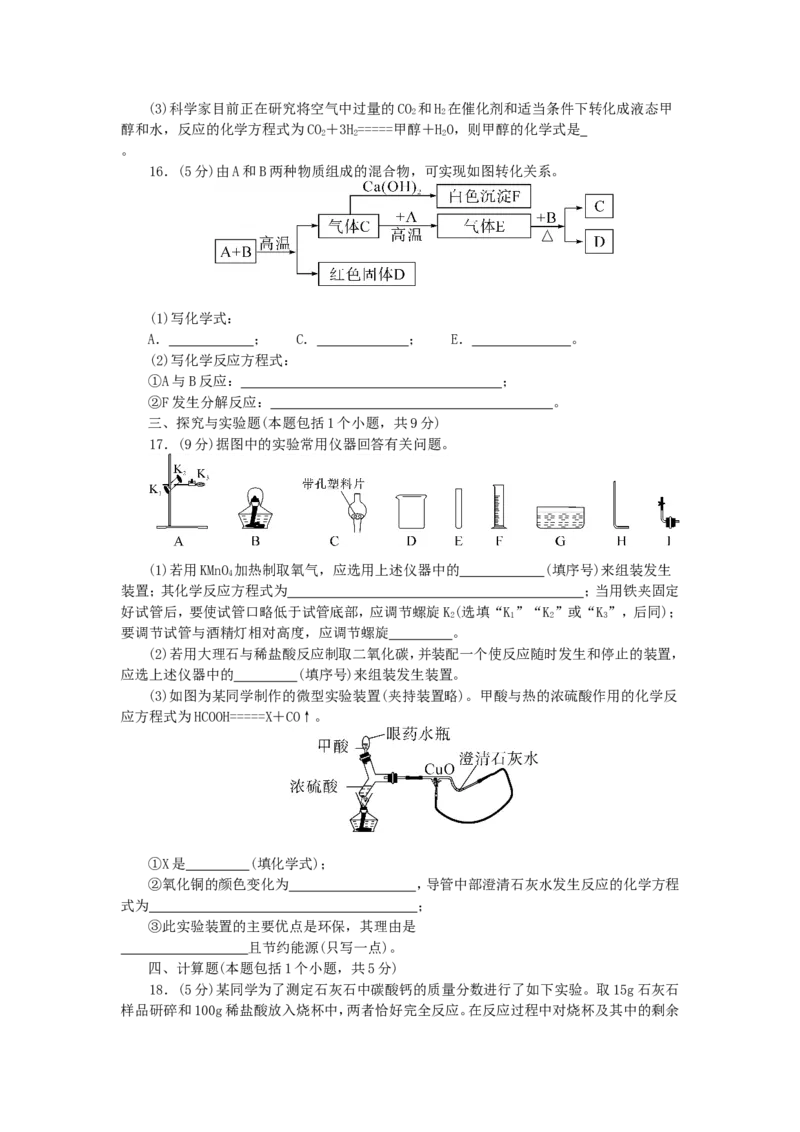
15.(6分)自然界中碳氧循环过程如图所示:
(1)大气中,吸收CO 的主要环节是 。
2
(2)由于人类消耗 的增加和 ,使空气中CO 的
2
含量上升,从而导致 增强,全球气候变暖。“低碳生活,从我做起”,请写出一
条你能做到的可行措施:
。(3)科学家目前正在研究将空气中过量的CO 和H 在催化剂和适当条件下转化成液态甲
2 2
醇和水,反应的化学方程式为CO+3H=====甲醇+HO,则甲醇的化学式是
2 2 2
。
16.(5分)由A和B两种物质组成的混合物,可实现如图转化关系。
(1)写化学式:
A. ; C. ; E. 。
(2)写化学反应方程式:
①A与B反应: ;
②F发生分解反应: 。
三、探究与实验题(本题包括1个小题,共9分)
17.(9分)据图中的实验常用仪器回答有关问题。
(1)若用KMnO 加热制取氧气,应选用上述仪器中的 (填序号)来组装发生
4
装置;其化学反应方程式为 ;当用铁夹固定
好试管后,要使试管口略低于试管底部,应调节螺旋K(选填“K”“K”或“K”,后同);
2 1 2 3
要调节试管与酒精灯相对高度,应调节螺旋 。
(2)若用大理石与稀盐酸反应制取二氧化碳,并装配一个使反应随时发生和停止的装置,
应选上述仪器中的 (填序号)来组装发生装置。
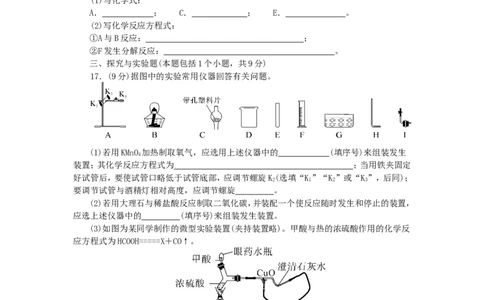
(3)如图为某同学制作的微型实验装置(夹持装置略)。甲酸与热的浓硫酸作用的化学反
应方程式为HCOOH=====X+CO↑。
①X是 (填化学式);
②氧化铜的颜色变化为 ,导管中部澄清石灰水发生反应的化学方程
式为 ;
③此实验装置的主要优点是环保,其理由是
且节约能源(只写一点)。
四、计算题(本题包括1个小题,共5分)
18.(5分)某同学为了测定石灰石中碳酸钙的质量分数进行了如下实验。取15g石灰石
样品研碎和100g稀盐酸放入烧杯中,两者恰好完全反应。在反应过程中对烧杯及其中的剩余物进行了五次称量,记录数据如下表(已知烧杯的质量为25g,样品中的杂质不溶于水、也不
与稀盐酸反应)。请计算:
反应时间/s 20 40 60 80 100
烧杯和所盛药品质量/g 137.8 135.6 134.5 m 134.5
(1)表中的“m”为 g。
(2)该石灰石样品中碳酸钙的质量分数(计算结果精确至0.1%)。
答案
1.A 2.B 3.A 4.D 5.D 6.A 7.D
8.D 点拨:反应后固体减少的质量除了氧化铜失去的氧元素质量外,还有参加反应的
碳的质量。
9.D 点拨:装置Ⅲ和Ⅴ可用于收集氧气,装置Ⅳ不可以用于收集氧气。
10.B 点拨:B装置虽然有带孔的塑料片,但是稀盐酸一直浸没大理石,所以无法控制反
应的进行。
11.C 点拨:可用于人工降雨的是CO。
2
12.A
13.(1)4 不活泼 (2)金刚石 石墨 C +60O=====60CO
60 2 214.(1)H 2H+O=====2HO
2 2 2 2
(2)CO CO+Ca(OH)===CaCO↓+HO
2 2 2 3 2
(3)CO CO+CuO=====Cu+CO
2
15.(1)绿色植物的光合作用
(2)化石能源 对森林的乱砍滥伐 温室效应 节约用电,随手关灯(其他如多参加义务
植树活动,爱护绿地草坪等合理均可)
(3)CHOH(或CHO)
3 4
16.(1)C CO CO
2
(2)①C+2CuO=====2Cu+CO↑ ②CaCO=====CaO+CO↑
2 3 2
17.(1)ABEI 2KMnO=====KMnO+MnO+O↑ K K
4 2 4 2 2 2 1
(2)CDI
(3)①HO
2
②由黑色变红色 Ca(OH)+CO===CaCO↓+HO
2 2 3 2
③一氧化碳被点燃生成二氧化碳,不污染环境,并且节约能源
18.(1)134.5
(2)解:反应生成二氧化碳的质量为15g+100g+25g-134.5g=5.5g。
设石灰石样品中碳酸钙的质量为x。
CaCO+2HCl===CaCl+HO+CO↑
3 2 2 2
100 44
x 5.5g
= x=12.5g
该石灰石样品中碳酸钙的质量分数为×100%=83.3%。
答:该石灰石样品中碳酸钙的质量分数为83.3%。