文档内容
第十至十二单元测试题
(满分:100分 时间:90分钟)
相对原子质量:H—1 C—12 O—16 Na—23 Cl—35.5
一、选择题(每小题3分,共45分)
1.(2017·盐城)“一带一路”赋予古丝绸之路崭新的时代内涵。古代染坊常用下列物质
中的一种盐来处理丝绸,这种盐是(B)
A.熟石灰 B.碳酸钾 C.乙醇 D.烧碱
2.(2017·泰州)下列物质属于复合肥的是(A)
A.KNO B.CO(NH ) C.KCO D.Ca (PO )
3 2 2 2 3 3 4 2
3.(2017·邵阳)下列物品用到的主要材料,不属于有机合成材料的是(D)
A.塑胶水管 B.涤纶运动服 C.汽车轮胎 D.不锈钢饭盒
4.(2017·青岛)下表列出了一些常见物质在常温下的pH范围,其中呈碱性的是(A)
物质名称 鸡蛋清 牛奶 西红柿 柠檬汁
pH范围 7.6~8.0 6.3~6.6 4.0~4.4 2.0~3.0
A.鸡蛋清 B.牛奶 C.西红柿 D.柠檬汁
5.(2017·长沙)“端午佳节,粽叶飘香”,我们过节有吃盐蛋、粽子、糖包、肉包的习俗,从
均衡营养的角度分析,还需要补充的主要营养素是(C)
A.蛋白质 B.糖类 C.维生素 D.油脂
6.(2017·邵阳)下列试剂能将稀硫酸、氯化钠溶液、澄清石灰水三种溶液一步鉴别出来的
是(D)
A.稀盐酸 B.二氧化碳 C.碳酸钙 D.石蕊溶液
7.(2017·贵港)一些食物pH的近似值范围如下:橘子汁3.0~4.0;泡菜3.2~3.6;牛奶6.3
~6.6;鸡蛋清7.6~8.0。下列说法中,不正确的是(D)
A.鸡蛋清显碱性 B.胃酸过多的人应少吃泡菜
C.橘子汁能使紫色石蕊溶液变红 D.牛奶比橘子汁的酸性强
8.(2017·青岛)下列对实验现象的描述中,正确的是(C)
A.向稀盐酸中滴加紫色石蕊试液,溶液显蓝色
B.将红热的细铁丝放在氧气中,剧烈燃烧,火星四射,生成白色固体
C.将羊毛线放在酒精灯火焰上灼烧,闻到烧焦羽毛的特殊气味
D.向氯化铁溶液中滴加氢氧化钠溶液,生成蓝色沉淀
9.(2017·邵阳)化学与人体健康关系密切,下列做法或说法不合理的是(C)
A.食用加碘盐有助于预防甲状腺肿大 B.常食蔬菜和水果有助于补充维生素
C.用甲醛溶液浸泡海产品,以延长保鲜时间 D.老年人适量饮食奶制品,可以预防骨
质疏松症
10.(2017·内江)将一定量的氢氧化钠溶液与稀盐酸混合,二者恰好完全反应的微观示意
图如下。由此分析下列说法正确的是(C)
A.反应前后阴、阳离子的总数目不变
B.反应前后溶剂质量不变C.反应后溶液呈中性
D.反应前后元素种类发生了变化
11.(2017·孝感)推理是研究和学习化学的重要方法,以下推理正确的是(A)
A.若某雨水的pH<7,则该雨水一定呈酸性
B.过滤可以除去水中不溶性杂质,因此过滤后的水一定是软水
C.一氧化碳和二氧化碳的组成元素相同,所以它们的化学性质相同
D.可燃物燃烧时温度需要达到着火点,所以温度达到着火点时,可燃物就一定能燃烧
12.(2017·内江)下列各组物质在同一溶液中可以大量共存的是(D)
A.NaOH、FeCl 、KSO B.NaCl、HNO、AgNO
3 2 4 3 3
C.NaCl、KCO、Ca(OH) D.KNO、NaCl、Ba(OH)
2 3 2 3 2
13.(2017·威海)在实验室中,仅用下表提供的仪器和药品,就能达到相应实验目的的是
(A)
选项 仪器 药品 实验目的
未知溶液、Ba(NO ) 溶液、 检验未知溶液中是否含有
A 试管、胶头滴管 3 2
稀硝酸 SO 2-
4
证明Cu、Zn、Fe的金属活动
B 试管、胶头滴管 ZnSO 溶液、铜片、铁丝
4 性
检验久置的NaOH溶液是
C 试管、胶头滴管 久置的NaOH溶液、酚酞
否完全变质
烧杯、漏斗、滤纸、铁
D 粗盐、蒸馏水 除去粗盐中的难溶性杂质
架台(带铁圈)、药匙
14.(2017·长沙)下列各组物质的溶液,不另加试剂就不能鉴别出来的一组是(D)
A.CuSO NaOH KNO B.FeCl AgNO NaNO
4 3 3 3 3
C.NaCO HCl BaCl D.CaCl KCO NaCl
2 3 2 2 2 3
15.(2017·兰州)下列图象与所对应操作相符的是(D)
A.用两份等质量、等质量分数的过氧化氢溶液制取氧气
B.向一定质量分数的盐酸中不断加水
C.向等质量的锌片、镁片中分别加入足量的等质量分数的稀硫酸
D.向一定质量的氯化铜和稀盐酸的混合溶液中不断加NaOH溶液
二、填空题(共34分)
16.(8分)(2017·无锡)化学就在我们身边,人类的衣、食、住、行都离不开化学。
(1)在厨房里蕴藏着许多化学知识。
①下列食物中,能提供大量维生素的是C(填字母)。
②加铁酱油中的“铁”是指元素(填“元素”或“原子”),身体缺铁会引起贫血。③厨房中能用来除水垢的物质是醋。
④为防止菜刀生锈,可采用的一种措施是在表面涂一层油。
(2)汽车、高铁、飞机等已成为人们出行的常用交通工具。
①汽油是汽车常用的一种燃料。将石油加热,利用各成分的沸点不同将它们分离可得到
汽油,该过程属于物理变化。汽车的铅蓄电池工作时,发生如下化学反应:2Pb+O +
2
2HSO ===2PbSO+2HO,该反应涉及的物质中属于氧化物的HO。
2 4 4 2 2
②高铁车头的玻璃是用无机玻璃、树脂、塑料等粘合而成,能耐受强大的撞击力,这种玻
璃属于A(填字母)。
A.复合材料 B.合成材料 C.金属材料
③制造飞机使用了硬铝(铝铜镁硅合金),其中镁元素的某种粒子结构示意图为 ,
镁原子的最外层电子数是2。
17.(11分)(2017·天津)酸、碱、盐在生产生活中具有广泛的用途。
(1)制作“叶脉书签”需用到10%的氢氧化钠溶液。现配制50 g质量分数为10%的氢氧
化钠溶液。
①若用氢氧化钠固体配制,需称量氢氧化钠的质量为5g。
②用氢氧化钠固体配制10%的氢氧化钠溶液过程中需要用到的仪器除了托盘天平、药
匙、量筒、烧杯、胶头滴管、试剂瓶外,还需要玻璃棒。
③下列操作正确的是D(填字母)。
A.称量氢氧化钠固体时,左盘放砝码
B.在托盘天平的左右托盘上垫滤纸称量氢氧化钠固体
C.将准确称量的氢氧化钠固体放入装有水的量筒中溶解
D.将配制好的氢氧化钠溶液装入试剂瓶中,塞好瓶塞并贴上标签
④若用20%的氢氧化钠溶液加水(水的密度为1 g/cm3)配制50 g质量分数为10%的氢氧
化钠溶液,需20%的氢氧化钠溶液的质量为25g;配制时应选用50(填“10”或“50”)mL的量
筒量取水。
(2)某固体粉末可能含有碳酸钙、硫酸钠、氯化钠、氯化钡、硫酸铜中的一种或几种。为确
定该固体粉末的成分,进行了如下实验:
回答下列问题:
①反应Ⅰ的化学方程式为CaCO +2HCl===CaCl +CO↑+HO。
3 2 2 2
②白色沉淀C是BaSO(填化学式)。
4
③原固体粉末中一定不含CuSO 、BaCl (填化学式)。
4 2
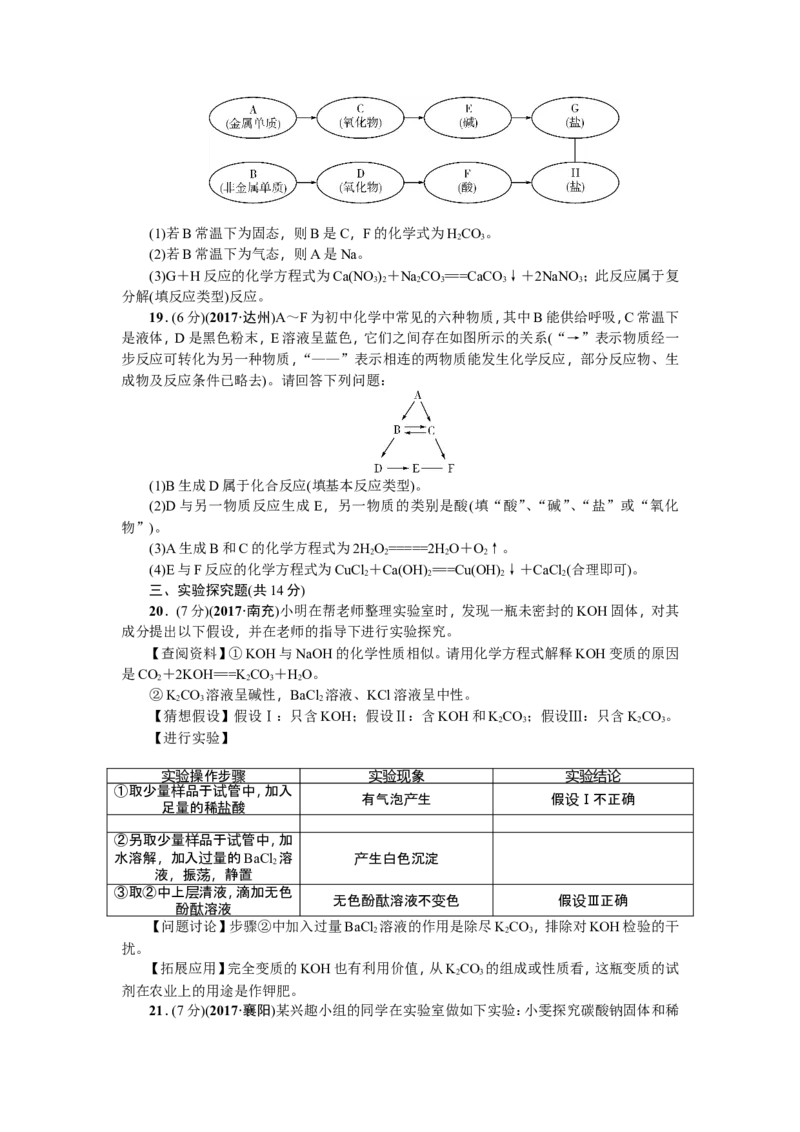
18.(9分)(2017·广东)A~H分别是氢、氧、碳、氮、钠、钙六种元素中的一种或几种组成的
初中化学常见物质(如下图所示,箭头表示物质间能转化,实线表示物质间能反应)。请回答:(1)若B常温下为固态,则B是C,F的化学式为HCO。
2 3
(2)若B常温下为气态,则A是Na。
(3)G+H反应的化学方程式为Ca(NO )+NaCO===CaCO ↓+2NaNO ;此反应属于复
3 2 2 3 3 3
分解(填反应类型)反应。
19.(6分)(2017·达州)A~F为初中化学中常见的六种物质,其中B能供给呼吸,C常温下
是液体,D是黑色粉末,E溶液呈蓝色,它们之间存在如图所示的关系(“→”表示物质经一
步反应可转化为另一种物质,“——”表示相连的两物质能发生化学反应,部分反应物、生
成物及反应条件已略去)。请回答下列问题:
(1)B生成D属于化合反应(填基本反应类型)。
(2)D与另一物质反应生成E,另一物质的类别是酸(填“酸”、“碱”、“盐”或“氧化
物”)。
(3)A生成B和C的化学方程式为2HO=====2HO+O↑。
2 2 2 2
(4)E与F反应的化学方程式为CuCl +Ca(OH) ===Cu(OH) ↓+CaCl (合理即可)。
2 2 2 2
三、实验探究题(共14分)
20.(7分)(2017·南充)小明在帮老师整理实验室时,发现一瓶未密封的KOH固体,对其
成分提出以下假设,并在老师的指导下进行实验探究。
【查阅资料】①KOH与NaOH的化学性质相似。请用化学方程式解释KOH变质的原因
是CO+2KOH===K CO+HO。
2 2 3 2
②KCO 溶液呈碱性,BaCl 溶液、KCl溶液呈中性。
2 3 2
【猜想假设】假设Ⅰ:只含KOH;假设Ⅱ:含KOH和KCO;假设Ⅲ:只含KCO。
2 3 2 3
【进行实验】
实验操作步骤 实验现象 实验结论
①取少量样品于试管中,加入
有气泡产生 假设Ⅰ不正确
足量的稀盐酸
②另取少量样品于试管中,加
水溶解,加入过量的BaCl 溶 产生白色沉淀
2
液,振荡,静置
③取②中上层清液,滴加无色
无色酚酞溶液不变色 假设Ⅲ正确
酚酞溶液
【问题讨论】步骤②中加入过量BaCl 溶液的作用是除尽KCO,排除对KOH检验的干
2 2 3
扰。
【拓展应用】完全变质的KOH也有利用价值,从KCO 的组成或性质看,这瓶变质的试
2 3
剂在农业上的用途是作钾肥。
21.(7分)(2017·襄阳)某兴趣小组的同学在实验室做如下实验:小雯探究碳酸钠固体和稀盐酸之间的反应,请写出该反应的化学方程式:NaCO+2HCl===2NaCl+HO+CO↑;小
2 3 2 2
棋探究HSO 、NaOH、CuSO 、BaCl 四种溶液之间的反应。
2 4 4 2
实验完毕,小雯和小棋将试管中的剩余物都倒入同一大烧杯中,过滤后得到了沉淀A和
无色滤液M,并接着进行如下探究:
(查阅资料:NaSO 溶液呈中性,NaCO 溶液呈碱性)
2 4 2 3
实验步骤 实验现象 实验结论
①向所得沉淀A中加入过量 出现白色沉淀B和蓝色溶 白色沉淀B是BaSO(或硫酸
4
稀盐酸,充分反应 液,没有气泡产生 钡)
②取少量无色滤液M于试管
溶液不变色
中,滴入酚酞溶液
③取步骤②中溶液,加入适量
无明显现象
NaSO 溶液,充分反应
2 4
④另取少量无色滤液M于试 无明显现象(或锌粒表面无红 则滤液M中一定含有的溶质
管中,加入几粒锌粒 色固体生成、无气体放出) 是NaCl(或氯化钠)
小棋分析后认为:步骤④中加入锌粒没有必要;滤液M中还可能存在其他成分。如果将
步骤④中的锌粒换成另一种试剂,可确定该成分是否存在。请写出小棋用所选试剂鉴定可能
存在成分的化学方程式:BaCl +NaSO ===BaSO ↓+2NaCl(合理即可)。
2 2 4 4
四、计算题(7分)
22.(2017·达州)NaCl和NaCO 的固体混合物与一定质量的稀盐酸恰好完全反应,得到
2 3
4.4 g CO 和100 g 21.1%的NaCl溶液,求:
2
(1)稀盐酸中溶质的质量为7.3g。
(2)原混合物中NaCl的质量分数(写出计算过程)。
解:设碳酸钠的质量为x,反应生成的氯化钠质量为y,参加反应的盐酸中溶质质量为z。
NaCO+2HCl===2NaCl+HO+CO↑
2 3 2 2
106 73 117 44
x z y 4.4 g
===
x=10.6 g y=11.7 g z=7.3 g
原混合物中氯化钠的质量:100 g×21.1%-11.7 g=9.4 g
原混合物中NaCl的质量分数=×100%=47%
答:原混合物中NaCl的质量分数为47%。