文档内容
专题一 信息给予题
一、选择题
1.真空包装、食品包装袋内充氮气、放铁粉包或生石灰包等都是常用的食品防腐、保鲜
方法。对上述方法的分析,错误的是(D)
A.真空包装:能使食品不与氧气接触
B.充氮气:能隔绝空气并防止食品变形
C.放铁粉包:能除去食品包装袋内的氧气和水蒸气
D.放生石灰包:能除去食品包装袋内的氧气
2.(2017,武威)下列对化学基本观念的认识不正确的是(C)(导学号 58504397)
A.微粒观:一氧化碳分子由一个碳原子和一个氧原子构成
B.能量观:天然气燃烧放出大量的热
C.分类观:纯碱和烧碱从组成上都属于碱
D.守恒观:电解水反应前后,元素种类和原子数目均不变
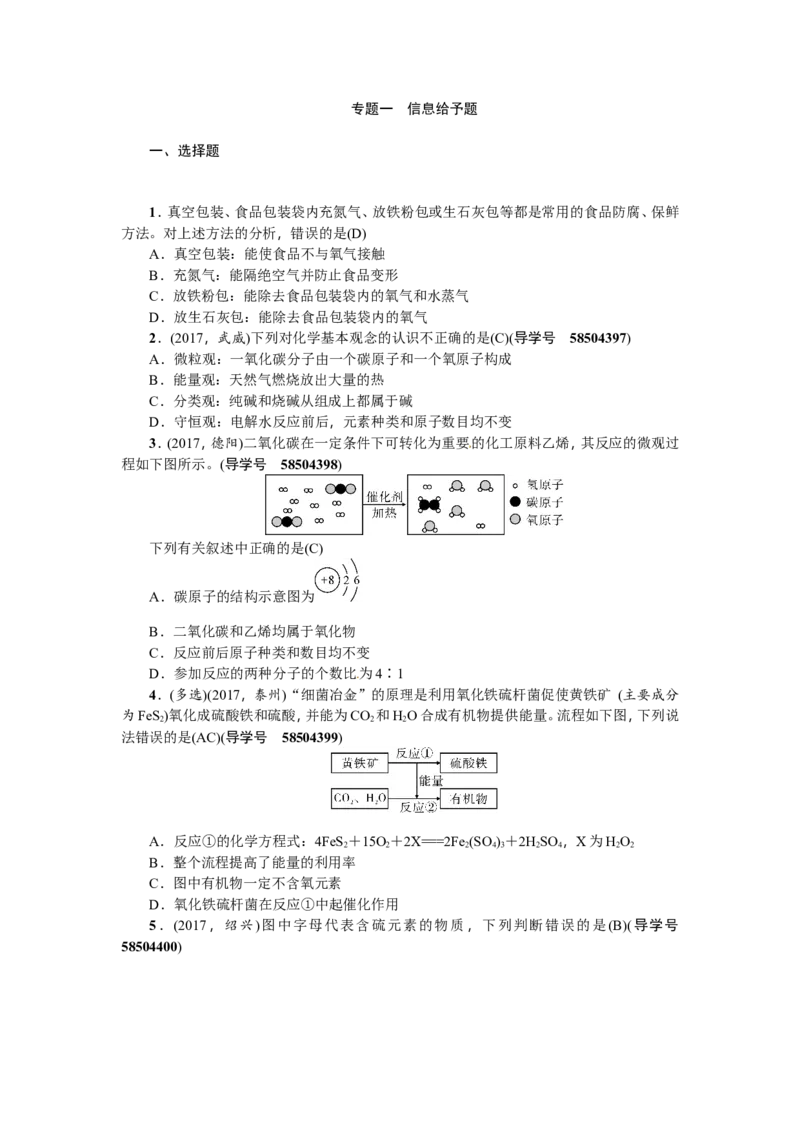
3.(2017,德阳)二氧化碳在一定条件下可转化为重要的化工原料乙烯,其反应的微观过
程如下图所示。(导学号 58504398)
下列有关叙述中正确的是(C)
A.碳原子的结构示意图为
B.二氧化碳和乙烯均属于氧化物
C.反应前后原子种类和数目均不变
D.参加反应的两种分子的个数比为4∶1
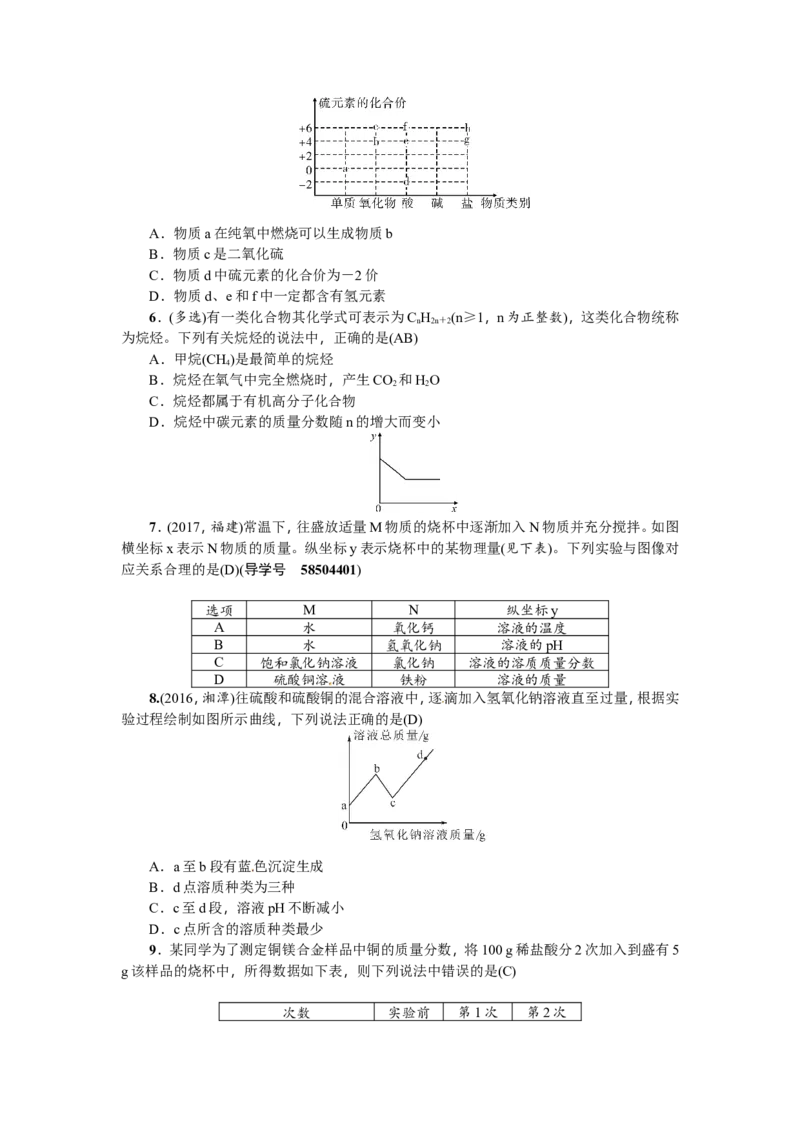
4.(多选)(2017,泰州)“细菌冶金”的原理是利用氧化铁硫杆菌促使黄铁矿 (主要成分
为FeS)氧化成硫酸铁和硫酸,并能为CO 和HO合成有机物提供能量。流程如下图,下列说
2 2 2
法错误的是(AC)(导学号 58504399)
A.反应①的化学方程式:4FeS+15O+2X===2Fe (SO )+2HSO ,X为HO
2 2 2 4 3 2 4 2 2
B.整个流程提高了能量的利用率
C.图中有机物一定不含氧元素
D.氧化铁硫杆菌在反应①中起催化作用
[来源:学科网]
5.(2017,绍兴)图中字母代表含硫元素的物质,下列判断错误的是(B)(导学号
58504400)A.物质a在纯氧中燃烧可以生成物质b
B.物质c是二氧化硫
C.物质d中硫元素的化合价为-2价
D.物质d、e和f中一定都含有氢元素
6.(多选)有一类化合物其化学式可表示为C H (n≥1,n为正整数),这类化合物统称
n 2n+2
为烷烃。下列有关烷烃的说法中,正确的是(AB)
A.甲烷(CH)是最简单的烷烃
4
B.烷烃在氧气中完全燃烧时,产生CO 和HO
2 2
C.烷烃都属于有机高分子化合物
D.烷烃中碳元素的质量分数随n的增大而变小
7.(2017,福建)常温下,往盛放适量M物质的烧杯中逐渐加入N物质并充分搅拌。如图
横坐标x表示N物质的质量。纵坐标y表示烧杯中的某物理量(见下表)。下列实验与图像对
应关系合理的是(D)(导学号 58504401)
选项 M N 纵坐标y
A 水 氧化钙 溶液的温度
B 水 氢氧化钠 溶液的pH
C 饱和氯化钠溶液 氯化钠 溶液的溶质质量分数
D 硫酸铜溶液 铁粉 溶液的质量
8.(2016,湘潭)往硫酸和硫酸铜的混合溶液中,逐滴加入氢氧化钠溶液直至过量,根据实
验过程绘制如图所示曲线,下列说法正确的是(D)
A.a至b段有蓝色沉淀生成
B.d点溶质种类为三种
C.c至d段,溶液pH不断减小
D.c点所含的溶质种类最少
9.某同学为了测定铜镁合金样品中铜的质量分数,将100 g稀盐酸分2次加入到盛有5
g该样品的烧杯中,所得数据如下表,则下列说法中错误的是(C)
次数 实验前 第1次 第2次加入稀盐酸的质量/g 0 50 50
剩余固体的质量/g 5 3 2
A.第1次加入稀盐酸后剩余固体中还有镁
B.第2次所加入的稀盐酸未反应完
C.每50 g稀盐酸和1 g镁恰好完全反应
D.合金样品中铜的质量分数为40%
10.(2017,黄冈)Si是重要的半导体材料,半导体工业中有一句行话“从沙滩到用户”,
指的是利用沙子(主要成分SiO)制取高纯度的Si,已知硅与碳有相似的化学性质,SiHCl (三
2 3
氯氢硅)能与水反应,其工艺流程和主要化学反应如下:(导学号 58504402)
①2C+SiO=====Si(不纯)+2CO↑
2
②3HCl+Si(不纯)=====SiHCl +H
3 2
③SiHCl +H=====3HCl+Si(高纯)
3 2
下列说法不正确的(D)
A.①的目的是将二氧化硅转化成单质硅
B.物质A可循环利用
C.整个制备过程必须达到无水无氧
D.反应③中SiHCl 是还原剂
3
二、填空题
11.(2017,成都)根据图文回答下列问题。
(1)汽水是常见的饮料,打开瓶盖汽水会自动喷出。
①汽水属于__混合物____(填“纯净物”或“混合物”)。
②汽水中的气体的溶解度随压强减小而 __减小(填“增大”或“减小”)。
③汽水瓶的材质属于__合成____(填“金属”或“合成”)材料。
④汽水的 pH 范围是 2.2~4.9,呈__酸__(填“酸”“碱”或“中”)性。
(2)在中秋节,人们有食用月饼的习俗。
①营养成分表中的“钠”是指__元素__(填“元素”或“单质”)。
[来源:学科网ZXXK]
②营养成分表中“蛋白质”属于__有机__(填“无机”或“有机”)物。
③下列制月饼的原料,属于糖类的是__A__(填序号)。
A.面粉 B.植物油 C.鸡蛋
④纸袋内的生石灰的作用是__ 吸收水分 ( 或防潮等 )__。12.(2017,福建)农业废弃物是指农业生产过程中废弃的有机物,如秸秆、蔗渣等。(导学
号 58504403)
(1)农业废弃物经发酵处理可获得沼气(主要成分为甲烷)。甲烷完全燃烧的化学方程式:
__CH + 2O ===== CO + 2H O__。
4 2 2 2
(2)闽籍科学家张俐娜发明了一种快速溶解农业废弃物的“神奇溶剂”。该“神奇溶剂”
中氢氧化钠、尿素和水的质量比为7∶12∶81。
①“神奇溶剂”是一种溶液,其溶质有__氢氧化钠、尿素__。
②某次生产需用到100 kg“神奇溶剂”。现仅用氢氧化钠溶液和尿素来配制,所用的氢
氧化钠溶液的溶质质量分数为__ × 100% __(列出计算式即可)。
③利用该“神奇溶剂”溶解农业废弃物生产的新型纤维素膜,在土壤中能完全降解。利
用此膜替代普通塑料,可缓解的环境问题是__ 白色污染 ( 或其他合理答案 )__(写一点)。
13.(2017,安徽)五氧化二钒(V O)是一种工业催化剂,下图是制取VO 的工艺流程。
2 5 2 5
(1)写出反应①的化学方程式:
__KVO + NH Cl == =NH VO ↓ + KC l__。
3 4 4 3
(2)操作a的名称是__过滤__,实验室进行该操作所需的玻璃仪器有烧杯、玻璃棒和__漏
斗__。
[来源:学,科,网]
(3)反应②的反应类型是__分解反应__,物质X中一定含有的元素是__ N( 或 N 或 H) __。
(4)写出副产物KCl的一种用途__用作钾肥__。
14.(2017,广州)菱锰矿(含有MnCO )常用稀HSO 来浸出Mn2+:(导学号 58504404)
3 2 4
(1)浸出Mn2+发生的是复分解反应,该化学方程式是__MnCO + H SO == =MnSO + H O
3 2 4 4 2
+ CO ↑__。
2
(2)为探究浸锰的最佳工艺条件,某研究小组首先进行了单因素实验,数据如下:
矿酸比 1∶0.4 1∶0.5 1∶0.6 1∶0.7 1∶0.8
浸出率/% 75.9 83.8 91.8 92.8 93.0
①矿酸比从1∶0.4到1∶0.8的过程中,稀HSO 的用量__增大__(填“增大”或
2 4
“减小”)。
②分析数据得知:当矿酸比从1∶0.4到1∶0.6时,Mn2+浸出率__明显增大__;当矿酸比
从1∶0.6到1∶0.8时,Mn2+浸出率__略微增大__。
(3)该研究小组选定两个因素作为研究条件进行对比实验,数据如下:
矿酸比 温度/℃ 浸出率/%
1 1∶0.5 60 80.2
2 1∶0.5 80 83.8
3 1∶0.6 60 X
[来
源:Zxxk.Com]
4 1∶0.6 80 91.8
①表中X最有可能的数值为__C__(填字母)。
A.79.7 B.80.8C.87.6 D.92.8
②该工艺的最佳条件为:矿酸比:__ 1 ∶ 0.6 __;温度:__80_℃__。
三、计算题
15.(2017,滨州)小滨同学为了测定某珍珠粉中碳酸钙的质量分数,称取12.5 g珍珠粉样
品,进行四次高温煅烧、冷却、称量剩余固体的重复操作(杂质不参加反应),记录数据如下:
(导学号 58504405)
操作次序 第一次 第二次 第三次 第四次
[来源:Z。
xx。k.Com]
剩余固体质量/g 10.8 9.6 8.1 8.1
试计算:
(1)完全反应后生成二氧化碳的质量为__4.4__ g。
(2)求该珍珠粉中碳酸钙的质量分数。
解:(1)由质量守恒定律可知,生成二氧化碳的质量=12.5 g-8.1 g=4.4 g
(2)设样品中碳酸钙的质量为x
CaCO =====CaO+CO↑
3 2
100 44
x 4.4 g
=
x=10 g
该珍珠粉中碳酸钙的质量分数=×100%=80%
答:该珍珠粉中碳酸钙的质量分数为80%。