文档内容
中考总复习分类专题训练化学(八)
(内容:盐和化肥)
班级 姓名 学号 成绩
说明:1.测试时间45分钟,满分100分。
2. 可能用到的相对原子质量:H:1 C:12 Ca:40 O : 16 Cl:35.5
一、单项选择题(以下第1-10小题,每小题3分,共30分。每小题只有一个正确答案)
1.下列物质可通过相应的金属与稀酸发生反应而得到的是( )
A.ZnCl B.AgCl C.CuCl D.Fe (SO )
2 2 2 4 3
2.下列化学肥料属于复合肥料的是( )
A.尿素〔CO(NH)〕 B.重过磷酸钙〔Ca(HPO )〕
2 2 2 4 2
C.氯化钾〔KCl〕 D.磷酸二氢铵〔NH HPO 〕
4 2 4
3.下列物质的溶液中能与氢氧化钠溶液反应生成蓝色沉淀的是( )
A.HCl B.MgCl C.KNO D.CuSO
2 3 4
4.在发酵面团中加入某种物质糅合,既能使蒸出的面包疏松多孔,又能除去面团中的酸,该种
物质可能是( )
A.白糖 B.NaHCO C.NaOH D.CHCOOH
3 3
5.用水作试剂,不可能区分开来的一组物质是( )
A.氯化镁、食盐、烧碱 B.汽油、酒精、浓硫酸
C.无水硫酸铜、碳酸钠、碳酸钙 D.氯化钾、硝酸钠、硫酸钾
6.下列各组物质中的杂质(括号内为杂质)只需加入适量稀硫酸就能除去的是( )
A.NaCl(Na CO) B.Fe(Cu)
2 3
C.Na CO(CaCO) D.HCl(BaCl )
2 3 3 2
7.石灰浆新抹的墙壁上掉下一块白色固体,小红为探究其成分,她应该选用的试剂是( )
A.酚酞、氢氧化钠溶液 B.酚酞、稀盐酸
C.酚酞、氯化钠溶液 D.盐酸、氢氧化钠溶液
8.向25 mL含有HSO 和MgCl 的混合溶液中逐滴加入NaOH溶液,若纵坐标表示产生的沉淀
2 4 2
量,横坐标表示NaOH溶液的加入量,以下图象正确的是( )
9.下列两种溶液混合后能发生化学反应,且溶液的总质量不会发生变化的是( )
A.氢氧化钾溶液和硫酸溶液 B.碳酸钠溶液和稀盐酸
1C.食盐溶液和稀硝酸 D.三氯化铁溶液和烧碱溶液
10.下列四种物质中,一次就能将AgNO、NaCO、KSO 三种溶液区分开的是 ( )
3 2 3 2 4
A.NaNO B.NaCl C.NaOH D.稀盐酸
3
二、双项选择题(以下第11-13小题,每小题3分,共9分。每小题有两个选项符合题意,全部
选对的得3分,漏选得1分,错选不选得0分。)
11.如图所示,在烧瓶里收集满某种气体,烧瓶用带导管的胶塞塞紧(导管一端
已事先绑好一个气球)。拔开胶塞迅速倒入浓氢氧化钠溶液,立即塞紧振荡,
可以看到气球逐渐膨胀,这种气体可能是( )
A.H B.HCl C.SO D.O
2 2 2
12.除去下列物质中的杂质(括号内为杂质),所用的试剂和方法不正确的是( )
A.Na CO(NaOH):通入适量二氧化碳 B.CO(CO):通过灼热的氧化铜
2 3 2
C.HNO (HCl):AgNO 溶液,过滤 D.Cu(OH) (CuCl ):加入适量稀盐酸
3 3 2 2
13.对实验现象的观察和分析,有助于获得化学知识并学会科学探究的方法。下列对实验现象的
分析合理的是 ( )
A.向某无色溶液中滴入酚酞试液,呈红色,证明该溶液是碱性溶液
B.向某无色溶液中滴入硝酸银溶液,产生白色沉淀,证明该溶液是盐酸
C.某白色固体与熟石灰混合加热,产生可使湿润红色石蕊试纸变蓝的气体,证明该固体是铵盐
D.把燃着的木条伸入某无色气体的集气瓶中,火焰熄灭,证明该气体是二氧化碳
三、填空题与简答题(本大题共6小题,共33分)
14.(5分)从氢气、盐酸、干冰、氢氧化钠、碳酸钙中,选出适当的物质,按要求填空。
(1)可用于人工降雨的物质是_______________。
(2)可用作理想的高能燃料的气体是_______________。
(3)可用于除铁锈的酸是_______________。
(4)化工生产中的一种重要原料,其水溶液能使酚酞试液变红的是_______________。
(5)用作建筑材料的大理石,其主要成分是_______________。
15. (4分)从下列H、Na、O、N、S元素中,选择由适当元素组成的符合下列要求的化合物,将其
化学式填入相应的空格中:
(1)人体内含量最多的物质是_______________。
(2)能与水反应生成酸的氧化物_______________。
(3)具有强烈腐蚀性,广泛用于肥皂、造纸工业的化合物_______________。
(4)一种常见的氮肥,且属于盐的是_______________________________________________。
16. (6分)“果导片”是一种常用缓泻剂,主要成分是酚酞。某同学欲将其作为酚酞指示剂的
替代品,他将“果导片”研成粉末放入酒精中,搅拌、静置,取上清液滴入白醋和食盐水,看到
_________________________,滴入澄清石灰水发现_________ __;确定“果导片”可作
酸碱指示剂使用。当他用饮料吸管向滴有“果导片”清液的澄清石灰水吹气时,可观察到
__________________________ 现象。
17.(5分)构建知识网络是一种重要的学习方法。下图是关于盐酸化 B 学
性质的知识网络,“——”表示相连的两种物质能发生反应,“ → ”
表示一种物质转化成另一种物质,A、C属于不同类别的化合物。完 善
这个知识网络: A HCl C
(1)写出A、B、C可能的化学式:A______;B______;C______。
2 Zn(2)根据自己得出的知识网络写出一个复分解反应化学方程式: 。
18.(6分)某镇硫酸厂排出的尾气中含有SO ,废水中含有HSO 。请回答:
2 2 4
(1)该镇经常下酸雨,酸雨的pH 5.6(填:>、<、=);
(2)请举二例酸雨的危害: 、 。
(3)用熟石灰处理该厂废水的化学方程式为: 。
(4)该厂的下列整治措施不妥的是 (填序号):
A.废气循环利用 B.将废气点燃后排放
C.废水用碱中和后排放 D.改进工艺,减少废气废水的产生
19.(7分)通过一年的化学学习,我们认识了“酸”和“碱”,请回答下列问题:
(1)常见的酸有硫酸、盐酸等,在它们的水溶液里由于存在有相同的 离子(填符号),因
此,它们有很多相似的化学性质,如: 、
……等(写二条即可)。
(2)碱有氢氧化钠、氢氧化钙等,氢氧化钠可作某些气体的干燥剂,如:干燥 等气体,氢氧化
钙可由生石灰与水反应制得,化学方程式为: 。
(3)大地震灾害发生后,为了灾区人民群众的饮用水安全,卫生防疫部门要经常对灾区水源进行
监测,获得可靠的科学依据。若现有一瓶水样,要获取它的酸碱度,应如何操作:
。
四、实验探究题(本大题共3小题,共20分)
20. (9分)实验室中可以除去粗盐中的可溶性杂质,这样就实现了粗盐的初步提纯,这个过程的
实验步骤是____________________、________________________、________________________、
______________________。在这四步中,每一步都需要用到的玻璃仪器是________________,
它在每一步中的作用分别是______________________、__________________________、
__________________________________、______________________________。
21.(7分)痕迹检验是公安机关提取犯罪嫌疑人指纹的一种重要方法,AgNO 显现就是其中一种。
3
其原理是:人的手上有汗渍,接触过白纸后,手指纹线就留在纸上。如果将AgNO 溶液小心地
3
涂到纸上,AgNO 就与汗渍中的NaCl反应,化学方程式为:NaCl+AgNO ====AgCl↓(白)
3 3
+NaNO ,光照后即可显示黑色指纹线。现对痕迹检验所用的AgNO 溶液进行质量分析时,不知
3 3
道加入的NaCl溶液与AgNO 溶液是否恰好完全反应,需设计实验方案进行探究,请你把下面
3
的实验方案补充完整。
探究步骤 可能观察到的现象 结论
(1)取反应后的上层清液于试管中,滴加 若有白色沉淀生成 _______________溶液过量
___________________溶液 若无白色沉淀生成 还需进行下一步探究
(2)另取反应后的上层清液于试管中,滴加
_________________溶液
22.(4分)用珍珠(主要成分CaCO )加工成的“珍珠粉”是一种名贵中药材、保健品,可近年来市
3
场上出现了一些假冒的“珍珠粉”,仅用肉眼观察难辨真假。为了向消费者提供鉴别方法,需
找出真假“珍珠粉”理化性质上的差异,工商局提供了真、假“珍珠粉”样品,请你展开探究:
(主要写出猜想、方案,不需要说出方案实施的具体结果)
猜想一:真、假“珍珠粉”的气味可能不同。
方案一:取样,分别闻一闻它们的气味,分辨气味有无差异。
猜想二:_____________________________________________________________________。
3方案二:_____________________________________________________________________。
猜想三:_____________________________________________________________________。
方案三:_____________________________________________________________________。
五、计算题(本大题包括1小题,共8分)
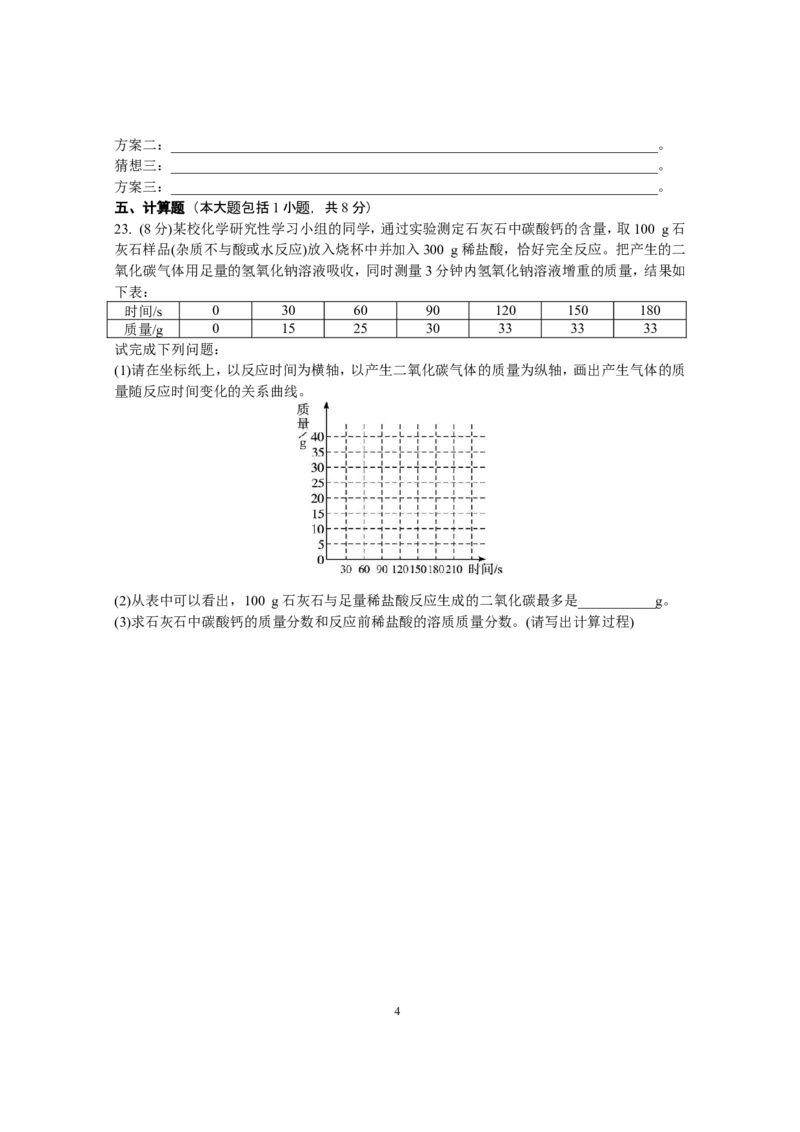
23. (8分)某校化学研究性学习小组的同学,通过实验测定石灰石中碳酸钙的含量,取100 g石
灰石样品(杂质不与酸或水反应)放入烧杯中并加入300 g稀盐酸,恰好完全反应。把产生的二
氧化碳气体用足量的氢氧化钠溶液吸收,同时测量3分钟内氢氧化钠溶液增重的质量,结果如
下表:
时间/s 0 30 60 90 120 150 180
质量/g 0 15 25 30 33 33 33
试完成下列问题:
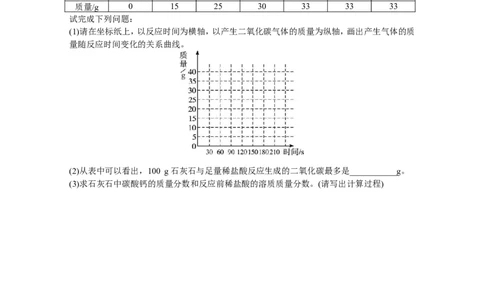
(1)请在坐标纸上,以反应时间为横轴,以产生二氧化碳气体的质量为纵轴,画出产生气体的质
量随反应时间变化的关系曲线。
(2)从表中可以看出,100 g石灰石与足量稀盐酸反应生成的二氧化碳最多是___________g。
(3)求石灰石中碳酸钙的质量分数和反应前稀盐酸的溶质质量分数。(请写出计算过程)
4