文档内容
亳州二中 2025-2026 学年第一学期第一次教学质量检测
高一化学试卷
(考试时间:75分钟 试卷满分:100分)
注意事项:
1.本试卷分第I卷(选择题)和第I卷(非选择题)两部分。答卷前,考生务必将自己的姓名、准
考证号填写在答题卡上。
2.回答第I卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需
改动,用橡皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.测试范围:第1章第一、二节物质的分类及转化、离子反应(人教版2019)。
可能用到的相对原子质量:O 16 N 14 S 32 K 39 Ba 137
一、选择题:本题共14个小题,每小题3分,共42分。每小题只有一个最佳选项。
1. 化学是在原子、分子水平上研究物质的组成、结构、性质及其应用的基础自然科学,下列说法错误的是
A. 在资源、材料、健康、环境等领域,化学都发挥着极其重要的作用
B. 学习化学需坚持实验和理论并重,有利于我们提升对物质及其变化的认识水平
C. 依据物质类别和元素价态,可以解释和预测物质的性质
D. 意大利科学家阿伏加德罗发现了元素周期律,使化学的研究变得有规律可循
2. 中国古籍《黄帝九鼎神丹经诀》记载了利用石胆( )来制取硫酸的过程。制取时
首先发生如下分解反应: ,该反应中没有涉及的物
质类别是
A. 盐 B. 酸性氧化物 C. 含氧酸 D. 碱性氧化物
3. 下列反应不属于四大基本反应类型的是
A. B.
C. D.
4. 下列说法中正确的是
①电解质本身一定能导电②能导电的物质一定是电解质
③酸一定含有氢元素
④碱性氧化物常温下一定可以和水反应生成相应的碱
A. ①②③ B. ②③④ C. ② D. ③
5. 意大利罗马大学的Fulvio Cacace等人获得了极具理论研究意义的N 分子。N 分子结构如图所示,下
4 4
列说法正确的是
A. N 的相对分子质量为28 B. N 与N 属于同种物质
4 4 2
C. N 属于一种新型化合物 D. N 与N 互为同素异形体
4 4 2
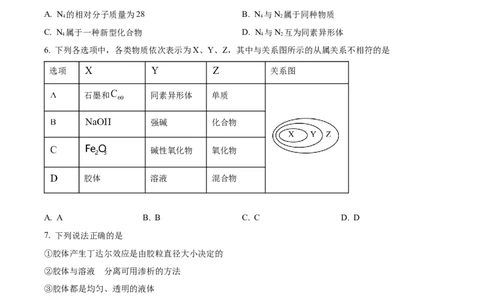
6. 下列各选项中,各类物质依次表示为X、Y、Z,其中与关系图所示的从属关系不相符的是
选项 关系图
石墨和 同素异形体 单质
强碱 化合物
碱性氧化物 氧化物
胶体 溶液 混合物
A. A B. B C. C D. D
7. 下列说法正确的是
①胶体产生丁达尔效应是由胶粒直径大小决定的
②胶体与溶液 的分离可用渗析的方法
③胶体都是均匀、透明的液体
④江河入海口处形成沙洲与胶体的性质有关
⑤胶体不稳定,静置后容易产生沉淀
A. ①②⑤ B. ①③④ C. ①②④ D. ②③④
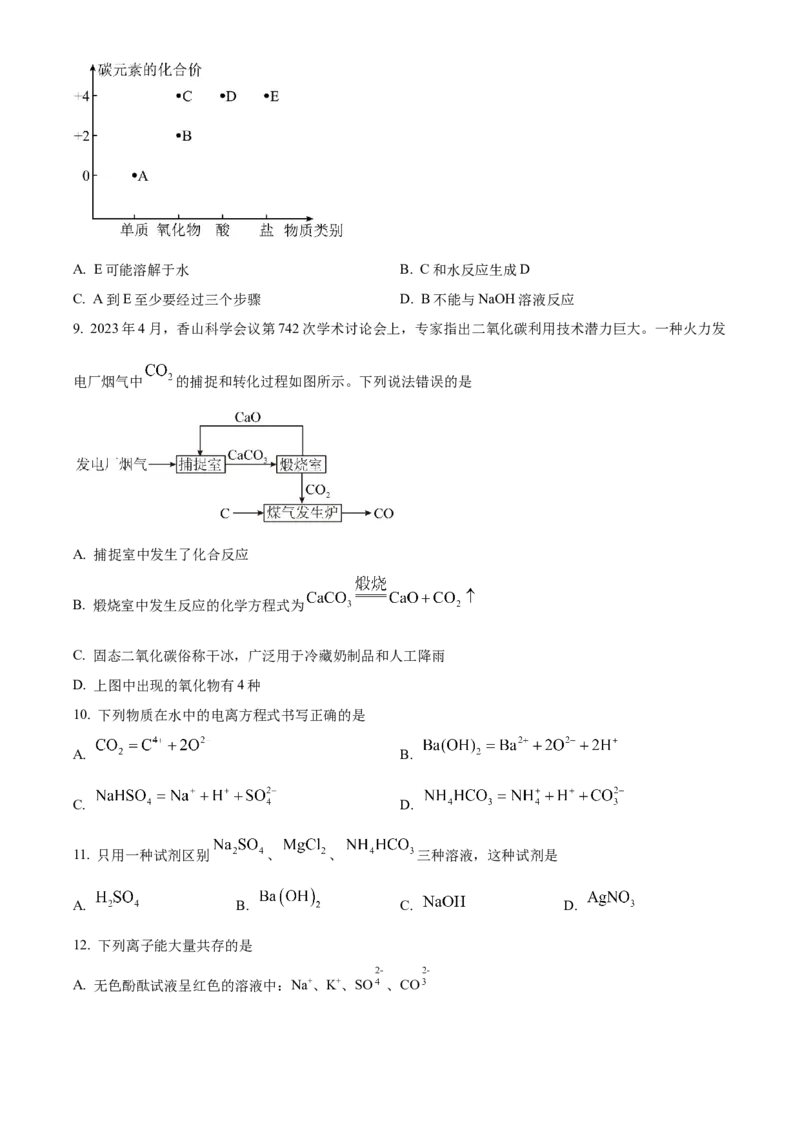
8. 如图是碳元素的价类二维图,A、B、C、D、E代表常见的含碳物质,下列说法错误的是A. E可能溶解于水 B. C和水反应生成D
C. A到E至少要经过三个步骤 D. B不能与NaOH溶液反应
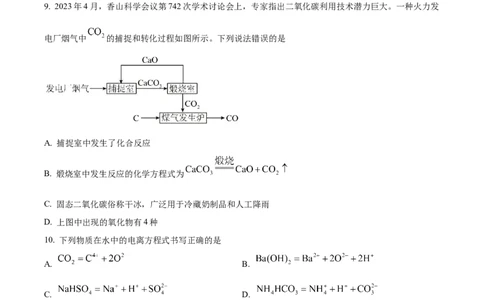
9. 2023年4月,香山科学会议第742次学术讨论会上,专家指出二氧化碳利用技术潜力巨大。一种火力发
电厂烟气中 的捕捉和转化过程如图所示。下列说法错误的是
A. 捕捉室中发生了化合反应
B. 煅烧室中发生反应的化学方程式为
C. 固态二氧化碳俗称干冰,广泛用于冷藏奶制品和人工降雨
D. 上图中出现的氧化物有4种
10. 下列物质在水中的电离方程式书写正确的是
A. B.
C. D.
11. 只用一种试剂区别 、 、 三种溶液,这种试剂是
A. B. C. D.
12. 下列离子能大量共存的是
A. 无色酚酞试液呈红色的溶液中:Na+、K+、SO 、COB. 无色透明的溶液中:Cu2+、K+、SO 、NO
C. 含有大量Ba(NO ) 的溶液中:Mg2+、NH 、SO 、Cl-
3 2
D. 紫色石蕊试液呈红色的溶液中:Ca2+、K+、HCO 、NO
的
13. 铁、稀盐酸、澄清石灰水、氯化铜溶液是初中化学中常见 物质,四种物质间的反应关系如图所示。
图中两圆相交部分(A、B、C、D)表示物质间的反应,其中对应反应的离子方程式书写正确的是
A. OH-+HCl=H O+Cl- B. Ca(OH) +Cu2+=Ca2++Cu(OH)
2 2 2
C. Fe+Cu2+=Cu+Fe2+ D. Fe+2H+=Fe3++H ↑
2
14. 不能用离子方程 CO +2H+=CO↑+HO表示的反应是
2 2
A. NaCO + 2HCl=2NaCl + CO↑+ HO B. NaHCO + HCl=NaCl + CO↑+ HO
2 3 2 2 3 2 2
C. KCO + HSO =KSO + CO↑+ HO D. KCO + 2HNO=2KNO + CO↑+ HO
2 3 2 4 2 4 2 2 2 3 3 3 2 2
二、非选择题(本题共包含4题,共58分)
15. 有下列物质:①碳酸 ②稀硫酸 ③氢氧化钡固体 ④二氧化硫 ⑤熔融氯化钠 ⑥铁片 ⑦纯碱。
请用序号填空:
(1)属于酸的是_______。
(2)属于碱的是_______。
(3)属于盐的是_______。
的
(4)属于电解质 是_______。
(5)上述状态下能导电的是_______。
(6)属于非电解质的是_______。
16. 某课外活动小组进行 胶体的制备实验并检验其性质。
(1)在小烧杯中加入20mL 蒸馏水,加热至沸腾后,向沸水中滴入几滴饱和 溶液,继续煮沸至溶
液呈红褐色,停止加热,即制得 胶体。写出该反应的化学方程式_______。(2)将制得的胶体放入半透膜制成的袋内,如图所示,放置一段时间后,取少量半透膜外的液体于试管
中,置于暗处,用一束强光从侧面照射,观察_______(填“有”或“无”)丁达尔现象。
(3)向制得的 胶体滴加硫酸溶液,现象是_______; 与硫酸反应的离子方程式为
_______。
(4)明胶是水溶性蛋白质混合物,溶与水形成胶体。明胶水溶液和氢氧化铁胶体共同具备的性质是
_______。
A. 都不能稳定存在 B. 通电,无明显现象
.
C 分散质粒子可通过滤纸 D. 分散质粒径均大于 100nm
(5)下列现象或应用,不能运用胶体知识解释的是_______。
A. 用石膏或盐卤点制豆腐
B. 江河入海口,容易形成三角洲
C. 硝酸银溶液与溴化钠溶液混合,生成淡黄色沉淀
D. 一支钢笔使用两种不同的蓝黑墨水(墨水是胶体),易出现堵塞
17. I、写出下列电离方程式或离子反应方程式:
(1) 溶液_______。
(2) 溶液_______。
(3) _______。
(4)澄清石灰水和硝酸反应:_______。
Ⅱ、有一瓶澄清的无色溶液,其中可能含有 、 、 、 、 、 、 、 。
取该溶液进行以下实验:
(5)由题干信息可知原溶液中一定不存在_______(填离子符号,下同)。
(6)用 试纸检验该溶液,呈强酸性,则可证明原溶液中存在_______,同时可以排除原溶液中一定不
存在_______。
(7)取部分原溶液滴加过量的 溶液,产生白色沉淀,则可证明原溶液中存在_______。(8)取少量(3)反应后的溶液,滴加 溶液,有白色沉淀生成,证明原溶液中存在_______,可以排
除原溶液中一定不存在_______。
18. 探究电解质在水溶液中反应的实质
实验
操作
实验 随 溶液 的滴入,电导率①_______,同时溶液中
现象 出现②_______,溶液颜色③_______
稀硫酸与 溶液反应的实质是溶液中的
④_______结合生成水、 和 结合生成
解释
⑤_______沉淀,溶液中离子的浓度⑥_______;随着稀
硫酸的继续加入,溶液中离子浓度升高。写出稀硫酸与
溶液反应的离子方程式:⑦_______。