文档内容
2021 学年第二学期九年级化学阶段检测试题
一、选择题
相对原子质量:H-1 C-12 N-14 O-16 S-32 Cl-35.5
Na-23 Ca-40
1. 空气中,含量最多的气体是
A. 氧气 B. 氮气 C. 二氧化碳 D. 水蒸气
2. 属于化学变化的是
A. 玻璃破碎 B. 水果榨汁 C. 滴水成冰 D. 木柴燃烧
3. 不属于碳元素的同素异形体的是
A. 金刚石 B. 石墨 C. 碳60 D. 一氧化碳
4. 属于纯净物的是
A. 空气 B. 加碘食盐 C. 蒸馏水 D. 泥水
5. 物质加入水中不能形成溶液的是
A. 味精 B. 食盐 C. 白糖 D. 芝麻油
6. 物质在氧气中燃烧的现象与事实不相符的是
A. 铁丝:火星四射 B. 木炭:白光
C. 硫粉:淡蓝色火焰 D. 甲烷:蓝色火焰
7. 物质俗名正确的是
A. 氢氧化钠:食盐 B. 氯化钠:烧碱 C. 氧化钙:熟石灰 D. 碳酸钠:纯碱
8. 物质用途错误的是
A. 干冰:作制冷剂 B. 稀有气体:作电光源 C. 金刚石:作电极 D. 氢气:作燃料
9. 下列各图中 和 分别表示不同元素 的原子,其中表示混合物的
A. B. C. D.
10. 实验室用草酸(HC O)制取CO的化学方程式为 ,其中X的化学式为
2 2 4
( )
A. H O B. HO C. CH D. H
2 2 2 4 2
11. 化学方程式书写正确且属于复分解反应的是
A. B.C. D.
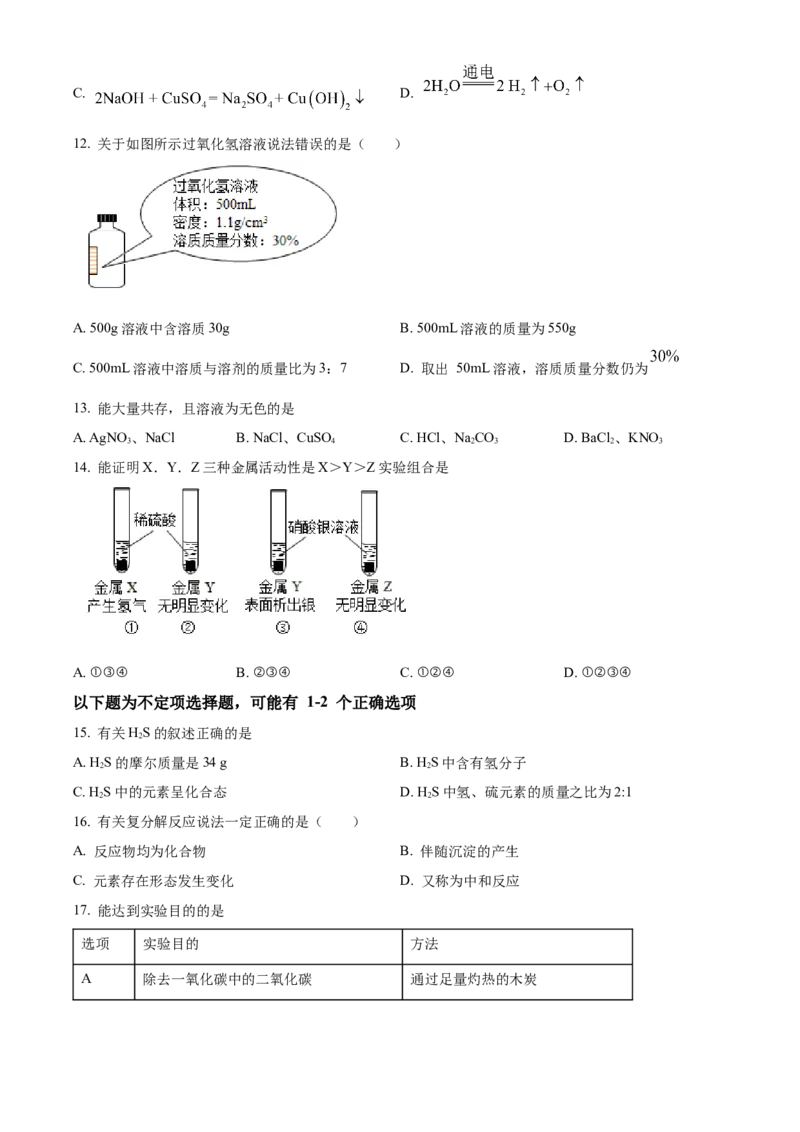
12. 关于如图所示过氧化氢溶液说法错误的是( )
A. 500g溶液中含溶质30g B. 500mL溶液的质量为550g
C. 500mL溶液中溶质与溶剂的质量比为3:7 D. 取出 50mL溶液,溶质质量分数仍为
13. 能大量共存,且溶液为无色的是
A. AgNO 、NaCl B. NaCl、CuSO C. HCl、NaCO D. BaCl 、KNO
3 4 2 3 2 3
14. 能证明X.Y.Z三种金属活动性是X>Y>Z实验组合是
A. ①③④ B. ②③④ C. ①②④ D. ①②③④
以下题为不定项选择题,可能有 1-2 个正确选项
15. 有关HS的叙述正确的是
2
A. H S的摩尔质量是34 g B. HS中含有氢分子
2 2
C. HS中的元素呈化合态 D. H S中氢、硫元素的质量之比为2:1
2 2
16. 有关复分解反应说法一定正确的是( )
A. 反应物均为化合物 B. 伴随沉淀的产生
C. 元素存在形态发生变化 D. 又称为中和反应
17. 能达到实验目的的是
选项 实验目的 方法
A 除去一氧化碳中的二氧化碳 通过足量灼热的木炭B 除去氯化钠中的碳酸钠 加入过量的稀盐酸,蒸发
C 洗去试管壁上附着的铜 加入稀硫酸
D 检验硫酸钠中是否含有氯化钠 滴加硝酸酸化的硝酸银
A. A B. B C. C D. D
二、简答题(30 分)
18. 生活垃圾分类事关绿色可持续发展 。可回收垃圾包括纸张、金属、塑料等。
(1)某种易拉罐的材质中含有铝。铝的金属活动性 _____(选填“>”“<”)铁。氧化铝中铝元素的化合价
为_______。以下垃圾属于金属的是_________(选填编号)。
.
A 厨余垃圾 B.铜导线 C.过期药品 D.废弃衣物
(2)生物全降解餐盒主要以淀粉为原料,可减少对环境的影响。淀粉属于_____(选填“有机”“无 机”)物,
淀粉可转化为葡萄糖(C H O)。葡萄糖含有_______种元素,每摩尔葡萄糖分子中含______摩尔碳原子,
6 12 6
葡萄糖的中碳元素与氧元素的质量比为_____。
19. KCl 有着广泛的用途。
①农业生产中 KCl 可用作 ______ (选填“钾”“氮”或“磷”)肥。
②对 KCl 溶液进行焰色反应,透过蓝色钴玻璃片,火焰呈 ______ 色。
③固体物质的溶解度与溶解性的关系下表所示。
20℃时溶解度(g/100g
>10 1~10 0.01~1 <0.01
水)
溶解性 易溶 可溶 微溶 难溶
20℃时,KCl 属于 ______ 溶物质。
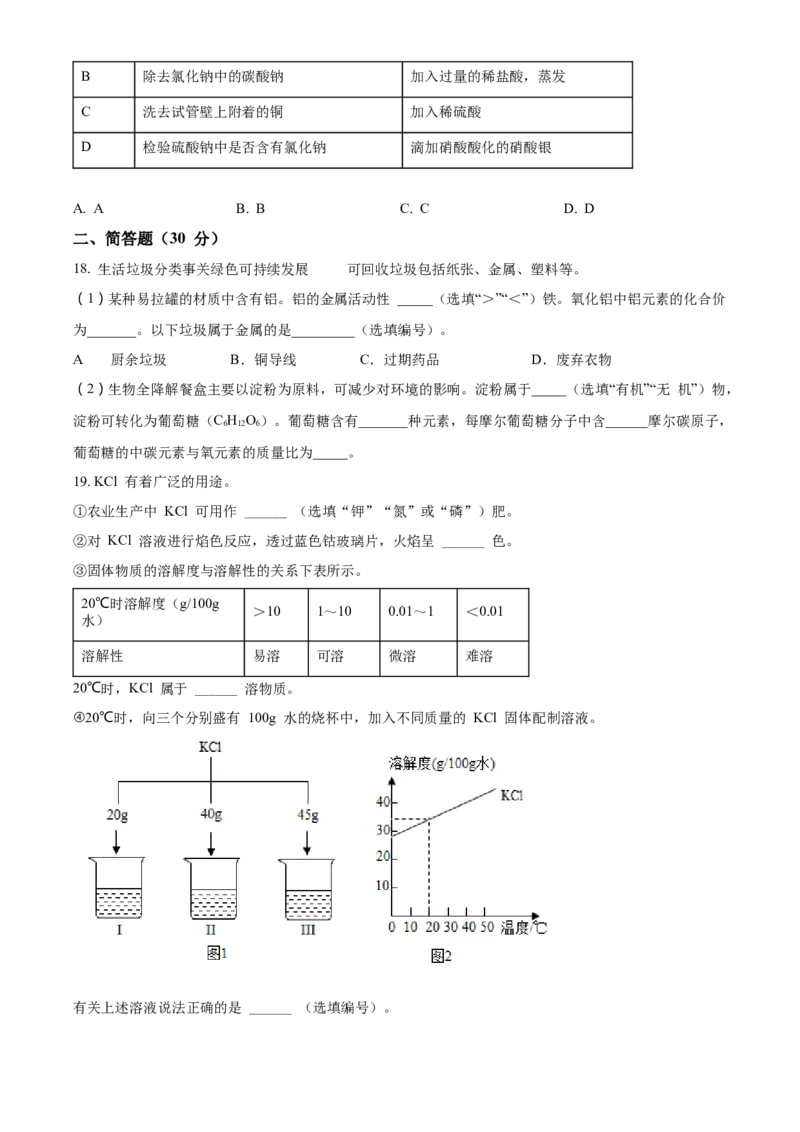
④20℃时,向三个分别盛有 100g 水的烧杯中,加入不同质量的 KCl 固体配制溶液。
有关上述溶液说法正确的是 ______ (选填编号)。a.I 中溶质质量分数为 20% b.I 升温至 40℃,溶质质量不变
c.II 和 III 中溶质质量相等 d.III 降温至 10℃,析出固体 45g
⑤写出鉴别 KCl 溶液和 KSO 溶液的一种方法 ______ 。
2 4
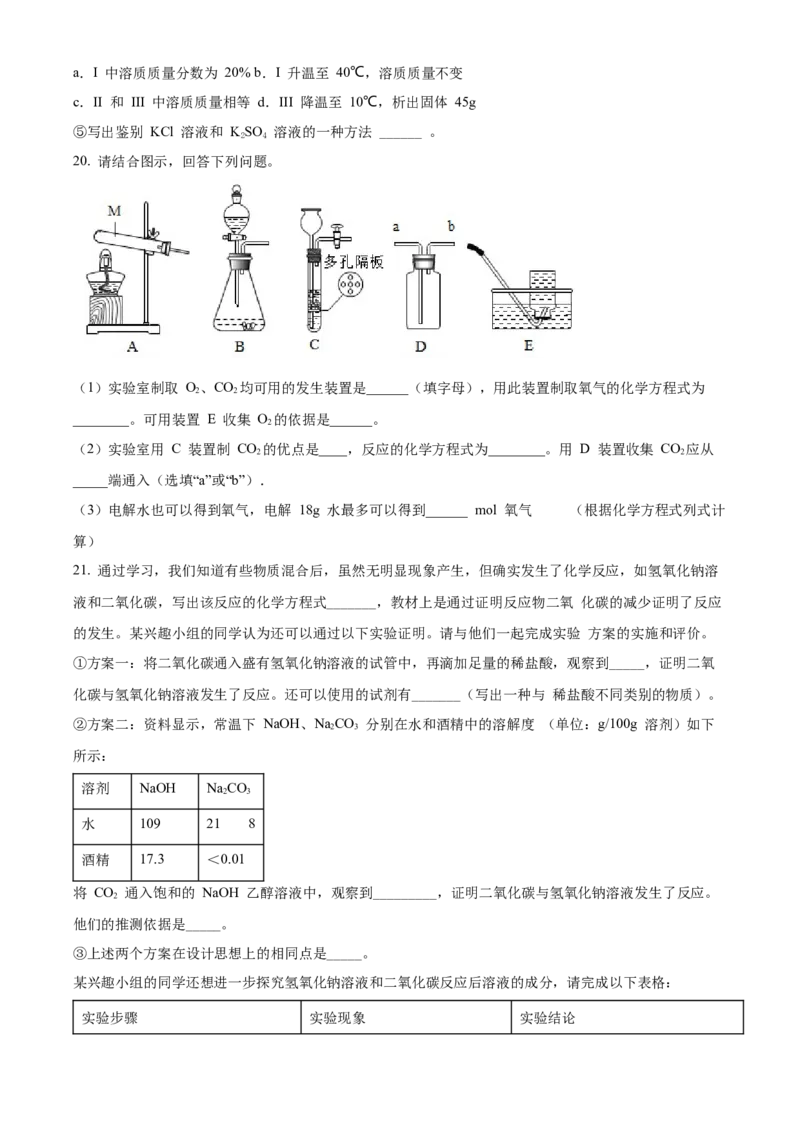
20. 请结合图示,回答下列问题。
(1)实验室制取 O、CO 均可用的发生装置是______(填字母),用此装置制取氧气的化学方程式为
2 2
________。可用装置 E 收集 O 的依据是______。
2
(2)实验室用 C 装置制 CO 的优点是____,反应的化学方程式为________。用 D 装置收集 CO 应从
2 2
_____端通入(选填“a”或“b”).
(3)电解水也可以得到氧气,电解 18g 水最多可以得到______ mol 氧气 。(根据化学方程式列式计
算)
21. 通过学习,我们知道有些物质混合后,虽然无明显现象产生,但确实发生了化学反应,如氢氧化钠溶
液和二氧化碳,写出该反应的化学方程式_______,教材上是通过证明反应物二氧 化碳的减少证明了反应
的发生。某兴趣小组的同学认为还可以通过以下实验证明。请与他们一起完成实验 方案的实施和评价。
①方案一:将二氧化碳通入盛有氢氧化钠溶液的试管中,再滴加足量的稀盐酸,观察到_____,证明二氧
化碳与氢氧化钠溶液发生了反应。还可以使用的试剂有_______(写出一种与 稀盐酸不同类别的物质)。
②方案二:资料显示,常温下 NaOH、NaCO 分别在水和酒精中的溶解度 (单位:g/100g 溶剂)如下
2 3
所示:
溶剂 NaOH NaCO
2 3
.
水 109 21 8
酒精 17.3 <0.01
将 CO 通入饱和的 NaOH 乙醇溶液中,观察到_________,证明二氧化碳与氢氧化钠溶液发生了反应。
2
他们的推测依据是_____。
③上述两个方案在设计思想上的相同点是_____。
某兴趣小组的同学还想进一步探究氢氧化钠溶液和二氧化碳反应后溶液的成分,请完成以下表格:
实验步骤 实验现象 实验结论步骤一:取少量样品,滴加_____ 产生白色沉淀
溶质成分为碳酸钠和氢氧化钠
步骤二:在上步反应后的溶 液中
______
继续滴加______