文档内容
独山中学2025-2026学年度第一学期高一化学10月月考试卷
考试时间:75分钟
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
第I卷(选择题)
一、单选题(共42分)
1.(本题3分)向一定量下列物质的溶液中逐滴加入氢氧化钠溶液,先生成白色沉淀,后
沉淀逐渐溶解,这种物质是( )
A.硫酸镁 B.四羟基合铝酸钠 C.氯化铝 D.氯化铁
2.(本题3分)下列物质属于纯净物的是
A.柠檬水 B.泥水 C.盐酸 D.液态氧
3.(本题3分)下列对各组物质所属类别的判断中正确的是
选项 物质 物质类别
A KOH、Ba(OH) 、Ca(OH) 、Cu(OH) 强碱
2 2 2
B 盐酸、Fe(OH) 胶体、蛋白质溶液 混合物
3
C NaHCO 、NaHSO、HCO、KHSO 酸式盐
3 4 2 3 3
D CO、CO、SO 、MnO 酸性氧化物
2 2 2 7
A.A B.B C.C D.D
4.(本题3分)甲、乙、丙、丁四位同学分别进行实验,测定四份不同澄清溶液的成分,
记录如下:
甲 BaCl 、NH NO 、KSO
2 4 3 2 4
乙 NaCl、Ca(OH) 、KSO
2 2 3
丙 HCl、NaCO、NaCl
2 3
丁 KCl、KSO 、NaNO
2 4 3
其中记录合理的是
A.甲 B.乙 C.丙 D.丁
5.(本题3分)下列叙述中正确的是A.含有一种元素的物质是纯净物
B.根据分散系的稳定性大小将混合物分为胶体、溶液和浊液
C.根据是否具有丁达尔效应,将分散系分为溶液、浊液和胶体
D.胶体、分散系、混合物概念间的从属关系可用上图表示
6.(本题3分)一定条件下硝酸铵受热分解的化学方程式为:5NH NO 2HNO+4N↑+
4 3 3 2
9HO,在反应中还原产物与氧化产物的质量之比为( )
2
A.5∶3 B.5∶4 C.1∶1 D.3∶5
7.(本题3分)钛(Ti)被称为继铁、铝之后的第三金属,以 制取Ti的主要反应有:①
② ,下列说法不正确的是
A. 是中间产物 B.反应①中 是还原产物
C.反应①②都是置换反应 D.反应②中Mg有还原性
8.(本题3分)25℃时,下列各组离子在指定溶液中一定能大量共存的是
A.氯化钡溶液中:K+、Cu2+、 、
B.使酚酞变红的溶液中: 、Na+、 、H+
C.无色透明的溶液中:Cu2+、Al3+、 、
D.0.1mol/LNaCl溶液中:Fe2+、 、Cl-、
9.(本题3分)《本草图经》记载,中药矾红(又称煅绿矾)具有燥湿化痰、止血补血、解
毒敛疮之功效。其炮制过程如下:将绿矾(主要成分为FeSO ∙7H O)剔除杂质,和米醋同放
4 2
在砂锅内混合均匀,置于炭炉上小火加热至绿矾完全溶解,用竹片搅拌,炒至固体干燥呈
绦色(略浅于红棕色)为止,取出放冷即成。下列有关说法错误的是
试卷第2页,共6页A.米醋的作用是防止溶解时产生沉淀阻碍绿矾的溶解
B.用绿矾炮制矾红时,O 与HO均参与了过程中发生的化学反应
2 2
C.将矾红加入水中充分搅拌,静置后向上层清液中加入数滴KSCN溶液,无明显现象
D.胃酸分泌过少、消化能力较弱的人应慎用矾红
10.(本题3分)下列反应不属于四大基本反应类型的是:
A.氢气在氧气中点燃 B.碳酸钙与盐酸反应
C.加热高锰酸钾制氧气 D.一氧化碳还原氧化铜
11.(本题3分)下列离子方程式不正确的是
A. 溶液中加入过量的氨水:
B. 溶液中通入少量
C. 和HI的反应:
D.澄清石灰水与过量二氧化碳气体反应:
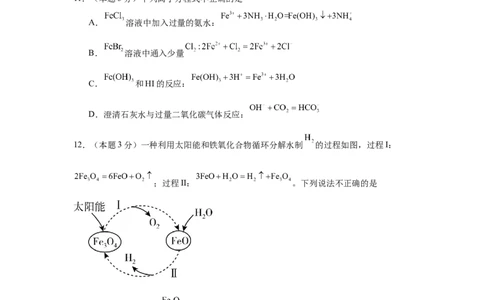
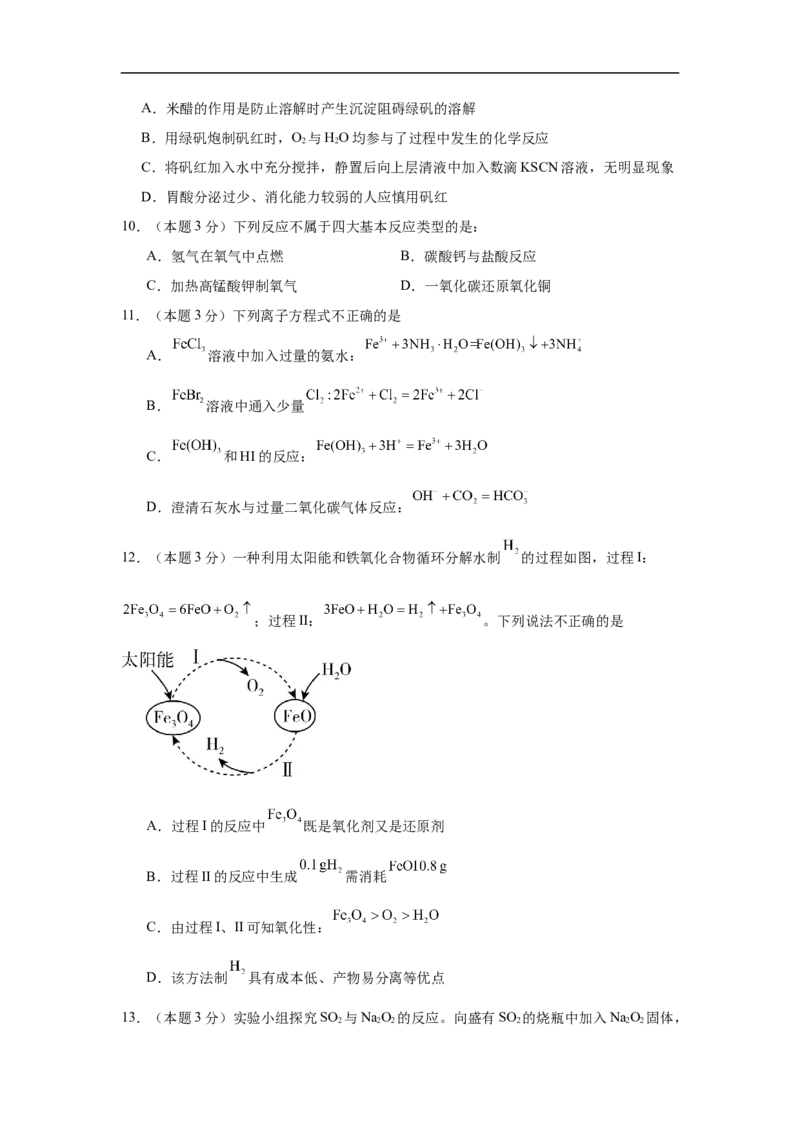
12.(本题3分)一种利用太阳能和铁氧化合物循环分解水制 的过程如图,过程I:
;过程II: 。下列说法不正确的是
A.过程I的反应中 既是氧化剂又是还原剂
B.过程II的反应中生成 需消耗
C.由过程I、II可知氧化性:
D.该方法制 具有成本低、产物易分离等优点
13.(本题3分)实验小组探究SO 与NaO 的反应。向盛有SO 的烧瓶中加入NaO 固体,
2 2 2 2 2 2测得反应体系中O 含量的变化如图。
2
下列说法不正确的是
A.有O 生成推测发生了反应:2NaO + 2SO = 2Na SO + O
2 2 2 2 2 3 2
B.bc段O 含量下降与反应O + 2Na SO = 2Na SO 有关
2 2 2 3 2 4
C.c点剩余固体中含有NaSO
2 3
D.实验过程中NaO 仅体现氧化性
2 2
14.(本题3分)南宋著名法医学家宋慈的《洗冤集录》中有“银针验毒”的记载;“银
针验毒”的原理为4Ag +2H S + O = 2X +2H O。下列说法正确的是( )
2 2 2
A.X的化学式为AgS B.银针验毒时,O 失去电子
2
C.反应中Ag和HS均发生氧化反应 D.每生成1个X,反应转移2e-
2
第II卷(非选择题)
二、填空题(共58分)
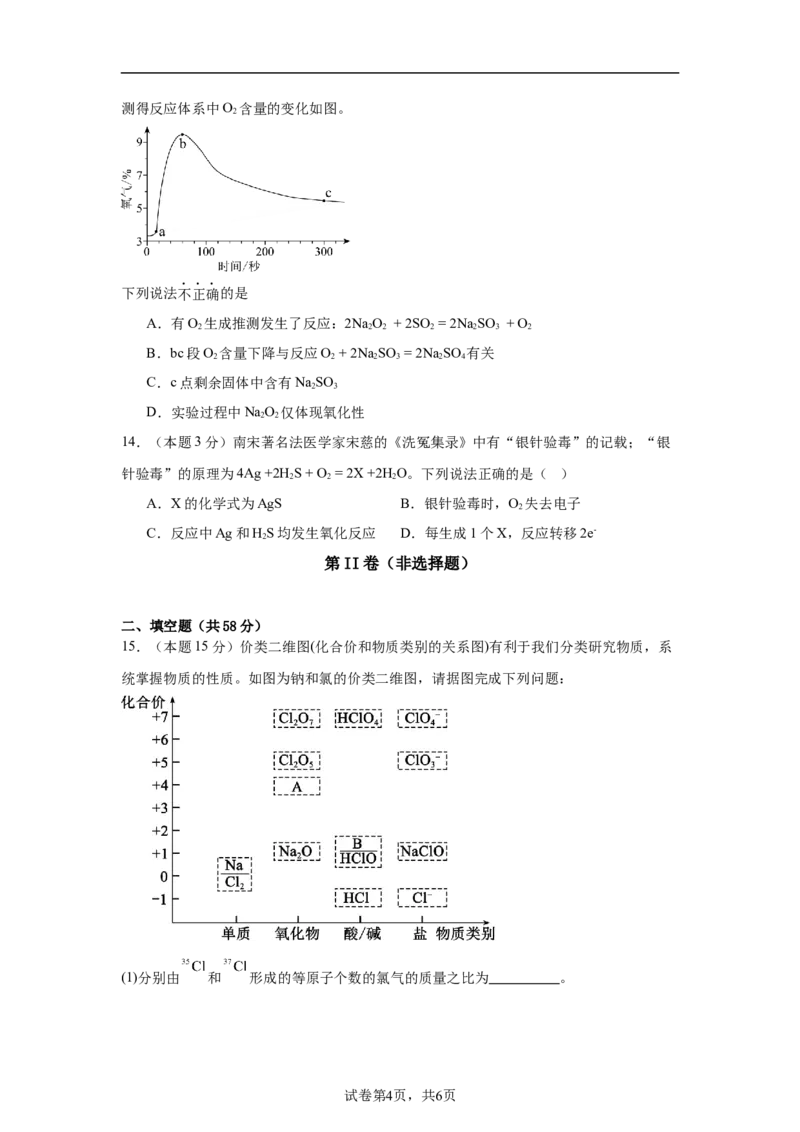
15.(本题15分)价类二维图(化合价和物质类别的关系图)有利于我们分类研究物质,系
统掌握物质的性质。如图为钠和氯的价类二维图,请据图完成下列问题:
(1)分别由 和 形成的等原子个数的氯气的质量之比为 。
试卷第4页,共6页(2) 属于 (填“酸性”或“碱性”)氧化物,与 相遇会生成
(填化学式)。
(3) A、B两处分别对应的物质是 、 。(填化学式)
(4)A可用于自来水消毒,是因为该物质具有 性,与氯气相比,其用于消毒的优
点有 。
(5)将 和 按一定比例混合后,用稀硫酸酸化,能够生成一种刺激性气味的气体,
写出该反应的离子方程式 。
(6)研究发现, 具有漂白性是因为 不稳定,会分解释放出活性氧原子 ,
具有很强的氧化性,可将部分有颜色的物质氧化成无色(或白色)物质,则下列与 性质相
似的物质是 。(填序号)
① ② ③活性炭
16.(本题17分)现有下列六种物质:①液态氯化氢;②二氧化碳;③硫酸铜溶液;④氢
氧化铁胶体; ⑤KOH固体;⑥铁丝。
(1)上述六种物质中,属于电解质的有 (填序号,下同),属于非电解质的有 ,
上述状态下能导电的有 。
(2)区分③和④的简单方法是 。
(3)氯化氢在水溶液中的电离方程式为 。
(4)③和⑥反应的基本反应类型为 ,其离子方程式为 。
(5)向③中加入⑤的水溶液的现象为 。
(6)Cl 与⑤可能会发生如下反应,配平该方程式,并用双线桥标出电子得失: 。
2
_______ _______ _______ _______ _______ 。
17.(本题14分)在抗击新冠肺炎疫情的战役中,病毒在不断发生变异,现有疫苗对变异
病毒的有效性有待进一步的验证,因此民众的防疫意识不能松懈。
(1)口罩作为基础防疫物资,可以有效防止飞沫的传播。最新的研究表明新冠病毒可能通过
气溶胶传播。气溶胶属于 (填“胶体”或“溶液”);常利用 区分溶液和胶
体。(2)为有效防止新冠病海的传播,除了戴口罩,还需加强对隔离场所的消毒。常用的消毒剂
有双氧水、医用酒精以及含氯消毒剂。其中含氯消毒剂的家族最庞大、应用最广泛。实验
室制备Cl 有三种常用方法:
2
a.MnO +4HCl(浓) MnCl +2H O+Cl ↑
2 2 2 2
b.2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O
4 2 2 2
c.KClO +6HCl(浓)=KCl+3Cl ↑+3H O
3 2 2
①写出反应a的离子方程式 ,氧化剂与还原剂的化学计量数之比为 。
②反应b中,还原产物是 ,每生成1个Cl 转移的电子数为 。
2
③反应c中氧化产物与还原产物的质量之比为 。
④当三个反应中得到等质量的Cl 时,消耗HCl的质量最多的是 反应 (填
2
“a”、“b”、“c”)。
18.(本题12分)近年来我国储氢碳纳米管研究获得重大进展,电弧法合成碳纳米管常伴
有大量物质——碳纳米颗粒,这种碳纳米颗粒可用氧化气化法提纯,其反应的化学方程式
为___________C+___________ ___________ (稀)=___________
___________ ___________ 。
(1)完成并配平上述反应的化学方程式。
(2)此反应的氧化剂是 ,还原剂是 。
(3)硫酸在上述反应中表现出的性质是___________(填字母序号)。
A.酸性 B.氧化性 C.吸水性 D.还原性
(4)该反应中转移的电子数为 。
试卷第6页,共6页《2025-2026学年度高中化学期中考试卷》参考答案
题号 1 2 3 4 5 6 7 8 9 10
答案 C D B D D D C D C D
题号 11 12 13 14
答案 C C D D
1.C
【详解】A、MgSO 和NaOH反应产生的Mg(OH) 白色沉淀不溶于NaOH溶液,A错误;
4 2
B、四羟基合铝酸钠不和NaOH溶液反应,不会产生白色沉淀,B错误;
C、AlCl 和NaOH反应产生的Al(OH) 白色沉淀能溶于NaOH溶液,C正确;
3 3
D、FeCl 和NaOH反应产生的Fe(OH) 呈红棕色,且该沉淀不溶于NaOH溶液,D错误;
3 3
故选C。
2.D
【详解】纯净物由单一成分组成。柠檬水、盐酸均为不同物质混合的溶液,泥水是不同物
质混合的悬浊液,属于混合物;液态氧仅含液态氧(O),成分单一,是纯净物;
2
答案选D。
3.B
【详解】A.Cu(OH) 不能完全电离出OH-,属于弱碱,A错误;
2
B.盐酸由HCl和水形成、Fe(OH) 胶体含Fe(OH) 和水、蛋白质溶液含蛋白质和水,都是
3 3
由两种物质形成,都属于混合物,B正确;
C.HCO 电离的阳离子全部是H+,属于酸,不属于酸式盐,C错误;
2 3
D.CO不能与水反应,也不能与碱液反应,不属于酸性氧化物,D错误;
故选B。
4.D
【详解】A. 甲会形成BaSO 沉淀而不能共存,故A错误;
4
B. 乙会形成CaSO 沉淀而不能共存,故B错误;
3
C. 丙会产生CO 气体而不能共存,故C错误;
2
D. 丁的各物质彼此不会反应,可以共存,故D正确;
故选D。
5.D
【详解】A.含有一种元素的物质可能是混合物,如O 和O 的混合气体,故A错误;
2 3
B.胶体区别于其他分散系的本质特征是分散质粒子直径的大小不同,根据分散质粒子直
径大小来分类,故B错误;
C.胶体区别于其他分散系的本质特征是分散质粒子直径的大小不同,根据分散质粒子直径大小来分类,故C错误;
D.分散系是混合物的一种,所以混合物包括分散系,胶体是分散系的一种,分散系包括
胶体,故D正确;
故选D。
6.D
【详解】NH NO 中NH +中N元素的化合价为-3价、NO -中N元素的化合价为+5价,反应
4 3 4 3
中N元素化合价由−3价、+5价变为0价,则氮气既是氧化产物也是还原产物,转移电子个
数是15,根据转移电子守恒知,生成的氮气中有 的是氧化产物,有 的是还原产物,所
以还原产物与氧化产物的质量之比为 : =3:5,故答案选D。
7.C
【详解】A.由方程式可知,四氯化钛是反应①的生成物、反应②的反应物,则四氯化钛
是制取钛的中间产物,故A正确;
B.由方程式可知,反应①中氯元素化合价降低被还原,则氯气是反应的氧化剂,四氯化
钛是反应的还原剂,故B正确;
C.由方程式可知,反应①有单质参加,但没有单质生成,不属于置换反应,故C错误;
D.由方程式可知,反应②中镁元素的化合价升高被氧化,镁是反应的还原剂,表现还原
性,故D正确;
故选C。
8.D
【详解】A.Ba2+、 反应生成沉淀,不可以共存,A错误;
B.使酚酞变红的溶液显碱性,OH-、H+反应生成水,不能共存,B错误;
C.含铜离子的溶液显蓝色,不能共存,C错误;
D.0.1mol/LNaCl溶液中:Fe2+、 、Cl-、 各离子不反应,能共存,D正确;
故选D。
9.C
【详解】A.米醋抑制亚铁离子水解,防止溶解时产生的Fe(OH) 以及后续氧化产生的
2
Fe(OH) 包夹绿矾,阻碍其溶解,A正确;
3
答案第2页,共8页B.炮制绿矾时,Fe2+可被氧化为Fe3+,且二者均能发生水解反应,在氧化反应过程中O 与
2
HO均参与了过程中发生的化学反应,B正确;
2
C.根据物料守恒,矾红中有一定量的Fe (SO ) 生成,因而上清液中加入KSCN会呈现红
2 4 3
色,C错误;
D.矾红中Fe O 本身能与胃酸即盐酸发生反应消耗胃酸,服食后可使胃酸进一步减少,影
2 3
响消化能力,D正确;
故合理选项是C。
10.D
【详解】A.氢气在氧气中点燃生成水,为化合反应,故A正确;
B.碳酸钙与盐酸反应生成氯化钙、水、二氧化碳,为复分解反应,故B正确;
C.加热高锰酸钾制氧气,生成锰酸钾、二氧化锰、氧气,为分解反应,故C正确;
D.CO与CuO反应生成Cu和二氧化碳,不符合置换反应的条件,不属于四种基本反应类
型,故D错误;
故选D。
【点睛】解答本题要充分理解反应类型的分类方法方面的知识,只有这样才能对各种反应
类型做出正确的判断。化合反应是指由两种或两种以上物质反应生成一种物质的反应。分
解反应是指由一种物质生成两种或两种以上物质的反应。置换反应是指由一种单质和一种
化合物反应,生成另外一种单质和一种化合物的反应。复分解反应是指由两种化合物反应,
生成另外两种化合物的反应。
11.C
【详解】A.FeCl 溶液中加入过量的氨水生成氢氧化铁沉淀和氯化铵,离子方程式正确,
3
故A正确;
B.FeBr 溶液中通入少量Cl,亚铁离子反应生成铁离子,B正确;
2 2
C.Fe(OH) 和HI发生氧化还原反应 ,C错误;
3
D.澄清石灰水与过量二氧化碳气体反应生成碳酸氢钙,离子方程式正确,D正确;
答案选C。
12.C
【分析】根据图像分析可知,反应物是水,产物是氢气和氧气。
【详解】A.反应过程中, 中铁元素化合价降低,氧元素化合价升高, 既是氧化剂又是还原剂,A正确;
B.根据题中方程式可以列式计算,设需要氧化亚铁 克, ,生成 需
消耗 ,B正确;
C.过程 中 是氧化剂, 是氧化产物,氧化性 ,无法通过过程 判断氧
气和水的氧化性强弱,C错误;
D.该方法只需要太阳能提供能量,所以制 具有成本低、 产物易分离等优点,D正确;
故选C。
13.D
【详解】A.起始阶段有 大量产生,说明 与 发生了反应并生成了 ,则反应
的方程式为: ,A正确;
B.bc段 含量下降,说明有物质在消耗 ,根据容器内物质的成分可知,可能是生成的
继续与 反应导致的,反应的方程式为: ,B正确;
C.根据前面的信息, 与 发生总反应为: ,在c点时,氧
气含量还在减小,说明反应 还在发生,则c点剩余固体中还含有
,C正确;
D.根据反应 可知 既体现了氧化性,被还原为 ,
又体现了还原性,被氧化为 ,D错误;
故答案为:D。
答案第4页,共8页14.D
【详解】A. 由质量守恒可知X的化学式为Ag S,故A错误;
2
B. 银针验毒时,空气中氧气分子得到电子,化合价从反应前的0价变为反应后的-2
价,化合价降低,做氧化剂,故B错误;
C. 在反应中Ag的化合价从单质的0价变为反应后中的+1价,失去电子,作还原剂;
HS中的H、S两元素的化合价都没有发生变化,既不是氧化剂也不是还原剂,故C错误;
2
由方程式:4Ag +2H S + O = 2X +2H O可知,,则每生成1molAg S,反应转移
2 2 2 2
2mol e-,故D正确;
故选D。
15.(1)
(2) 碱性
(3)
(4) (强)氧化 高效、安全、无异味
(5)
(6)②
【详解】(1) 的相对原子质量是35, 的相对原子质量是37,分别由 和
形成的等原子个数的氯气的质量之比为35:37;
(2) 能与元素反应生成氯化钠和水, 属于碱性氧化物; 是酸性氧化物,
与 相遇会生成 。
(3)A是+4价氧化物,Na没有+4价,A是氯的+4价氧化物,A是 ,B是碱,B表示
;
(4)A处是高价态氯的氧化物,该物质具有强氧化性,与氯气相比,相同质量的该物质被
还原时,能得到更多的电子,氧化能力更强,消毒能力大大增加;同时更安全:不会产生
对人体有害的有机氯化物,排除了氯气本身的毒性,也减少了消毒时残留的氯气的气味。
(5)在酸性条件下,Cl-、 发生归中反应生成氯气,该反应的离子方程式为;
(6)根据题意,物质不稳定,且分解时能产生氧气,故选②。
16.(1) ①⑤ ② ③④⑥
(2)丁达尔效应
(3)HCl=H++Cl-
(4) 置换反应 Fe+Cu2+=Fe2++Cu
(5)溶液中出现蓝色絮状沉淀
(6)
【详解】(1)①液态氯化氢是共价化合物,由HCl分子构成,无自由移动的离子,因此
不能导电;在水溶液中能够发生电离而导电,因此属于电解质;
②二氧化碳是共价化合物,由CO 分子构成,无自由移动的离子,因此不能导电;在水溶
2
液中及熔融状态下都不能因自身发生电离而导电,因此属于非电解质;
③硫酸铜溶液中含有自由移动的离子,因此能够导电;该物质是混合物,因此既不属于电
解质,也不属于非电解质;
④氢氧化铁胶体中含有能够自由的带电荷的微粒,因此能够导电;氢氧化铁胶体是混合物,
因此既不属于电解质,也不属于非电解质;
⑤KOH固体是离子化合物,其中的离子不能自由移动,因此不能导电;该物质在水溶液中
和熔融状态下能够导电,因此属于电解质;
⑥铁丝中含有自由移动的电子,因此能够导电;铁丝属于单质,不是化合物,因此既不属
于电解质,也不属于非电解质;
综上所述可知:上述物质中属于电解质的有①⑤;属于非电解质的有②;上述状态下能导
电的有③④⑥;
(2)③是硫酸铜溶液,④是氢氧化铁胶体,胶体能够使光线发生散射作用而沿直线传播,
用光照射时会发生丁达尔效应,而溶液不能产生丁达尔效应,故区分二者的简单方法是利
用丁达尔效应;
(3)HCl溶于水,电离产生H+、Cl-,因此其电离方程式为:HCl=H++Cl-;
(4)③是硫酸铜溶液;⑥铁丝,由于金属活动性:Fe>Cu,所以二者在溶液中会发生置
换反应产生FeSO 、Cu,反应的离子方程式为:Fe+Cu2+=Fe2++Cu;
4
答案第6页,共8页(5)③是硫酸铜溶液,⑤是KOH固体,二者在溶液中发生反应产生Cu(OH) 蓝色沉淀和
2
KSO ,反应的离子方程式为:Cu2++2OH-=Cu(OH) ↓;
2 4 2
(6)在该反应中,Cl元素化合价由反应前Cl 中的0价变为反应后KCl中的-1价,化合价
2
降低1价;Cl元素化合价由反应前Cl 中的0价变为反应后KClO 中的+5价,化合价升高5
2 3
价,化合价升降最小公倍数是5,所以KCl的系数是5,KClO 的系数是1,根据反应前后
3
Cl元素守恒可知Cl 的系数是3;根据K元素守恒,可知KOH的系数是6,最后根据H、O
2
原子守恒,可知HO的系数是3,则配平后化学方程式为:
2
3Cl+6KOH=5KCl+KClO +3H O。元素化合价升降总数等于反应过程中电子转移总数,则
2 3 2
反应过程中电子转移数目是5e-,用双线桥标出电子得失为:
17.(1) 胶体 丁达尔效应
(2) MnO +4H++2Cl- Mn2++2H O+Cl ↑ 1:2 MnCl 2 5:1 a
2 2 2 2
【详解】(1)气溶胶是指分散剂是空气的胶体;胶体具有丁达尔效应,溶液没有,常利用
丁达尔效应区分溶液和胶体;答案为:胶体;丁达尔效应;
(2)①反应a:MnO +4HCl(浓) MnCl +2H O+Cl ↑对应的离子方程式为MnO +4H++2Cl-
2 2 2 2 2
Mn2++2H O+Cl ↑;根据反应可知,氧化剂MnO 与还原剂HCl的化学计量数之比为1:
2 2 2
2;
②反应b为2KMnO +16HCl(浓)=2KCl+2MnCl +5Cl↑+8H O,反应中KMnO 中锰元素由+7
4 2 2 2 4
价变为+2价被还原生成MnCl ,故还原产物是MnCl ;反应中转移电子数为10,故每生成
2 2
1个Cl 转移的电子数为2;
2③反应c:KClO+6HCl(浓)=KCl+3Cl ↑+3H O中KClO 中Cl元素的化合价由+5→0,被还
3 2 2 3
原,为氧化剂,HCl中Cl元素化合价有-1→0,被氧化,为还原剂,其中6molHCl生成
1molKCl,被氧化的HCl为5mol,则氧化剂与还原剂物质的量之比为1:5,故对应的氧化
产物和还原产物的物质的量质量之比为5:1;
④当三个反应中参与反应的HCl的质量相同时,根据反应a、反应b、反应c中HCl与Cl
2
物质的量关系分别是: 、 、 ,得到Cl 的质量最少的是
2
a反应,所以当得到等质量的Cl 时,消耗HCl的质量最多的是a反应。
2
18.(1)3C+2 8 (稀)=3 2 2
(2) C
(3)A
(4)12
【解析】(1)
该反应中C元素化合价由0升高为+4、Cr元素化合价由+6降低为+3,根据得失电子守恒、
元素守恒,配平反应方程式为3C+2 8 (稀)=3 2 2
;
(2)
3C+2 8 (稀)=3 2 2 反应, 中Cr元
素化合价由+6降低为+3, 是氧化剂;C元素化合价由0升高为+4、C是还原剂。
(3)
硫酸中元素化合价不变,硫酸表现酸性,选A。
(4)
该反应中C元素化合价由0升高为+4,每个碳原子失4个电子,该反应中转移的电子数为
4×3=12。
答案第8页,共8页