文档内容
化学试卷
说明:1. 满分100分,考试时间70分钟;2. 本卷共五大题,24小题;3. 可能用到的相对原子质量:
H-1 C-12 O-16
一、单项选择题(本大题包括10小题。每小题2分。共20分。每小题有四个选项,其中只有一个选项
符合题意。)
1. 下列古代文化遗迹与化学变化密切相关的是( )
A. 冶炼并铸造青铜器皿 B. 用巨石筑金字塔
C. 磨制玉石饰品 D. 在甲骨上刻字
2. 水是生命之源,下列关于水的说法正确的是( )
A. 地球上有很多水,所以水是取之不尽用之不竭的
B. 电解水实验中,负极产生的气体能燃烧产生淡蓝色火焰
C. 水体有自我净化的能力,因此生活污水的任意排放不会造成水体污染
D. 自来水厂通过沉淀、过滤、吸附、消毒可将海水淡化
3. 据报道,毒淀粉是在淀粉中添加了对人体有害的马来酸(C HO)。马来酸是无色晶体,能溶于水。
4 4 4
下列关于马来酸的说法中正确的是( )
A. 马来酸属于氧化物 B. 马来酸由三种原子构成
C. 马来酸的相对分子质量为106 D. 马来酸中氧元素的质量分数最大
4. 下列生活中常见现象用微观粒子解释正确的是( )
A. 深色衣服和浅色衣服浸泡在一起,会使衣服上染上颜色,这是因为原子发生了变化
B. 温度计中的水银球受热体积膨胀。这是因为汞原子受热体积变大了
C. 碘蒸气和碘溶液都能使淀粉变蓝色,是因为它们都含有碘分子
D. 擦黑板时看到粉尘在空中飞舞,这是分子在运动
5. 正确的实验操作对实验结论、人身安全都非常重要。下列实验操作正确的是( )
6. 下列物质的用途利用其化学性质的是( )
A. 手术麻醉时用液氮作冷冻剂 B. 急救病人时用氧气供人呼吸
C. 电解水时用石墨作电极材料 D. 稀有气体制作电光源
7. 在探究二氧化锰、氧化铜、氧化铁对过氧化氢溶液分解速率的影响的过程中,没有必要进行控制
的变量是( )
A. 过氧化氢溶液中溶质的质量分数 B. 催化剂的质量C. 反应容器的形状 D. 反应前过氧化氢溶液的温度
8. 从2013年9月1日起,国家气象中心便于每天8时和20时进行全国24小时空气污染气象条件
预报。发布重度污染预警启动应急措施的条件为:连续12小时AOI大于200,且当前PM2.5小时浓度
大于150微克/立方米,预计未来24小时不会明显好转。下列情况不会增加空气中PM2.5的是( )
A. 汽车排放尾气 B. 秸秆焚烧还田 C. 工厂排放的废气 D. 植树造林
9. 甲、乙、丙、丁表示四种物质,其微观示意图见下表,甲和乙在一定条件下反应生成丙丁。下列说
法正确的是( )
物质 甲 乙 丙 丁
微观示意图
[来源:学|科|网Z|X|X|K] [来源:Z_xx_k.Com] [来源:学.科.网]
[来源:Z.xx.k.Com][来源:学,科,网Z,X,X,K]
A. 甲、丁的化学式相同
B. 只有丙物质属于单质
C. 若16g乙参加反应,则生成的丙质量为32g
D. 反应中,反应物分子中所含氧原子总数是生成物分子中所含氧原子总数的2倍
10. 在下列实验中,试管内固体质量随时间变化关系如下图的是( )
A. 给装有木炭和氧化铜粉末的试管加强热
B. 往装有锌粒的试管里逐滴加入过量的稀盐酸
C. 往装有硫酸铜溶液的试管里逐滴加入一定量的氢氧化钠溶液
D. 往有铁钉的试管中逐滴加入一定量的硫酸铜溶液
二、选择填充题(本大题包括5小题,每小题3分,共15分。先在
A、B、C中选择一个正确选项,然后在D处再补充一个符合题意的答案。每小题的选择2分,填充
1分。)
11. 某粒子结构示意图如图所示,下列有关说法正确的是( )
A. 该粒子易失去电子 B. 该粒子是阳离子
C. 该元素属于非金属元素
D.12. 下列有关分子和原子的说法中,正确的是( )
A. 分子一定比原子大
B. 分子可直接构成物质,而原子要先构成分子后才能构成物质
C. 分子在化学变化中可分解产生原子,这些原子又重新组合构成别的分子
D.
13. 鉴别下列物质所使用的方法或试剂,正确的是( )
A. 氧化铜和木炭:看颜色 B. 铝与铝合金:比较硬度
C. 硬水与软水:加明矾 D. :滴入紫色石蕊溶液
14. 下列有关铜、铁、铝的说法正确的是( )
A. 缺铁性贫血里所说的铁是指铁元素 B. 黄铜不是合金,而是纯金属
C. 铝是地壳中含量最高的元素
D. 人类最早大规模使用的金属是
15. 关于下列化学用语中数字“3”的含义正确的是( )
① ; ②Fe3+; ③3H; ④SO
3
A. ①中的数字“3”表示铝原子有三个电子层
B. ②中的数字“3”表示铁元素的化合价为+3价
C. ③中的数字“3”表示三个氢原子
D.
三、填空与说明题(本大题包括5小题。共有30分)
温馨提示:本大题的选择填空有不定项选择符合题意,漏选给1分,错选、多选不给分。
16. (5分)用化学用语填空:
(1)氟元素 ; (2)2个氢氧根离子 ;
(3)4个五氧化二磷分子 ; (4)硝酸银中氮元素的化合价 ;
(5)写出一个既能表示一种元素,又能表示一个原子,还能表示一种物质的化学用语:
。
17. (6分)多彩的“碳”,多姿的生活,让我们一起走进“碳”的世界:
(1)“碳海绵”是已知最轻的固体材料(如图所示),由碳元素组成,具有多孔结构,弹性好。它对
石油有很强的吸附能力(不吸水),将吸入的石油挤出后仍可恢复原状。下列关于碳海绵的说法不正
确的是 (填字母序号)。A. 具有吸附性 B. 不可重复使用
C. 可处理海上石油泄漏
(2)目前,人类以煤、石油、天然气等含碳的化石燃料为主要能源。请从下列表格中分析,与煤相
比,用天然气做燃料的优点是 。
1g物质完全燃烧
产生二氧化质量/g 放出热量/kJ
甲烷 2.75 56
碳 3.67 32
请写出天然气燃烧的化学方程式: (2分)
(3)过多的二氧化碳会加剧温室效应,但另一方面二氧化碳也是一种宝贵的资源。液态二氧化碳
灭火器可用于扑救档案资料室发生的火灾,这是因为 。(2分)
18. (5分)美国两位科学家利用碘元素,借助放射学进行了“G蛋白偶联受体”研究,揭开了“细
胞如何感知周围环境”之谜,获得了2012年诺贝尔化学奖。图①和图②是碘元素在元素周期表中的
部分信息及碘原子的结构示意图。请回答:
(1)由图①可知碘元素的一点信息是: ;
(2)A、B、C中与碘元素化学性质相似的是 (填字母);
(3)碘元素在元素周期表中排在第 周期;
(4)碘化镁的化学式是 。(2分)
19. (6分)生活离不开水。净化水的知识在日常生活中有着广泛的应用:
(1)茶杯内的纱网,可将茶叶与茶水分离,便于饮用,该设计利用的化学原理是
;
(2)自制净水器中常加入 ,用于除去水中的异味和色素;
(3)井水中含有较多的钙、镁 离子,为降低硬度,生活中可采用的方法是
;
(4)采用如图所示装置进行过滤。图中还缺少的一种仪器是 ,其作用是
; 过 滤 后 观 察 发 现 , 滤 液 仍 然 浑 浊 。 可 能 的 原 因 有 :
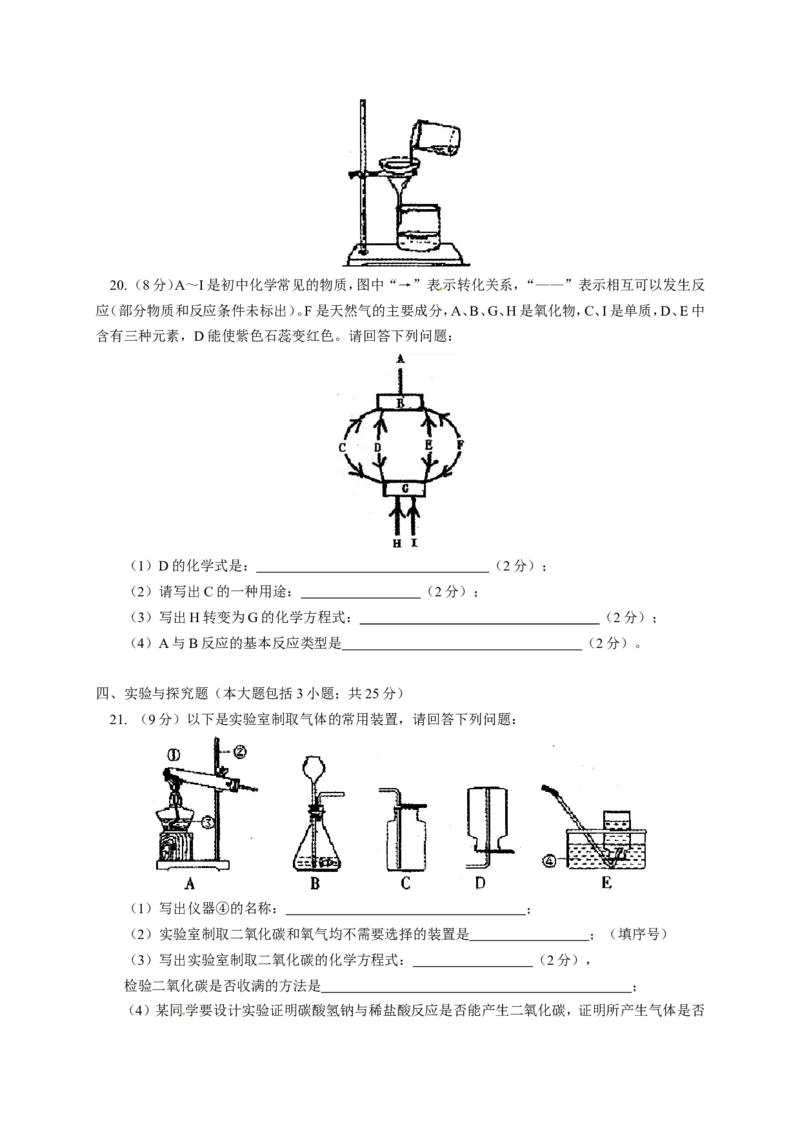
(写出一点即可)。20. (8分)A~I是初中化学常见的物质,图中“→”表示转化关系,“——”表示相互可以发生反
应(部分物质和反应条件未标出)。F是天然气的主要成分,A、B、G、H是氧化物,C、I是单质,D、E中
含有三种元素,D能使紫色石蕊变红色。请回答下列问题:
(1)D的化学式是: (2分);
(2)请写出C的一种用途: (2分);
(3)写出H转变为G的化学方程式: (2分);
(4)A与B反应的基本反应类型是 (2分)。
四、实验与探究题(本大题包括3小题;共25分)
21. (9分)以下是实验室制取气体的常用装置,请回答下列问题:
(1)写出仪器④的名称: ;
(2)实验室制取二氧化碳和氧气均不需要选择的装置是 ;(填序号)
(3)写出实验室制取二氧化碳的化学方程式: (2分),
检验二氧化碳是否收满的方法是 ;
(4)某同学要设计实验证明碳酸氢钠与稀盐酸反应是否能产生二氧化碳,证明所产生气体是否二氧化碳的操作是 ;另一位同学要用实验证明氨气具有还原
性,能将氧化铜还原,他应将装置 (填序号)略加改进,改进的方法是:
。(2分)
22. (8分)某校兴趣小组同学为探究铁的化学性质,如图进行了以下三个实验,请回答有关问题:
(1)实验一:所发生反应的化学方程式是 (2分),
实验结束后可能产生的不良后果是 ;
(2)实验二:关闭K一段时间后,观察到导管内液面上升;打开K,滴加稀盐酸,观察到导管内液
面 下 降 , 导 管 口 有 气 泡 冒 出 , 关 闭 K , 导 管 内 液 面 上 升 的 原 因 是
;导管内液面下降的原因是 。(用化学方程
式解释)(2分)
(3)实验三:实验观察到的现象是: ,
这一现象说明 (填“铁”或“铜”)的活动性更强。
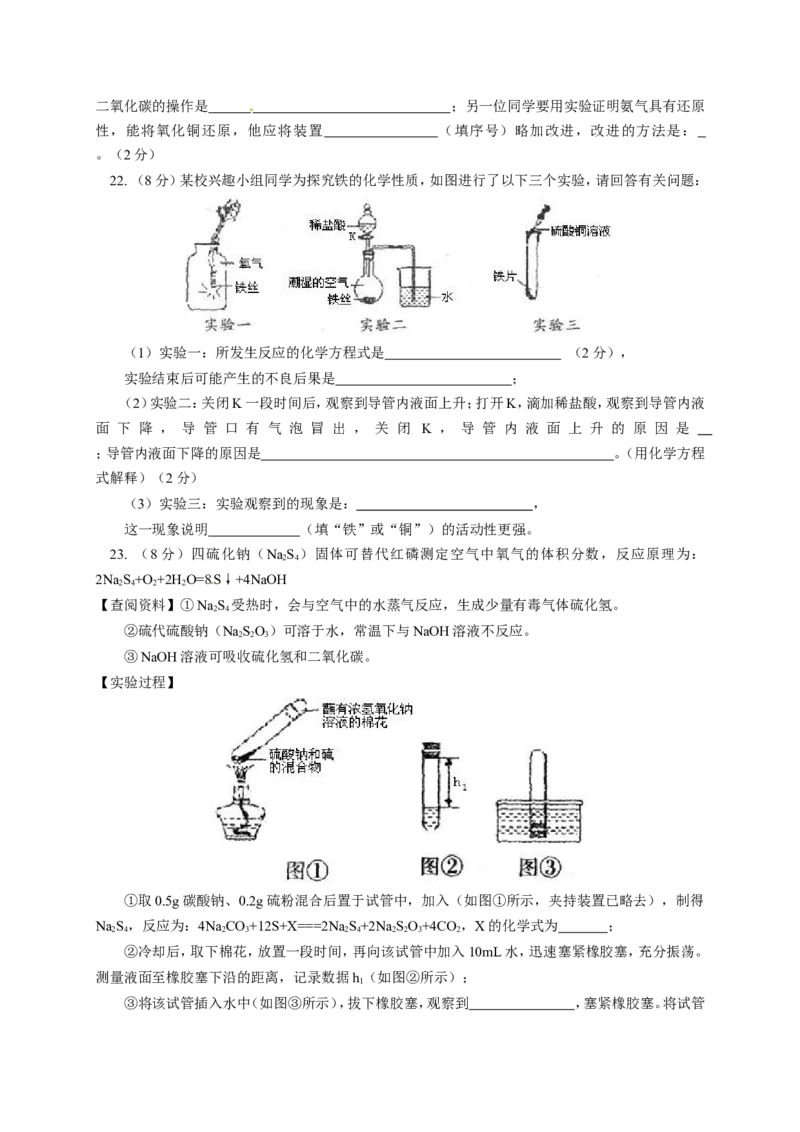
23. (8分)四硫化钠(NaS )固体可替代红磷测定空气中氧气的体积分数,反应原理为:
2 4
2NaS+O +2H O=8S↓+4NaOH
2 4 2 2
【查阅资料】①NaS 受热时,会与空气中的水蒸气反应,生成少量有毒气体硫化氢。
2 4
②硫代硫酸钠(NaSO)可溶于水,常温下与NaOH溶液不反应。
2 2 3
③NaOH溶液可吸收硫化氢和二氧化碳。
【实验过程】
①取0.5g碳酸钠、0.2g硫粉混合后置于试管中,加入(如图①所示,夹持装置已略去),制得
NaS,反应为:4NaCO+12S+X===2NaS+2Na SO+4CO ,X的化学式为 ;
2 4 2 3 2 4 2 2 3 2
②冷却后,取下棉花,放置一段时间,再向该试管中加入10mL水,迅速塞紧橡胶塞,充分振荡。
测量液面至橡胶塞下沿的距离,记录数据h(如图②所示);
1
③将该试管插入水中(如图③所示),拔下橡胶塞,观察到 ,塞紧橡胶塞。将试管取出,倒转过来,测量液面至橡胶塞下沿的距离h,记录数据h。理论上h:h= ;
2 2 2 1
④按照①~③再重复实验2次。3次实验数据如下表所示。
第1次 第2次 第3次
h/cm 11.0 11.4 11.6
1
h/cm 8.7 9.1 9.2
2
【解释与结论】根据第1次实验数据,计算空气中氧气的体积分数为 %(结果精确到
0.1%);
【反思与评价】实验过程①中浓NaOH溶液的作用是 ;若实验过程
②中,取下棉花后,未放置一段时间即进行后续操作,测定结果 (填“偏大”、“偏小”
或“无影响”),理由是: 。(2分)
五、计算题(本大题包括1小题,共10分)
24. 某同学需测定某100g过氧化氢溶液中所含过氧化氢的质量。他取10g二氧化锰放入烧杯中,
并将该过氧化氢溶液全部加入,不同时间用电子天平测量其质量,所得读数如下表所示:
反应时间/min 0 1 2 3 4 5 6
烧杯及所盛物质总质量/g 335.70 334.30 334.00 333.50 333.00 332.50 332.50
(1)试分析,100g过氧化氢溶液完全反应后生成氧气的质量为 。(2分)
(2)计算100g过氧化氢溶液中过氧化氢质量分数为多少?(写出计算过程)(6分)
(3)请分析该方法测定结果可能会偏大的原因有 (写出一点即
可)(2分)吉州区2013—2014学年度第一学期期末检测
九年级化学试卷参考答案
一、1. A 2. B 3. D 4. C 5. B 6. B 7. C 8. D 9. C 10. A
二、11. B 该粒子化学性质较稳定或该元素属于金属元素等(合理即可);
12. C 分子是由原子构成的等(合理即可);
13. B CO 和CO(合理即可);
2
14. A 铜;
15. C ①中的数字“3”表示铝原子的最外电子层上有3个电子或②中的“Fe3+”数字“3+”铁
离子带3个单位正电荷或④中的数字“3”表示一个三氧化硫分子中含有3个硫原子。
三、16. (5分) (1)F; (2)2OH-; (3)4PO; (4)
2 5
(5)C、S、He等(合理即可)
17. (6分)
(1)B;
(2)燃烧热值高或单位质量燃烧排放二氧化碳量少(写到一点即可);
(3)CH+2O =====CO+2H O(2分)
4 2 2 2
液态二氧化碳气化时吸热、二氧化碳不支持燃烧也不燃烧且密度比空气大。(2分)
18. (5分)
(1)碘的相对原子质量为126.9(合理即可); (2)B; (3)五; (4)MgI ;
2
19. (6分)
(1)过滤; (2)活性炭; (3)煮沸; (4)玻璃棒;引流;滤纸破损等(合理即可)
20. (8分)
(1)HCO(2分);
2 3
(2)支持燃烧或供给呼吸等(合理即可);(2分)
(3)CO+CuO====Cu+CO 或2CO+O=====2CO(2分)
2 2 2
(4)化合反应;(2分)
四、21. (9分)(1)水槽;(2)D
(3)CaCO +2HCl=CaCl +H O+CO↑(2分)
3 2 2 2
将燃着的木条放于集气瓶口,若木条熄灭则满
(5)将产生的气体通入澄清石灰水中;A;
将橡皮塞除去,并将导管伸入到试管底部(2分)
22. (8分)
(1)3Fe+2O =====Fe O(2分);集气瓶破裂
2 3 4
(2)铁生锈消耗了瓶内的氧气,瓶内气压小于外界大气压,液面上升;Fe+2HCl=FeCl +H ↑(2分)
2 2
(3)有红色固体析出,蓝色溶液变浅绿色;铁
22. (8分)实验过程①O;②试管内液面上升;③4:5(79:100)
2
解释与结论:20.9%
反思与评价:吸收二氧化碳和硫化氢气体;偏小;氧气没有完全消耗(2分)
五、23. (1)3.2g;(2分)
(2)解:设100g过氧化氢溶液中过氧化氢的质量为x。 (0.5分)
2HO=====2HO+O↑ ……(1分)
2 2 2 2
68 32 ………………(1分)
x 3.2g
…………(1分)
…………(1分)
碳酸钙的质量分数 …………(1分)
答:石灰石样品中碳酸钙的质量分数为6.8%。 ……(0.5分)
(3)该反应放热使水分蒸发。(2分)