文档内容
说明:1.本试卷共6页,满分100分,考试时间90分钟。
2.可能用到的相对原子质量:H-1 C-12 O-16 S-32 Ca-40 Fe-56 Cu-64
一、单项选择题(本题共15小题,每小题2分,共30分。每小题只有一个选项符合题意)
1.下列变化属于物理变化的是
A.光合作用 B.粮食酿酒 C.动物呼吸 D.煤块制蜂窝煤
2.下列物质属于纯净物的是
A.牛奶 B.可口可乐 C.蒸馏水 D.空气
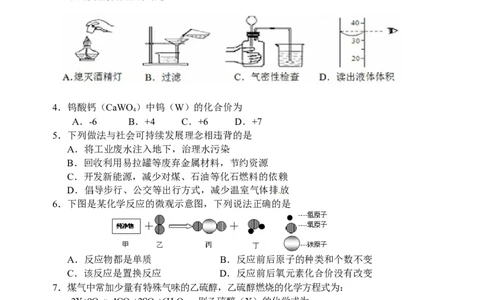
3.下列实验操作正确的是
[来源:学+科+网Z+X+X+K]
4.钨酸钙(CaWO )中钨(W)的化合价为
4
A.-6 B.+4 C.+6 D.+7
[来源:学.科.网Z.X.X.K]
5.下列做法与社会可持续发展理念相违背的是
[来源:学。科。网Z。X。X。K]
A.将工业废水注入地下,治理水污染
B.回收利用易拉罐等废弃金属材料,节约资源
C.开发新能源,减少对煤、石油等化石燃料的依赖
D.倡导步行、公交等出行方式,减少温室气体排放
6.下图是某化学反应的微观示意图,下列说法正确的是
A.反应物都是单质 B.反应前后原子的种类和个数不变
C.该反应是置换反应 D.反应前后氧元素化合价没有改变
7.煤气中常加少量有特殊气味的乙硫醇,乙硫醇燃烧的化学方程式为:
2X+9O 2 C b o i m n 4CO 2 +2SO 2 +6H 2 O, 则乙硫醇(X)的化学式为
A.C HSH B.CHSH C、C HSH D.C HOH
2 3 3 2 5 2 5
8.下列说法正确的是
A.“真金不怕火炼” 是指黄金的化学性质稳定
B.“众人拾柴火焰高”是指可燃物与氧气的接触面积越大,燃烧越旺
C.“百炼成钢”与“只要功夫深,铁杵磨成针”蕴含的化学原理相同
D.“满架蔷薇一院香”的原因是分子间有空隙
9.下列实验数据或现象合理的是
①用托盘天平称取5.6g氯化钠固体 ②铜粉中加入稀硫酸,产生大量气泡
③铁在空气中剧烈燃烧,火星四射 ④用10mL量筒量取6.6mL某溶液;A.①③ B.①③④ C.①④ D.①②③④
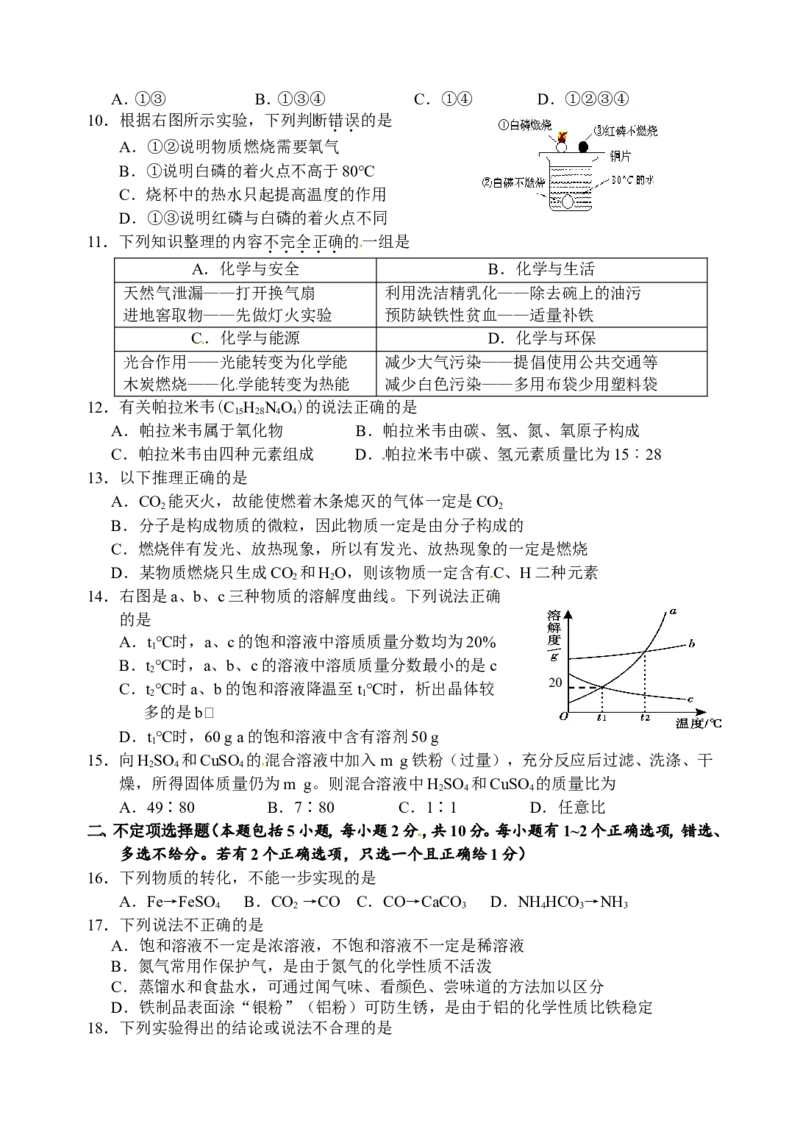
10.根据右图所示实验,下列判断错误的是
A.①②说明物质燃烧需要氧气
B.①说明白磷的着火点不高于80℃
C.烧杯中的热水只起提高温度的作用
D.①③说明红磷与白磷的着火点不同
11.下列知识整理的内容不完全正确的一组是
A.化学与安全 B.化学与生活
天然气泄漏——打开换气扇 利用洗洁精乳化——除去碗上的油污
进地窖取物——先做灯火实验 预防缺铁性贫血——适量补铁
C.化学与能源 D.化学与环保
光合作用——光能转变为化学能 减少大气污染——提倡使用公共交通等
木炭燃烧——化学能转变为热能 减少白色污染——多用布袋少用塑料袋
12.有关帕拉米韦(C H NO)的说法正确的是
15 28 4 4
A.帕拉米韦属于氧化物 B.帕拉米韦由碳、氢、氮、氧原子构成
C.帕拉米韦由四种元素组成 D.帕拉米韦中碳、氢元素质量比为15︰28
13.以下推理正确的是
A.CO 能灭火,故能使燃着木条熄灭的气体一定是CO
2 2
B.分子是构成物质的微粒,因此物质一定是由分子构成的
C.燃烧伴有发光、放热现象,所以有发光、放热现象的一定是燃烧
D.某物质燃烧只生成CO 和HO,则该物质一定含有C、H二种元素
2 2
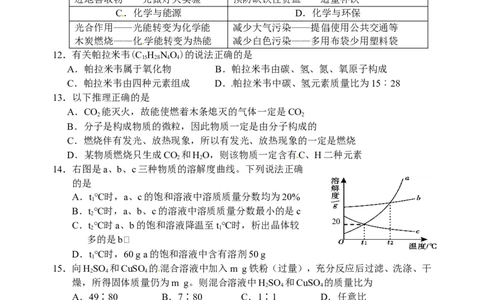
14.右图是a、b、c三种物质的溶解度曲线。下列说法正确
的是
A.t℃时,a、c的饱和溶液中溶质质量分数均为20%
1
B.t℃时,a、b、c的溶液中溶质质量分数最小的是c
2
20
C.t℃时a、b的饱和溶液降温至t℃时,析出晶体较
2 1
多的是b
D.t℃时,60 g a的饱和溶液中含有溶剂50 g
1
15.向HSO 和CuSO 的混合溶液中加入m g铁粉(过量),充分反应后过滤、洗涤、干
2 4 4
燥,所得固体质量仍为m g。则混合溶液中HSO 和CuSO 的质量比为
2 4 4
A.49∶80 B.7∶80 C.1∶1 D.任意比
二、不定项选择题(本题包括5小题,每小题2分,共10分。每小题有1~2个正确选项,错选、
多选不给分。若有2个正确选项,只选一个且正确给1分)
16.下列物质的转化,不能一步实现的是
A.Fe→FeSO B.CO →CO C.CO→CaCO D.NH HCO→NH
4 2 3 4 3 3
17.下列说法不正确的是
A.饱和溶液不一定是浓溶液,不饱和溶液不一定是稀溶液
B.氮气常用作保护气,是由于氮气的化学性质不活泼
C.蒸馏水和食盐水,可通过闻气味、看颜色、尝味道的方法加以区分
D.铁制品表面涂“银粉”(铝粉)可防生锈,是由于铝的化学性质比铁稳定
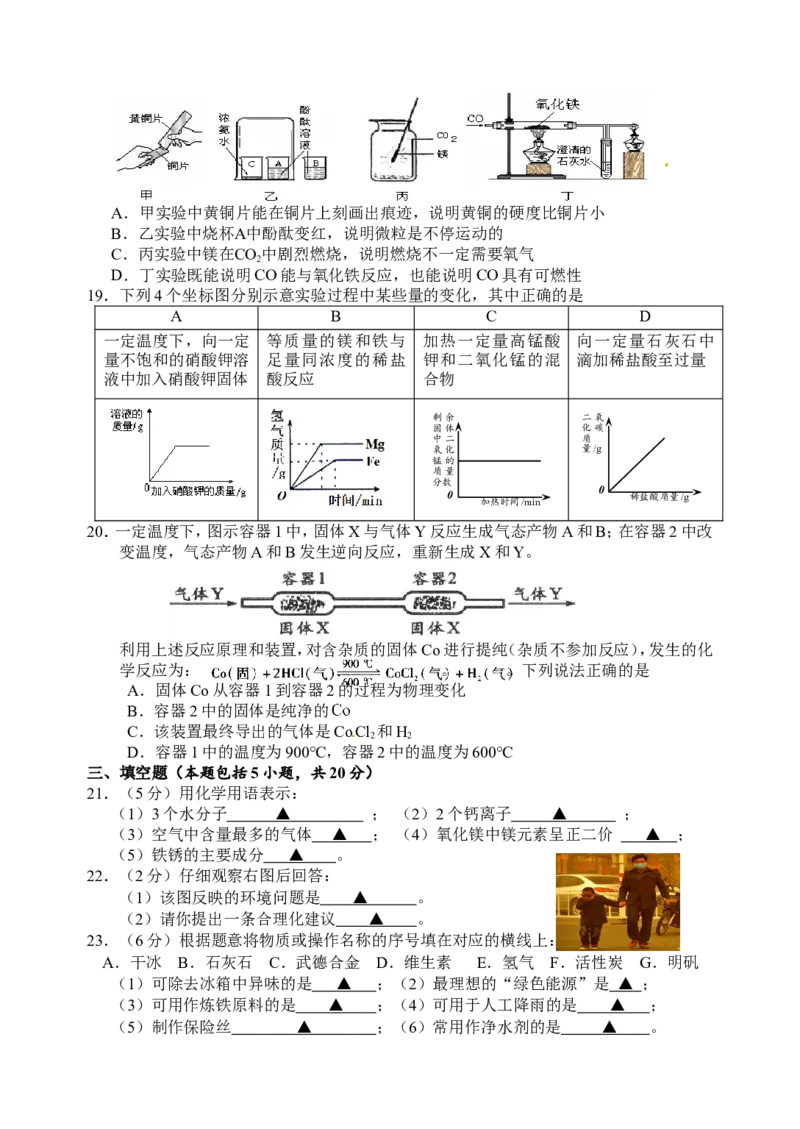
18.下列实验得出的结论或说法不合理的是A.甲实验中黄铜片能在铜片上刻画出痕迹,说明黄铜的硬度比铜片小
B.乙实验中烧杯A中酚酞变红,说明微粒是不停运动的
C.丙实验中镁在CO中剧烈燃烧,说明燃烧不一定需要氧气
2
D.丁实验既能说明CO能与氧化铁反应,也能说明CO具有可燃性
19.下列4个坐标图分别示意实验过程中某些量的变化,其中正确的是
A B C D
一定温度下,向一定 等质量的镁和铁与 加热一定量高锰酸 向一定量石灰石中
量不饱和的硝酸钾溶 足量同浓度的稀盐 钾和二氧化锰的混 滴加稀盐酸至过量
液中加入硝酸钾固体 酸反应 合物
剩余 二氧
固体 化碳
中二 质
氧化 量/g
锰的
质量
分数
0
0
加热时间/min
稀盐酸质量/g
20.一定温度下,图示容器1中,固体X与气体Y反应生成气态产物A和B;在容器2中改
变温度,气态产物A和B发生逆向反应,重新生成X和Y。
利用上述反应原理和装置,对含杂质的固体Co进行提纯(杂质不参加反应),发生的化
学反应为: 。 。下列说法正确的是
A.固体Co从容器1到容器2的过程为物理变化
B.容器2中的固体是纯净的
C.该装置最终导出的气体是CoCl 和H
2 2
D.容器1中的温度为900℃,容器2中的温度为600℃
三、填空题(本题包括5小题,共20分)
21.(5分)用化学用语表示:
(1)3个水分子 ▲ ; (2)2个钙离子 ▲ ;
(3)空气中含量最多的气体 ▲ ; (4)氧化镁中镁元素呈正二价 ▲ ;
(5)铁锈的主要成分 ▲ 。
22.(2分)仔细观察右图后回答:
(1)该图反映的环境问题是 ▲ 。
(2)请你提出一条合理化建议 ▲ 。
23.(6分)根据题意将物质或操作名称的序号填在对应的横线上:
A.干冰 B.石灰石 C.武德合金 D.维生素 E.氢气 F.活性炭 G.明矾
(1)可除去冰箱中异味的是 ▲ ;(2)最理想的“绿色能源”是 ▲ ;
(3)可用作炼铁原料的是 ▲ ;(4)可用于人工降雨的是 ▲ ;
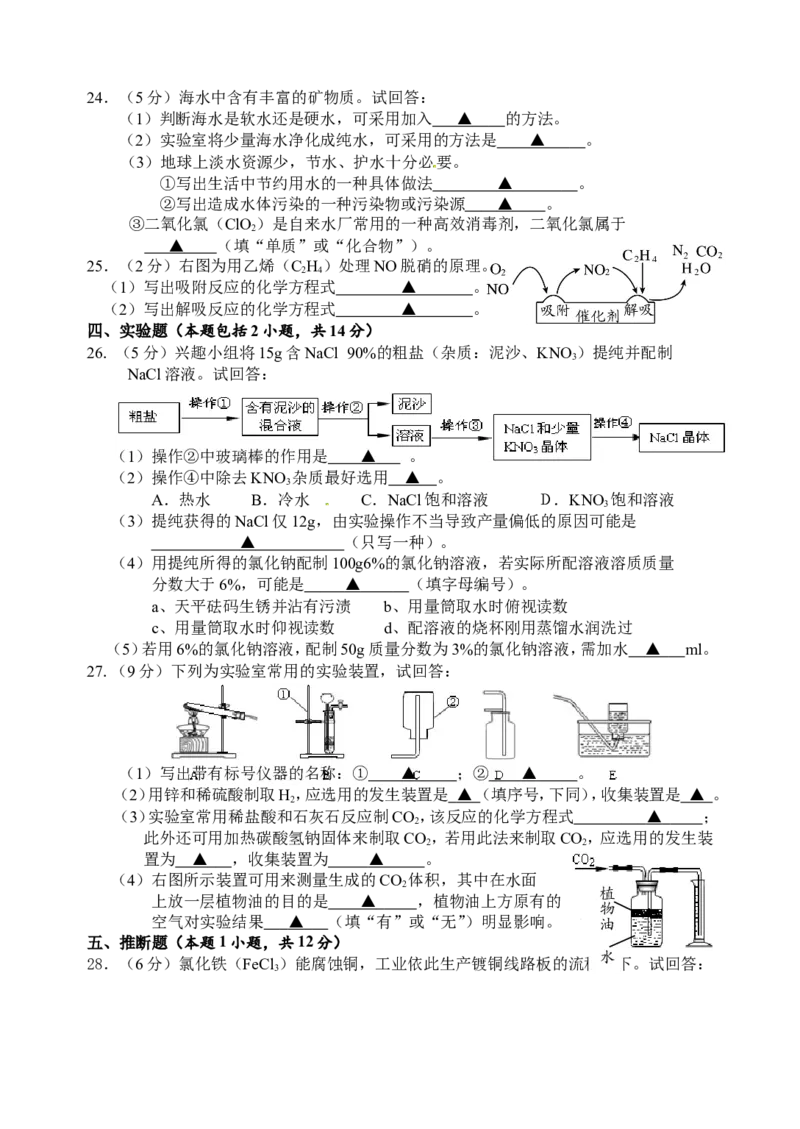
(5)制作保险丝 ▲ ;(6)常用作净水剂的是 ▲ 。24.(5分)海水中含有丰富的矿物质。试回答:
(1)判断海水是软水还是硬水,可采用加入 ▲ 的方法。
(2)实验室将少量海水净化成纯水,可采用的方法是 ▲ 。
(3)地球上淡水资源少,节水、护水十分必要。
①写出生活中节约用水的一种具体做法 ▲ 。
②写出造成水体污染的一种污染物或污染源 ▲ 。
③二氧化氯(ClO )是自来水厂常用的一种高效消毒剂,二氧化氯属于
2
▲ (填“单质”或“化合物”)。
25.(2分)右图为用乙烯(C H)处理NO脱硝的原理。
2 4
(1)写出吸附反应的化学方程式 ▲ 。
(2)写出解吸反应的化学方程式 ▲ 。
四、实验题(本题包括2小题,共14分)
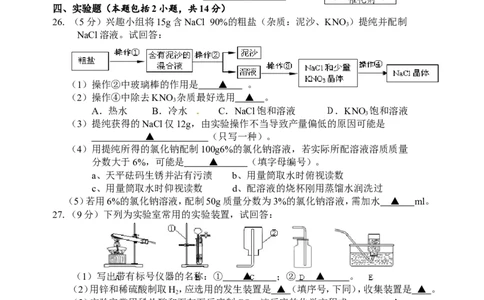
26. (5分)兴趣小组将15g含NaCl 90%的粗盐(杂质:泥沙、KNO)提纯并配制
3
NaCl溶液。试回答:
(1)操作②中玻璃棒的作用是 ▲ 。
(2)操作④中除去KNO 杂质最好选用 ▲ 。
3
A.热水 B.冷水 C.NaCl饱和溶液 D.KNO 饱和溶液
3
(3)提纯获得的NaCl仅12g,由实验操作不当导致产量偏低的原因可能是
▲ (只写一种)。
(4)用提纯所得的氯化钠配制100g6%的氯化钠溶液,若实际所配溶液溶质质量
分数大于6%,可能是 ▲ (填字母编号)。
a、天平砝码生锈并沾有污渍 b、用量筒取水时俯视读数
c、用量筒取水时仰视读数 d、配溶液的烧杯刚用蒸馏水润洗过
(5)若用6%的氯化钠溶液,配制50g质量分数为3%的氯化钠溶液,需加水 ▲ ml。
27.(9分)下列为实验室常用的实验装置,试回答:
(1)写出带有标号仪器的名称:① ▲ ;② ▲ 。
(2)用锌和稀硫酸制取H,应选用的发生装置是 ▲ (填序号,下同),收集装置是 ▲ 。
2
(3)实验室常用稀盐酸和石灰石反应制CO,该反应的化学方程式 ▲ ;
2
此外还可用加热碳酸氢钠固体来制取CO,若用此法来制取CO,应选用的发生装
2 2
置为 ▲ ,收集装置为 ▲ 。
(4)右图所示装置可用来测量生成的CO 体积,其中在水面
2
植
上放一层植物油的目的是 ▲ ,植物油上方原有的
物
空气对实验结果 ▲ (填“有”或“无”)明显影响。 油
五、推断题(本题1小题,共12分)
水
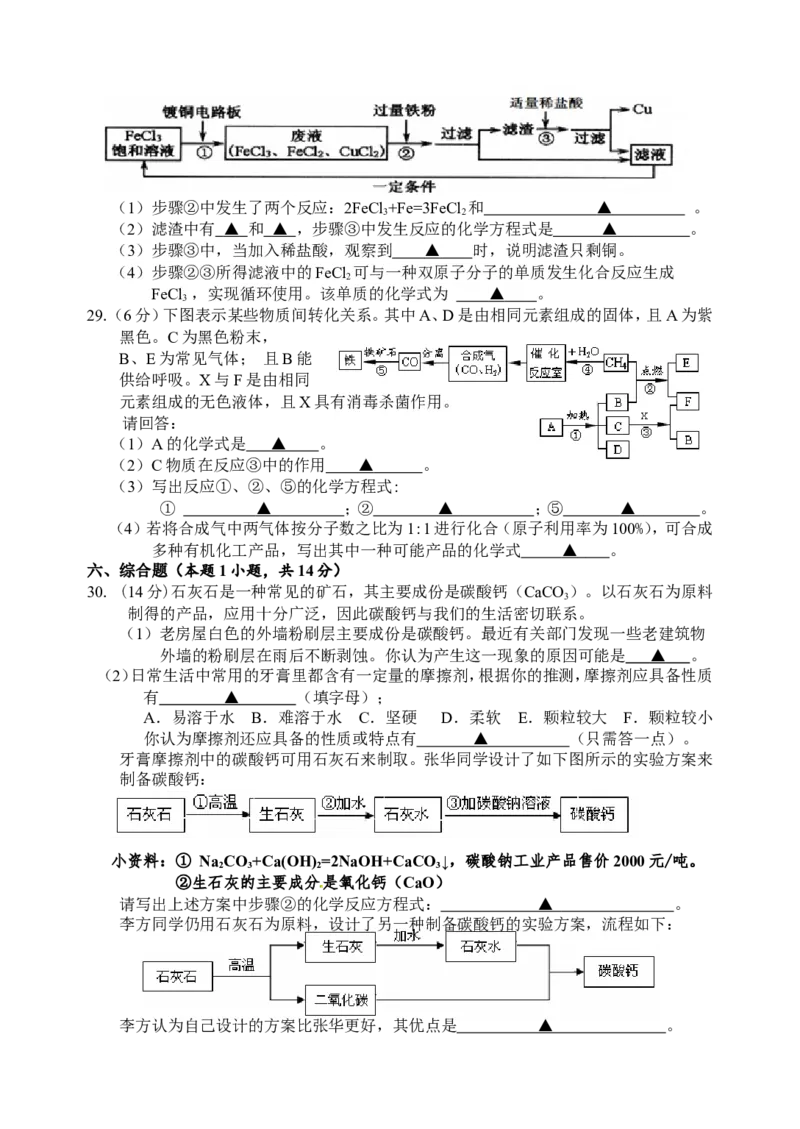
28.(6分)氯化铁(FeCl )能腐蚀铜,工业依此生产镀铜线路板的流程如下。试回答:
3(1)步骤②中发生了两个反应:2FeCl +Fe=3FeCl 和 ▲ 。
3 2
(2)滤渣中有 ▲ 和 ▲ ,步骤③中发生反应的化学方程式是 ▲ 。
(3)步骤③中,当加入稀盐酸,观察到 ▲ 时,说明滤渣只剩铜。
(4)步骤②③所得滤液中的FeCl 可与一种双原子分子的单质发生化合反应生成
2
FeCl ,实现循环使用。该单质的化学式为 ▲ 。
3
29.(6分)下图表示某些物质间转化关系。其中A、D是由相同元素组成的固体,且A为紫
黑色。C为黑色粉末,
B、E为常见气体; 且B能
供给呼吸。X与F是由相同
元素组成的无色液体,且X具有消毒杀菌作用。
请回答:
(1)A的化学式是 ▲ 。
(2)C物质在反应③中的作用 ▲ 。
(3)写出反应①、②、⑤的化学方程式:
① ▲ ;② ▲ ;⑤ ▲ 。
(4)若将合成气中两气体按分子数之比为1:1进行化合(原子利用率为100%),可合成
多种有机化工产品,写出其中一种可能产品的化学式 ▲ 。
六、综合题(本题1小题,共14分)
30. (14分)石灰石是一种常见的矿石,其主要成份是碳酸钙(CaCO )。以石灰石为原料
3
制得的产品,应用十分广泛,因此碳酸钙与我们的生活密切联系。
(1)老房屋白色的外墙粉刷层主要成份是碳酸钙。最近有关部门发现一些老建筑物
外墙的粉刷层在雨后不断剥蚀。你认为产生这一现象的原因可能是 ▲ 。
(2)日常生活中常用的牙膏里都含有一定量的摩擦剂,根据你的推测,摩擦剂应具备性质
有 ▲ (填字母);
A.易溶于水 B.难溶于水 C.坚硬 D.柔软 E.颗粒较大 F.颗粒较小
你认为摩擦剂还应具备的性质或特点有 ▲ (只需答一点)。
牙膏摩擦剂中的碳酸钙可用石灰石来制取。张华同学设计了如下图所示的实验方案来
制备碳酸钙:
小资料:① Na CO +Ca(OH) =2NaOH+CaCO ↓,碳酸钠工业产品售价2000元/吨。
2 3 2 3
②生石灰的主要成分是氧化钙(CaO)
请写出上述方案中步骤②的化学反应方程式: ▲ 。
李方同学仍用石灰石为原料,设计了另一种制备碳酸钙的实验方案,流程如下:
李方认为自己设计的方案比张华更好,其优点是 ▲ 。检验牙膏中是否含有碳酸钙的实验方法是 ▲ 。
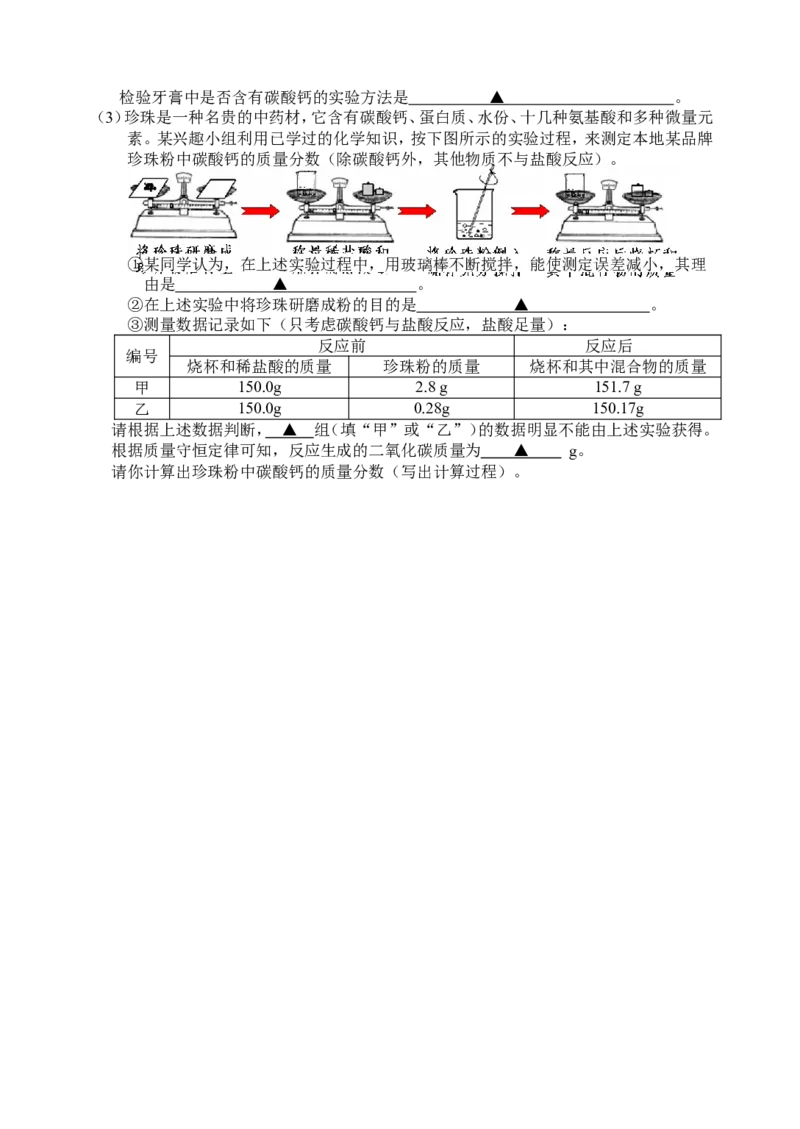
(3)珍珠是一种名贵的中药材,它含有碳酸钙、蛋白质、水份、十几种氨基酸和多种微量元
素。某兴趣小组利用已学过的化学知识,按下图所示的实验过程,来测定本地某品牌
珍珠粉中碳酸钙的质量分数(除碳酸钙外,其他物质不与盐酸反应)。
[来源:学科网]
①某同学认为,在上述实验过程中,用玻璃棒不断搅拌,能使测定误差减小,其理
由是 ▲ 。
②在上述实验中将珍珠研磨成粉的目的是 ▲ 。
③测量数据记录如下(只考虑碳酸钙与盐酸反应,盐酸足量):
反应前 反应后
编号 [来源:学科网]
烧杯和稀盐酸的质量 珍珠粉的质量 烧杯和其中混合物的质量
甲 150.0g 2.8 g 151.7 g
乙 150.0g 0.28g 150.17g
请根据上述数据判断, ▲ 组(填“甲”或“乙”)的数据明显不能由上述实验获得。
根据质量守恒定律可知,反应生成的二氧化碳质量为 ▲ g。
请你计算出珍珠粉中碳酸钙的质量分数(写出计算过程)。2013-2014学年度第一学期九年级化学期末试卷参考答案
说明:1.化学专用名词或仪器名称写错不给分。
2.化学方程式中化学式写错不给分;若化学方程式不配平、未注明反应条件、未标出
“↑”或“↓”及出现差错,每错一个扣0.5分,一个化学方程式共扣1分。
3.与参考答案不同的合理答案均给分。
一、选择题(本题包括15小题,每小题2分共30分,只有一个选项符合题意)
二、选择题(本题包括5小题,每小题2分,共10分。每小题有一个或两个选项符合题意。错
选、多选不给分,有两个答案的,只选一个且正确给1分)
16. C 17.CD 18.A 19.B 20.BD
三、填空题(本题包括5小题,共20分)
+2
21.(5分,每空1分) (1)3HO (2)2Ca2+ (3)N (4)MgO (5)FeO
2 2 2 3
四、实验题(本题包括2小题,共14分)
26.(5分,每空1分)(1)引流
(2)C
(3)蒸发时液滴溅出(其它合理答案正确)
(4)ab (5)25mL
27.(9分,每空1分)(1)铁架台 集气瓶
(2)B C(或E,或CE)
(3)CaCO + 2HCl = CaCl + HO + CO↑ A D
3 2 2 2
(4)防止CO 溶于水(或防止CO 与水反应) 无
2 2
五、推断题(本题包括2小题,共12分)
28.(6分,每空1分)(1)Fe + CuCl = FeCl+ Cu
2 2
(2)Fe 和 Cu Fe + 2HCl= FeCl+ H↑
2 2
(3)无气泡
(4)Cl
2
29.(6分,每空1分) (1) KMnO (2)催化作用
4
(3) ① 2KMnO Δ KMnO + MnO + O↑
4 2 4 2 2② CH + 2O 点燃 CO + 2HO
4 2 2 2
⑤ 3CO+ FeO 高温 2 Fe + 3CO(或FeO+ 4CO高温 3Fe +4 CO)
2 3 2 3 4 2
(4)CHO(其他合理答案也给分,1分)
2
六、综合题(本题包括1小题,共14分)(除计算外,每空1分)
(3)①不断搅拌,促使珍珠粉与盐酸充分反应,同时有利于二氧化碳的散逸;(1分)
增大与盐酸的接触面积,使珍珠中的碳酸钙完全反应(其它合理答案)(1分)
②乙(1分) 1.1或0.11(1分)
(以下共4分)
解:设CaCO 的质量为x
3
CaCO+2HCl==CaCl +CO↑+HO (1分,关系式对也得分)
3 2 2 2
100 44
x (152.8g – 151.7g)=1.1g (1分)
100∶44 = x∶1.1g
解得: x =2.5g (1分)
=89.3%(1分)
答:珍珠粉中碳酸钙的质量分数约为89.3%(或89%)。
注:用乙组数据计算亦可,评分标准同上。