文档内容
物质构成的奥秘单元练习
1.地壳中含量最多的元素是
A.硅 B.氧 C.铁 D.铝
2. 决定元素种类的是
A.核外电子数 B.中子数 C.最外层电子数 D.质子数
3. 下列粒子都能直接构成物质的是
A.分子、中子 B.原子、电子 C.原子、离子 D.离子、中子
4. 豆类、动物肝脏中含有丰富的铁和锌,这里的“铁”、“锌”是指
A.原子 B.分子 C.元素 D.单质
5. 下列物质属于纯净物的是
A.空气 B.蔗糖水 C.75%的医用酒精 D.蒸馏水
6. “墙角数枝梅,凌寒独自开,遥知不是雪,为有暗香来”(王安石《梅花》)。诗人在远处就
能闻到梅花香味的原因是
A.分子很小 B.分子是可分的
C.分子之间有间隔 D.分子在不断地运动
7. 分子和原子的主要区别是
A.分子大、原子小 B.分子间有间隔,原子间没有间隔
C.在化学变化中,分子可以再分,而原子不可再分 D.分子在不停运动,原子不运动
8.压瘪的乒乓球放入热水中重新鼓起,是因为球内的气体分子
A.体积增大 B.间隔增大 C.质量增大 D.个数增多
9.下列化学用语既能表示一种元素,又能表示一个原子,还能表示一种物质的是
A.O B.Zn C.N D.CO
2
10. 下列能保持氢气(H)化学性质的粒子模型是
2
H H
O
H H O O
O H H
A B C D
11.下列关于分子、原子、离子的说法,正确的是
A.原子是微小的实心球体,可以再分
B.单个SO 分子有刺激性气味
2
C.纯净的氢气在氧气中完全燃烧后,生成的物质是由同一种粒子构成的
D.离子是原子失去电子后生成的粒子
12.与元素化学性质最密切的是原子的
A、质子数 B、中子数 C、电子层数 D、最外层电子数
13. 关于钠离子(Na+)和钠原子的认识不正确的
A.它们质子数相同 B.Na+的最外层是稳定结构
C.Na比Na+少一个电子 D.它们属于同种元素
14. 下图是气体物质的粒子示意图,图中“ ● ”和“O”分别表示两种不同的原子,其中表
示纯净物的是
15.下列四种粒子的结构示意图中,属于金属元素原子的是
16.下列微粒中,质子数与电子数相等的是
1A.Na+ B.Cl— C.OH— D.N
17.化学上常用元素符号左下角的数字表示原子的质子数,左上角的数字表示原子的中子数
与质子数之和,如 13C表示核内有6个质子和7个中子的碳原子。下列关于 131I和 127I
6 53 53
的说法中错误的是
A.各一个原子相比较,中子数相同 B.属于同种元素
C.各一个原子相比较,核外电子数相同 D.各一个原子相比较,质子数相.同
18. 下列四种粒子的结构示意图中,最容易失去电子的粒子是
19.右图是水分子在一定条件下分解的示意图,从中获得的信息不正确的是
A.一个水分子由二个氢原子和一个氧原子构成
B.反应物是纯净物
C.水分解过程中,分子的种类、原子的数目都不变
D.该反应属于分解反应
20.发生化学变化的实质是( )
A. 分子重新组合 B.分子间间隔发生了改变
C. 分子分解为原子,原子重新组合 D. 物质的状态发生了改变
21.下列物质中,都是由原子直接构成的一组物质是( )
A. 氢气、氧气、氯气 B.硫、铁、氖气
C.水、氩气、铁 D.空气、氮气、木炭
22.在室温时,将1g葡萄糖放入100g水中,充分搅拌后,配成水溶液。则在此过程中,
葡萄糖分子的下列哪种性质会发生改变( )
A. 分子的大小 B. 分子的总数目
C. 分子间的间隔 D. 分子中原子的数目
23.从分子角度看,水的蒸发和水结成冰块的实质都是( )
A.分子运动速度的改变 B.分子间间隔发生变化
C.分子的质量减小 D.分子的种类发生了改变
24.保持水的化学性质的最小粒子是( )
A.氧气分子和氢气分子 B.水分子
C.氢离子 D.氢原子和氧原子
25.在化学反应里,元素的原子结构可能发生变化的是( )
A. 质子数 B. 最外层电子 C. 中子数 D. 核电荷数
26. 下图是钠与氯气(Cl)反应生成氯化钠的模拟图。下列说法中错误的是( )
2
A. 每个钠原子失去1个电子形成钠离子Na+
B. 每个氯原子得到1个电子形成氯离子Cl-
C.Na+ 和 Cl-由于静电作用而结合成化合物氯化钠
D. 氯化钠由氯化钠分子构成
227.某物质加热分解后有氧气生成,说明该物质中含有( )
A. 氧元素 B.氧分子 C. 氧原子 D.氧离子
28.下列有关分子、原子、离子的叙述中,错误的是( )
A.带有电荷的原子或原子团叫做离子
B.分子是保持物质化学性质的最小粒子
C.原子是不能再分的一种粒子
D. 分子、原子、离子都是构成物质的粒子
29.下列各组元素的原子结构示意图中,具有相似化学性质的一组元素是( )
30.下列粒子在化学变化中一定改变的是( )
A.离子 B.原子 C.分子 D. 原子核
31.某粒子最外层有8个电子,下列对该粒子的判断正确的是( )
A. 一定是阳离子 B. 一定是阴离子
C. 一定是稀有气体原子 D.无法确定
32.地壳中含量最多的元素是( )
A.硅 B.铁 C.氧 D.铝
33.一种元素与另一种元素的本质区别是( )
A.质子数不同 B.中子数不同 C.相对原子质量不同 D.电子数不同
34.对于Na和Na+ 的说法,正确的是( )
A.属于同一种元素 B.属于同一种粒子
C.核外电子数相同 D.具有相同的电子层数
35.元素的化学性质主要决定于原子的( )
A.核外电子数 B.核电荷数 C.最外层电子数 D.中子数
36. 下列粒子结构示意图中,表示阳离子的是( )
37. 下列不属于道尔顿提出的原子论观点的是( )
A. 物质是由看不见的原子构成的
B. 同种原子的形状、质量和性质都是相同的
C. 在化学变化中,不同原子以简单的整数比相结合
D. 在化学反应前后,参加反应的各物质的质量等于生成物的质量
38. 根据右表提供的信息,下列判断正确的是 ( )
A.元素所在的周期数等于其原子的最外层
电子层数
B.钠离子核外有三个电子层
C.第二、三周期元素的原子从左至右最外
层电子数逐渐增多
D.在化学变化中镁元素容易失去最外层2
个电子形成镁离子,其离子符号是Mg+2
39.在①分子、②原子、③质子、④中子、⑤电子、⑥离子这些微粒中:
(1)能构成物质的微粒有_______; (2)显示电中性的微粒有____________;
3(3)质量最小的微粒是_________; (4)一定带正电荷的微粒有__________;
(5)一定带负电的微粒有_______; (6)可能带正电也可能带负电的是 ___。
40.右图是某粒子的结构示意图,回答下列问题:
(1)X表示 ,Y表示
(2)当X=12时,该粒子不显电性,Y = ;
+X 2 8 Y
(3)当X=17时,该粒子带1个单位负电荷,则Y = 。
7
(4)当Y=1时,该粒子易________电子,变成带 ________电荷的__________。
41.从①质子数 ②中子数 ③最外层电子数④原子核等选项中选择填空。(填序号)
(1)原子的核电荷数决定于原子结构中的 ;(2)原子序数主要决定于原子结构中的
;
(3)原子的相对原子质量决定于原子结构中的 ;(4)原子的质量主要集中在原子结
构中的 ;
(5)元素的种类决定于原子结构中的 ;(6)元素的化学性质主要决定于原子结构中的
;
(7)元素的分类主要决定于原子结构中的 ;(8)元素的化合价主要决定于原子
结构中的 。
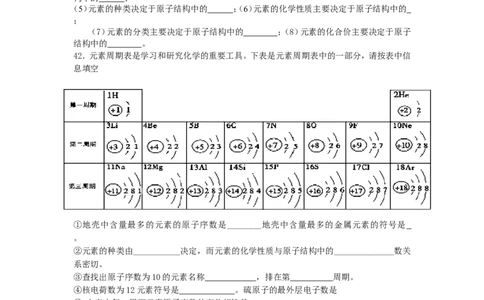
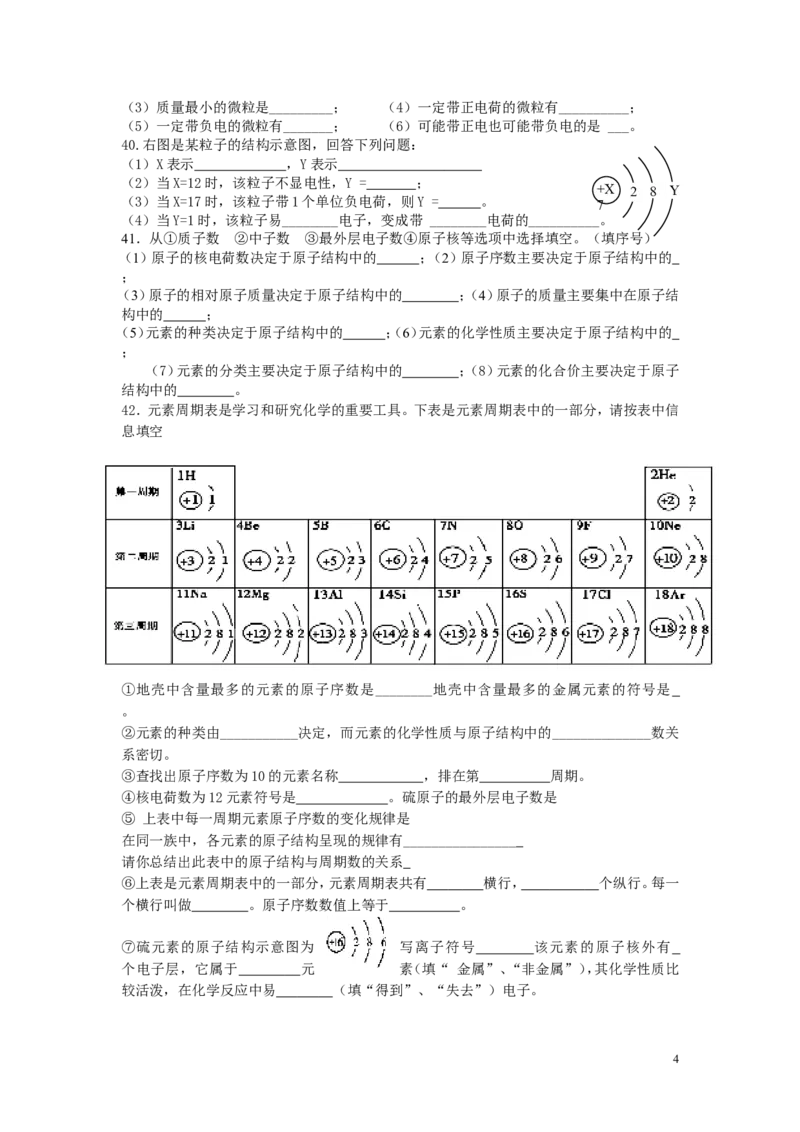
42.元素周期表是学习和研究化学的重要工具。下表是元素周期表中的一部分,请按表中信
息填空
①地壳中含量最多的元素的原子序数是________地壳中含量最多的金属元素的符号是
。
②元素的种类由___________决定,而元素的化学性质与原子结构中的______________数关
系密切。
③查找出原子序数为10的元素名称 ,排在第 周期。
④核电荷数为12元素符号是 。硫原子的最外层电子数是
⑤ 上表中每一周期元素原子序数的变化规律是
在同一族中,各元素的原子结构呈现的规律有________________
请你总结出此表中的原子结构与周期数的关系
⑥上表是元素周期表中的一部分,元素周期表共有 横行, 个纵行。每一
个横行叫做 。原子序数数值上等于 。
⑦硫元素的原子结构示意图为 写离子符号 该元素的原子核外有
个电子层,它属于 元 素(填“ 金属”、“非金属”),其化学性质比
较活泼,在化学反应中易 (填“得到”、“失去”)电子。
4