文档内容
附参考答案
第十单元 酸和碱 单元测试题
一、我会选择 (每小题只有一个选项符合题意,每小题2分)
1、酸类物质具有相似的化学性质,本质的原因是
A.能与指示剂作用 B.能与碱发生中和反应
C. 能解离出H+ D.都含有氢元素
2、下列各组内物质表示同一种物质是
A.氢氧化钠 烧碱 火碱 苛性钠 B.氢氧化钙 消石灰 生石灰
C.盐酸 氯化氢 食盐 D.冰 干冰 水
3、下列物质暴露在空气中,溶质的质量不变而溶质的质量分数减小的是
A.浓盐酸 B.浓硫酸 C.食盐水 D.浓硝酸
4、有一种“即食即热型快餐”适合外出旅行时使用。其内层用铝箔包裹食品,外层则是分
别包装的两种化学物质,使用拉动预留在外的开关,使两种化学物质发生反应,此时便
可以对食物进行加热。这两包化学物质最合适的选择是
A.浓硫酸与水 B. 熟石灰与水 C.生石灰与水 D.氯化钠与水
5、在NaOH溶液中滴入一滴酚酞,溶液呈红色,为了让红色褪去,不能使用
A.盐酸 B.活性碳 C.SO D.熟石灰
2
6、下列气体中,既可以用浓HSO 干燥,又可以用NaOH固体干燥的是( )
2 4
A.SO B.NH C.H D.CO
2 3 2 2
7、如右图是盐酸滴入氢氧化钠溶液中有关粒子之间反应的示意图。下列说法错误的是
A.盐酸中含有氢离子和氯离子
B.氢氧化钠溶液中含有钠离子和氢氧根离子
C.两种溶液混合时,氢离子和氢氧根离子结合生成了水分子
D.两种溶液混合时,钠离子与氯离子结合生成了氯化钠分子
8、下列各组物质不能发生反应的是
A.氧化铜与稀硫酸 B.氢氧化钠与盐酸 C.二氧化硫与氢氧化钠 D. 氢氧化钠与
水
9、要使右图装置中的小气球鼓起来,则使用的固体和液体可以是
①锌和稀硫酸 ②石灰石和盐酸 ③氯化钠和水 ④氧化钙和水
A.①②③ B.①②④
C.②③④ D.①③④
10、下列实例不属于中和反应的是( )
A.土壤酸化后加入熟石灰改良
B.胃酸分泌过多的病人遵医嘱服用含有氢氧化铝的药物以中和过多胃酸
C.蚊虫叮咬人的皮肤分泌出蚁酸,如果涂含碱性物质的药水就可减轻痛痒
D.金属表面锈蚀后,可用稀盐酸进行清洗
11、以下说法正确的是
A.中和反应有盐和水生成,因此有盐和水生成的反应一定是中和反应
B.氧化物中含有氧元素,而含氧元素的化合物不一定是氧化物
1C.碱中都含有氢元素,所以含有氢元素的化合物一定是碱
D.置换反应一定有单质生成,所以有单质生成的反应一定是置换反应
12、 向含有AgNO、Cu(NO) 的混合溶液中加入一定量的铁粉,充分反应后过滤,向滤出的
3 3 2
固体中滴加稀硫酸,有气体生成,则滤出的固体一定为
A.Ag、Cu两种单质的混合物 B.Cu、Fe两种单质的混合物
C.Ag、Fe两种单质的混合物 D.Ag、Cu、 Fe三种单质的混合物
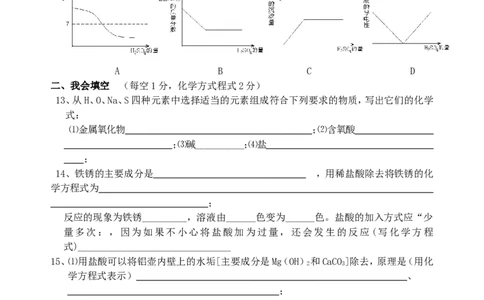
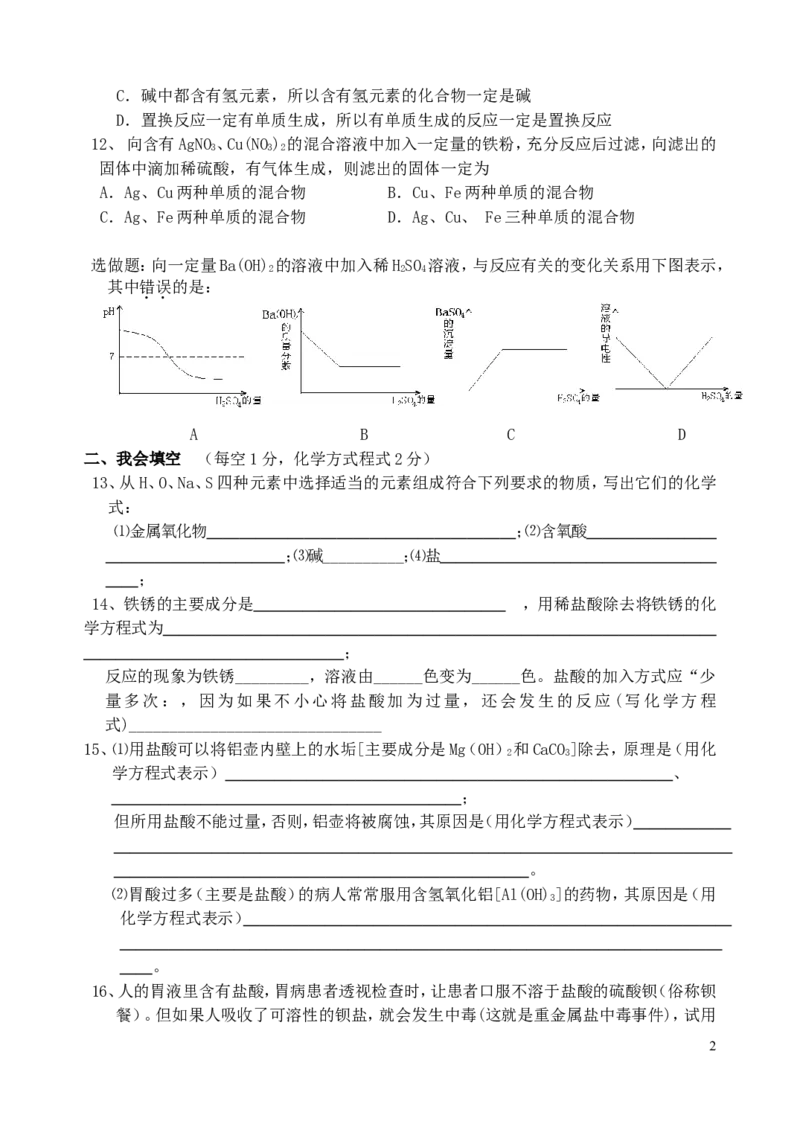
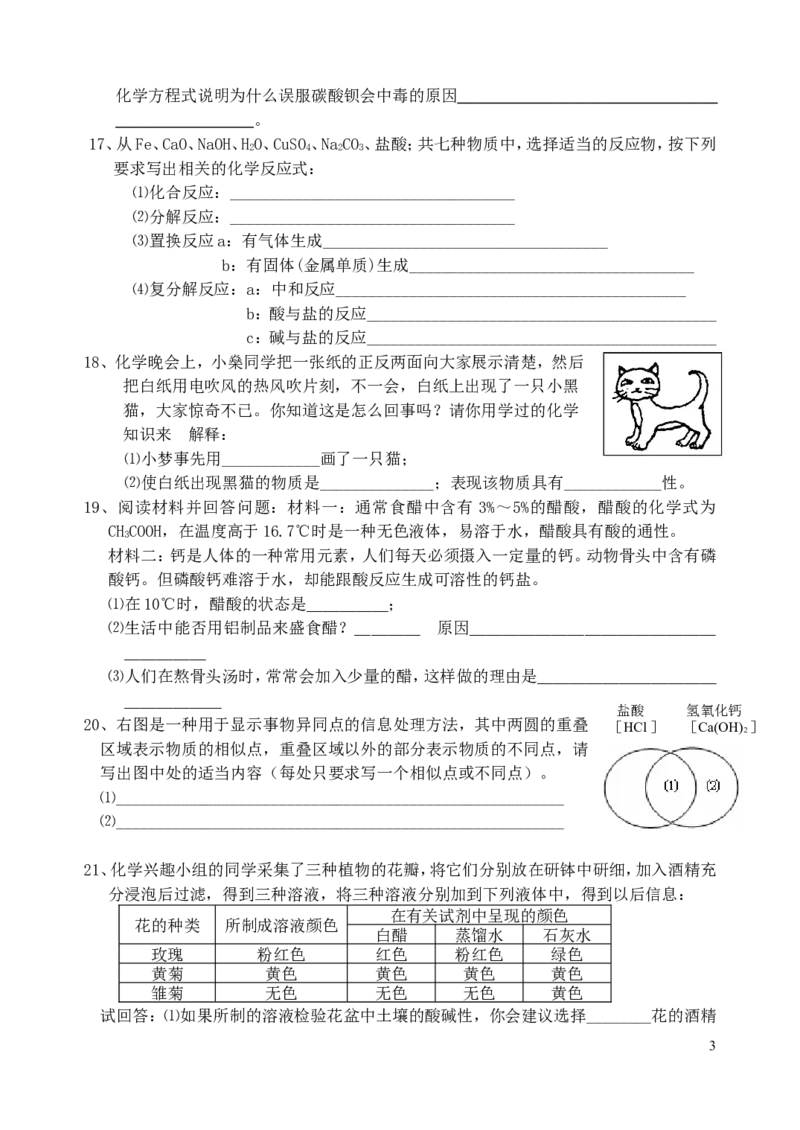
选做题:向一定量Ba(OH) 的溶液中加入稀HSO 溶液,与反应有关的变化关系用下图表示,
2 2 4
其中错误的是:
A B C D
二、我会填空 (每空1分,化学方式程式2分)
13、从H、O、Na、S四种元素中选择适当的元素组成符合下列要求的物质,写出它们的化学
式:
⑴金属氧化物 ;⑵含氧酸
;⑶碱__________;⑷盐
;
14、铁锈的主要成分是 ,用稀盐酸除去将铁锈的化
学方程式为
;
反应的现象为铁锈_________,溶液由______色变为______色。盐酸的加入方式应“少
量多次:,因为如果不小心将盐酸加为过量,还会发生的反应(写化学方程
式)_______________________________
15、⑴用盐酸可以将铝壶内壁上的水垢[主要成分是Mg(OH)和CaCO]除去,原理是(用化
2 3
学方程式表示) 、
;
但所用盐酸不能过量,否则,铝壶将被腐蚀,其原因是(用化学方程式表示)
。
⑵胃酸过多(主要是盐酸)的病人常常服用含氢氧化铝[Al(OH)]的药物,其原因是(用
3
化学方程式表示)
。
16、人的胃液里含有盐酸,胃病患者透视检查时,让患者口服不溶于盐酸的硫酸钡(俗称钡
餐)。但如果人吸收了可溶性的钡盐,就会发生中毒(这就是重金属盐中毒事件),试用
2化学方程式说明为什么误服碳酸钡会中毒的原因
。
17、从Fe、CaO、NaOH、HO、CuSO、NaCO、盐酸;共七种物质中,选择适当的反应物,按下列
2 4 2 3
要求写出相关的化学反应式:
⑴化合反应:___________________________________
⑵分解反应:___________________________________
⑶置换反应a:有气体生成___________________________________
b:有固体(金属单质)生成___________________________________
⑷复分解反应:a:中和反应___________________________________________
b:酸与盐的反应___________________________________________
c:碱与盐的反应___________________________________________
18、化学晚会上,小燊同学把一张纸的正反两面向大家展示清楚,然后
把白纸用电吹风的热风吹片刻,不一会,白纸上出现了一只小黑
猫,大家惊奇不已。你知道这是怎么回事吗?请你用学过的化学
知识来 解释:
⑴小梦事先用____________画了一只猫;
⑵使白纸出现黑猫的物质是______________;表现该物质具有____________性。
19、阅读材料并回答问题:材料一:通常食醋中含有 3%~5%的醋酸,醋酸的化学式为
CHCOOH,在温度高于16.7℃时是一种无色液体,易溶于水,醋酸具有酸的通性。
3
材料二:钙是人体的一种常用元素,人们每天必须摄入一定量的钙。动物骨头中含有磷
酸钙。但磷酸钙难溶于水,却能跟酸反应生成可溶性的钙盐。
⑴在10℃时,醋酸的状态是_____;
⑵生活中能否用铝制品来盛食醋?____ 原因_______________
_____
⑶人们在熬骨头汤时,常常会加入少量的醋,这样做的理由是___________
______
盐酸 氢氧化钙
20、右图是一种用于显示事物异同点的信息处理方法,其中两圆的重叠 [HCl] [Ca(OH) ]
2
区域表示物质的相似点,重叠区域以外的部分表示物质的不同点,请
写出图中处的适当内容(每处只要求写一个相似点或不同点)。
⑴_______________________________________________________
⑵_______________________________________________________
21、化学兴趣小组的同学采集了三种植物的花瓣,将它们分别放在研钵中研细,加入酒精充
分浸泡后过滤,得到三种溶液,将三种溶液分别加到下列液体中,得到以后信息:
在有关试剂中呈现的颜色
花的种类 所制成溶液颜色
白醋 蒸馏水 石灰水
玫瑰 粉红色 红色 粉红色 绿色
黄菊 黄色 黄色 黄色 黄色
雏菊 无色 无色 无色 黄色
试回答:⑴如果所制的溶液检验花盆中土壤的酸碱性,你会建议选择________花的酒精
3溶液来作酸碱指示剂:在以上三种酒精溶液中,酒精属于__________,(“溶质”或“溶
剂”)
⑵如果得知花盆中土壤显酸性,不适合花卉生长,若要进行改良,你认为选择上面表格中
的________来进行,写出主要成分的化学式__________。
三、我会实验探究
22、三种离子的检验(操作、现象、结论)
⑴溶液中含有氢离子(H+),检验的方法
___________________________________________________
⑵溶液中含有氢氧根离子(OH-),检验的方法
_______________________________________________
⑶溶液中含有碳酸根离子(CO2-),检验的方法
3
______________________________________________
23、“◇◇雪饼”袋内有一个小纸袋,上面写着“干燥剂”主要成分是生石灰。
⑴生石灰(CaO)可作干燥剂的理由是(用化学方程式表示)
_____________________________
⑵有人对它作了一系列探究,收获颇多。其实验方案发下:
问题与猜想 实验步骤 实验现象 结论
问题1:小纸袋
取足量小纸袋中的固体放入烧
中的物质能否继 不能作干
杯中,加入适量的水,触摸杯
续做干燥剂? 燥剂
壁
问题2:变质后
的物质可能是
______________
24、化学反应往往伴随着发生一些现象,但CO 与NaOH溶液反应没有明显现象发生。为了通
2
过一些现象说时CO 与NaOH溶液发生了反应,某班同学分组做了如下实验:
2
⑴第一组同学把一支收集有CO 的试管倒立在装有NaOH溶液的烧杯中(如右图所示),看
2
到试管内液面上升。这种现象是因为试管内外产生( )
A、温度差 B、重力差 C、压强差 D、浮力差
⑵第二组同学从中得到启发,也设计了如下实验装置进行探究:
4你认为能达到实验设计要求的是(填序号)_____
⑶同学们经过分析讨论,认为第一组实验中产生液面上升这种现象的原因可能有两种:
一种是因为CO 与NaOH溶液反应,消耗了CO:你认为另一种可能是________
2 2
_______
⑷为了进一步证实CO 与NaOH溶液发生了反应,请你设计一个实验验证(要求写出实验
2
步骤、现象和结论)
____________________________________
___________________________________
四、我会计算
25、10g石灰石与100g盐酸恰好完全反应,生成CO 质量为2.2g,求⑴求石灰石中CaCO 的
2 3
质量分数;⑵反应后所得溶液中溶质质量分数是多少?
解:
5第十单元 酸和碱 单元测试题 答案
一、我会选择 1-5 CABCD 6-10 CDDBD 11-12 B D 选做题 B
二、我会填空 13、⑴NaO ⑵HSO ⑶ NaOH ⑷NaSO
2 2 4 2 4
14、FeO FeO+6HCl=2FeCl+3HO 溶解 无 黄 Fe+2HCl=FeCl+H↑
2 3 2 3 3 2 2 2
15、⑴Mg(OH)+2HCl=MgCl+2HO CaCO+2HCl=CaCl+HO+CO↑
2 2 2 3 2 2 2
2Al+6HCl=2AlCl+3H↑ ⑵ Al(OH)+3HCl=AlCl+3HO
3 2 3 3 2
16、BaCO+2HCl=BaCl+HO+CO↑
3 2 2 2
17、⑴ CaO+HO=Ca(OH) (或CuSO+5HO=CuSO·5HO ) ⑵ 2HO 通电 2 H↑+O
2 2 4 2 4 2 2 2 2
↑
⑶ Fe+2HCl=FeCl+H Fe+CuSO=Cu+FeSO
2 2 4 4
⑷ 中和反应:HCl+NaOH=NaCl+HO 酸与盐的反应: 2HCl+NaCO=2NaCl+HO+
2 2 3 2
CO ↑
2
碱与盐的反应 2NaOH+CuSO=Cu(OH)↓+NaSO
4 2 2 4
18、⑴稀硫酸 ⑵浓硫酸 脱水性
19、⑴ 固态 ⑵不能 醋酸会与铝反应 ⑶醋与磷酸钙反应,生成可溶性的钙盐,便于
人体吸收
20、⑴ 组成上:都含有氢元素 性质上:都能使石蕊变色 或都能发生复分解反应
⑵ 组成上:氢氧化钙含有氢氧根离子 氢氧化钙能使酚酞变红 氢氧化钙能与CO
2
反应
21、玫瑰 溶剂 石灰水 Ca(OH)
2
22、⑴取待测溶液少许于试管中,滴入紫色石蕊,溶液变红,说明溶液中有氢离子。
⑵取待测溶液少许于试管中,滴入酚酞,溶液变红,说明溶液中有氢氧根离子
⑶取待测溶液少许于试管中,滴入稀HCl,有气泡产生,说明溶液中有碳酸根离子
23、⑴CaO+HO=Ca(OH) ⑵问题1: 杯壁温度无变化
2 2
问题2:可能是CaCO3,取少量固体,于试管中,加入稀HCl,有气体产生,则固体中有
CaCO。
3
(其他答案合理也给分)
24、⑴C ⑵ABC ⑶可能CO 溶于水 或可能是CO 与水反应
2 2
⑷向CO 与NaOH充分接触的溶液中,滴加稀HCl,若有气泡产生,则证明CO 与NaOH溶
2 2
液反应。(其他合理答案也给分)
25、解:设石灰石中CaCO 3 的质量为x 解:设生成CaCl 2 的质量为y
CaCO+2HCl=CaCl+HO+CO↑
CaCO
3
+2HCl=CaCl
2
+H
2
O+CO
2
↑ 3
111
2 2
44
2
100 44 y 2.2 g
=
x 2.2 g
y =5.55 g
= 反应后溶液的质量:
X=5 g
10g+100g-2.2 g-(10g-5g)=102.8g
CaCl%=×100%=5.4%
CaCO%=×100%=50% 2
3 答:略
6答:略
7