文档内容
第二章 晶体结构与性质
考点卷
核心知识1 物质聚集状态与晶体
核心知识2 晶胞及其计算
核心知识3 分子晶体
核心知识4 共价晶体
核心知识5 金属晶体
核心知识6 离子晶体
核心知识7 过渡晶体与混合型晶体
核心知识8 配合物与超分子
核心知识1 物质聚集状态与晶体
1.下列物质中,属于晶体的是
A.玻璃 B.石蜡和沥青 C.塑料 D.干冰
2.(2022·浙江丽水·高二期末)下列关于晶体和非晶体的说法不正确的是
A.破损的NaCl晶体能在饱和NaCl溶液中自动变成规则的立方体
B.晶体某些物理性质的各向异性反映了晶体内部质点排列的有序性
C.导电性可用于区别晶体和玻璃体
D.固体 可能是晶体,也可能是非晶体
3.(2022·广东清远·高二期末)下列关于晶体的说法中正确的是
A.自然形成的水晶柱是晶体,从水晶柱上切削下来的粉末不是晶体
B.晶胞中任何一个粒子都属于该晶胞
C.玻璃制成的弹珠具有规则的几何外形,所以玻璃弹珠是晶体
D.缺角的NaCl晶体在饱和NaCl溶液中慢慢变为完美的立方体块,体现了晶体的自范性
4.下列叙述中,正确的是
A.石英玻璃和水晶都是晶体
B.具有各向异性的固体可能是晶体
C.粉末状的固体肯定不是晶体
D.晶体与非晶体的根本区别在于固体是否具有规则的几何外形
5.金属玻璃是由金属元素或金属元素为主要成分的熔体通过快速冷却得到的具有非晶态结构的金属固体。
以下关于金属玻璃的说法正确的是
A.金属玻璃能自发呈现多面体外形
B.金属玻璃具有固定的熔点
C.鉴别金属玻璃是否为晶体最可靠的科学方法为X射线衍射实验D.金属玻璃是金属与二氧化硅的混合物
核心知识2 晶胞及其计算
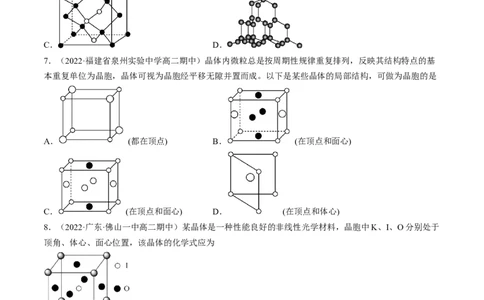
6.(2022·广东广州·高二期末)下列结构示意图中,表示晶胞的是
A. B.
C. D.
7.(2022·福建省泉州实验中学高二期中)晶体内微粒总是按周期性规律重复排列,反映其结构特点的基
本重复单位为晶胞,晶体可视为晶胞经平移无隙并置而成。以下是某些晶体的局部结构,可做为晶胞的是
A. (都在顶点) B. (在顶点和面心)
C. (在顶点和面心) D. (在顶点和体心)
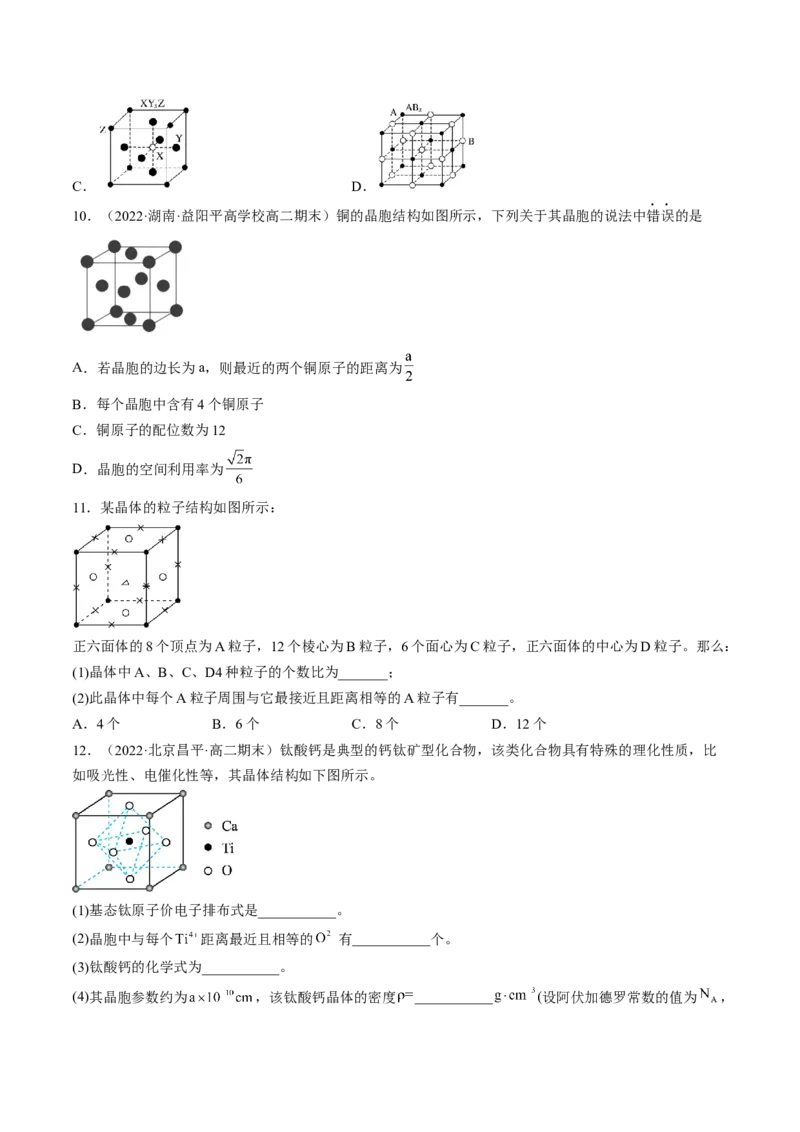
8.(2022·广东·佛山一中高二期中)某晶体是一种性能良好的非线性光学材料,晶胞中K、I、O分别处于
顶角、体心、面心位置,该晶体的化学式应为
A.KIO B.KIO C.KIO D.KIO
2 3 4
9.现有四种晶体,其构成粒子(均为单原子核粒子)排列方式如下图所示,其化学式正确的是
A. B.C. D.
10.(2022·湖南·益阳平高学校高二期末)铜的晶胞结构如图所示,下列关于其晶胞的说法中错误的是
A.若晶胞的边长为a,则最近的两个铜原子的距离为
B.每个晶胞中含有4个铜原子
C.铜原子的配位数为12
D.晶胞的空间利用率为
11.某晶体的粒子结构如图所示:
正六面体的8个顶点为A粒子,12个棱心为B粒子,6个面心为C粒子,正六面体的中心为D粒子。那么:
(1)晶体中A、B、C、D4种粒子的个数比为_______;
(2)此晶体中每个A粒子周围与它最接近且距离相等的A粒子有_______。
A.4个 B.6个 C.8个 D.12个
12.(2022·北京昌平·高二期末)钛酸钙是典型的钙钛矿型化合物,该类化合物具有特殊的理化性质,比
如吸光性、电催化性等,其晶体结构如下图所示。
(1)基态钛原子价电子排布式是___________。
(2)晶胞中与每个 距离最近且相等的 有___________个。
(3)钛酸钙的化学式为___________。
(4)其晶胞参数约为 ,该钛酸钙晶体的密度 ___________ (设阿伏加德罗常数的值为 ,用含a、 的代数式表示)
核心知识3 分子晶体
13.下列关于分子晶体的说法不正确的是
A.分子晶体中含有分子
B.固态或熔融态时均能导电
C.分子间以分子间作用力相结合
D.熔、沸点一般比较低
14.(2022·广东云浮·高二期末)下列物质中,属于含有非极性共价键的分子晶体的是
A.Si B.HCl C.N D.NH Cl
2 4
15.(2022·北京市宣武外国语实验学校高二期中)下列有关冰和干冰的叙述不正确的是
A.干冰和冰都是由分子密堆积形成的晶体
B.冰中存在氢键,每个水分子周围有4个紧邻的水分子
C.干冰比冰的熔点低,常压下易升华
D.干冰中只存在范德华力不存在氢键
16.下列关于CH 和CO 的说法错误的是
4 2
A.固态时两者均属于分子晶体
B.CH 分子中含有极性共价键是非极性分子
4
C.CH 和CO 分子中碳原子的杂化类型分别是sp3和sp
4 2
D.因为碳氢键键能小于碳氧双键,所以CH 的熔点低于CO
4 2
17.(2022·新疆·乌市八中高二期末)下列说法正确的是
A.分子晶体中一定存在分子间作用力,不一定存在共价键
B.水加热到很高的温度都难以分解,与氢键有关
C. 晶体是分子晶体,分子间通过共价键结合
D.HF、 的沸点随着相对分子质量的增大依次升高
18.下列有关分子晶体的说法正确的有
①分子晶体的构成微粒是分子,都具有分子密堆积的特征
②冰融化时,分子中H-O键发生断裂
③分子晶体在水溶液中均能导电
④分子晶体中,分子间作用力越大,通常熔点越高
⑤分子晶体中,共价键键能越大,该分子晶体的沸点一定越高
⑥所有的非金属氢化物都是分子晶体
⑦所有分子晶体中既存在分子间作用力又存在化学键
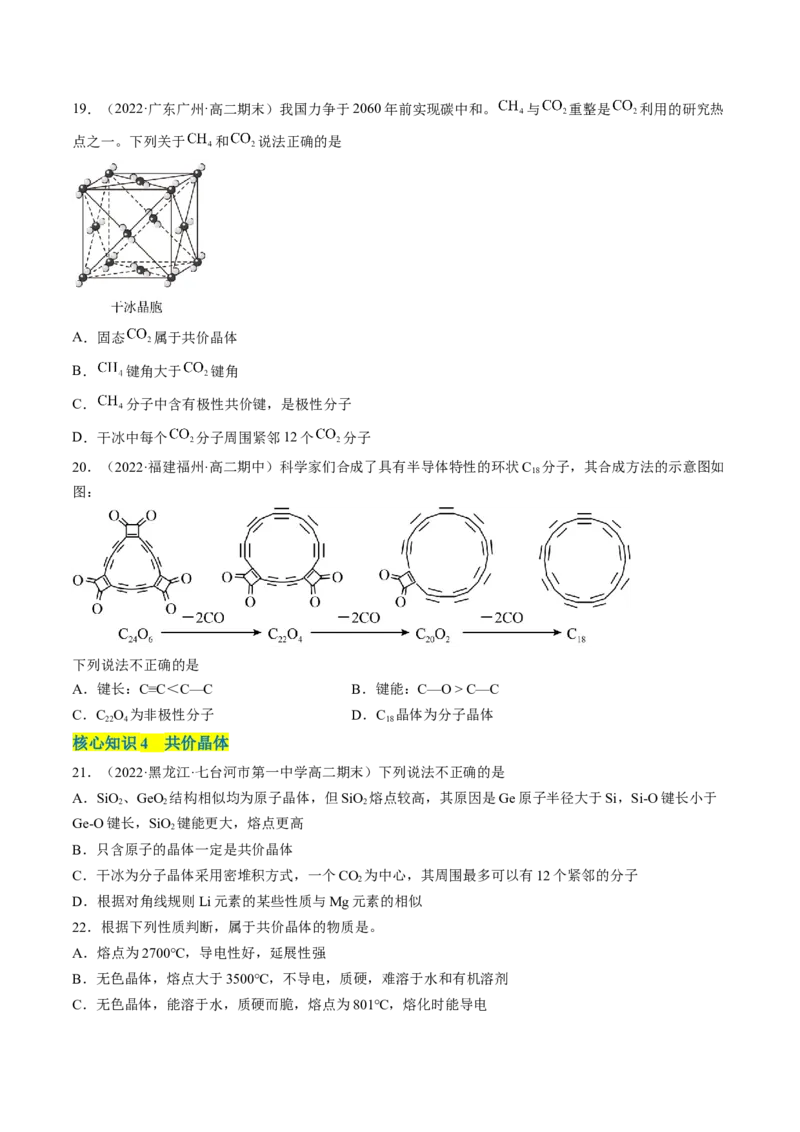
A.1项 B.2项 C.3项 D.4项19.(2022·广东广州·高二期末)我国力争于2060年前实现碳中和。 与 重整是 利用的研究热
点之一。下列关于 和 说法正确的是
A.固态 属于共价晶体
B. 键角大于 键角
C. 分子中含有极性共价键,是极性分子
D.干冰中每个 分子周围紧邻12个 分子
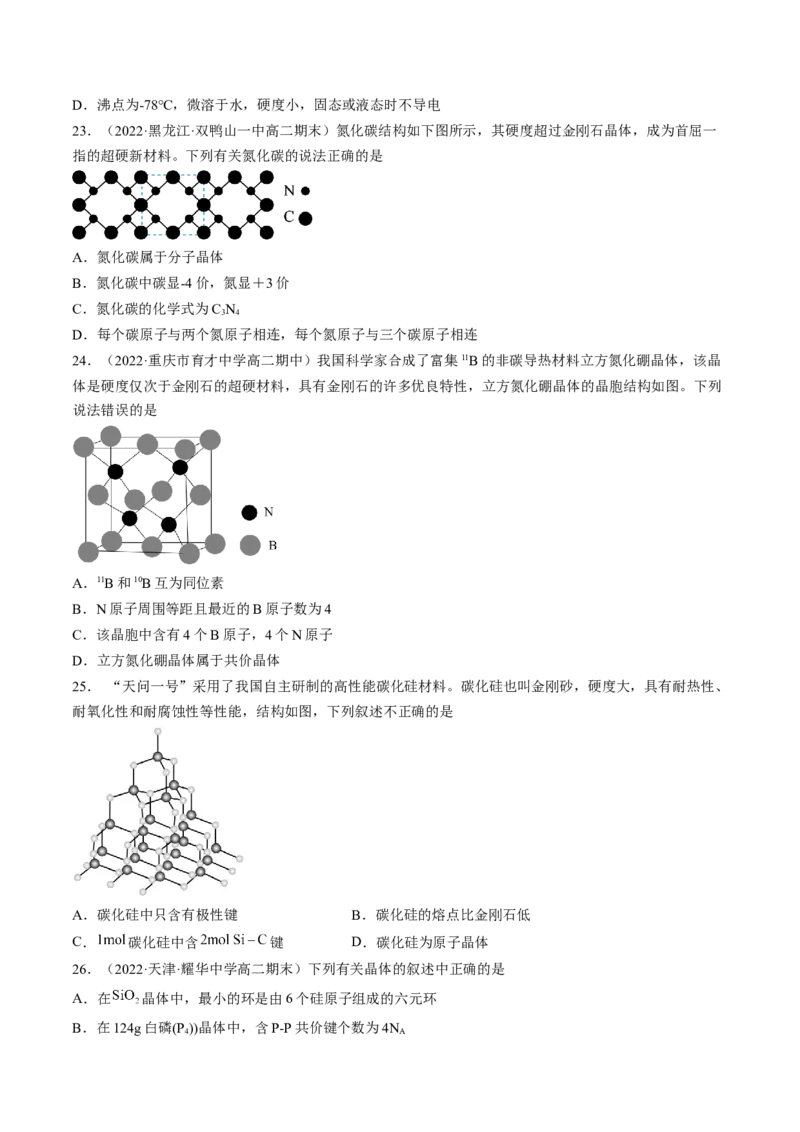
20.(2022·福建福州·高二期中)科学家们合成了具有半导体特性的环状C 分子,其合成方法的示意图如
18
图:
下列说法不正确的是
A.键长:C≡C<C—C B.键能:C—O > C—C
C.C O 为非极性分子 D.C 晶体为分子晶体
22 4 18
核心知识4 共价晶体
21.(2022·黑龙江·七台河市第一中学高二期末)下列说法不正确的是
A.SiO、GeO 结构相似均为原子晶体,但SiO 熔点较高,其原因是Ge原子半径大于Si,Si-O键长小于
2 2 2
Ge-O键长,SiO 键能更大,熔点更高
2
B.只含原子的晶体一定是共价晶体
C.干冰为分子晶体采用密堆积方式,一个CO 为中心,其周围最多可以有12个紧邻的分子
2
D.根据对角线规则Li元素的某些性质与Mg元素的相似
22.根据下列性质判断,属于共价晶体的物质是。
A.熔点为2700℃,导电性好,延展性强
B.无色晶体,熔点大于3500℃,不导电,质硬,难溶于水和有机溶剂
C.无色晶体,能溶于水,质硬而脆,熔点为801℃,熔化时能导电D.沸点为-78℃,微溶于水,硬度小,固态或液态时不导电
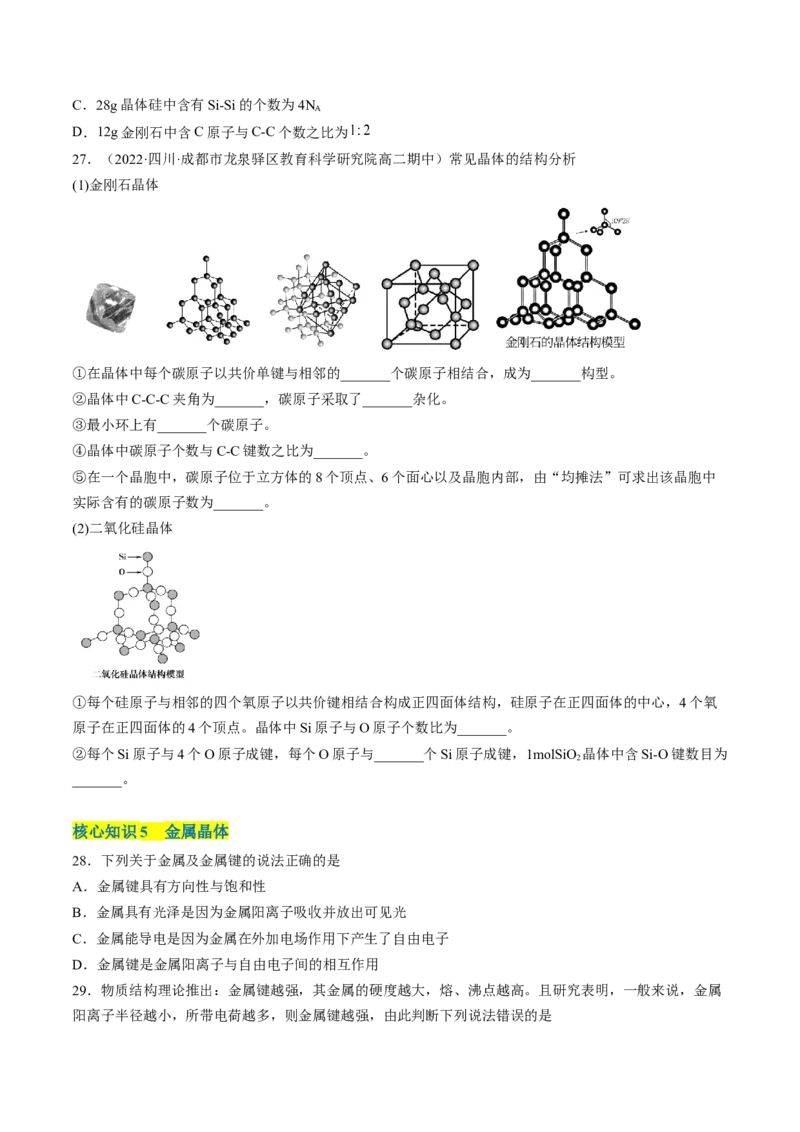
23.(2022·黑龙江·双鸭山一中高二期末)氮化碳结构如下图所示,其硬度超过金刚石晶体,成为首屈一
指的超硬新材料。下列有关氮化碳的说法正确的是
A.氮化碳属于分子晶体
B.氮化碳中碳显-4价,氮显+3价
C.氮化碳的化学式为C N
3 4
D.每个碳原子与两个氮原子相连,每个氮原子与三个碳原子相连
24.(2022·重庆市育才中学高二期中)我国科学家合成了富集11B的非碳导热材料立方氮化硼晶体,该晶
体是硬度仅次于金刚石的超硬材料,具有金刚石的许多优良特性,立方氮化硼晶体的晶胞结构如图。下列
说法错误的是
A.11B和10B互为同位素
B.N原子周围等距且最近的B原子数为4
C.该晶胞中含有4个B原子,4个N原子
D.立方氮化硼晶体属于共价晶体
25. “天问一号”采用了我国自主研制的高性能碳化硅材料。碳化硅也叫金刚砂,硬度大,具有耐热性、
耐氧化性和耐腐蚀性等性能,结构如图,下列叙述不正确的是
A.碳化硅中只含有极性键 B.碳化硅的熔点比金刚石低
C. 碳化硅中含 键 D.碳化硅为原子晶体
26.(2022·天津·耀华中学高二期末)下列有关晶体的叙述中正确的是
A.在 晶体中,最小的环是由6个硅原子组成的六元环
B.在124g白磷(P ))晶体中,含P-P共价键个数为4N
4 AC.28g晶体硅中含有Si-Si的个数为4N
A
D.12g金刚石中含C原子与C-C个数之比为
27.(2022·四川·成都市龙泉驿区教育科学研究院高二期中)常见晶体的结构分析
(1)金刚石晶体
①在晶体中每个碳原子以共价单键与相邻的_______个碳原子相结合,成为_______构型。
②晶体中C-C-C夹角为_______,碳原子采取了_______杂化。
③最小环上有_______个碳原子。
④晶体中碳原子个数与C-C键数之比为_______。
⑤在一个晶胞中,碳原子位于立方体的8个顶点、6个面心以及晶胞内部,由“均摊法”可求出该晶胞中
实际含有的碳原子数为_______。
(2)二氧化硅晶体
①每个硅原子与相邻的四个氧原子以共价键相结合构成正四面体结构,硅原子在正四面体的中心,4个氧
原子在正四面体的4个顶点。晶体中Si原子与O原子个数比为_______。
②每个Si原子与4个O原子成键,每个O原子与_______个Si原子成键,1molSiO 晶体中含Si-O键数目为
2
_______。
核心知识5 金属晶体
28.下列关于金属及金属键的说法正确的是
A.金属键具有方向性与饱和性
B.金属具有光泽是因为金属阳离子吸收并放出可见光
C.金属能导电是因为金属在外加电场作用下产生了自由电子
D.金属键是金属阳离子与自由电子间的相互作用
29.物质结构理论推出:金属键越强,其金属的硬度越大,熔、沸点越高。且研究表明,一般来说,金属
阳离子半径越小,所带电荷越多,则金属键越强,由此判断下列说法错误的是A.硬度:Mg>Al B.熔点:Mg>Ca
C.硬度:Mg>K D.熔点:Ca>K
30.(2022·陕西西安·高二期末)金属晶体的堆积方式、空间利用率和配位数关系正确的是
A.锌 ——镁型——68%——8 B.钠 ——钾型——74%——12
C.钋 ——简单立方堆积——52%——6 D.银 ——铜型——74%——8
31.下图是金属晶体内部的电子气理论示意图。电子气理论可以用来解释金属的性质,其中正确的是
A.金属能导电是因为金属阳离子在外加电场作用下定向移动
B.金属能导热是因为自由电子在热的作用下相互碰撞,从而发生热的传导
C.金属具有延展性是因为在外力的作用下,金属中各原子层间会出现相对滑动,但自由电子可以起到润
滑剂的作用,使金属不会断裂
D.合金与纯金属相比,由于增加了不同的金属或非金属,使电子数目增多,所以合金的延展性比纯金属
强,硬度比纯金属小
32.金晶体采用面心立方最密堆积方式,其晶胞如图所示。设金原子的直径为d,用N 表示阿伏加德罗常
A
数的值,M表示金的摩尔质量。则下列说法错误的是
A.每个晶胞中含有4个Au原子
B.金属键无方向性,金属原子尽可能采取紧密堆积
C.一个晶胞的体积是16 d3
D.晶体中Au的配位数为12
33.回答下列问题:
(1)将等径圆球在二维空间里进行排列,可形成密置层和非密置层,在如图所示的半径相等的圆球的排列中,
A属于___________层,配位数是___________;B属于___________层,配位数是___________。(2)辽宁号航母飞行甲板等都是由铁及其合金制造的。铁有 三种同素异形体,其晶胞结构如图所示。
① 、 晶胞中含有的铁原子数之比为___________。
② 、 两种晶体中铁原子的配位数之比为___________。
③若 晶胞的边长为a cm, 晶胞的边长为b cm,则两种晶体的密度之比为___________。
核心知识6 离子晶体
34.(2022·江苏·响水县第二中学高二期中)关于晶体的下列说法正确的是
A.任何晶体中,若含有阳离子就一定有阴离子
B.氯化钠溶于水时晶体中的离子键被破坏
C.晶体中分子间作用力越大,分子越稳定
D.离子晶体中只含有离子键,不含有共价键
35.(2022·新疆·乌鲁木齐市第三十一中学高二期中)下列有关离子晶体的叙述错误的是
A. 氯化钠晶体中有 个 分子
B.氯化钠晶体中,每个 周围与它距离相等且最近的 有 个
C.氯化铯晶体中,每个 周围紧邻 个
D.平均每个 晶胞中有 个 、 个
36.(2022·新疆兵团农六师芳草湖农场中学高二期末)下面的排序不正确的是
A.晶体沸点由低到高:CF<CCl <CBr B.晶格能由大到小: NaF> NaCl> NaBr
4 4 4
C.硬度由大到小:金刚石>碳化硅>晶体硅D.熔点由高到低:Na>Mg>Al
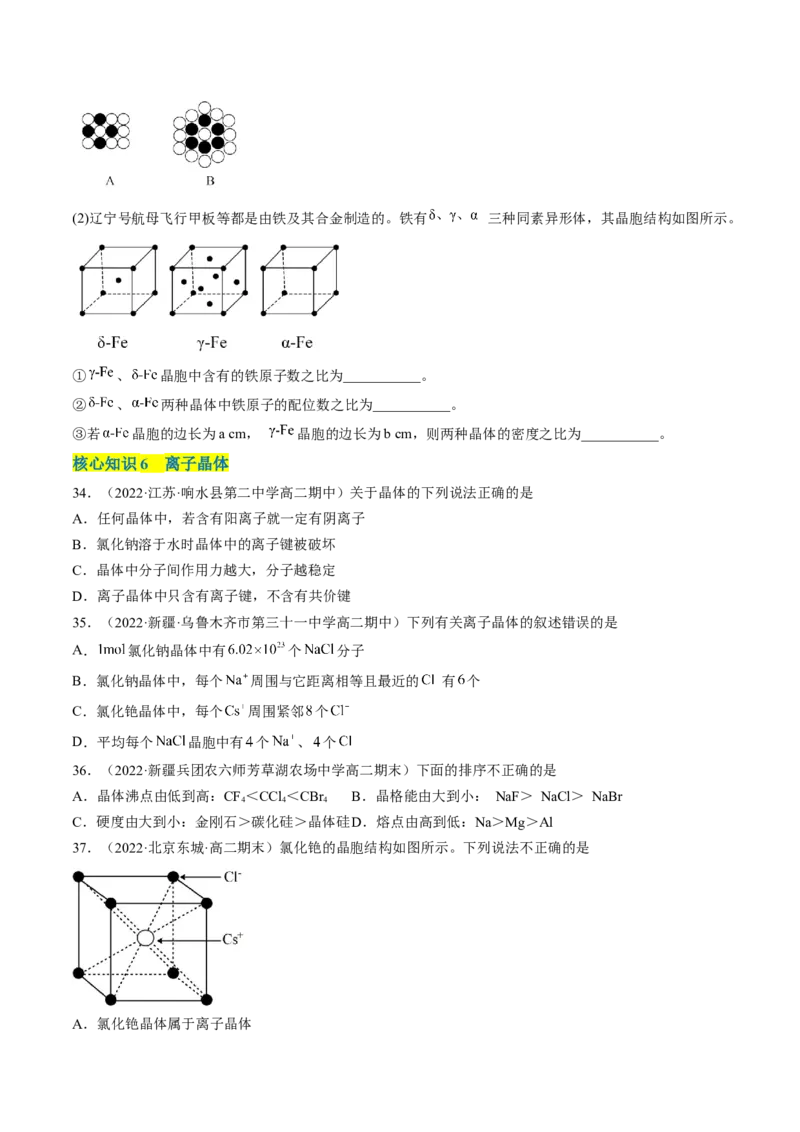
37.(2022·北京东城·高二期末)氯化铯的晶胞结构如图所示。下列说法不正确的是
A.氯化铯晶体属于离子晶体B.氯化铯晶胞中有3套平行棱,3套平行面
C.在氯化铯晶体中,每个Cl-周围紧邻1个Cs+
D.在氯化铯晶体中,每个Cs+周围与它最近且等距离的Cs+共有6个
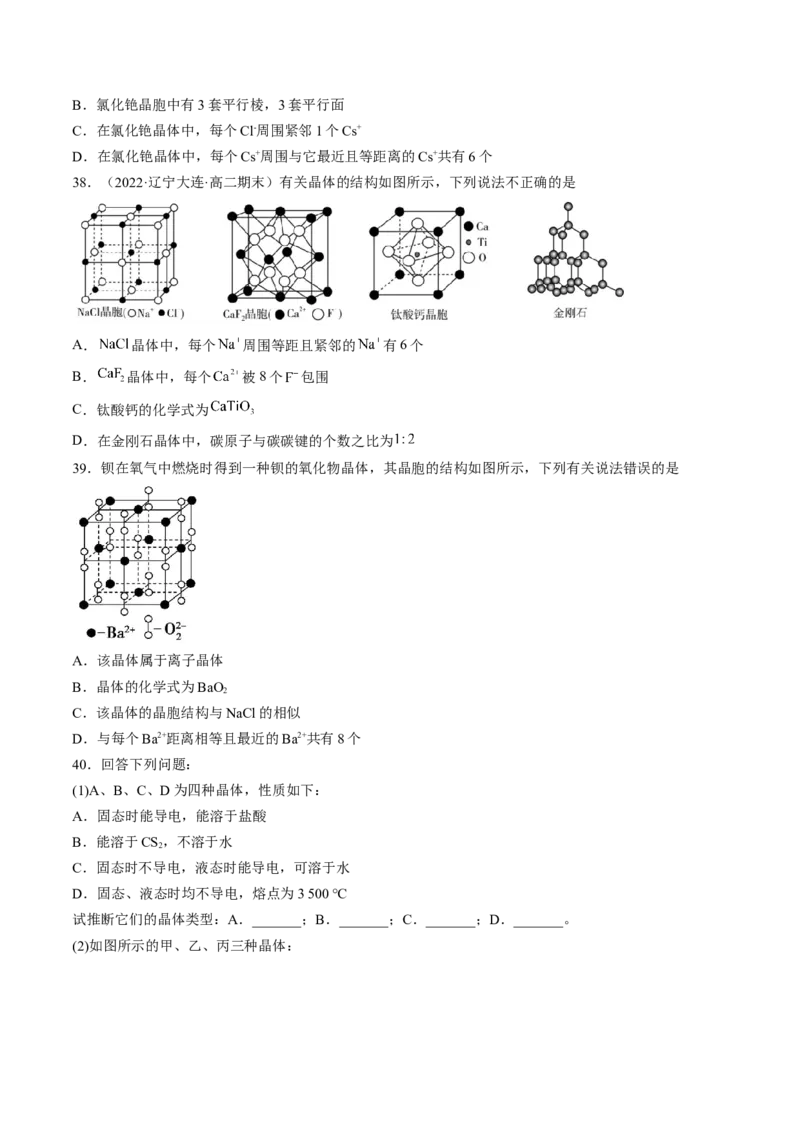
38.(2022·辽宁大连·高二期末)有关晶体的结构如图所示,下列说法不正确的是
A. 晶体中,每个 周围等距且紧邻的 有6个
B. 晶体中,每个 被8个 包围
C.钛酸钙的化学式为
D.在金刚石晶体中,碳原子与碳碳键的个数之比为
39.钡在氧气中燃烧时得到一种钡的氧化物晶体,其晶胞的结构如图所示,下列有关说法错误的是
A.该晶体属于离子晶体
B.晶体的化学式为BaO
2
C.该晶体的晶胞结构与NaCl的相似
D.与每个Ba2+距离相等且最近的Ba2+共有8个
40.回答下列问题:
(1)A、B、C、D为四种晶体,性质如下:
A.固态时能导电,能溶于盐酸
B.能溶于CS,不溶于水
2
C.固态时不导电,液态时能导电,可溶于水
D.固态、液态时均不导电,熔点为3 500 ℃
试推断它们的晶体类型:A._______;B._______;C._______;D._______。
(2)如图所示的甲、乙、丙三种晶体:试推断,甲晶体的化学式(X为阳离子):_______;
乙晶体中A、B、C三种微粒的个数比是_______;丙晶体中每个D周围结合E的个数是_______。
核心知识7 过渡晶体与混合型晶体
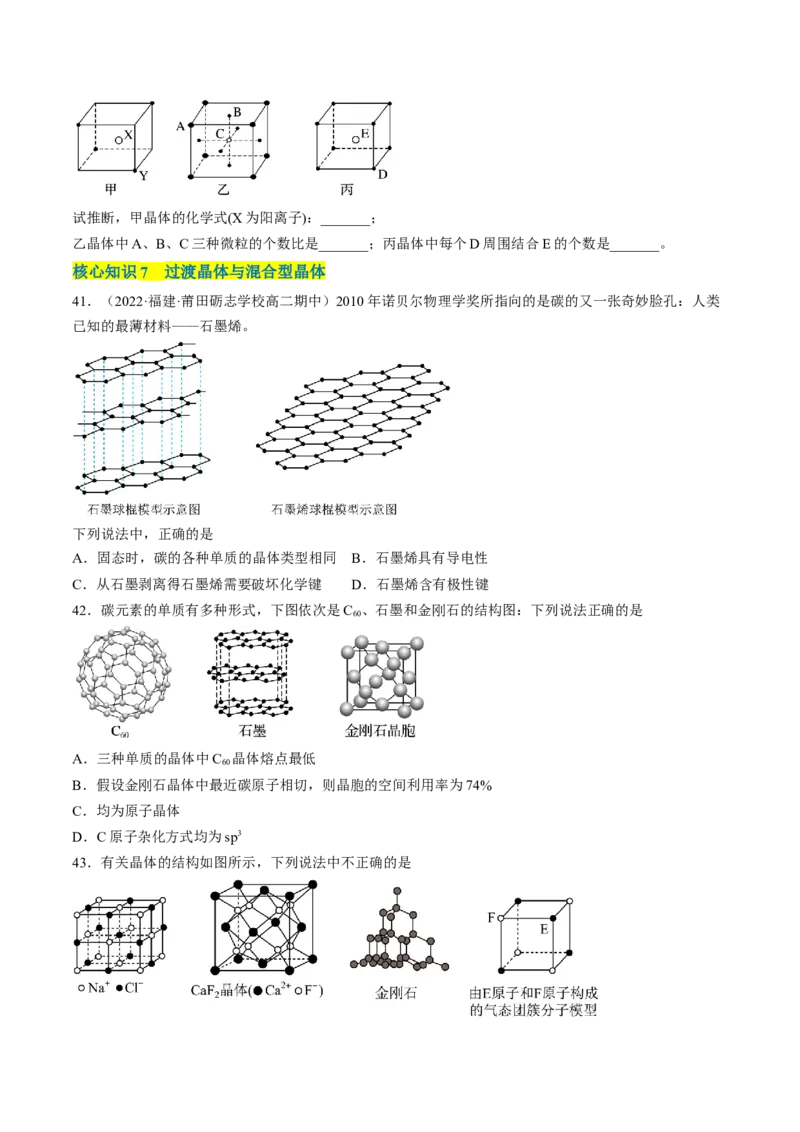
41.(2022·福建·莆田砺志学校高二期中)2010年诺贝尔物理学奖所指向的是碳的又一张奇妙脸孔:人类
已知的最薄材料——石墨烯。
下列说法中,正确的是
A.固态时,碳的各种单质的晶体类型相同 B.石墨烯具有导电性
C.从石墨剥离得石墨烯需要破坏化学键 D.石墨烯含有极性键
42.碳元素的单质有多种形式,下图依次是C 、石墨和金刚石的结构图:下列说法正确的是
60
A.三种单质的晶体中C 晶体熔点最低
60
B.假设金刚石晶体中最近碳原子相切,则晶胞的空间利用率为74%
C.均为原子晶体
D.C原子杂化方式均为sp3
43.有关晶体的结构如图所示,下列说法中不正确的是A.在NaCl晶体中,距Cl—最近的Na+形成正八面体
B.在CaF 晶体中,每个晶胞平均含有4个Ca2+
2
C.在金刚石晶体中,碳原子与碳碳键个数的比为1∶2
D.该气态团簇分子的分子式为EF
44.完成下列问题。
(1)石墨晶体由层状石墨“分子”按ABAB……方式堆积而成,如图甲所示,图中用虚线标出了石墨的一个
六方晶胞。该晶胞中含有的碳原子数为_______。
(2)石墨烯是一种由单层碳原子构成的平面结构新型碳材料,如图乙所示。设N 为阿伏加德罗常数的值,
A
1mol石墨烯中含有的六元环个数为_______。下列有关石墨烯的说法正确的是_______(填字母)。
a.晶体中碳原子间全部是单键
b.石墨烯中所有碳原子可以处于同一个平面
c.从石墨中剥离得到石墨烯需克服分子间作用力
(3)石墨烯可转化为 , 的结构如图丙所示,该分子是由五边形和六边形构成的球体,其中五边形有
12个,则六边形有_______个(注:简单多面体的顶点数V、面数F及棱数E间的关系为 )。
(4)金刚石晶胞如图丁所示,则金刚石晶胞中原子的配位数为_______。核心知识8 配合物与超分子
45.下列关于超分子的叙述中正确的是
A.超分子就是高分子 B.超分子都是无限伸展的
C.形成超分子的微粒都是分子 D.超分子具有分子识别和自组装的特征
46.下列配合物的水溶液中加入硝酸银不能生成沉淀的是
A. B.
C. D.
47.配合物 可用于离子检验,下列说法不正确的是
A.此配合物中存在离子键、配位键、极性键、非极性键
B.配体为CN-,与N、CO互为等电子体
2
C.1mol配合物中 键数目为
D.该配合物为离子化合物,易电离,1mol该配合物电离得到阴、阳离子的数目共
48.利用超分子可分离 和 。将 、 混合物加入一种空腔大小适配 的杯酚中进行分离的流程
如图所示。
下列说法错误的是
A.该流程体现了超分子具有“分子识别”的特征
B.杯酚分子中存在大 键
C.杯酚与 形成氢键
D. 与金刚石晶体类型不同
49.配合物[Cu(NH )](OH) 的中心离子、配体、中心离子的电荷数和配位数分别为
3 4 2
A.Cu2+、OH-、2+、2 B.Cu+、NH 、1+、4
3
C.Cu2+、NH 、2+、4 D.Cu2+、NH 、2+、2
3 3
50.许多过渡金属离子对多种配体有很强结合力,能形成种类繁多的配合物。下列说法错误的是
A.CuSO 溶液呈蓝色,是由于存在配离子[Cu(H O) ]2+
4 2 4
B.配合物[PtCl (NH )]为平面结构,存在顺反异构体
2 3 2
C.配合物[Ti(OH) (H O) ]2+中Ti4+的配位数是4
4 2 2D.向配合物[TiCl(H O) ]Cl ·H O溶液中加入足量AgNO 溶液,只有 的Cl-被沉淀
2 5 2 2 3
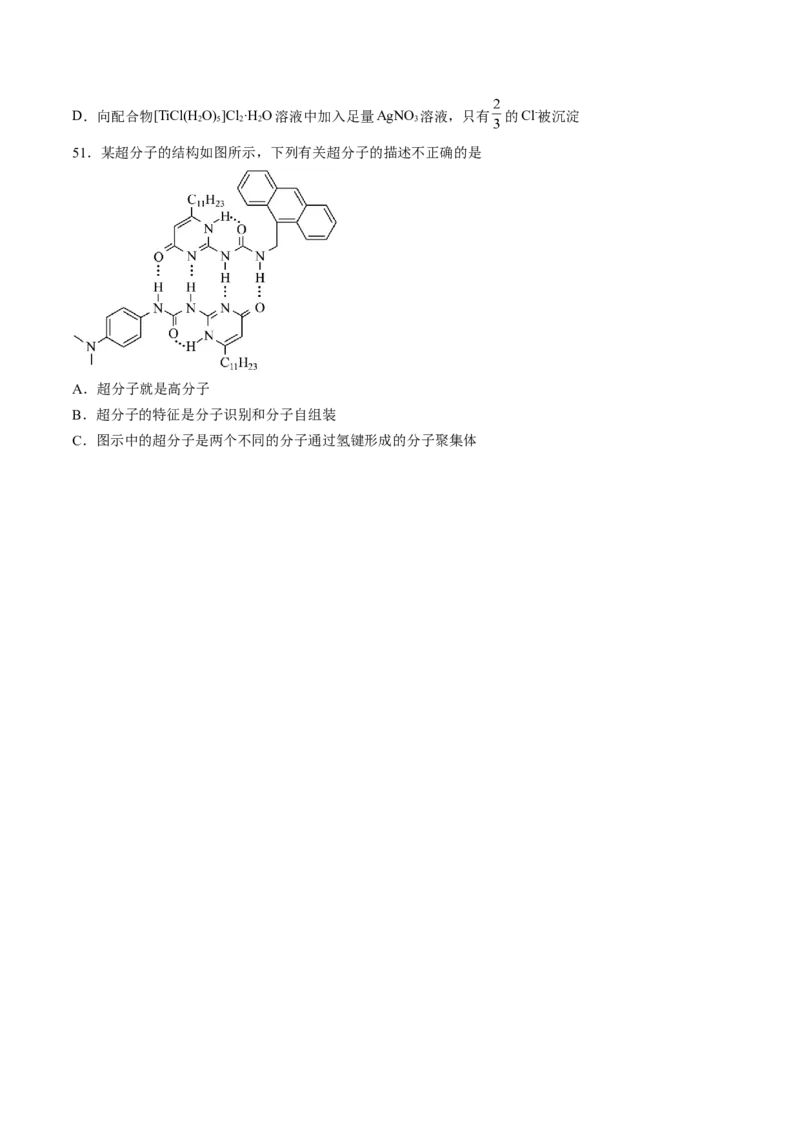
51.某超分子的结构如图所示,下列有关超分子的描述不正确的是
A.超分子就是高分子
B.超分子的特征是分子识别和分子自组装
C.图示中的超分子是两个不同的分子通过氢键形成的分子聚集体