文档内容
本部分共10小题,每小题1.5分,共15分。在每小题给出的四个选项中,只有一项符合题目要求。
1.下列化学用语表示正确的是
A.五氧化二磷的化学式:PO B.硅的元素符号:SI
2 5
C.碳酸根离子:CO D.三个氧原子:O
3 3
2.化学与生产、生活密切相关。下列说法错误的是
A.干冰可作制冷剂,广泛用于食品冷藏保鲜
B.N 、NO、NO 等含氮物质均为空气污染物
2 2
C.明矾溶于水的胶状物可吸附杂质,达到净水的目的
D.废旧电池的分类回收有利于保护环境
3.规范的实验操作是安全地进行实验并获得成功的保证。下列实验操作正确的是
4.下列说法中正确的是
A.检验电解水的产物,可判断水的组成元素
B.将pH试纸用水湿润后,测定柠檬汁的pH
C.凡是无色的、均一的液体一定是溶液
D.硫在O 中燃烧发出淡蓝色火焰,生成SO
2 3
5.碘是人体必需的微量元素之一,有“智力元素”之称。下图为碘在元素周期表中的相关信息及原子结构示
意图,据此判断下列说法正确的是
A.碘是一种金属元素 B.碘原子的核外有7个电子层
C.碘原子的核电荷数为53 D.碘的相对原子质量为126.9g6.丙氨酸是一种常见的氨基酸,其化学式为C HON,相对分子质量是89.下列说法正确的是
3 x 2
A.丙氨酸属于无机化合物 B.丙氨酸中碳、氮元素的质量比为3:1
C.丙氨酸化学式中x=7 D.每个丙氨酸分子中含有一个氧气分子
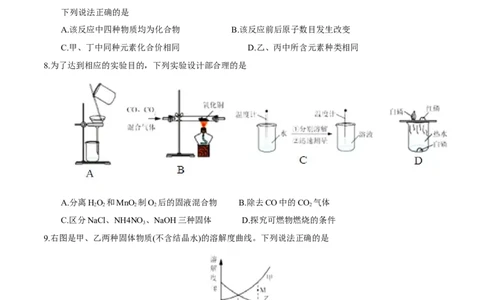
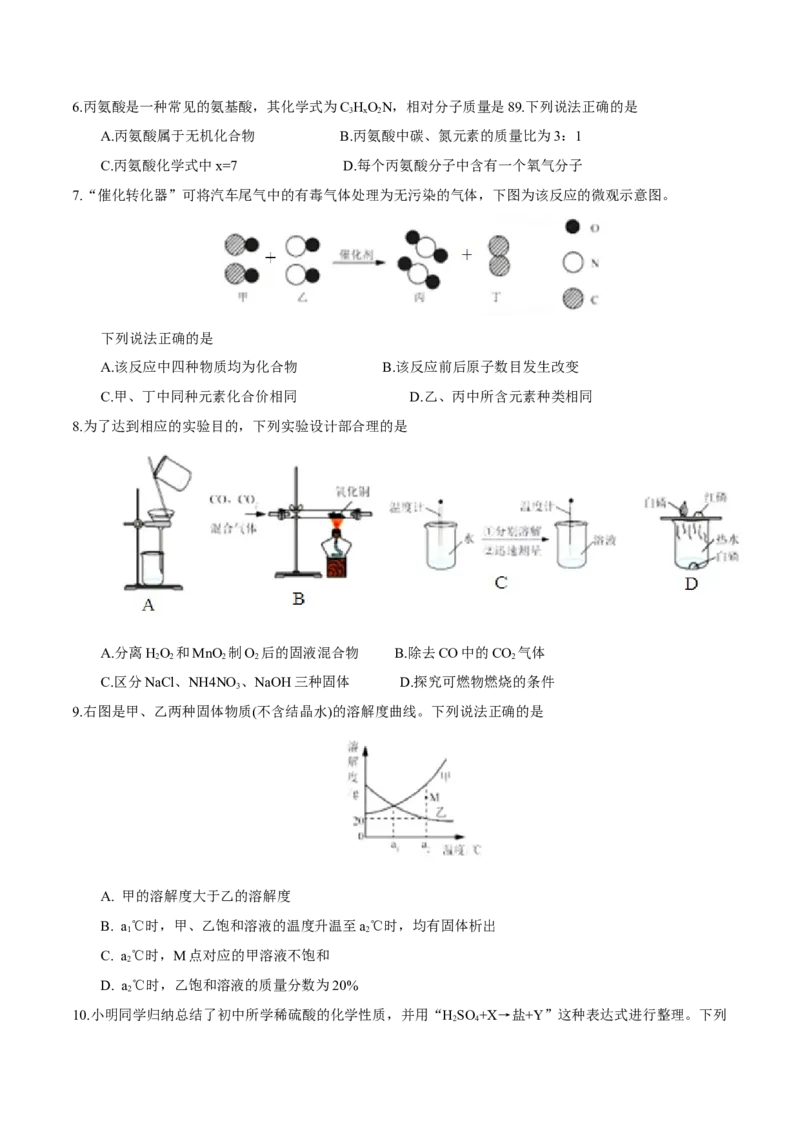
7.“催化转化器”可将汽车尾气中的有毒气体处理为无污染的气体,下图为该反应的微观示意图。
下列说法正确的是
A.该反应中四种物质均为化合物 B.该反应前后原子数目发生改变
C.甲、丁中同种元素化合价相同 D.乙、丙中所含元素种类相同
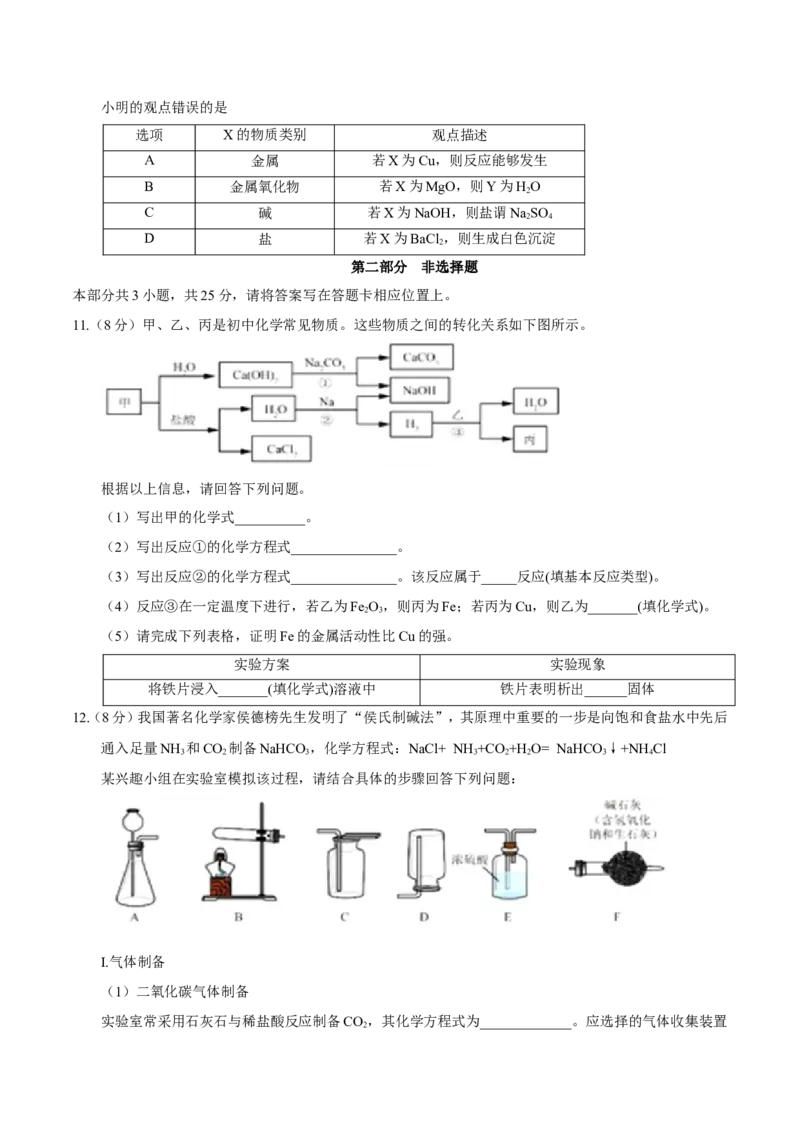
8.为了达到相应的实验目的,下列实验设计部合理的是
A.分离HO 和MnO 制O 后的固液混合物 B.除去CO中的CO 气体
2 2 2 2 2
C.区分NaCl、NH4NO 、NaOH三种固体 D.探究可燃物燃烧的条件
3
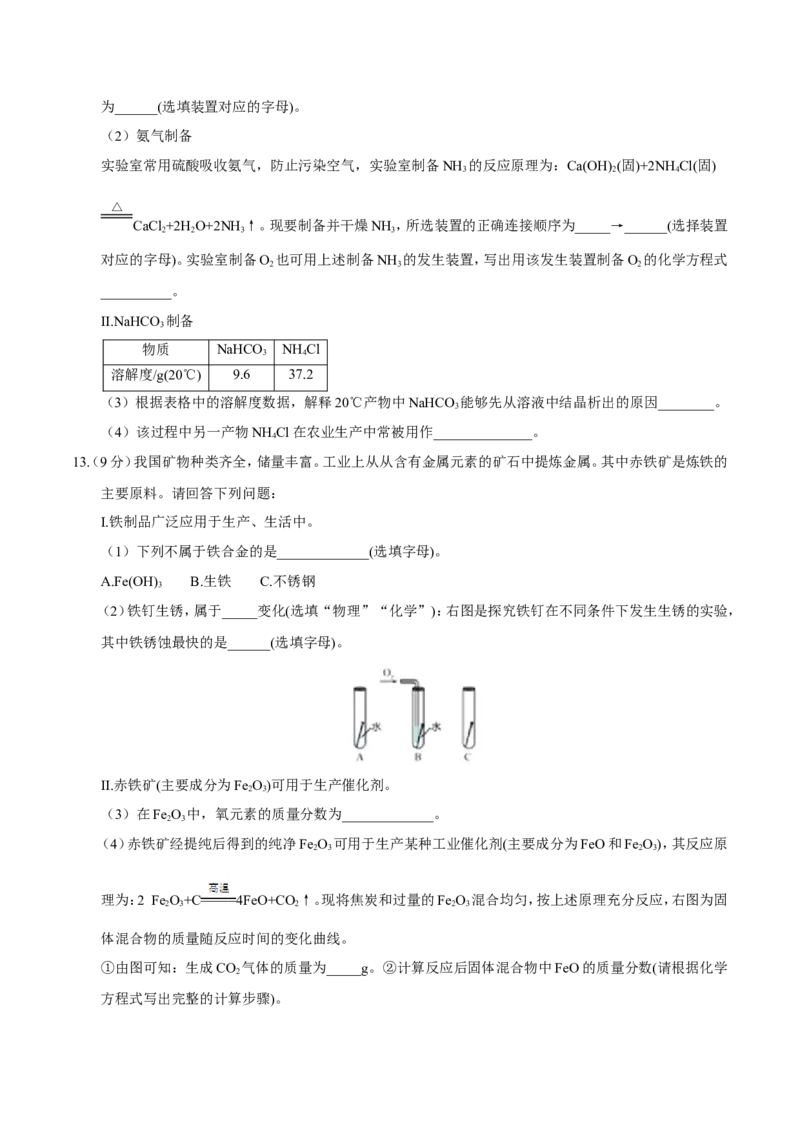
9.右图是甲、乙两种固体物质(不含结晶水)的溶解度曲线。下列说法正确的是
A. 甲的溶解度大于乙的溶解度
B. a℃时,甲、乙饱和溶液的温度升温至a℃时,均有固体析出
1 2
C. a℃时,M点对应的甲溶液不饱和
2
D. a℃时,乙饱和溶液的质量分数为20%
2
10.小明同学归纳总结了初中所学稀硫酸的化学性质,并用“HSO +X→盐+Y”这种表达式进行整理。下列
2 4小明的观点错误的是
选项 X的物质类别 观点描述
A 金属 若X为Cu,则反应能够发生
B 金属氧化物 若X为MgO,则Y为HO
2
C 碱 若X为NaOH,则盐谓NaSO
2 4
D 盐 若X为BaCl ,则生成白色沉淀
2
第二部分 非选择题
本部分共3小题,共25分,请将答案写在答题卡相应位置上。
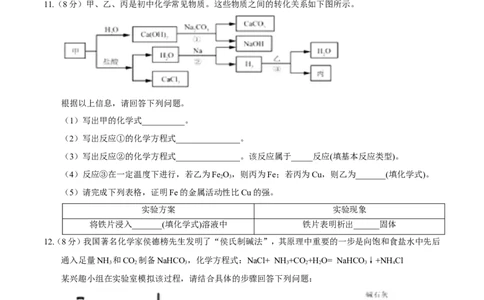
11.(8分)甲、乙、丙是初中化学常见物质。这些物质之间的转化关系如下图所示。
根据以上信息,请回答下列问题。
(1)写出甲的化学式__________。
(2)写出反应①的化学方程式_______________。
(3)写出反应②的化学方程式_______________。该反应属于_____反应(填基本反应类型)。
(4)反应③在一定温度下进行,若乙为Fe O,则丙为Fe;若丙为Cu,则乙为_______(填化学式)。
2 3
(5)请完成下列表格,证明Fe的金属活动性比Cu的强。
实验方案 实验现象
将铁片浸入_______(填化学式)溶液中 铁片表明析出______固体
12.(8分)我国著名化学家侯德榜先生发明了“侯氏制碱法”,其原理中重要的一步是向饱和食盐水中先后
通入足量NH 和CO 制备NaHCO ,化学方程式:NaCl+ NH +CO +H O= NaHCO ↓+NHCl
3 2 3 3 2 2 3 4
某兴趣小组在实验室模拟该过程,请结合具体的步骤回答下列问题:
I.气体制备
(1)二氧化碳气体制备
实验室常采用石灰石与稀盐酸反应制备CO,其化学方程式为_____________。应选择的气体收集装置
2为______(选填装置对应的字母)。
(2)氨气制备
实验室常用硫酸吸收氨气,防止污染空气,实验室制备NH 的反应原理为:Ca(OH) (固)+2NHCl(固)
3 2 4
△
CaCl +2H O+2NH ↑。现要制备并干燥NH ,所选装置的正确连接顺序为_____→______(选择装置
2 2 3 3
对应的字母)。实验室制备O 也可用上述制备NH 的发生装置,写出用该发生装置制备O 的化学方程式
2 3 2
__________。
II.NaHCO 制备
3
物质 NaHCO NH Cl
3 4
溶解度/g(20℃) 9.6 37.2
(3)根据表格中的溶解度数据,解释20℃产物中NaHCO 能够先从溶液中结晶析出的原因________。
3
(4)该过程中另一产物NH Cl在农业生产中常被用作______________。
4
13(. 9分)我国矿物种类齐全,储量丰富。工业上从从含有金属元素的矿石中提炼金属。其中赤铁矿是炼铁的
主要原料。请回答下列问题:
I.铁制品广泛应用于生产、生活中。
(1)下列不属于铁合金的是_____________(选填字母)。
A.Fe(OH) B.生铁 C.不锈钢
3
(2)铁钉生锈,属于_____变化(选填“物理”“化学”):右图是探究铁钉在不同条件下发生生锈的实验,
其中铁锈蚀最快的是______(选填字母)。
II.赤铁矿(主要成分为Fe O)可用于生产催化剂。
2 3
(3)在Fe O 中,氧元素的质量分数为_____________。
2 3
(4)赤铁矿经提纯后得到的纯净Fe O 可用于生产某种工业催化剂(主要成分为FeO和Fe O),其反应原
2 3 2 3
理为:2 Fe O+C 4FeO+CO↑。现将焦炭和过量的Fe O 混合均匀,按上述原理充分反应,右图为固
2 3 2 2 3
体混合物的质量随反应时间的变化曲线。
①由图可知:生成CO 气体的质量为_____g。②计算反应后固体混合物中FeO的质量分数(请根据化学
2
方程式写出完整的计算步骤)。1-5:ABDAC 6-10:CDBCA
11.(1)CaO;(2)Ca(OH) +Na CO=CaCO ↓+2NaOH;
2 2 3 3
(3)2Na+2HO=2NaOH+H ↑;置换;(4)CuO;(5)CuSO (或CuCl );红色。
2 2 4 2
12.(1)CaCO +2HCl=CaCl +H O+CO↑;C;
3 2 2 2
(2)B;F;2KClO MnO2 2 KCl+3O ↑;(3)20℃时NaHCO 的溶解度小;(4)氮肥。
3 2 3
△
13.(1)A;(2)化学;B;(3)30%;(4)①1.1;②36%。