文档内容
化学模拟试题 ( 一 )
[时间:60分钟 满分:50分]
可能用到的相对原子量:H-1 O-16 C-12 Na-23 Cl-35.5
一、选择题(下列各题的四个选项中只有一个符合题意。共15小题,每小题1分,共15分)[来源:学科网]
1.下列变化中,不属于化学变化的是( )
A.气球充入过量空气发生爆炸
B.水通电分解
C.铁钉在潮湿空气中生锈
D.铜片加热时变黑
2.下列物质属于纯净物的是( )
A.海水 B.水泥砂浆
C.干冰 D.汽水
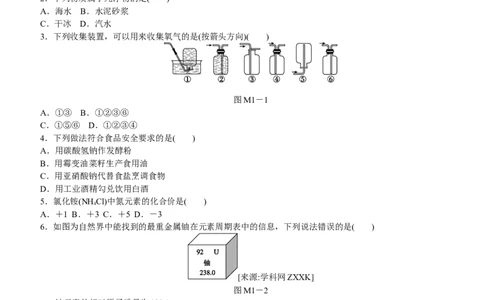
3.下列收集装置,可以用来收集氧气的是(按箭头方向)( )
图M1-1
A.①③ B.①②③⑥
C.①⑤⑥ D.①②③④
4.下列做法符合食品安全要求的是( )
A.用碳酸氢钠作发酵粉
B.用霉变油菜籽生产食用油
C.用亚硝酸钠代替食盐烹调食物
D.用工业酒精勾兑饮用白酒
5.氯化铵(NH Cl)中氮元素的化合价是( )
4
A.+1 B.+3 C.+5 D.-3
6.如图为自然界中能找到的最重金属铀在元素周期表中的信息,下列说法错误的是( )
[来源:学科网ZXXK]
图M1-2
A.铀元素的相对原子质量为238.0
B.铀原子的中子数为92[来源:Z#xx#k.Com]
C.铀原子核内质子数为92[来源:Z#xx#k.Com]
D.铀原子核内中子数和质子数之和约等于238
7.由化学方程式:CHO+5O===4CO +4HO,可知x、y、z分别是( )[来源:Zxxk.Com]
x y z 2 2 2
A.4、8、2 B.1、2、3
C.2、4、1 D.4、4、2
8.下列化学符号中数字表示意义错误的是( )
A.CO:“2”表示一个二氧化碳分子中含有两个氧原子
2
B.2Na:“2”表示两个钠元素
C.Mg:“+2”表示镁元素的化合价为+2
D.2OH-:“2”表示两个氢氧根离子9.有甲、乙、丙三种金属,只有甲在自然界中主要以单质形式存在,丙的盐溶液不能用乙制的容器盛放。则这三种金
属的活动性由强到弱的顺序是( )
A.甲>乙>丙 B.丙>乙>甲
C.丙>甲>乙 D.乙>丙>甲
图M1-3
10.图M1-3是A、B两种固体物质的溶解度曲线,下列说法正确的是( )
A.A的溶解度大于B的溶解度
B.A、B两种物质的饱和溶液都从t ℃降温到t ℃,析出的晶体的质量一定是A>B
3 2
C.t ℃时,用等质量水配制的A、B饱和溶液中,所含溶质的质量:A>B
1
D.t ℃时,100 g饱和溶液A和50 g饱和溶液B中,溶质的质量分数相等
2
11.一些食物的近似pH如下:
食物 葡萄汁 苹果汁 牛奶 鸡蛋清
pH 3.5~4.5 2.9~3.3 6.3~6.6 7.6~8.0
下列说法中不正确的是( )
A.鸡蛋清和牛奶显碱性
B.苹果汁和葡萄汁显酸性
C.苹果汁比葡萄汁的酸性强
D.胃酸过多的人应少饮葡萄汁和苹果汁
12.X、Y、Z三种金属中,只有Z能与稀硫酸反应,当把Y放入X的盐溶液时,Y表面有X析出,则X、Y、Z三种金属
的活动性顺序为( )
A.X>Y>Z B.Z>X>Y
C.Y>Z>X D.Z>Y>X
13.区别CO和CO 最简便的方法是( )
2
A.测量它们的密度
B.检验它们是否有毒
C.分别通入水中
D.分别通入澄清石灰水中
14.下列各组物质间的反应,需要加入酸碱指示剂才能判断反应是否发生的是( )
A.Fe和CuSO 溶液
4
B.Zn和稀硫酸
C.NaOH溶液和稀盐酸
D.澄清石灰水和CO
2
15.下列离子能在pH=1的溶液中大量共存且为无色的是( )
A.SO 2-、K+、Na+、OH-
4
B.K+、SO 2-、Cu2+、NO -
4 3
C.Cl-、K+、SO 2-、Na+
4
D.Ca2+、Cl-、CO2-、Na+
3
二、填空与简答题(本题2个小题,共10分)
16.(6分)用元素符号或化学式填空:[来源:Zxxk.Com]
(1)氢元素________。(2)4个二氧化硫分子________。
(3)氮气________。
(4)2个硫酸根离子________。
(5)3个铜原子________。
(6)标出五氧化二氮中氮元素化合价______。
17.(4分)南宁至钦州段的高速铁路正在建设中。请回答下列问题。
(1)铁路建设中大量使用了以下材料:①石子;②钢筋水泥柱;③钢轨等,其中钢轨属于________(填序号)。
A.金属材料 B.合成材料
C.有机天然材料 D.无机非金属材料
(2)建设中,常用铝和氧化铁(Fe O)在高温条件下,反应生成熔融状态下的铁单质对钢轨中的缝隙进行焊接。反应的
2 3
化学方程式为Fe O+2Al===X+2Fe,则X的化学式为____________。
2 3
(3)钢轨长时间使用后会生锈。铁锈的主要成分是Fe O·xHO;除铁锈常用的一种试剂是______________。
2 3 2
(4)请写出防止铁制品锈蚀的一种常用方法:_____________________________________。
三、实验与探究题(本题3个小题,共18分)
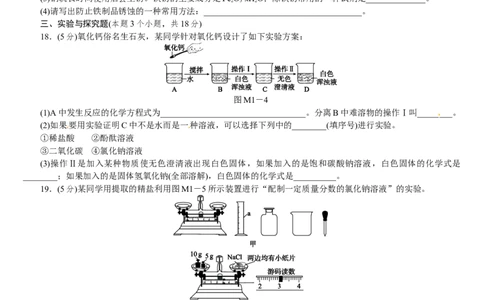
18.(5分)氧化钙俗名生石灰,某同学针对氧化钙设计了如下实验方案:
图M1-4
(1)A中发生反应的化学方程式为__________________________________。分离B中难溶物的操作Ⅰ叫________。
(2)如果要用实验证明C中不是水而是一种溶液,可以选择下列中的________(填序号)进行实验。
①稀盐酸 ②酚酞溶液
③二氧化碳 ④氯化钠溶液
(3)操作Ⅱ是加入某种物质使无色澄清液出现白色固体,如果加入的是饱和碳酸钠溶液,白色固体的化学式是
________;如果加入的是固体氢氧化钠(全部溶解),白色固体的化学式是__________。
19.(5分)某同学用提取的精盐利用图M1-5所示装置进行“配制一定质量分数的氯化钠溶液”的实验。
图M1-5
(1)图甲中仪器a的名称是________。
(2)按实验要求,图甲中还缺少的玻璃仪器是__________(填名称),作用是________________________________。
(3)小红按图乙的操作称取氯化钠,小民发现小红的操作有错误。你认为小红操作中的错误是
____________________________________。
(4)反思:若称取的氯化钠中含有水分,其他操作均正确,则所配制的溶液溶质质量分数会________(填“偏大”
“偏小”或“无影响”)。
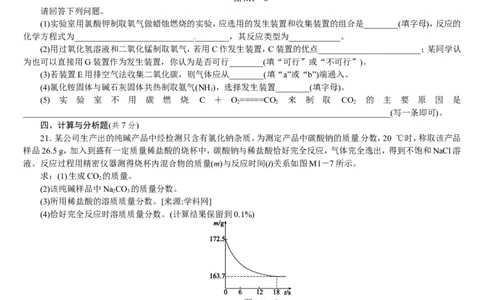
20.(8分)如图M1-6所示为实验室中常见的气体制备和收集装置。图M1-6
请回答下列问题。
(1)实验室用氯酸钾制取氧气做蜡烛燃烧的实验,应选用的发生装置和收集装置的组合是________(填字母),反应的
化学方程式为____________________________________,其反应类型为____________。
(2)用过氧化氢溶液和二氧化锰制取氧气,若用C作发生装置,C装置的优点________________________;某同学认
为也可以直接用G装置作为发生装置,你认为是否可行________(填“可行”或“不可行”)。
(3)若装置E用排空气法收集二氧化碳,则气体应从________(填“a”或“b”)端通入。
(4)氯化铵固体与碱石灰固体共热制取氨气(NH ),选择发生装置________(填字母)。
3
(5) 实 验 室 不 用 碳 燃 烧 C + O=====CO 来 制 取 CO 的 主 要 原 因 是
2 2 2
______________________________________________________________________________________(写一条即可)。
四、计算与分析题(共7分)
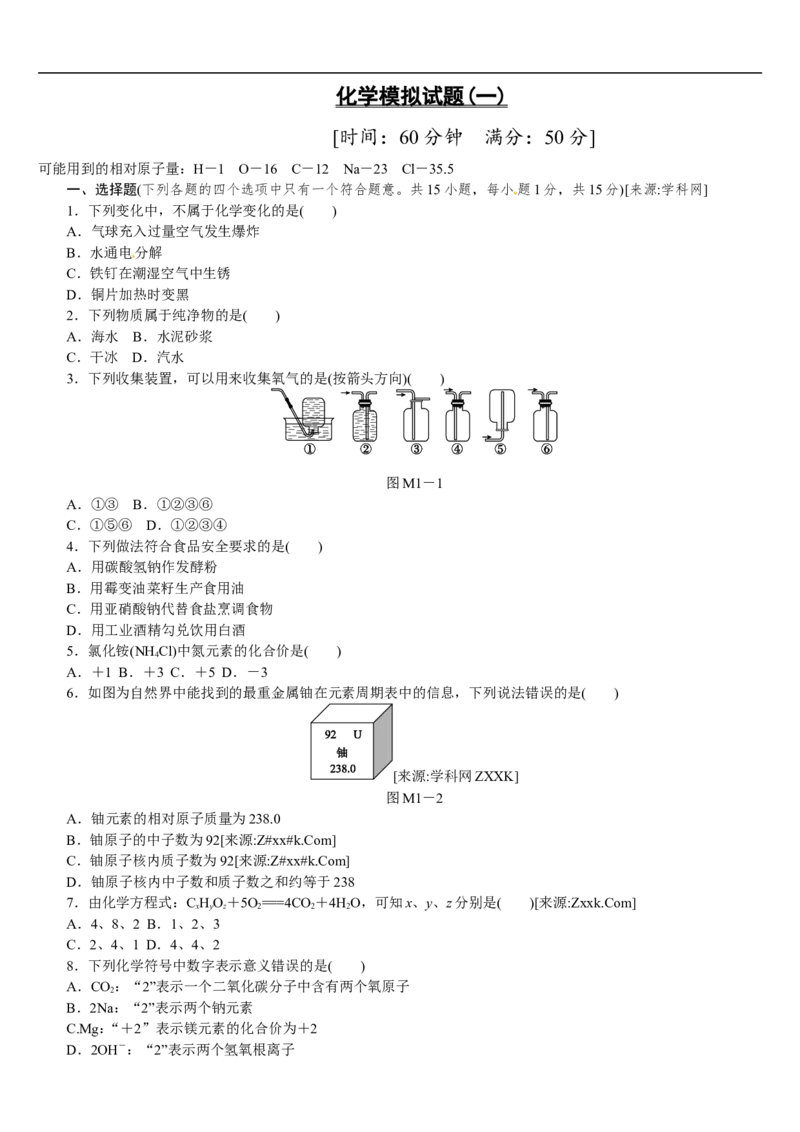
21.某公司生产出的纯碱产品中经检测只含有氯化钠杂质。为测定产品中碳酸钠的质量分数,20 ℃时,称取该产品
样品26.5 g,加入到盛有一定质量稀盐酸的烧杯中,碳酸钠与稀盐酸恰好完全反应,气体完全逸出,得到不饱和NaCl溶
液。反应过程用精密仪器测得烧杯内混合物的质量(m)与反应时间(t)关系如图M1-7所示。
求:(1)生成CO 的质量。
2
(2)该纯碱样品中NaCO 的质量分数。
2 3
(3)所用稀盐酸的溶质质量分数。[来源:学科网]
(4)恰好完全反应时溶质质量分数。(计算结果保留到0.1%)
图M1-7参考答案
1.A 2.C 3.D 4.A 5.D 6.B 7.A 8.B 9.D 10.D 11.A 12.D 13.D 14.C 15.C
16.(1)H (2)4SO (3)N (4)2SO 2- (5)3Cu (6)NO
2 2 4 2 5
17.(1)A (2)AlO (3)稀盐酸(或稀硫酸)
2 3
(4)保持铁制品表面的干燥和清洁(合理即可)
18.(1)CaO+HO===Ca(OH) 过滤
2 2
(2)②③ (3)CaCO Ca(OH)
3 2
19.(1)量筒
(2)玻璃棒 搅拌,加快氯化钠的溶解速率
(3)称量物与砝码放反了,应该是左物右码 (4)偏小
20.(1)AD(或AE) 2KClO=====2KCl+3O ↑ 分解反应
3 2
(2)可以控制反应速率 不可行[来源:学科网ZXXK]
(3) a
(4)A
(5)反应物中有气体,这样很难收集到纯净的CO 气体(或燃烧的条件下,很难将其控制在一个密闭的环境中进行,因
2
而无法收集等)
21.解:(1)生成二氧化碳的质量为172.5 g-163.7 g=8.8 g。
(2)设样品中碳酸钠的质量为x,稀盐酸中溶质质量为y,生成氯化钠质量为z。
NaCO+2HCl===2NaCl+CO↑+HO[来源:学。科。网]
2 3 2 2
106 73 117 44
x y z 8.8 g
= x=21.2 g
= y=14.6 g
= z=23.4 g
则该纯碱样品中碳酸钠的质量分数为[来源:Z&xx&k.Com]
×100%=80%。
(3)所用稀盐酸的质量为172.5 g-26.5 g=146 g;
则该稀盐酸的溶质质量分数为×100%=10%。
(4)原混合物中氯化钠的质量为26.5 g-21.2 g=5.3 g;
反应后溶质的质量为23.4 g+5.3 g=28.7 g;
则反应后溶液的溶质质量分数为×100%=17.5%。
答:(1)生成二氧化碳的质量为8.8 g;
(2)该纯碱样品中NaCO 的质量分数为80%;
2 3
(3)稀盐酸的溶质质量分数为10%;
(4)恰好完全反应时溶液的溶质质量分数为17.5%。