文档内容
第二节 乙烯与有机高分子材料
学业要求 核心素养对接
1.了解乙烯的物理性质、工业制取原理和在化工生
产中的应用。
2.掌握乙烯的分子结构,初步体会其结构特点对性
通过对乙烯结构与性质的学
质的影响。
习,培养学生宏观辨识与微观
3.掌握乙烯的化学性质,认识加成反应的特点。 探析的能力。
4.了解烃的概念与分类。
5.了解常见高分子材料。
[知 识 梳 理]
知识点一 乙烯
如上图,无公害的塑料小鸭子,是由工厂先制取乙烯,再制取聚乙烯,最终到小鸭
子,那么乙烯有什么样的结构和性质呢?请完成下列知识点:
1.组成和结构
2.物理性质
颜色 状态 气味 水溶性 密度无色 气体 稍有气味 难溶于水 比空气略小
3.化学性质
(1)氧化反应[实验7-2]
(2)加成反应
①概念:有机物分子中不饱和碳原子与其他原子或原子团直接结合生成新的化合
物的反应。
②乙烯的加成反应:[实验7-3]
(3)聚合反应
由相对分子质量小的化合物分子互相结合成相对分子质量大的聚合物的反应,叫
做聚合反应。由于发生加成反应而生成有机高分子化合物的聚合反应也叫加成聚
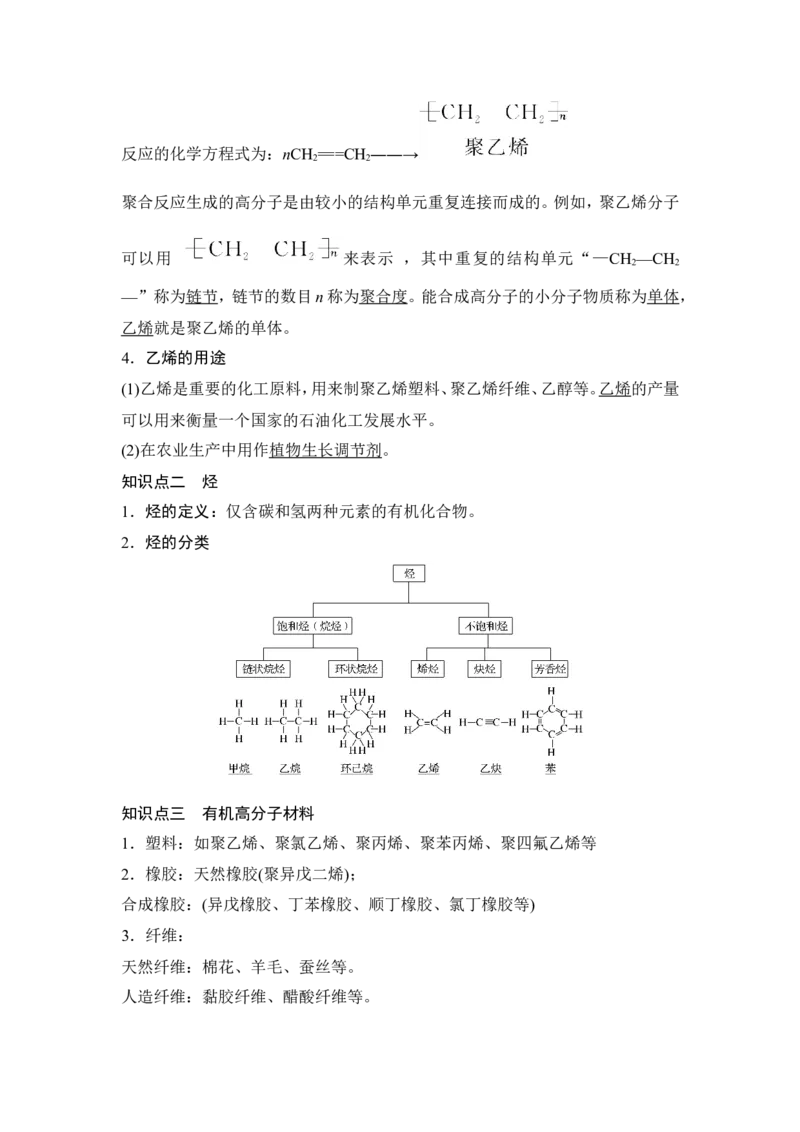
合反应,简称加聚反应。乙烯能发生自身的加成反应生成高分子化合物聚乙烯,反应的化学方程式为:nCH ===CH ――→
2 2
聚合反应生成的高分子是由较小的结构单元重复连接而成的。例如,聚乙烯分子
可以用 来表示 ,其中重复的结构单元“—CH —CH
2 2
—”称为链节,链节的数目n称为聚合度。能合成高分子的小分子物质称为单体,
乙烯就是聚乙烯的单体。
4.乙烯的用途
(1)乙烯是重要的化工原料,用来制聚乙烯塑料、聚乙烯纤维、乙醇等。乙烯的产量
可以用来衡量一个国家的石油化工发展水平。
(2)在农业生产中用作植物生长调节剂。
知识点二 烃
1.烃的定义:仅含碳和氢两种元素的有机化合物。
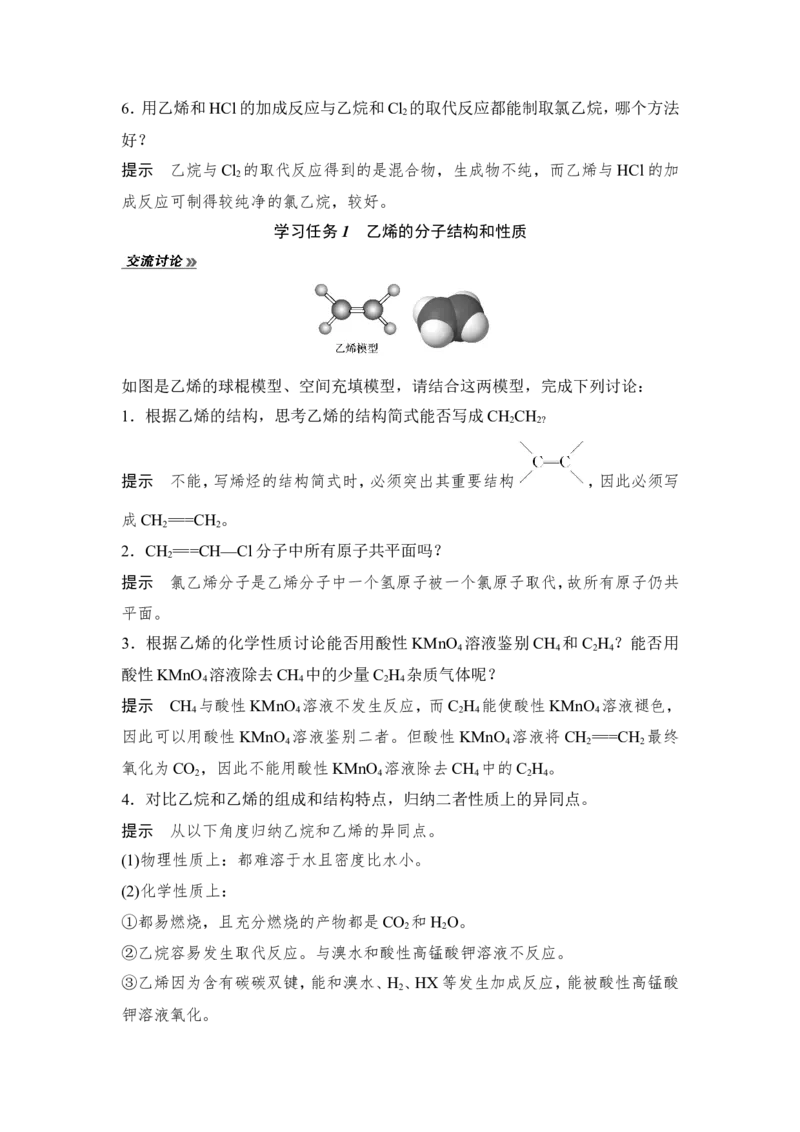
2.烃的分类
知识点三 有机高分子材料
1.塑料:如聚乙烯、聚氯乙烯、聚丙烯、聚苯丙烯、聚四氟乙烯等
2.橡胶:天然橡胶(聚异戊二烯);
合成橡胶:(异戊橡胶、丁苯橡胶、顺丁橡胶、氯丁橡胶等)
3.纤维:
天然纤维:棉花、羊毛、蚕丝等。
人造纤维:黏胶纤维、醋酸纤维等。合成纤维:腈纶、涤纶、锦纶、维尼纶等。
微判断
(1)烃 的分子式为C H ,符合通式C H ,故该分子属于烯烃( )
3 6 n 2n
(2)某无色气体通入酸性KMnO 溶液中,溶液褪色,该气体一定是烯烃( )
4
(3)某无色气体能使溴水褪色,该气体可能是烯烃( )
(4)甲烷和乙烯都属于烃,前者属于烷烃,后者属于烯烃( )
(5)甲烷和乙烯都是可燃性气体,点燃之前必须验纯,而且燃烧时现象相同( )
(6)以石油为原料可以获得乙烯( )
(7)乙烯比乙烷的化学性质活泼( )
答案 (1)× (2)× (3)√ (4)√ (5)×
(6)√ (7)√
微训练
1.刚摘的猕猴桃往往青涩难吃,但将熟透的红苹果与它共同装入袋内,三天后就
香甜可口了,原因是熟透的苹果挥发出的乙烯对猕猴桃起了催熟作用。下列有关
乙烯的说法中不正确的是( )
A.乙烯分子为平面结构,分子中C—H键之间的键角约为120°
B.乙烯与溴发生加成反应后的产物中所有原子都共平面
C.乙烯的产量常用来衡量一个国家石油化工水平的标志
D.乙烯是一种植物生长的调节剂,也可作水果催熟剂
解析 乙烯分子中的 6 个原子共平面,但与溴发生加成反应后生成
BrCH CH Br(1,2二溴乙烷),其结构相当于乙烷分子中的两个H原子(位于不同
2 2
的碳原子上)被Br原子代替,每个碳原子与其相连的4个原子构成四面体结构,
1,2二溴乙烷中的8个原子不共平面。
答案 B
2.下列关于乙烯的叙述中,正确的是( )
A.乙烯的化学性质比乙烷活泼
B.甲烷和乙烯在一定条件下都可以与氯气反应,且反应类型相同
C.乙烯分子中所有原子不可能在同一平面上D.乙烯分子的碳碳双键中的一个键易断裂,易发生加成反应和取代反应
解析 由乙烯可使酸性高锰酸钾溶液褪色而乙烷不能,可知乙烯比乙烷活泼,A
正确;甲烷和氯气发生取代反应,而乙烯和氯气发生加成反应,B项不正确;乙烯
分子中所有原子在同一平面上,C项不正确;乙烯分子的碳碳双键中的一个键易
断裂,易发生加成反应,而不易发生取代反应, D不正确。
答案 A
微思考
1.为什么甲烷燃烧没有黑烟,而乙烯燃烧有黑烟?
提示 因为甲烷分子里含碳量低,燃烧充分;乙烯分子里含碳量(85.7%)比较大,
未完全燃烧,产生碳的小颗粒。
2.乙烯可以作为水果的催熟剂,但是用浸泡过酸性KMnO 溶液的硅藻土与果实
4
放在一起,可以延长果实的成熟期,达到保鲜的目的。请你解释其原因。
提示 水果释放的乙烯能被酸性高锰酸钾溶液氧化。
3.乙烯能使酸性KMnO 溶液和溴的CCl 溶液褪色,二者的褪色原理是否相同?
4 4
提示 二者褪色原理不同。乙烯使酸性KMnO 溶液褪色是因为乙烯发生氧化反
4
应,KMnO 将乙烯氧化成CO ;乙烯使溴的CCl 溶液褪色是因为乙烯与Br 发生
4 2 4 2
加成反应。因此CH 中混有乙烯时,不能用酸性KMnO 溶液除去(引入新的杂质)
4 4
应用溴的CCl 溶液除去。
4
4.鉴别乙烯和甲烷有哪些方法?
提示 鉴别乙烯和甲烷的方法
乙烯 甲烷
燃烧法 火焰明亮 淡蓝色火
伴有黑烟 焰,无烟
酸性KMnO 溶液 褪色 不褪色
4
溴水或Br 的CCl 溶液 褪色 不褪色
2 4
5.用什么方法除去乙烷中的乙烯?能使用 H 或酸性KMnO 溶液除去乙烷中的乙
2 4
烯吗?为什么?
提示 用溴的CCl 溶液除去。因为Br 与乙烯反应生成液态的1,2二溴乙烷,气
4 2
液分离。不能用H 或酸性KMnO 溶液。因为H 的用量不易控制,乙烯不能完全
2 4 2
除去或引入新的杂质H ;乙烯被酸性KMnO 溶液氧化的产物是CO ,引入新的
2 4 2
杂质CO 。
26.用乙烯和HCl的加成反应与乙烷和Cl 的取代反应都能制取氯乙烷,哪个方法
2
好?
提示 乙烷与Cl 的取代反应得到的是混合物,生成物不纯,而乙烯与HCl的加
2
成反应可制得较纯净的氯乙烷,较好。
学习任务1 乙烯的分子结构和性质
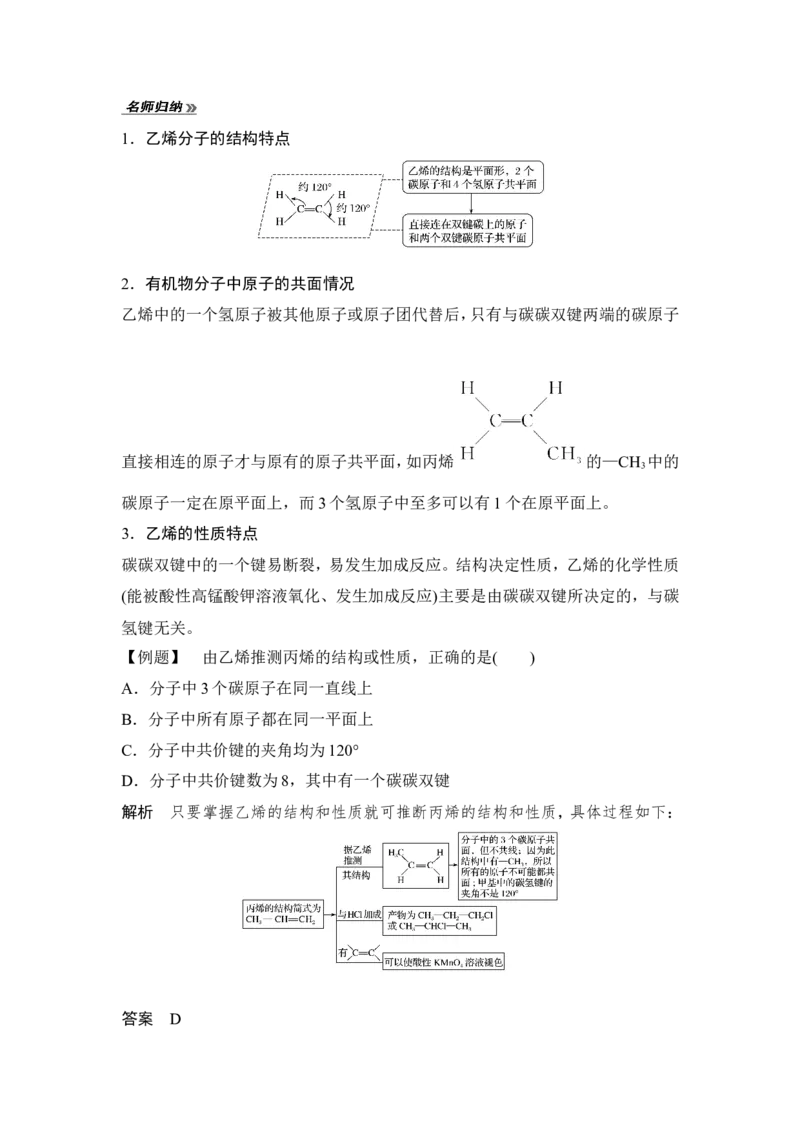
如图是乙烯的球棍模型、空间充填模型,请结合这两模型,完成下列讨论:
1.根据乙烯的结构,思考乙烯的结构简式能否写成CH CH
2 2?
提示 不能,写烯烃的结构简式时,必须突出其重要结构 ,因此必须写
成CH ===CH 。
2 2
2.CH ===CH—Cl分子中所有原子共平面吗?
2
提示 氯乙烯分子是乙烯分子中一个氢原子被一个氯原子取代,故所有原子仍共
平面。
3.根据乙烯的化学性质讨论能否用酸性KMnO 溶液鉴别CH 和C H ?能否用
4 4 2 4
酸性KMnO 溶液除去CH 中的少量C H 杂质气体呢?
4 4 2 4
提示 CH 与酸性KMnO 溶液不发生反应,而C H 能使酸性KMnO 溶液褪色,
4 4 2 4 4
因此可以用酸性KMnO 溶液鉴别二者。但酸性KMnO 溶液将CH ===CH 最终
4 4 2 2
氧化为CO ,因此不能用酸性KMnO 溶液除去CH 中的C H 。
2 4 4 2 4
4.对比乙烷和乙烯的组成和结构特点,归纳二者性质上的异同点。
提示 从以下角度归纳乙烷和乙烯的异同点。
(1)物理性质上:都难溶于水且密度比水小。
(2)化学性质上:
①都易燃烧,且充分燃烧的产物都是CO 和H O。
2 2
②乙烷容易发生取代反应。与溴水和酸性高锰酸钾溶液不反应。
③乙烯因为含有碳碳双键,能和溴水、H 、HX等发生加成反应,能被酸性高锰酸
2
钾溶液氧化。1.乙烯分子的结构特点
2.有机物分子中原子的共面情况
乙烯中的一个氢原子被其他原子或原子团代替后,只有与碳碳双键两端的碳原子
直接相连的原子才与原有的原子共平面,如丙烯 的—CH 中的
3
碳原子一定在原平面上,而3个氢原子中至多可以有1个在原平面上。
3.乙烯的性质特点
碳碳双键中的一个键易断裂,易发生加成反应。结构决定性质,乙烯的化学性质
(能被酸性高锰酸钾溶液氧化、发生加成反应)主要是由碳碳双键所决定的,与碳
氢键无关。
【例题】 由乙烯推测丙烯的结构或性质,正确的是( )
A.分子中3个碳原子在同一直线上
B.分子中所有原子都在同一平面上
C.分子中共价键的夹角均为120°
D.分子中共价键数为8,其中有一个碳碳双键
解析 只要掌握乙烯的结构和性质就可推断丙烯的结构和性质,具体过程如下:
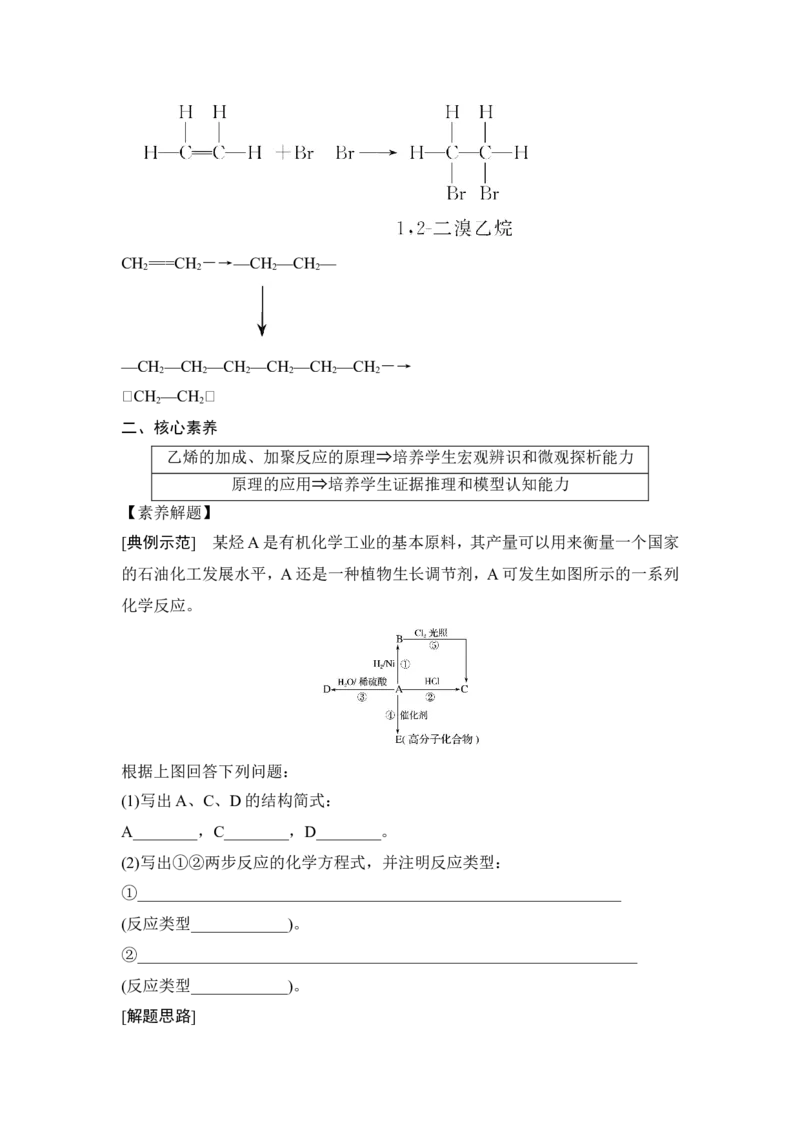
答案 D变式训练 以下是两种有机物的球棍模型: 代表H原子, 代表C原子,请回
答下列问题:
(1)Ⅰ、Ⅱ的分子式________、________。
(2)说出Ⅰ、Ⅱ结构上的两点差异:①_____________________________________;
②______________。
解析 从球棍模型可知,Ⅰ为乙烷,Ⅱ为乙烯。乙烷中有“C—C”,乙烯中有
“C===C”,且前者是空间立体结构,后者是平面结构。
答案 (1)C H C H
2 6 2 4
(2)①Ⅰ中含有碳碳单键,Ⅱ中含有碳碳双键 ②Ⅰ是空间立体结构,Ⅱ是平面结
构
学习任务2 (核心素养)乙烯的加成反应
一、知识要点
1.对乙烯性质的正确认识
(1)含有空气的乙烯点燃时易爆炸,所以点燃乙烯前要检验乙烯的纯度。
(2)乙烯使溴水或溴的四氯化碳溶液褪色,发生的是加成反应,生成无色的1,2二
溴乙烷;乙烯使酸性KMnO 溶液褪色,发生的是氧化反应,二者褪色的原理不同。
4
(3)定量分析。
①加成反应消耗的 Cl 的量由双键数决定,双键数与消耗 Cl 的分子数之比为
2 2
1∶1。
②取代反应消耗的Cl 的量由分子内氢原子个数决定,分子内氢原子个数与消耗
2
Cl 的分子数之比为1∶1。
2
2.烯烃加成反应的特点
加成反应是有机物分子中不饱和碳原子与其他原子或原子团直接结合生成新的
化合物的反应,其特点是:“断一加二,都进来”,“断一”是指双键中的一个不
稳定键断裂;“加二”是指加两个其他原子或原子团,每一个不饱和碳原子上各
加上一个。
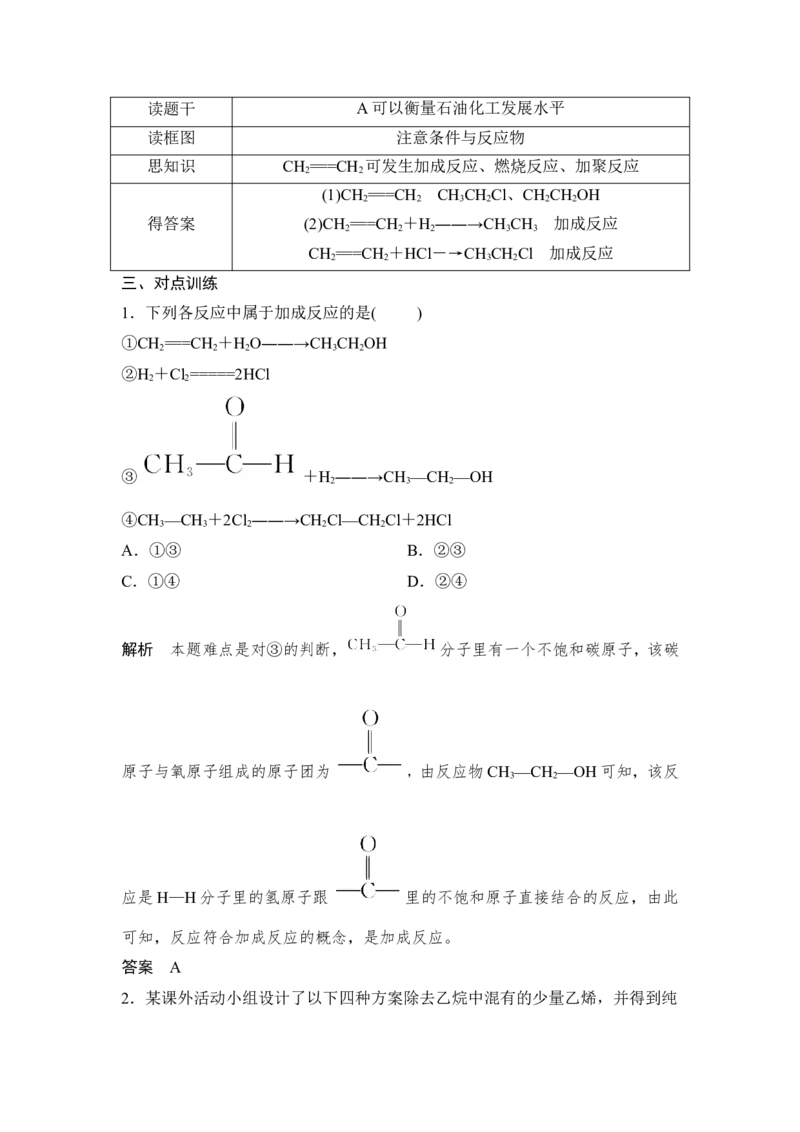
3.加成反应方程式CH ===CH ―→—CH —CH —
2 2 2 2
—CH —CH —CH —CH —CH —CH ―→
2 2 2 2 2 2
CH —CH
2 2
二、核心素养
乙烯的加成、加聚反应的原理⇒培养学生宏观辨识和微观探析能力
原理的应用⇒培养学生证据推理和模型认知能力
【素养解题】
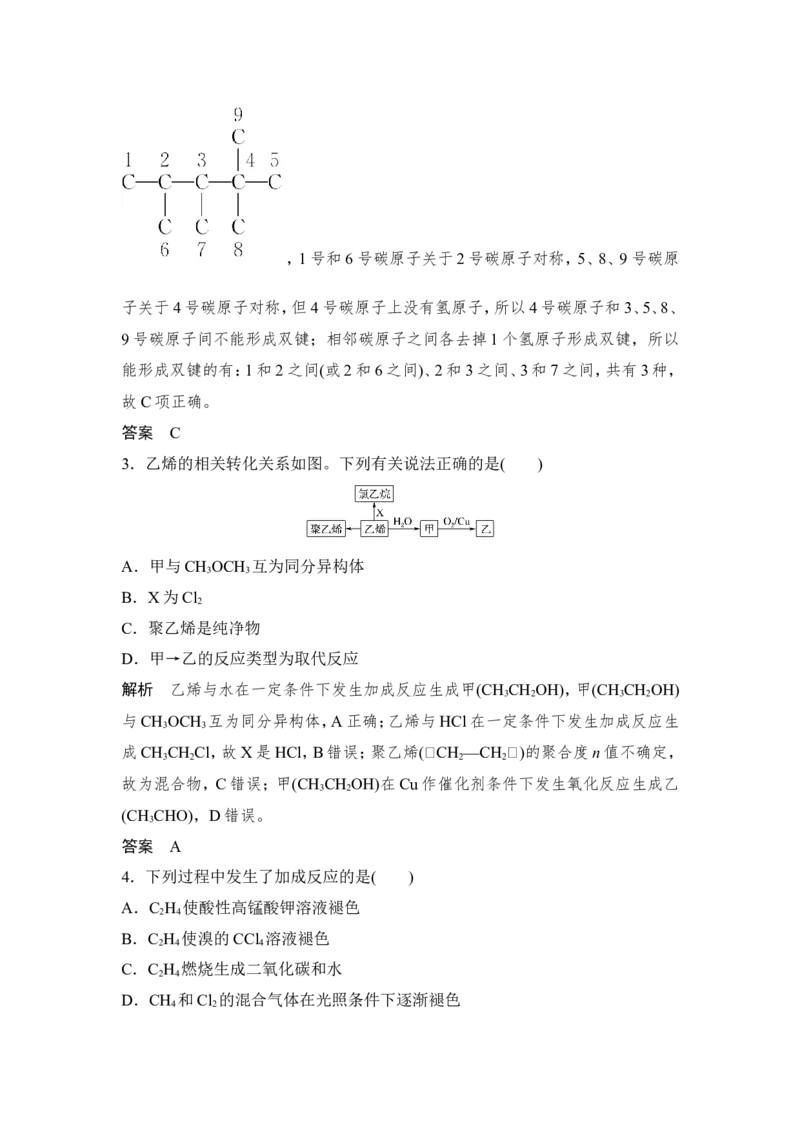
[典例示范] 某烃A是有机化学工业的基本原料,其产量可以用来衡量一个国家
的石油化工发展水平,A还是一种植物生长调节剂,A可发生如图所示的一系列
化学反应。
根据上图回答下列问题:
(1)写出A、C、D的结构简式:
A________,C________,D________。
(2)写出①②两步反应的化学方程式,并注明反应类型:
①____________________________________________________________
(反应类型____________)。
②______________________________________________________________
(反应类型____________)。
[解题思路]读题干 A可以衡量石油化工发展水平
读框图 注意条件与反应物
思知识 CH ===CH 可发生加成反应、燃烧反应、加聚反应
2 2
(1)CH ===CH CH CH Cl、CH CH OH
2 2 3 2 2 2
得答案 (2)CH ===CH +H ――→CH CH 加成反应
2 2 2 3 3
CH ===CH +HCl―→CH CH Cl 加成反应
2 2 3 2
三、对点训练
1.下列各反应中属于加成反应的是( )
①CH ===CH +H O――→CH CH OH
2 2 2 3 2
②H +Cl =====2HCl
2 2
③ +H ――→CH —CH —OH
2 3 2
④CH —CH +2Cl ――→CH Cl—CH Cl+2HCl
3 3 2 2 2
A.①③ B.②③
C.①④ D.②④
解析 本题难点是对③的判断, 分子里有一个不饱和碳原子,该碳
原子与氧原子组成的原子团为 ,由反应物CH —CH —OH可知,该反
3 2
应是H—H分子里的氢原子跟 里的不饱和原子直接结合的反应,由此
可知,反应符合加成反应的概念,是加成反应。
答案 A
2.某课外活动小组设计了以下四种方案除去乙烷中混有的少量乙烯,并得到纯净干燥的乙烷,合理的是( )
A.①②④ B.①②③
C.②③④ D.①②③④
解析 ①和② C H 与Br 发生加成反应生成液态 1,2二溴乙烷而除去C H ,
2 4 2 2 4
①NaOH溶液除去挥发出来的Br 蒸气,浓硫酸除去水蒸气,②碱石灰除去挥发
2
出来的Br 蒸气和水蒸气。①和②均正确;③和④酸性KMnO 溶液将C H 氧化为
2 4 2 4
CO ,NaOH溶液和碱石灰都能吸收CO ,碱石灰和浓硫酸都能吸收水蒸气,③和
2 2
④也正确。
答案 D
3.能证明乙烯分子里含有一个碳碳双键的事实是 ( )
A.乙烯分子里碳氢个数比为1∶2
B.乙烯完全燃烧生成的CO 和水的物质的量相等
2
C.乙烯能与Br 的CCl 溶液发生加成反应,且1 mol 乙烯完全加成需消耗1 mol
2 4
Br
2
D.乙烯能使酸性高锰酸钾溶液褪色
解析 碳氢个数比为1∶2,是对乙烯的组成分析,而不是证明碳碳双键存在的事
实,A不能证明;乙烯完全燃烧生成的CO 和水的物质的量相等,只能推断出乙
2
烯分子中碳、氢原子个数比为1∶2,B不能证明;1 mol 乙烯完全加成需要消耗1
mol Br ,说明乙烯分子中含有一个碳碳双键,C正确;能使酸性高锰酸钾溶液褪
2
色只能证明有机物具有还原性或含有不饱和键,不一定含有碳碳双键和只含有一
个碳碳双键,D不正确。答案 C
4.下列反应中,属于加成反应的是(双选)( )
A.乙烯使溴水褪色
B.丙烯和氯气在一定条件下反应生成ClCH CH===CH
2 2
C.乙烯使酸性KMnO 溶液褪色
4
D.乙烯与HCl气体反应生成一氯乙烷
答案 AD
[学 考 练]
1.甲烷、乙烯属于不同类型的有机化合物,但它们之间也有共性。下列关于它们
之间共同特点的说法正确的有( )
A.都含有碳碳双键
B.都能使酸性KMnO 溶液褪色
4
C.都能发生加成反应和取代反应
D.在氧气中完全燃烧后都生成CO 和H O
2 2
解析 A项,甲烷不含有碳碳双键,错误;B项,乙烯能使酸性KMnO 溶液褪色,
4
甲烷不能,错误;C项,甲烷不能发生加成反应,错误;D项,在氧气中完全燃烧后
都生成CO 和H O,正确。
2 2
答案 D
2.某单烯烃与H 加成后的产物: ,则该烯烃
2
的结构式可能有( )
A.1种 B.2种
C.3种 D.4种
解析 根据烯烃与H 加成反应的原理,推知该烷烃分子中相邻碳原子上均带氢
2
原子的碳原子间是对应烯烃存在碳碳双键的位置,该烷烃的碳链结构为,1号和6号碳原子关于2号碳原子对称,5、8、9号碳原
子关于4号碳原子对称,但4号碳原子上没有氢原子,所以4号碳原子和3、5、8、
9号碳原子间不能形成双键;相邻碳原子之间各去掉1个氢原子形成双键,所以
能形成双键的有:1和2之间(或2和6之间)、2和3之间、3和7之间,共有3种,
故C项正确。
答案 C
3.乙烯的相关转化关系如图。下列有关说法正确的是( )
A.甲与CH OCH 互为同分异构体
3 3
B.X为Cl
2
C.聚乙烯是纯净物
D.甲→乙的反应类型为取代反应
解析 乙烯与水在一定条件下发生加成反应生成甲(CH CH OH),甲(CH CH OH)
3 2 3 2
与CH OCH 互为同分异构体,A正确;乙烯与HCl在一定条件下发生加成反应生
3 3
成CH CH Cl,故X是HCl,B错误;聚乙烯(CH —CH )的聚合度n值不确定,
3 2 2 2
故为混合物,C错误;甲(CH CH OH)在Cu作催化剂条件下发生氧化反应生成乙
3 2
(CH CHO),D错误。
3
答案 A
4.下列过程中发生了加成反应的是( )
A.C H 使酸性高锰酸钾溶液褪色
2 4
B.C H 使溴的CCl 溶液褪色
2 4 4
C.C H 燃烧生成二氧化碳和水
2 4
D.CH 和Cl 的混合气体在光照条件下逐渐褪色
4 2解析 A项,酸性高锰酸钾溶液与C H 发生氧化反应;B项,C H 与溴发生加成
2 4 2 4
反应;C项,C H 燃烧属于氧化反应;D项,属于取代反应。
2 4
答案 B
5.下列各组物质在一定条件下反应,可以制得较纯净的1,2二氯乙烷的是( )
A.乙烷与氯气光照条件下反应
B.乙烯与氯化氢气体混合
C.乙烯与氯气加成
D.乙烯通入浓盐酸中
解析 制备二氯代烷烃常用烯烃与氯气的加成反应,而不用烷烃与氯气发生取代
反应,因其产物不纯。
答案 C
6.由乙烯的结构和性质推测丙烯(CH ===CH—CH )的结构或性质正确的是(
2 3
)
A.不能使酸性高锰酸钾溶液褪色
B.不能在空气中燃烧
C.能使溴的四氯化碳溶液褪色
D.与HCl在一定条件下能加成并只得到一种产物
解析 丙烯与乙烯都含有碳碳双键结构,性质有相似之处。丙烯同样能使酸性高
锰酸钾溶液褪色,A错;丙烯与乙烯的元素组成是相同的,可以燃烧,B错;丙烯
也能和溴的四氯化碳溶液发生加成反应,C正确;乙烯与HCl加成只生成一种产
物一氯乙烷,但是CH ===CH—CH 与HCl加成,由于氯原子连接的位置有两种
2 3
情况,加成产物也应该有两种,即:Cl—CH —CH —CH 和CH —CHCl—CH ,它
2 2 3 3 3
们互为同分异构体,不是同一物质,D错。
答案 C
7.由乙烯推测丙烯的结构或性质正确的是(双选)( )
A.分子中3个碳原子在同一直线上
B.分子中所有原子在同一平面上
C.与HCl加成只生成两种产物
D.能使酸性KMnO 溶液退色
4
解析 丙烯分子中的3个碳原子共面不共线;结构中有—CH ,所有原子不共面;
3丙烯与HCl加成生成CH ClCH CH 和CH CHClCH 两种产物。
2 2 3 3 3
答案 CD
8.既可以用来鉴别乙烷和乙烯,又可以用来除去乙烷中混有的乙烯,得到纯净乙
烷的方法是( )
A.与足量溴反应 B.通入足量溴水中
C.在一定条件下通入氢气 D.分别进行燃烧
解析 乙烷和乙烯均是无色气体,但前者易发生取代反应,后者易发生加成反应
若与足量溴作用,乙烷可以发生取代反应而生成溴代乙烷,乙烯发生加成反应生
成二溴乙烷,不仅不易鉴别,还会损失大量的乙烷且混入大量的溴蒸气杂质,不
合理;若在一定条件下通入氢气,虽可将乙烯转变为乙烷,但通入氢气的量不易
控制,很难得到纯净的乙烷;若分别进行燃烧,无法再得到乙烷;因此只能选B,
因为乙烷不和溴水反应,而乙烯能和溴水发生加成反应而使溴水褪色,且生成的
CH Br—CH Br为液体。
2 2
答案 B
9.对比甲烷和乙烯的燃烧反应,下列叙述中正确的是(双选)( )
①二者燃烧时现象完全相同 ②点燃前都应验纯 ③甲烷燃烧的火焰呈淡蓝色,
乙烯燃烧的火焰较明亮,并有大量黑烟生成 ④二者燃烧时都有黑烟生成
A.① B.②
C.③ D.④
解析 甲烷和乙烯燃烧现象不同,①错;可燃性气体点燃前都要验纯,②对;甲烷
燃烧无黑烟,④错、③对。
答案 BC
10.把m mol C H 跟n mol H 混合于密闭容器中,在一定条件下发生反应,生成p
2 4 2
mol C H (p<m),若将反应后的混合气体点燃,完全燃烧生成CO 和H O时,需要
2 6 2 2
O 的物质的量为( )
2
A.(3m+n)mol B.(3m+n/2)mol
C.(3m+3p+n/2)mol D.(3m+n/2-3p)mol
解析 m mol C H 完全燃烧消耗O 为m(2+)mol=3m mol,n mol H 完全燃烧消
2 4 2 2
耗O 为 mol;m mol C H 和n mol H 发生反应后的生成物和剩余的反应物的耗
2 2 4 2
氧量都与m mol C H 和n mol H 的耗氧量相同,B项正确。
2 4 2答案 B
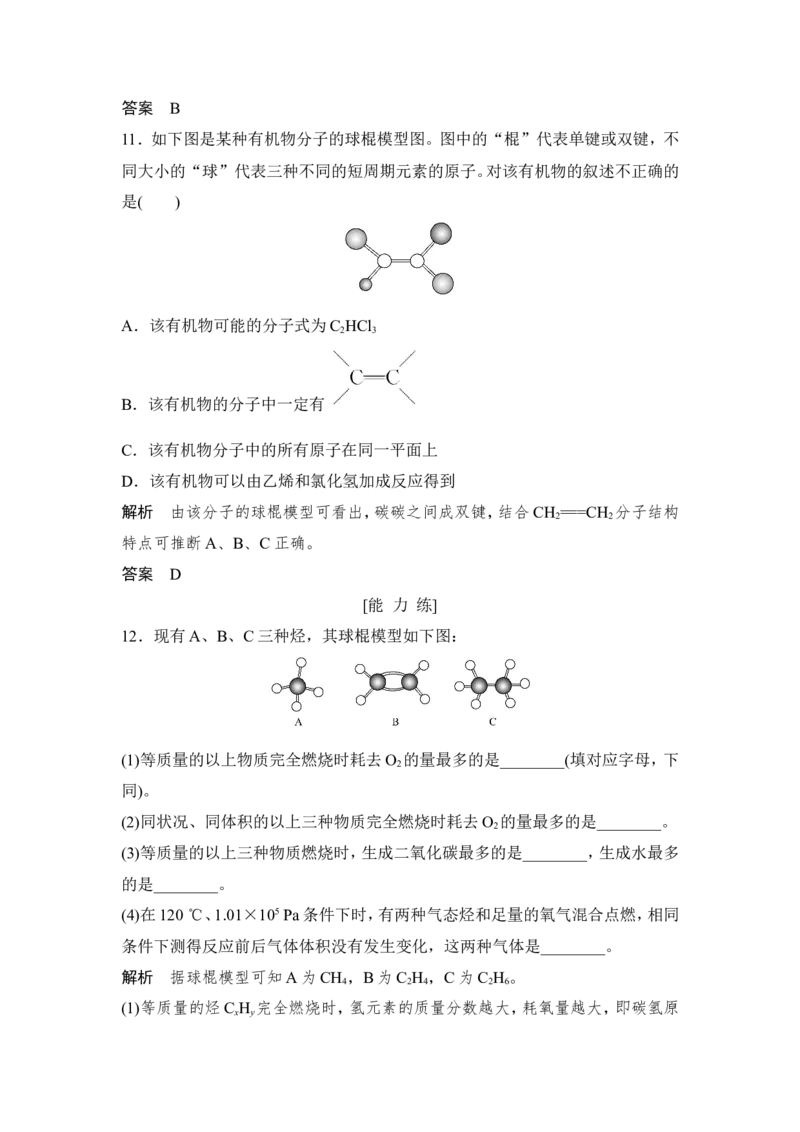
11.如下图是某种有机物分子的球棍模型图。图中的“棍”代表单键或双键,不
同大小的“球”代表三种不同的短周期元素的原子。对该有机物的叙述不正确的
是( )
A.该有机物可能的分子式为C HCl
2 3
B.该有机物的分子中一定有
C.该有机物分子中的所有原子在同一平面上
D.该有机物可以由乙烯和氯化氢加成反应得到
解析 由该分子的球棍模型可看出,碳碳之间成双键,结合CH ===CH 分子结构
2 2
特点可推断A、B、C正确。
答案 D
[能 力 练]
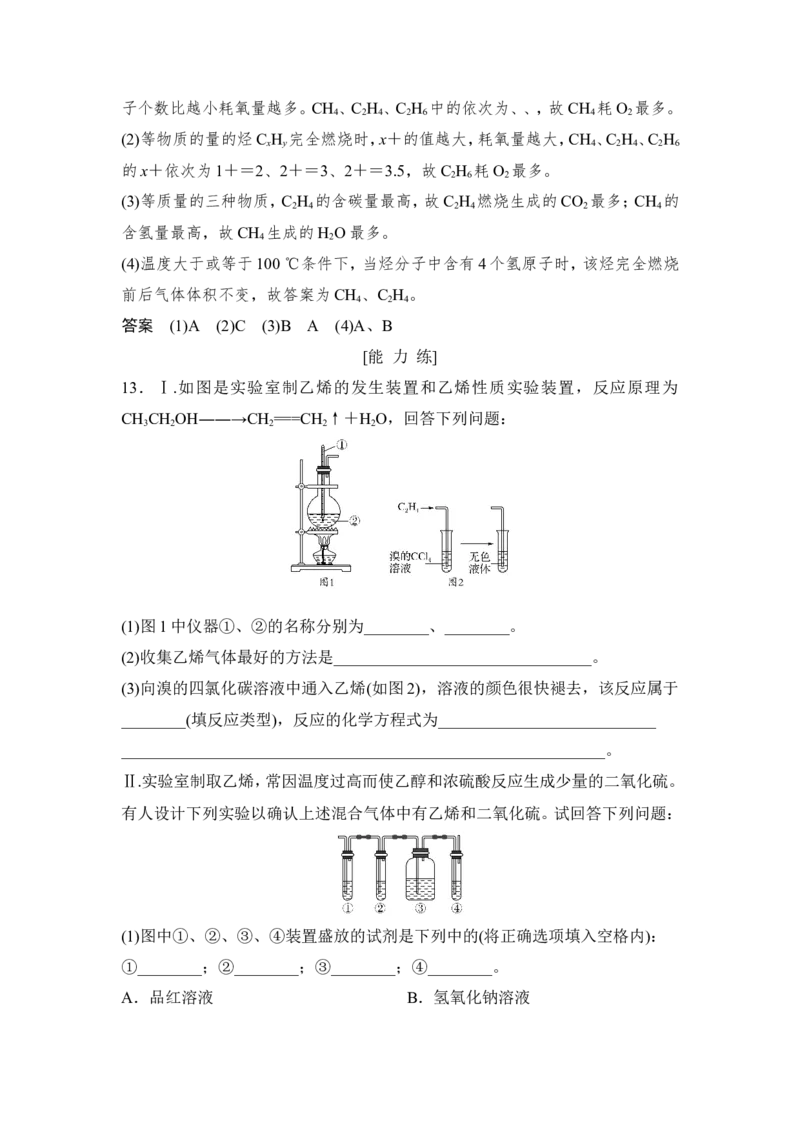
12.现有A、B、C三种烃,其球棍模型如下图:
(1)等质量的以上物质完全燃烧时耗去O 的量最多的是________(填对应字母,下
2
同)。
(2)同状况、同体积的以上三种物质完全燃烧时耗去O 的量最多的是________。
2
(3)等质量的以上三种物质燃烧时,生成二氧化碳最多的是________,生成水最多
的是________。
(4)在120 ℃、1.01×105 Pa条件下时,有两种气态烃和足量的氧气混合点燃,相同
条件下测得反应前后气体体积没有发生变化,这两种气体是________。
解析 据球棍模型可知A为CH ,B为C H ,C为C H 。
4 2 4 2 6
(1)等质量的烃C H 完全燃烧时,氢元素的质量分数越大,耗氧量越大,即碳氢原
x y子个数比越小耗氧量越多。CH 、C H 、C H 中的依次为、、,故CH 耗O 最多。
4 2 4 2 6 4 2
(2)等物质的量的烃C H 完全燃烧时,x+的值越大,耗氧量越大,CH 、C H 、C H
x y 4 2 4 2 6
的x+依次为1+=2、2+=3、2+=3.5,故C H 耗O 最多。
2 6 2
(3)等质量的三种物质,C H 的含碳量最高,故C H 燃烧生成的CO 最多;CH 的
2 4 2 4 2 4
含氢量最高,故CH 生成的H O最多。
4 2
(4)温度大于或等于100 ℃条件下,当烃分子中含有4个氢原子时,该烃完全燃烧
前后气体体积不变,故答案为CH 、C H 。
4 2 4
答案 (1)A (2)C (3)B A (4)A、B
[能 力 练]
13.Ⅰ.如图是实验室制乙烯的发生装置和乙烯性质实验装置,反应原理为
CH CH OH――→CH ===CH ↑+H O,回答下列问题:
3 2 2 2 2
(1)图1中仪器①、②的名称分别为________、________。
(2)收集乙烯气体最好的方法是________________________________。
(3)向溴的四氯化碳溶液中通入乙烯(如图2),溶液的颜色很快褪去,该反应属于
________(填反应类型),反应的化学方程式为___________________________
____________________________________________________________。
Ⅱ.实验室制取乙烯,常因温度过高而使乙醇和浓硫酸反应生成少量的二氧化硫。
有人设计下列实验以确认上述混合气体中有乙烯和二氧化硫。试回答下列问题:
(1)图中①、②、③、④装置盛放的试剂是下列中的(将正确选项填入空格内):
①________;②________;③________;④________。
A.品红溶液 B.氢氧化钠溶液C.浓硫酸 D.酸性高锰酸钾溶液
(2) 能 说 明 二 氧 化 硫 气 体 存 在 的 现 象 是
_____________________________________
___________________________________________________________。
(3)使用装置②的目的是_____________________________________
______________________________________________________。
(4)使用装置③的目的是________________________________________________
_______________________________________________________________。
(5)确认含有乙烯的现象是____________________________________________
__________________________________________________________。
答案 Ⅰ.(1)温度计 烧瓶(或圆底烧瓶) (2)排水集气法 (3)加成反应
CH ===CH +Br ―→CH BrCH Br
2 2 2 2 2
Ⅱ.(1)A B A D
(2)装置①中的品红溶液褪色
(3)除去SO 气体,以免干扰乙烯的检验
2
(4)检验SO 是否已被除尽
2
(5)装置③中的品红溶液不褪色,装置④中的酸性KMnO 溶液褪色
4
14.为探究乙烯与溴的加成反应,甲同学设计并进行了如下实验:先取一定量的
工业用乙烯气体(在储气瓶中),使气体通入溴水中,发现溶液褪色,即证明乙烯与
溴水发生了加成反应。
乙同学发现在甲同学的实验中,褪色后的溶液里有少许淡黄色浑浊物质,推测在
工业上制得的乙烯中还可能含有少量还原性的气体杂质,由此他提出必须先除去
杂质,然后再使乙烯与溴水反应。
请回答下列问题:
(1)甲同学的实验中有关的化学方程式为_________________________________
_________________________________________________________________。
(2)甲同学设计的实验________(填“能”或“不能”)验证乙烯与溴发生加成反
应,其理由是________(填字母)。
A.使溴水褪色的反应,未必是加成反应
B.使溴水褪色的反应,就是加成反应C.使溴水褪色的物质,未必是乙烯
D.使溴水褪色的物质就是乙烯
(3)乙同学推测此乙烯中必定含有的一种杂质气体是________,它与溴水反应的
化学方程式是______________________________________________________
________________________________________________________________。
在验证过程中必须全部除去,除去该杂质的试剂可选用________。
(4)为了验证乙烯与溴水的反应是加成反应而不是取代反应,可采取的方法有
______________________________________________________________
_____________________________________________________________。
解析 由“乙烯中可能含有少量还原性气体杂质”、“褪色后的溶液里有少许淡
黄色浑浊物质”可以推断还原性气体为H S。
2
答案 (1)CH ===CH +Br ―→CH BrCH Br
2 2 2 2 2
(2)不能 AC
(3)H S H S+Br ===2HBr+S↓ CuSO 溶液(或NaOH溶液等)
2 2 2 4
(4)分别用pH计测量反应前后溴水的pH,若反应后pH明显减小,则是取代反应