文档内容
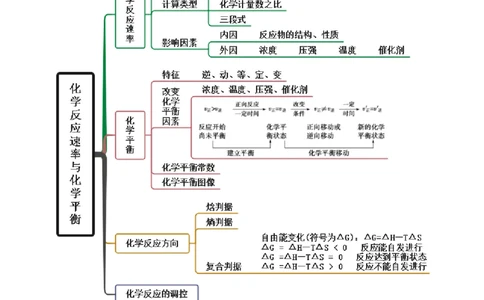
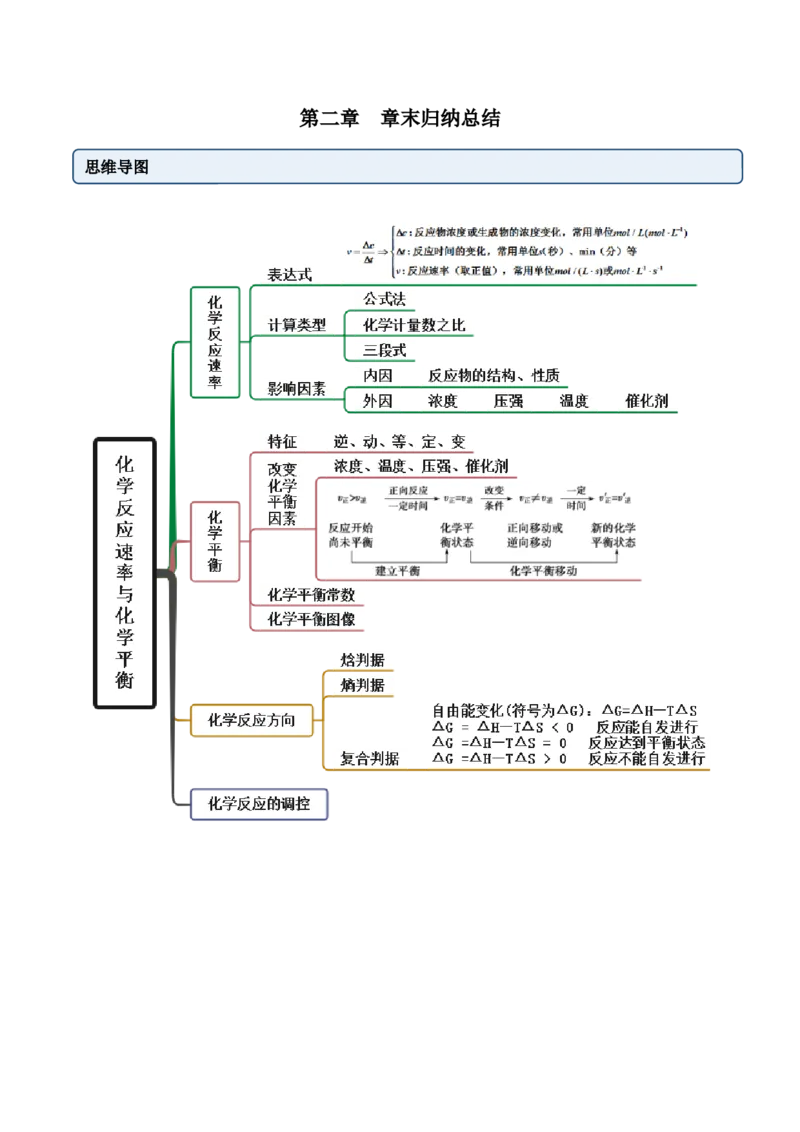
第二章 章末归纳总结
思维导图常见考向
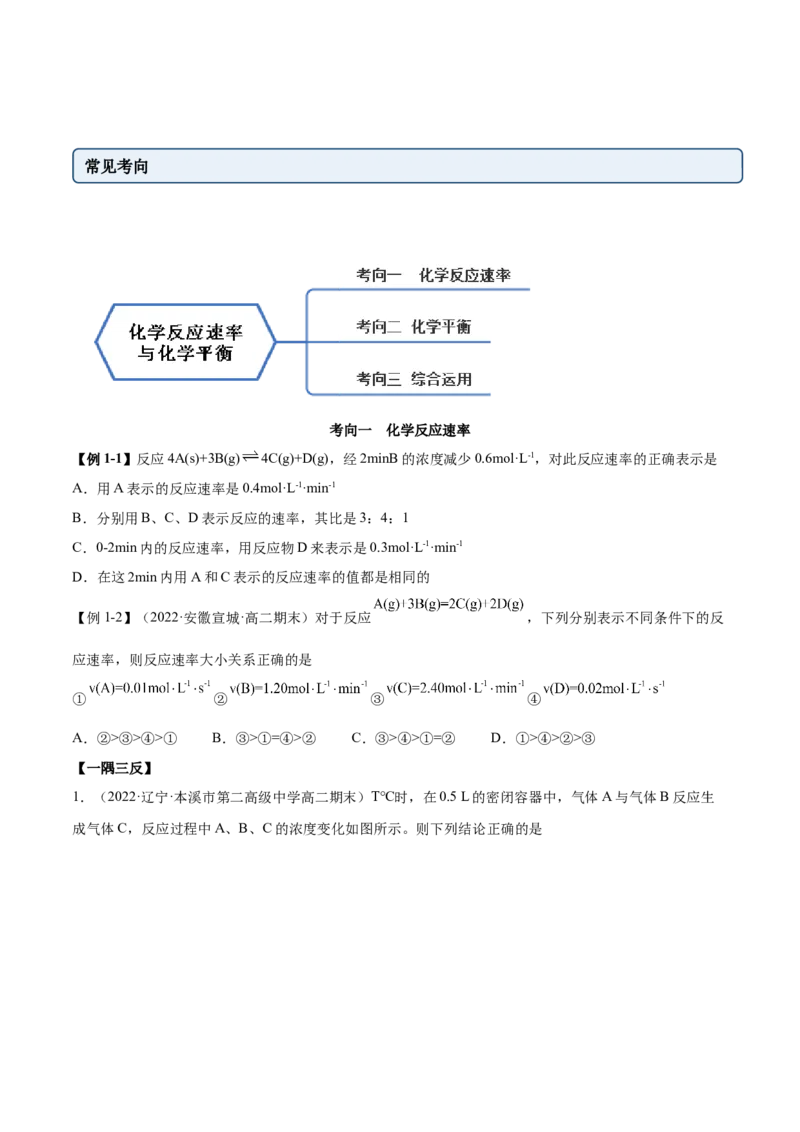
考向一 化学反应速率
【例1-1】反应4A(s)+3B(g) 4C(g)+D(g),经2minB的浓度减少0.6mol·L-1,对此反应速率的正确表示是
A.用A表示的反应速率是0.4mol·L-1·min-1
B.分别用B、C、D表示反应的速率,其比是3:4:1
C.0-2min内的反应速率,用反应物D来表示是0.3mol·L-1·min-1
D.在这2min内用A和C表示的反应速率的值都是相同的
【例1-2】(2022·安徽宣城·高二期末)对于反应 ,下列分别表示不同条件下的反
应速率,则反应速率大小关系正确的是
① ② ③ ④
A.②>③>④>① B.③>①=④>② C.③>④>①=② D.①>④>②>③
【一隅三反】
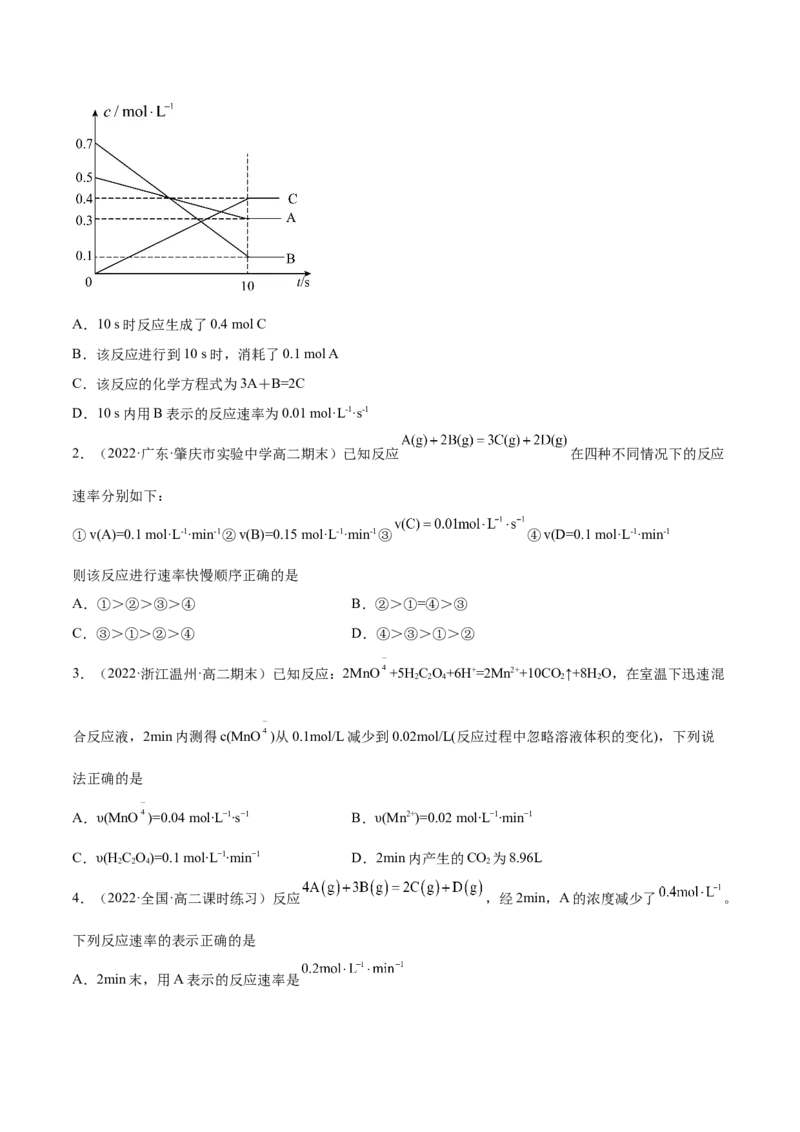
1.(2022·辽宁·本溪市第二高级中学高二期末)T℃时,在0.5 L的密闭容器中,气体A与气体B反应生
成气体C,反应过程中A、B、C的浓度变化如图所示。则下列结论正确的是A.10 s时反应生成了0.4 mol C
B.该反应进行到10 s时,消耗了0.1 mol A
C.该反应的化学方程式为3A+B=2C
D.10 s内用B表示的反应速率为0.01 mol·L-1·s-1
2.(2022·广东·肇庆市实验中学高二期末)已知反应 在四种不同情况下的反应
速率分别如下:
①v(A)=0.1 mol·L-1·min-1②v(B)=0.15 mol·L-1·min-1③ ④v(D=0.1 mol·L-1·min-1
则该反应进行速率快慢顺序正确的是
A.①>②>③>④ B.②>①=④>③
C.③>①>②>④ D.④>③>①>②
3.(2022·浙江温州·高二期末)已知反应:2MnO +5H C O+6H+=2Mn2++10CO ↑+8H O,在室温下迅速混
2 2 4 2 2
合反应液,2min内测得c(MnO )从0.1mol/L减少到0.02mol/L(反应过程中忽略溶液体积的变化),下列说
法正确的是
A.υ(MnO )=0.04 mol∙L−1∙s−1 B.υ(Mn2+)=0.02 mol∙L−1∙min−1
C.υ(H C O)=0.1 mol∙L−1∙min−1 D.2min内产生的CO 为8.96L
2 2 4 2
4.(2022·全国·高二课时练习)反应 ,经2min,A的浓度减少了 。
下列反应速率的表示正确的是
A.2min末,用A表示的反应速率是B.2min内,用B表示的反应速率是
C.2min内,用C表示的反应速率是
D.2min内,用B和C表示的反应速率之比为2∶3
考向二 化学平衡
【例2-1】(2022·陕西渭南·高二期末)在温度T 时,向一体积固定为2L的密闭容器中通入1molCO 和
1 2
3molH 发生反应:CO(g)+3H(g) CHOH(g)+H O(g) H<0,5min后反应达到平衡,CO 的转化率为
2 2 2 3 2 2
20%。下列说法正确的是 △
A.前5min,平均反应速率v(H )=0.06mol(L·min)
2
B.该温度下反应平衡常数的值为
C.当v (CO)=3v (H )时,说明反应已达到平衡状态
正 2 逆 2
D.若平衡后升温,正反应速率减小,逆反应速率增大,平衡左移
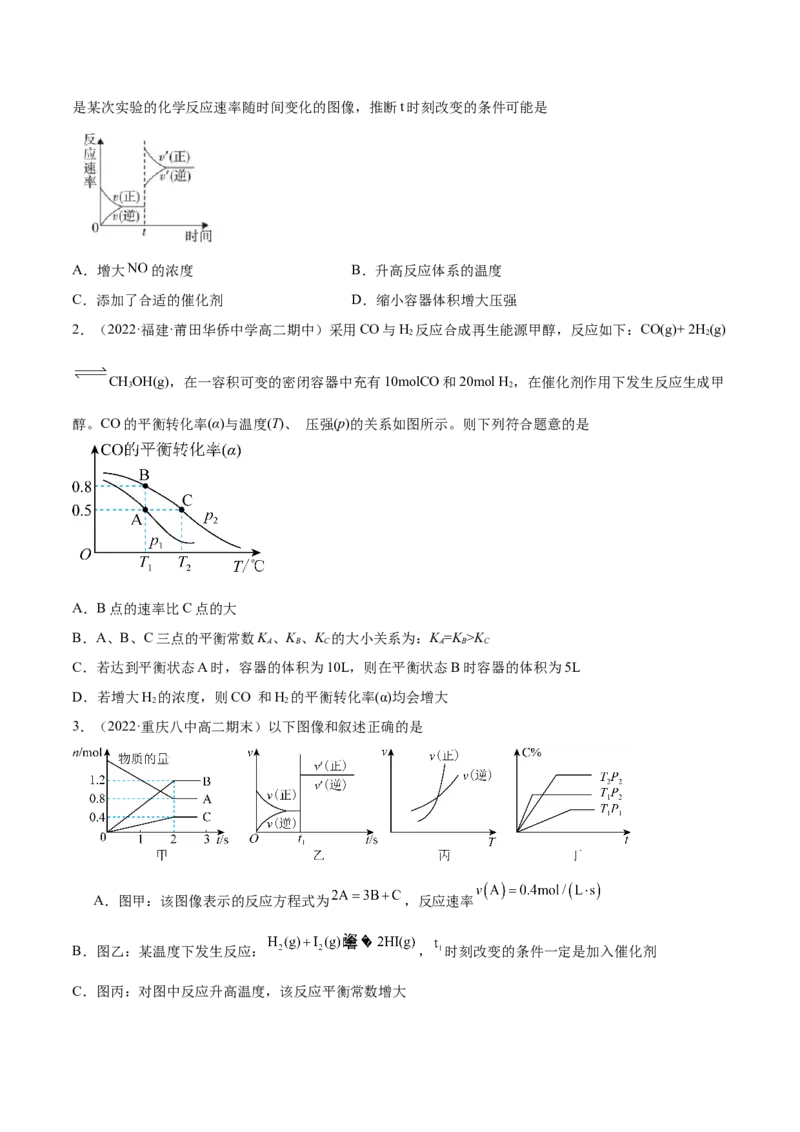
【例2-2】.(2022·陕西·铜川市第一中学高二期末)在某一密封体系中发生反应:
。如图为某一段时间段反应速率与反应时间的山线关系。下列说法正
确的是
A. 内氨的百分含量最高 B. 时刻,向体系中充入
C. 时刻,密封体系体积缩小 D. 时间段内,该反应停止了
【一隅三反】
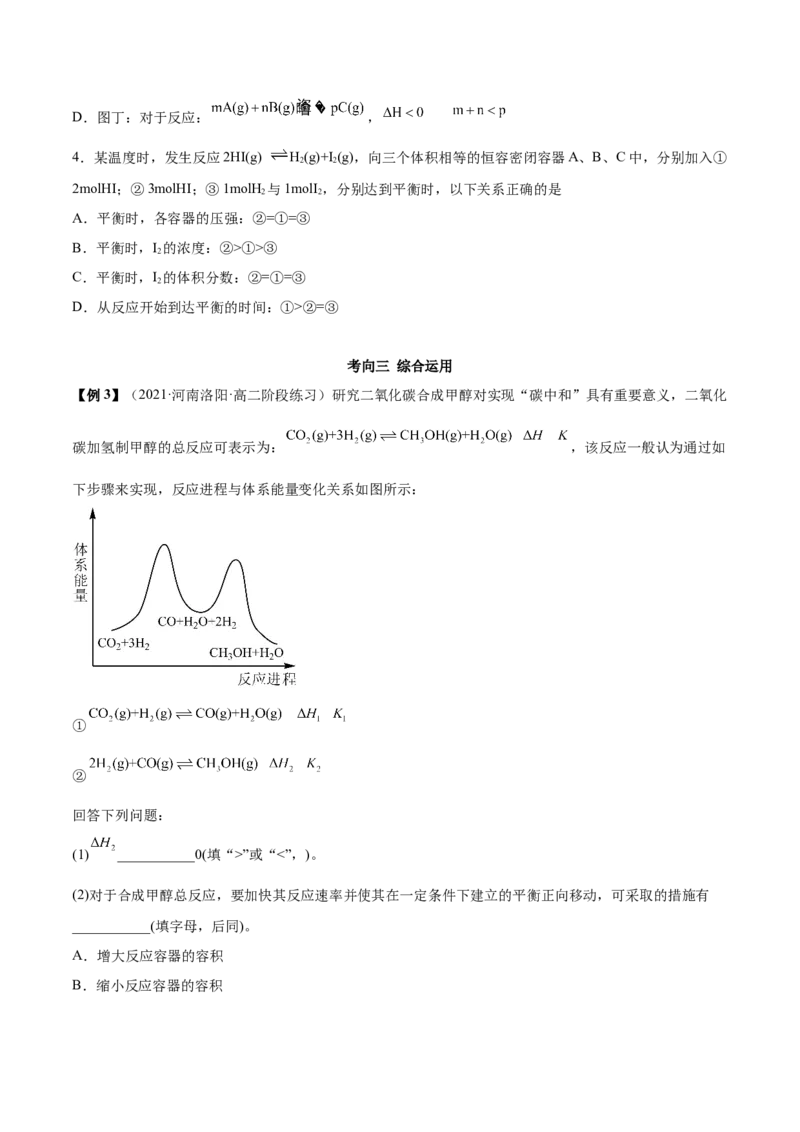
1.(2022·陕西渭南·高二期末)在密闭容器中进行反应: 。如图是某次实验的化学反应速率随时间变化的图像,推断t时刻改变的条件可能是
A.增大 的浓度 B.升高反应体系的温度
C.添加了合适的催化剂 D.缩小容器体积增大压强
2.(2022·福建·莆田华侨中学高二期中)采用CO与H 反应合成再生能源甲醇,反应如下:CO(g)+ 2H (g)
2 2
CHOH(g),在一容积可变的密闭容器中充有10molCO和20mol H,在催化剂作用下发生反应生成甲
3 2
醇。CO的平衡转化率(α)与温度(T)、 压强(p)的关系如图所示。则下列符合题意的是
A.B点的速率比C点的大
B.A、B、C三点的平衡常数K 、K 、K 的大小关系为:K =K >K
A B C A B C
C.若达到平衡状态A时,容器的体积为10L,则在平衡状态B时容器的体积为5L
D.若增大H 的浓度,则CO 和H 的平衡转化率(α)均会增大
2 2
3.(2022·重庆八中高二期末)以下图像和叙述正确的是
A.图甲:该图像表示的反应方程式为 ,反应速率
B.图乙:某温度下发生反应: , 时刻改变的条件一定是加入催化剂
C.图丙:对图中反应升高温度,该反应平衡常数增大D.图丁:对于反应: ,
4.某温度时,发生反应2HI(g) H(g)+I (g),向三个体积相等的恒容密闭容器A、B、C中,分别加入①
2 2
2molHI;②3molHI;③1molH 与1molI ,分别达到平衡时,以下关系正确的是
2 2
A.平衡时,各容器的压强:②=①=③
B.平衡时,I 的浓度:②>①>③
2
C.平衡时,I 的体积分数:②=①=③
2
D.从反应开始到达平衡的时间:①>②=③
考向三 综合运用
【例3】(2021·河南洛阳·高二阶段练习)研究二氧化碳合成甲醇对实现“碳中和”具有重要意义,二氧化
碳加氢制甲醇的总反应可表示为: ,该反应一般认为通过如
下步骤来实现,反应进程与体系能量变化关系如图所示:
①
②
回答下列问题:
(1) ___________0(填“>”或“<”,)。
(2)对于合成甲醇总反应,要加快其反应速率并使其在一定条件下建立的平衡正向移动,可采取的措施有
___________(填字母,后同)。
A.增大反应容器的容积
B.缩小反应容器的容积C.从平衡体系中及时分离出
D.升高温度
E.使用合适的催化剂
(3)一定温度下,将 和 以物质的量之比为1:1充入盛有催化剂的密闭容器中,发生合成甲醇总反应;
某时刻t,当下列量不再变化时,一定能说明该反应处于平衡状态的是___________(填字母)
1
A.平衡常数K不再变化 B. 的体积分数不再变化
C. 的体积分数不再变化 D.反应的焓变 不再变化
(4)500℃时,已知 , 。往2L恒容密闭容器中充入 和 ,测得某时刻t,合成
2
甲醇总反应中 的转化率为66.67%(约转化了 ),则t 时合成甲醇总反应的 ___________
2
(填“>、<”或“=”),并通过计算说明理由___________。
【一隅三反】
1.(2022·广西桂林·高二期末)CO选择性催化还原技术是治理汽车尾气中的CO和 的理想方案之一。
某小组对反应Ⅰ: 展开了如下研究。回答下列问题:
(1)已知:
则反应Ⅰ的 _______kJ/mol。从理论上分析反应Ⅰ在_______条件(填“高温”“低温”或“任何温
度”)可自发反应。
(2)下列能说明在恒温恒容的容器中反应Ⅰ达到平衡状态的是_______(填正确答案的字母代号)。
a.容器内 的百分含量不再随时间变化
b.每消耗4molCO(g)的同时生成1mol
c.容器内气体的压强不再随时间变化d.生成 的速率与消耗CO的速率存在
(3)一定温度下,向一2L密闭容器内充入4molCO(g)和2mol 发生反应Ⅰ,达到平衡时测得CO的物
质的量浓度为1mol/L。
①达到平衡时CO的转化率为_______;该温度下反应Ⅰ平衡常数K的值为_______。
②平衡后,再向容器内充入2mol 和2mol ,平衡会_______(填“向正方向”“向逆方向”或“不”)
移动。
③已知气体的颜色越深,透光率越小。若达到平衡后缩小容器的容积,下列气体透光率随时间变化的示意
图中正确的是_______(填正确答案的字母代号)。
2.(2022·云南·昆明一中高二期中)以煤为原料可合成一系列燃料。回答下列问题:
(1)向1L恒容密闭容器中加入2mol CO、4mol H,在适当的催化剂作用下,发生反应:2CO(g)+4H(g)
2 2
CHOCH (l)+H O(l) H=+71kJ·mol-l
3 3 2
△
①该反应_______自发进行(填“能”、“不能”或“无法判断”);
②下列叙述能说明此反应达到平衡状态的是_______。
a.混合气体的平均相对分子质量保持不变
b.CO和H 的转化率相等
2
c.CO和H 的体积分数保持不变
2
d.混合气体的密度保持不变
e.1mol CO生成的同时有1mol O-H 键断裂
(2)CO (g)+3H(g) CHOH(g)+H O(g) H<0,在一定条件下,某反应过程中部分数据如下表:
2 2 3 2
△
反应条件 反应时间 CO/mol H/mol CHOH/mol HO/mol
2 2 3 20min 2 6 0 0
10min 4.5
恒温恒容(T℃、2L)
1
20min 1
30min 1
①0~10min内,用HO(g)表示的化学反应速率v(H O)=_______mol/(L ·min)。
2 2
②T℃,该反应的平衡常数K=_______ (用分数表示),平衡时H 的转化率是_______。
1 2
③在其它条件不变的情况下,若30min时改变温度为T℃,再次平衡时H 的物质的量为3.2mol,则
2 2
T_______T(填“>”“<”或“=”),理由是_______; 在其他条件不变的情况下,若30min时向容器中
1 2
再充入1mol CO(g)和1mol HO(g),则平衡_______移动(填“正向”、“逆向”或“不”)。
2 2
3.(2022·湖南·株洲市第八中学高二期末)研究碳及其化合物的资源化利用具有重要的意义。回答下列问
题:
(1)已知下列热化学方程式:
反应Ⅰ:CO(g)+4H(g) = CH(g)+2HO(g) ΔH=-164.9kJ/mol。
2 2 4 2 1
反应Ⅱ:CO(g)+H(g)= CO(g)+H O(g) ΔH=+41.2kJ/mol
2 2 2 2
则反应CH(g)+HO(g)= CO(g)+3H (g)的ΔH=_______kJ/mol。
4 2 2 3
(2)在T℃时,将1molCO 和3molH 加入容积不变的密闭容器中,发生反应Ⅰ:CO(g)+4H(g) CH(g)
2 2 2 2 4
+2H O(g),实验测得CO 的体积分数φ(CO)如表所示:
2 2 2
t/min 0 10 20 30 40 50
φ(CO) 0.25 0.23 0.214 0.202 0.200 0.200
2
①能判断反应CO(g)+4H(g) CH(g)+2HO(g)达到平衡的是_______(填标号)。
2 2 4 2
A.CO 的消耗速率和CH 的生成速率相等
2 4
B.混合气体的密度不再发生变化
C.容器内气体压强不再发生变化
D.混合气体的平均相对分子质量不再发生变化
②达到平衡时CO 的转化率为_______%(结果保留三位有效数字)。
2
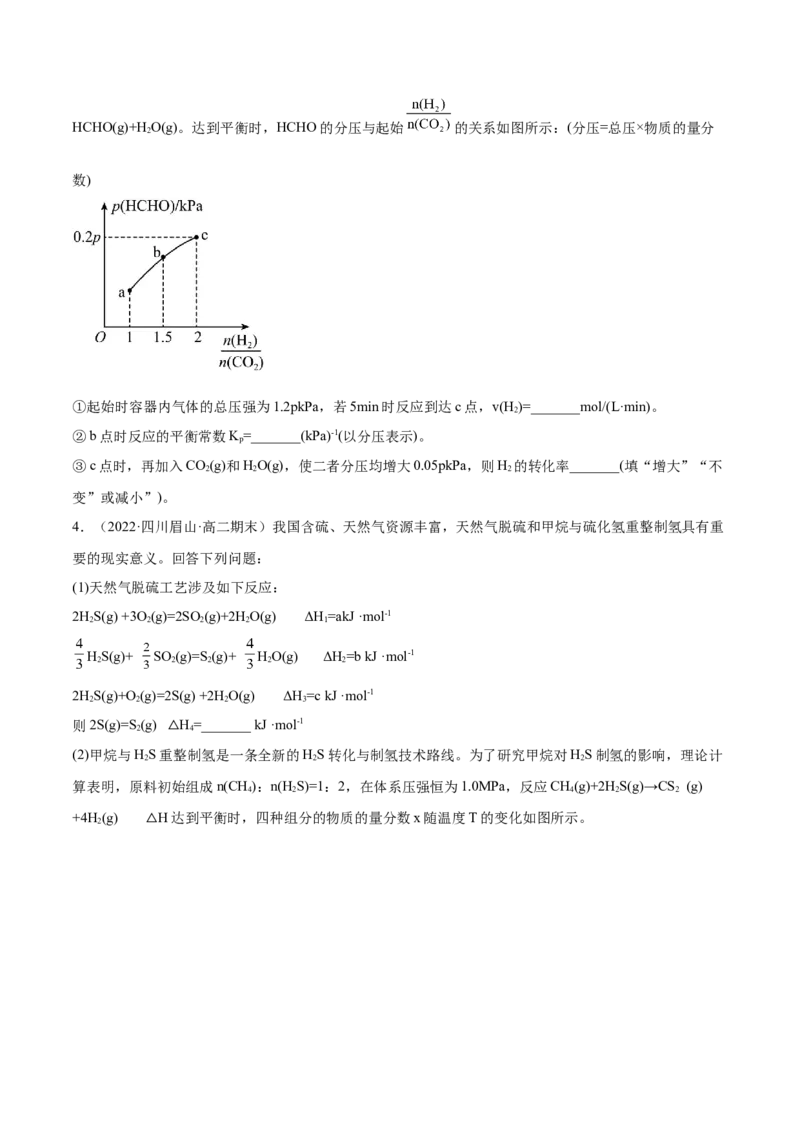
(3)在T℃时,向容积为2L的恒容密闭容器中充入1molCO 和一定量的H 发生反应:CO(g)+2H(g)
2 2 2 2HCHO(g)+HO(g)。达到平衡时,HCHO的分压与起始 的关系如图所示:(分压=总压×物质的量分
2
数)
①起始时容器内气体的总压强为1.2pkPa,若5min时反应到达c点,v(H )=_______mol/(L·min)。
2
②b点时反应的平衡常数K=_______(kPa)-1(以分压表示)。
p
③c点时,再加入CO(g)和HO(g),使二者分压均增大0.05pkPa,则H 的转化率_______(填“增大”“不
2 2 2
变”或减小”)。
4.(2022·四川眉山·高二期末)我国含硫、天然气资源丰富,天然气脱硫和甲烷与硫化氢重整制氢具有重
要的现实意义。回答下列问题:
(1)天然气脱硫工艺涉及如下反应:
2HS(g) +3O (g)=2SO(g)+2HO(g) ΔH=akJ ·mol-1
2 2 2 2 1
HS(g)+ SO (g)=S (g)+ HO(g) ΔH=b kJ ·mol-1
2 2 2 2 2
2HS(g)+O(g)=2S(g) +2H O(g) ΔH=c kJ ·mol-1
2 2 2 3
则2S(g)=S(g) H=_______ kJ ·mol-1
2 4
(2)甲烷与H
2
S重△整制氢是一条全新的H
2
S转化与制氢技术路线。为了研究甲烷对H
2
S制氢的影响,理论计
算表明,原料初始组成n(CH):n(H S)=1:2,在体系压强恒为1.0MPa,反应CH(g)+2HS(g)→CS (g)
4 2 4 2 2
+4H (g) H达到平衡时,四种组分的物质的量分数x随温度T的变化如图所示。
2
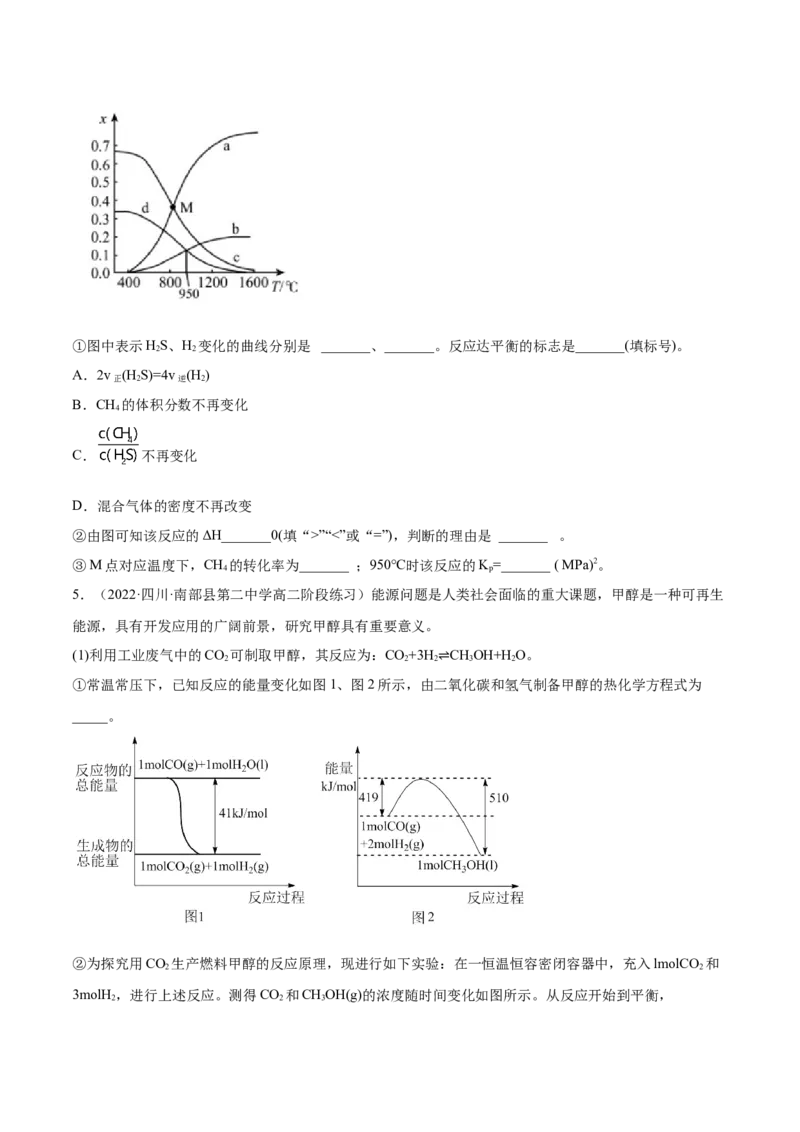
△①图中表示HS、H 变化的曲线分别是 _______、_______。反应达平衡的标志是_______(填标号)。
2 2
A.2v (H S)=4v (H )
正 2 逆 2
B.CH 的体积分数不再变化
4
C. 不再变化
D.混合气体的密度不再改变
②由图可知该反应的ΔH_______0(填“>”“<”或“=”),判断的理由是 _______ 。
③M点对应温度下,CH 的转化率为_______ ;950℃时该反应的K=_______ ( MPa)2。
4 p
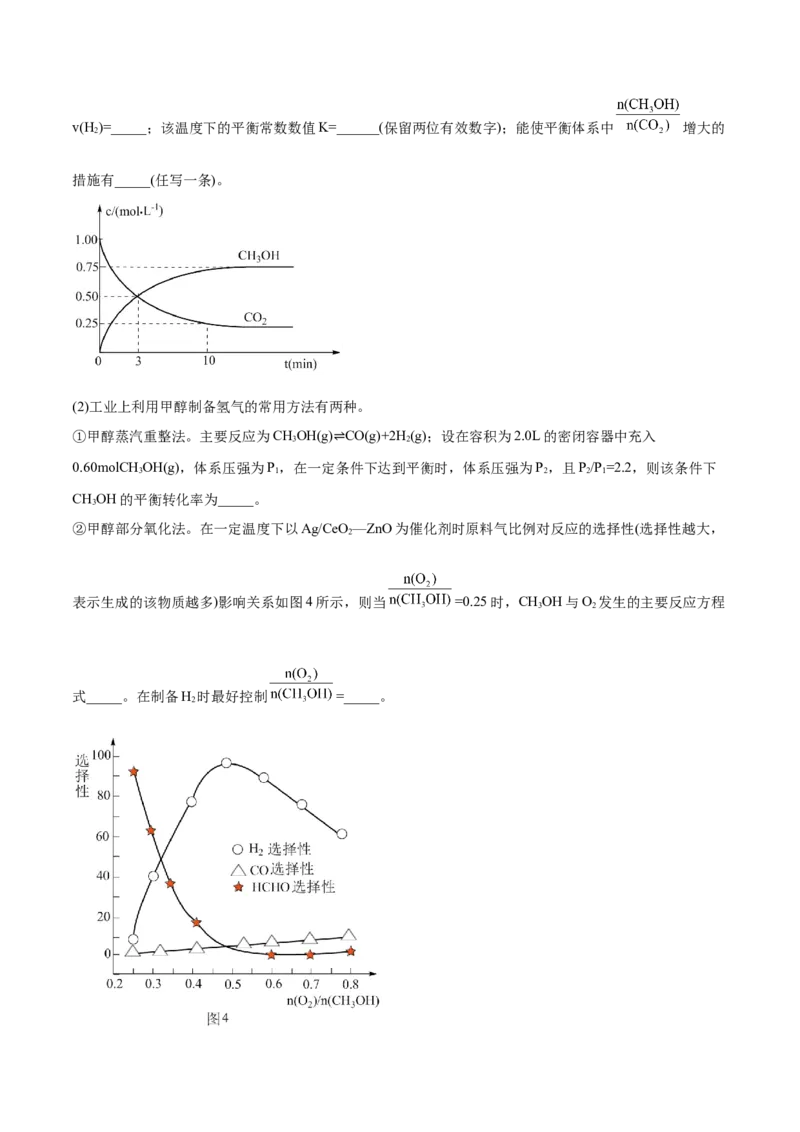
5.(2022·四川·南部县第二中学高二阶段练习)能源问题是人类社会面临的重大课题,甲醇是一种可再生
能源,具有开发应用的广阔前景,研究甲醇具有重要意义。
(1)利用工业废气中的CO 可制取甲醇,其反应为:CO+3H CHOH+H O。
2 2 2 3 2
①常温常压下,已知反应的能量变化如图1、图2所示,由二⇌氧化碳和氢气制备甲醇的热化学方程式为
_____。
②为探究用CO 生产燃料甲醇的反应原理,现进行如下实验:在一恒温恒容密闭容器中,充入lmolCO 和
2 2
3molH ,进行上述反应。测得CO 和CHOH(g)的浓度随时间变化如图所示。从反应开始到平衡,
2 2 3v(H )=_____;该温度下的平衡常数数值K=______(保留两位有效数字);能使平衡体系中 增大的
2
措施有_____(任写一条)。
(2)工业上利用甲醇制备氢气的常用方法有两种。
①甲醇蒸汽重整法。主要反应为CHOH(g) CO(g)+2H(g);设在容积为2.0L的密闭容器中充入
3 2
0.60molCHOH(g),体系压强为P,在一定⇌条件下达到平衡时,体系压强为P,且P/P =2.2,则该条件下
3 1 2 2 1
CHOH的平衡转化率为_____。
3
②甲醇部分氧化法。在一定温度下以Ag/CeO—ZnO为催化剂时原料气比例对反应的选择性(选择性越大,
2
表示生成的该物质越多)影响关系如图4所示,则当 =0.25时,CHOH与O 发生的主要反应方程
3 2
式_____。在制备H 时最好控制 =_____。
26.(2022·浙江绍兴·高二期末)合成气(CO+H)在煤化工和天然气化工中有着十分重要的地位,由合成气
2
可合成多种有机基础原料和产品。
(1)煤化工中生产合成气的反应为: ,
①该反应的平衡常数表达式为___________
②判断该反应的自发性___________
③在恒温恒容下,同时放入 、 、 、 四种物质,下列事实能够说明反应
已达到平衡的是___________。
A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有 键断裂的同时有 键断裂
D.混合气体的平均相对分子质量保持不变
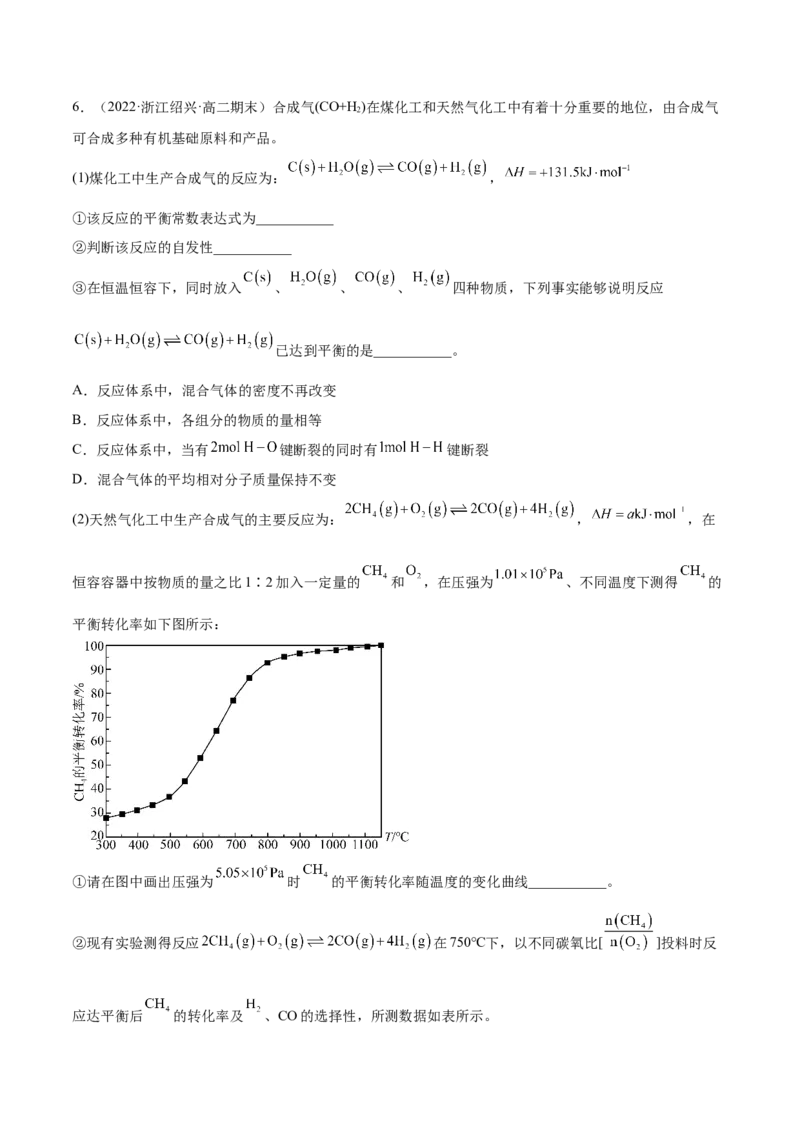
(2)天然气化工中生产合成气的主要反应为: , ,在
恒容容器中按物质的量之比1∶2加入一定量的 和 ,在压强为 、不同温度下测得 的
平衡转化率如下图所示:
①请在图中画出压强为 时 的平衡转化率随温度的变化曲线___________。
②现有实验测得反应 在750℃下,以不同碳氧比[ ]投料时反
应达平衡后 的转化率及 、CO的选择性,所测数据如表所示。已知:选择性=目标产物的产率/反应原料的转化率
1∶0.25 1∶0.5 1∶1 1∶1.25
碳氧比[ ]
转化率 0.40 0.88 0.98 0.99
选择性 0.98 0.93 0.67 0.40
CO选择性 0.99 0.94 0.65 0.32
最佳碳氧比[ ]为___________。
假设按碳氧比 投料,反应容器的体积为VL,通入 和 各amol,请列式表示平衡时容
器内CO的浓度___________(用a、V的代数式表示)倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育