文档内容
第二章 章末测试(提升)
满分100分,考试用时75分钟
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的
1.(2022·浙江 )下列有关化学及应速率的说法中错误的是
A.决定化学反应速率的主要因素是反应物本身的性质
B.同一化学反应,用不同物质的浓度变化所表示的化学反应速率的数值不一定相同
C.某些反向选用适当的催化剂,能降低反应所需活化能,可以降低反应所需的温度
D.对于反应 单位时间内的化学反应速率有
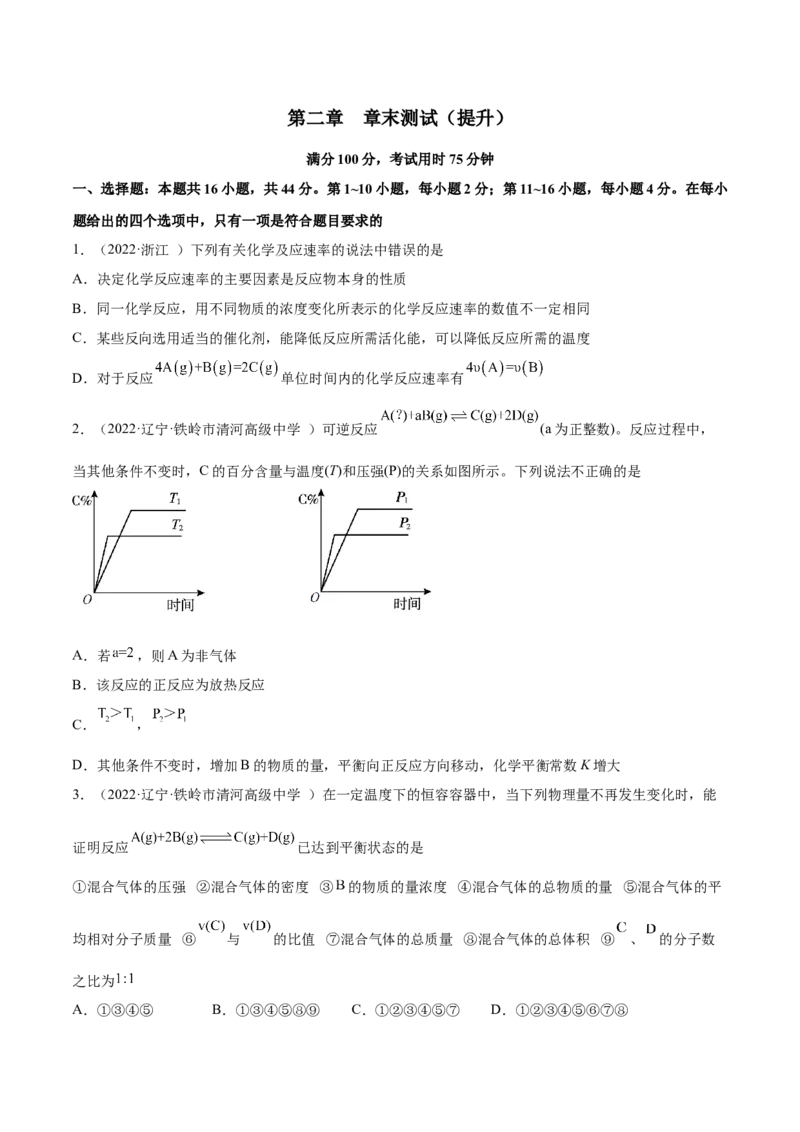
2.(2022·辽宁·铁岭市清河高级中学 )可逆反应 (a为正整数)。反应过程中,
当其他条件不变时,C的百分含量与温度(T)和压强(P)的关系如图所示。下列说法不正确的是
A.若 ,则A为非气体
B.该反应的正反应为放热反应
C. ,
D.其他条件不变时,增加B的物质的量,平衡向正反应方向移动,化学平衡常数K增大
3.(2022·辽宁·铁岭市清河高级中学 )在一定温度下的恒容容器中,当下列物理量不再发生变化时,能
证明反应 已达到平衡状态的是
①混合气体的压强 ②混合气体的密度 ③ 的物质的量浓度 ④混合气体的总物质的量 ⑤混合气体的平
均相对分子质量 ⑥ 与 的比值 ⑦混合气体的总质量 ⑧混合气体的总体积 ⑨ 、 的分子数
之比为
A.①③④⑤ B.①③④⑤⑧⑨ C.①②③④⑤⑦ D.①②③④⑤⑥⑦⑧4.(2021·全国·高二单元测试)升高温度时,化学反应速率加快,主要原因是
A.该化学反应的过程是吸热的
B.反应物分子能量增加,活化分子百分数增大,有效碰撞次数增多
C.该化学反应的过程是放热的
D.分子运动速率加快,使反应物分子间的碰撞机会增多
5.(2022广东)在25 ℃时,密闭容器中X+3Y 2Z三种气体的初始浓度和平衡浓度如表,下列说法错误
的是 ⇌
物质 X Y Z
初始浓度/molL-1 0.1 0.2 0
平衡浓度/mol ⋅ L-1 0.05 0.05 0.1
A.反应达到平⋅ 衡时,X的转化率为50%
B.改变温度可以改变此反应的平衡常数
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.降低温度,正逆反应速率都减小
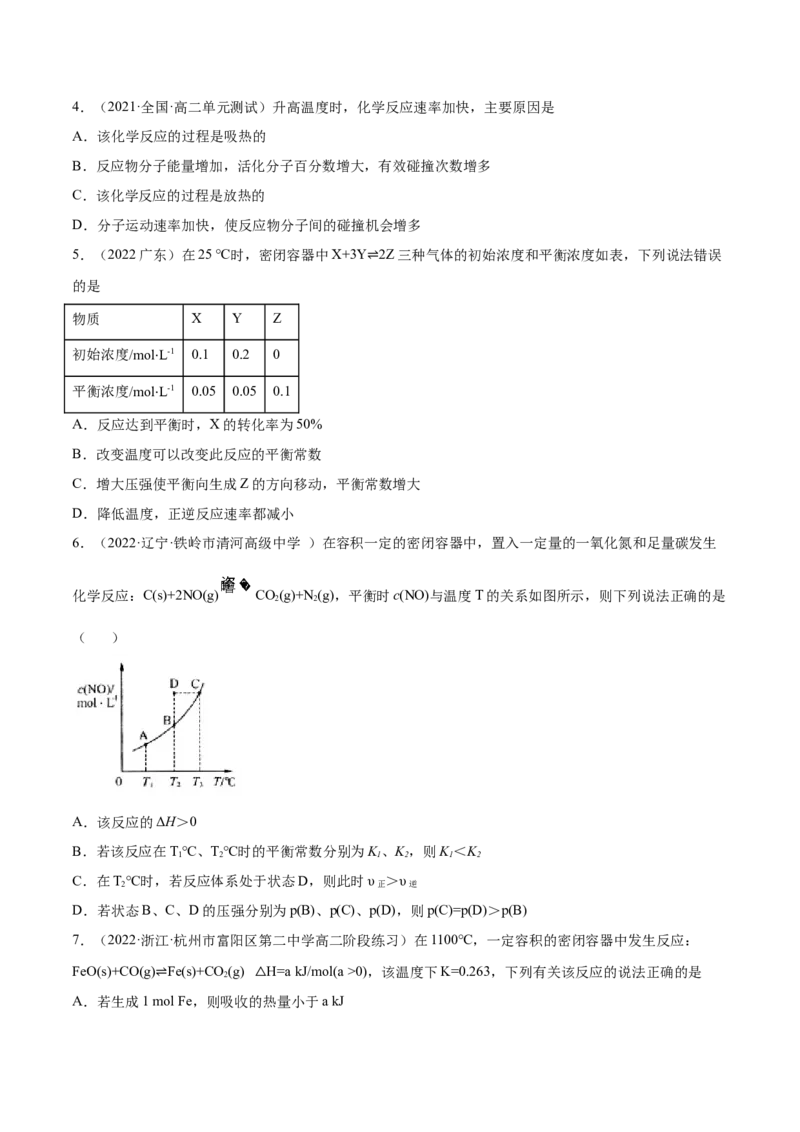
6.(2022·辽宁·铁岭市清河高级中学 )在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生
化学反应:C(s)+2NO(g) CO(g)+N(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是
2 2
( )
A.该反应的ΔH>0
B.若该反应在T℃、T℃时的平衡常数分别为K 、K ,则K <K
1 2 1 2 1 2
C.在T℃时,若反应体系处于状态D,则此时υ >υ
2 正 逆
D.若状态B、C、D的压强分别为p(B)、p(C)、p(D),则p(C)=p(D)>p(B)
7.(2022·浙江·杭州市富阳区第二中学高二阶段练习)在1100℃,一定容积的密闭容器中发生反应:
FeO(s)+CO(g) Fe(s)+CO (g) H=a kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是
2
A.若生成1 m⇌ol Fe,则吸收的△热量小于a kJB.若升高温度,则正反应速率加快,逆反应速率加快,化学平衡逆向移动
C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态
D.达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO)=0.0263 mol/L
2
8.(2022·吉林·吉化第一高级中学校 )实验室用 粒与稀盐酸反应制备 时反应速率太慢,为了加快
反应速率,下列方法可行的是
A.加入浓 B.加入
C.使 粒过量 D.滴入几滴 溶液
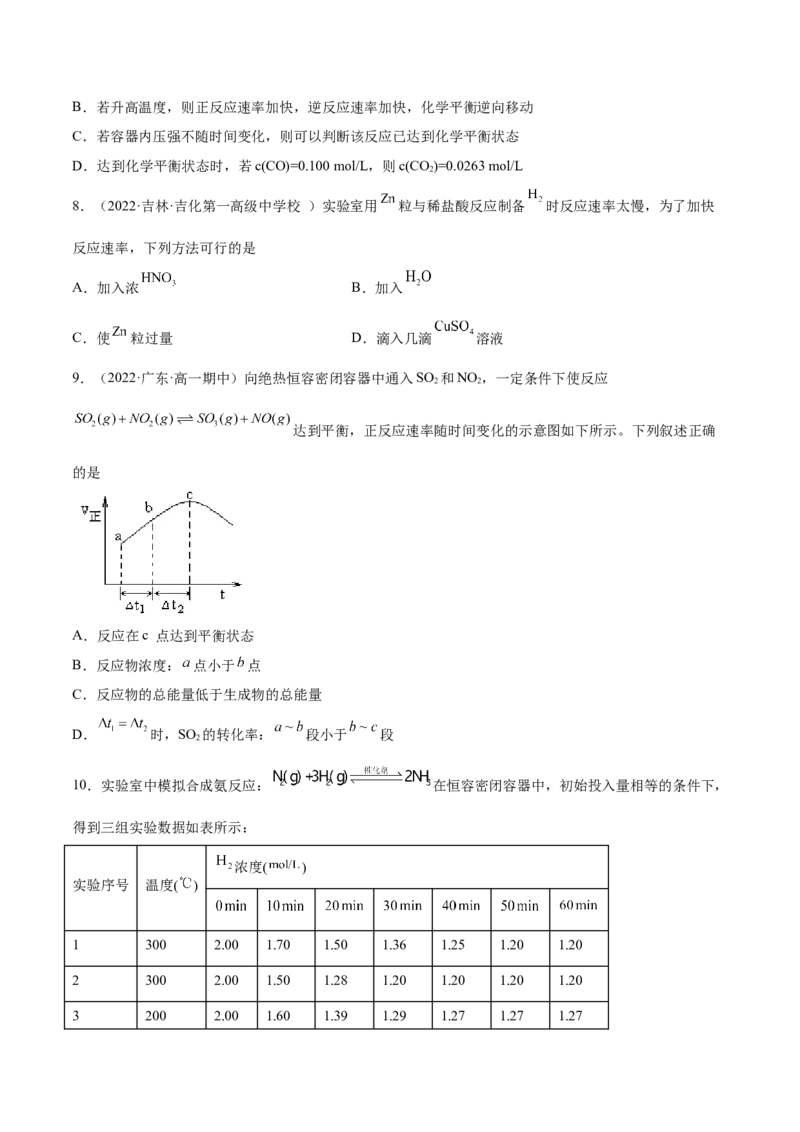
9.(2022·广东·高一期中)向绝热恒容密闭容器中通入SO 和NO ,一定条件下使反应
2 2
达到平衡,正反应速率随时间变化的示意图如下所示。下列叙述正确
的是
A.反应在c 点达到平衡状态
B.反应物浓度: 点小于 点
C.反应物的总能量低于生成物的总能量
D. 时,SO 的转化率: 段小于 段
2
10.实验室中模拟合成氨反应: 在恒容密闭容器中,初始投入量相等的条件下,
得到三组实验数据如表所示:
浓度( )
实验序号 温度( )
1 300 2.00 1.70 1.50 1.36 1.25 1.20 1.20
2 300 2.00 1.50 1.28 1.20 1.20 1.20 1.20
3 200 2.00 1.60 1.39 1.29 1.27 1.27 1.27下列有关说法不正确的是
A.当容器内的压强不再改变时,说明该可逆反应已达到化学平衡状态
B.实验2中,前 内以 的浓度变化表示的化学反应速率为
C.比较实验1和2,说明实验2使用了更高效的催化剂
D.实验3中, 时向容器中充入一定量 ,则正反应速率 不变
11.(2022·辽宁·铁岭市清河高级中学 )下列叙述与图对应的是
A.对于达到平衡状态的反应:N(g)+3H(g) 2NH (g),图①表示在t 时刻充入了一定量的NH ,平衡逆向
2 2 3 0 3
移动 ⇌
B.由图②可知,P>P、T>T 满足反应:2A(g)+B(g) 2C(g) ΔH<0
2 1 1 2
C.图③表示的反应方程式为:2A=B+3C ⇌
D.对于反应2X(g)+3Y(g) 3Z(g) ΔH<0,图④y轴可以表示Y的百分含量
12.(2022·吉林·吉化第一⇌高级中学校 )一定条件下,体积为2 L的密闭容器中,2 mol X和3 mol Y进行
反应:X(g)+Y(g) Z(g),经12 s达到平衡,生成0.6 mol Z。下列说法正确的是
A.以X浓度变化⇌表示的反应速率为0.05 mol/(L•s)
B.其他条件不变,增大X的浓度,平衡右移,X的转化率增大
C.其他条件不变,12 s后将容器体积扩大为10 L,Z的平衡浓度变为0.06 mol/L
D.12 s达平衡时Y的转化率为20%
13.下列说法正确的是
A.H(g)+I(g) 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变
2 2
B.C(s)+H
2
O(g)⇌ H
2
(g)+CO(g),碳的质量不再改变说明反应已达平衡
C.若压强不再随时⇌间变化能说明反应2A(?)+B(g) 2C(?)已达平衡,则A、C不能同时是气体
D.1 mol N
2
和3 mol H
2
反应达到平衡时H
2
转化率为⇌10%,放出的热量为Q
1
;在相同温度和压强下,当2
mol NH 分解为N 和H 的转化率为10%时,吸收的热量为Q,Q 不等于Q
3 2 2 2 2 1
14.(2022·陕西·西北农林科技大学附中高二期末)在3种不同条件下,分别向容积为2 L的恒容密闭容器中充入2 mol A和1 mol B,发生反应:2A (g)+B (g) 2C (g) H=Q kJ/mol,相关条件和数据
△
见表:
实验编号 实验I 实验II 实验III
反应温度/℃ 700 700 750
达平衡时间/min 40 5 30
平衡时n(C) /mol 1.5 1.5 1
化学平衡常数 K K K
1 2 3
下列说法正确的是( )
A.K<K<K
1 2 3
B.升高温度能加快反应速率的原因是降低了反应的活化能
C.实验II比实验I达平衡所需时间小的可能原因是使用了催化剂
D.实验Ⅲ达平衡后,恒温下再向容器中通入1 mol A和1 mol C,平衡正向移动
15.用CO合成甲醇(CHOH)的化学方程式为CO(g)+2H(g) CHOH(g) ΔH<0,按照相同的物质的量
3 2 3
投料,测得CO在不同温度下的平衡转化率与压强的关系如图所示。下列说法正确的是( )
A.温度:T>T>T
1 2 3
B.正反应速率:v(a)>v(c)、v(b)>v(d)
C.平衡常数:K(a)>K(c)、K(b)=K(d)
D.平均摩尔质量:M(a)<M(c)、M(b)>M(d)
16.(2021·全国·高二单元测试)如图,I是恒压密闭容器,II是恒容密闭容器。其它条件相同时,在I、II
中分n别加入2molX和2molY,起始时容器体积均为VL,发生如下反应并达到平衡(X、Y状态未知):
2X(?)+Y(?) aZ(g)。此时I中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是
⇌A.若X、Y均为气态,则平衡时气体平均摩尔质量:II>I,
B.若X、Y不均为气态,则平衡时气体平均摩尔质量:I>II
C.若X为固态,Y为气态,则I、II中从起始到平衡所需时间相同
D.平衡时I容器的体积小于VL
二、非选择题:共56分。
17.(2022云南)(14分)Ⅰ.一定条件下,在容积为 的密闭容器中, 、B、C三种气体的物质的量
随时间 的变化如图甲所示。已知达到平衡后,降低温度,A的体积分数减小。
(1)该反应的化学方程式为____________。
(2)该反应的反应速率 随时间 的关系如图乙所示。
①根据图乙判断,在 时刻改变的外界条件是_____________。
② 、 、 对应的平衡状态中,C的体积分数最大的是状态________。
③各阶段的平衡常数如下表所示:
、 、 之间的大小关系为__________(用“ ”“ ”或“ ”连接)。Ⅱ.在密闭容器中充入一定量的 ,发生反应: ,如图丙所示为 气体
分解生成 和 的平衡转化率与温度、压强的关系。
(3) ________(填“ ”“ ”或“ ”)0。
(4)图丙中压强( 、 、 )由大到小的顺序为________。
(5)图丙中 点对应的平衡常数 ________ (用平衡分压代替平衡浓度计算,分压 总压 物质的量
分数)。
(6)如果想进一步提高 的转化率,除改变温度、压强外,还可以采取的措施有__________。
18.(12分)回答下列问题:
(1)实验室用30%左右的硫酸溶液(约3.7mol/L)与锌粒反应制取氢气。下列措施中能加快反应速率的是
_______
A.降低反应温度 B.将锌粒改为锌粉
C.将所用硫酸加水稀释 D.加入少量的硫酸铜溶液
(2)目前工业上可用CO 来生产燃料甲醇,有关反应为: 。现向体
2
积为1L的密闭容器中,充入1molCO 和3molH ,反应过程中测得CO 和CHOH(g)的浓度随时间的变化如
2 2 2 3
图所示。①计算3min内用氢气表示的该反应的反应速率v(H )=_______;3min时,正反应速率_______逆反应速率
2
(填:“>”“=”或“<”)。
②10min反应达平衡,氢气的转化率为_______。当反应达平衡后,维持温度和压强不变,改变其它条件
使反应速率增大,采取的措施_______(写一条即可)
③在其他条件不变的情况下,将体系体积压缩到原来的二分之一,下列有关该体系的说法正确的是
_______
A.氢气的浓度减小 B.正反应速率增大 C.逆反应速率减小 D.达到平衡的时间不会
改变
19.(2022·云南省楚雄彝族自治州民族中学高二阶段练习)(16分) 、 、 均为大气污染物,
它们在一定条件下可以转化为其他物质,以减少对环境的污染。
(1)一定条件下,将 与 置于恒容密闭容器中发生反应 ,下列
状态能说明该反应达到化学平衡的是_____(填序号)。
A.混合气体的密度保持不变
B. 的转化率保持不变
C. 和 的物质的量之比保持不变
D. 的消耗速率和 的消耗速率相等
(2)已知反应 ,在不同条件时 的体积分数随时间 的变化如图甲所
示。根据图像可以判断曲线 、 对应的下列反应条件中不同的是_____(填序号)。
A.压强 B.温度 C.催化剂(3) 和 在一定条件下可以合成甲醇: 。现在体积为 的恒容
密闭容器(如图乙所示)中通入 和 ,测定不同时间、不同温度下容器中 的物质的量,
结果如表所示:
请回答下列问题。
① _____(填“>”或“<”或“=”) ,理由是______________。已知 时,第 时容器内压强不再
改变,此时 的转化率为_____,该温度下的化学平衡常数为________。
②若将 和 通入原体积为 的恒压密闭容器(如图丙所示)中, 时该反应的平衡常数为
______;若再向容器中通入 ,重新达到平衡时, 在体系中的体积分数______
(填“变大”“变小”或“不变”)。
20.(14分)研究氮氧化物之间的转化具有重要意义。
(1)已知:NO(g) 2NO (g)ΔH>0将一定量NO 充入恒容密闭容器中,控制反应温度为T。
2 4 2 2 4 1
①下列可以作为反⇌应达到平衡的判据是___。
A.气体的压强不变
B.v (N O)=2v (NO )
正 2 4 逆 2
C.K不变
D.容器内气体的密度不变E.容器内颜色不变
②t时刻反应达到平衡,混合气体平衡总压强为P,NO 气体的平衡转化率为75%,则反应的
2 4
NO(g) 2NO (g)的平衡常数K =___(对于气相反应,用某组分B的平街压强P(B)代替物质的量浓度c(B)也
2 4 2 p
可表示平⇌衡常数,记作K ,如P(B)= P∙x(B),P为平衡总压强,x(B)为平衡系统中B的物质的量分数)。
P
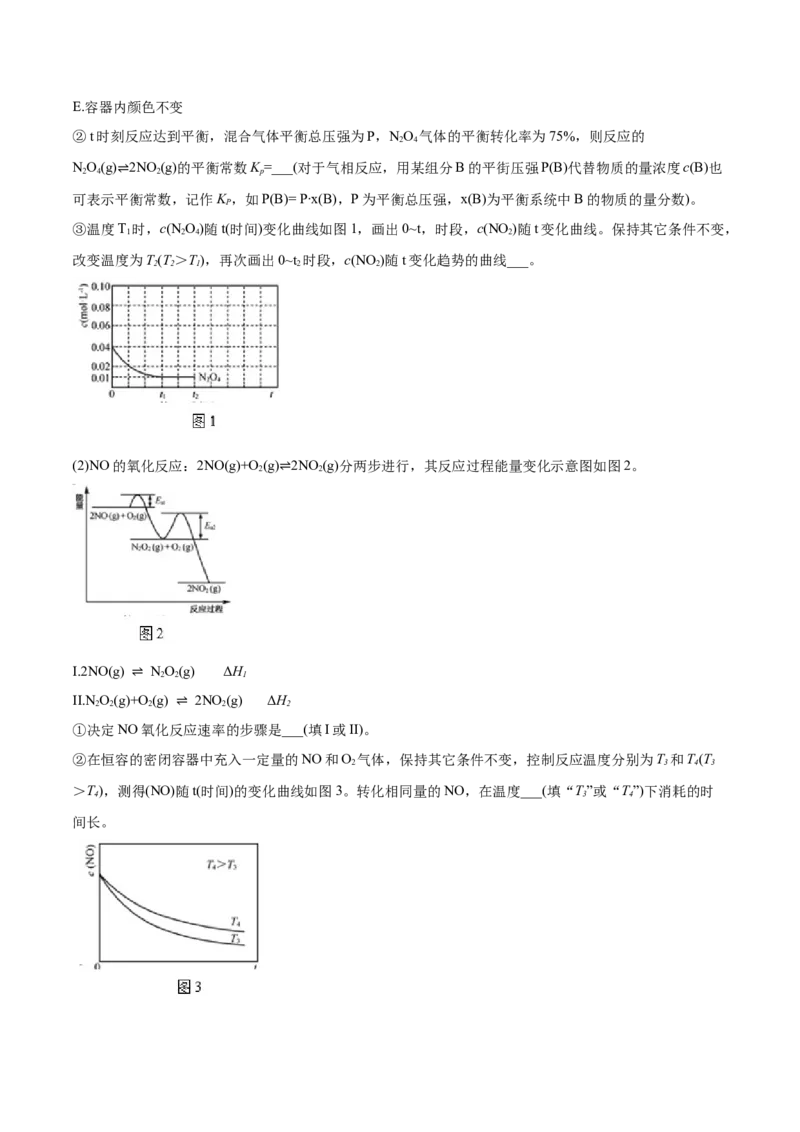
③温度T 时,c(N O)随t(时间)变化曲线如图1,画出0~t,时段,c(NO )随t变化曲线。保持其它条件不变,
1 2 4 2
改变温度为T(T>T),再次画出0~t 时段,c(NO )随t变化趋势的曲线___。
2 2 1 2 2
(2)NO的氧化反应:2NO(g)+O (g) 2NO (g)分两步进行,其反应过程能量变化示意图如图2。
2 2
⇌
I.2NO(g) NO(g) ΔH
2 2 1
II.N
2
O
2
(g)+⇌O
2
(g) 2NO
2
(g) ΔH
2
①决定NO氧化反⇌应速率的步骤是___(填I或II)。
②在恒容的密闭容器中充入一定量的NO和O 气体,保持其它条件不变,控制反应温度分别为T 和T(T
2 3 4 3
>T),测得(NO)随t(时间)的变化曲线如图3。转化相同量的NO,在温度___(填“T”或“T”)下消耗的时
4 3 4
间长。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育