文档内容
第一章章末检查
一、选择题
1.下列关于共价键的说法,正确的是( )
A. 分子内部一定会存在共价键
B. 由非金属元素组成的化合物内部一定全是共价键
C. 非极性键只存在于双原子单质分子中
D. 离子化合物的内部可能存在共价键
2.下列说法正确的是( )
A. 已知N—N键能为193kJ·mol-1,故NN的键能之和为193kJ·mol-1×3
B. H—H键能为436.0kJ·mol-1,F—F键能为157kJ·mol-1,故F 比H 稳定
2 2
C. 某元素原子最外层有1个电子,它跟卤素相结合时,所形成的化学键为离子键
D. N—H键键能为390.8kJ·mol-1,其含义为形成1mol N—H所释放的能量为390.8kJ
3.碘单质在水溶液中溶解度很小,但在CCl 中溶解度很大,这是因为( )
4
A. CCl 和I 都不含氢元素,而HO中含有氢元素
4 2 2
B. CCl 和I 都是非极性分子,而HO是极性分子
4 2 2
C. CCl 与I 都是直线形分子,而HO不是直线形分子
4 2 2
D. CCl 与I 相对分子质量相差较小,而HO与I 相对分子质量相差较大
4 2 2 2
4.下列物质中含离子键的是( )
A. Cl B. CO C. NaCl D. CH
2 2 4
5.下列说法正确的是( )
A. SO 与CO 的分子立体构型均为直线形
2 2
B. HO和NH 中的中心原子杂化方式相同
2 3
C. SiO 中的键长大于CO 中的键长,所以SiO 的熔点比CO 高
2 2 2 2
D. 凡是具有规则外形的固体都是晶体
6.用价层电子对互斥理论预测HO和CH 的立体结构两个结论都正确的是( )
2 4
A. 直线形,三角锥形 B. V形,三角锥形
C. 直线形,正四面体形 D. V形,正四面体形
7.通常把原子总数和价电子总数相同的分子或离子称为等电子体.人们发现等电子体的空间结构相
同,则下列有关说法中正确的是( )
A. CH 和NH +是等电子体,键角均为60°
4 4
B. NO ﹣和CO2﹣是等电子体,均为平面正三角形结构
3 3
C. HO+和PCl 是等电子体,均为三角锥形结构
3 3D. B NH 和苯是等电子体,B NH 分子中不存在“肩并肩”式重叠的轨道
3 3 6 3 3 6
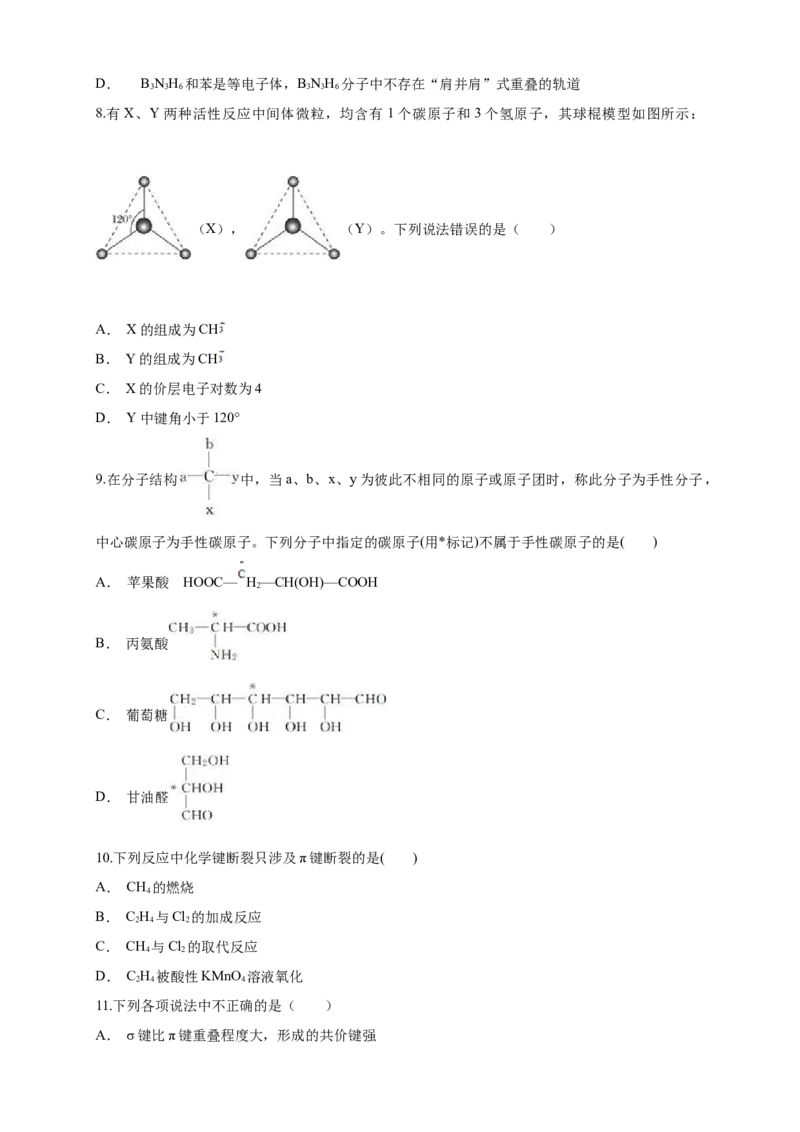
8.有X、Y两种活性反应中间体微粒,均含有1个碳原子和3个氢原子,其球棍模型如图所示:
(X), (Y)。下列说法错误的是( )
A. X的组成为CH
B. Y的组成为CH
C. X的价层电子对数为4
D. Y中键角小于120°
9.在分子结构 中,当a、b、x、y为彼此不相同的原子或原子团时,称此分子为手性分子,
中心碳原子为手性碳原子。下列分子中指定的碳原子(用*标记)不属于手性碳原子的是( )
A. 苹果酸 HOOC— H—CH(OH)—COOH
2
B. 丙氨酸
C. 葡萄糖
D. 甘油醛
10.下列反应中化学键断裂只涉及π键断裂的是( )
A. CH 的燃烧
4
B. C H 与Cl 的加成反应
2 4 2
C. CH 与Cl 的取代反应
4 2
D. C H 被酸性KMnO 溶液氧化
2 4 4
11.下列各项说法中不正确的是( )
A. σ键比π键重叠程度大,形成的共价键强B. 两个原子之间形成共价键时,最多有一个σ键
C. 气体单质中,一定有σ键,可能有π键
D. N 分子中有一个σ键,2个π键
2
12.下列各组物质中,化学键全部为共价键的是( )
A. NH Cl、CO、HCl
4 2
B. O、KF、SO
2 2
C. HCl、CHCOOH、CH
3 4
D. NaO、N、HO
2 2 2 2
13.S Cl 的结构式为Cl—S—S—Cl,下列有关该分子的说法正确的是( )
2 2
A. 每个中心原子上有3对孤电子对
B. 属于直线形分子
C. 分子中共有10对未成键电子对
D. 分子中含有三个π键
14.下列对分子的性质的解释中 ,不正确的是( )
A. 水很稳定(1 000 ℃以上才会部分分解)是因为水中含有大量的氢键所致
B. 乳酸( )分子中含有一个手性碳原子
C. 碘易溶于四氯化碳,甲烷难溶于水都可用“相似相溶”原理解释
D. 由上图知酸性:HPO >HClO,因为HPO 中非羟基氧原子数大于次氯酸中非羟基氧原
3 4 3 4
子数
15.根据价层电子对互斥理论,判断下列分子或离子的立体构型正确的是( )
A. ①② B. ②③ C. ②④ D. ①④
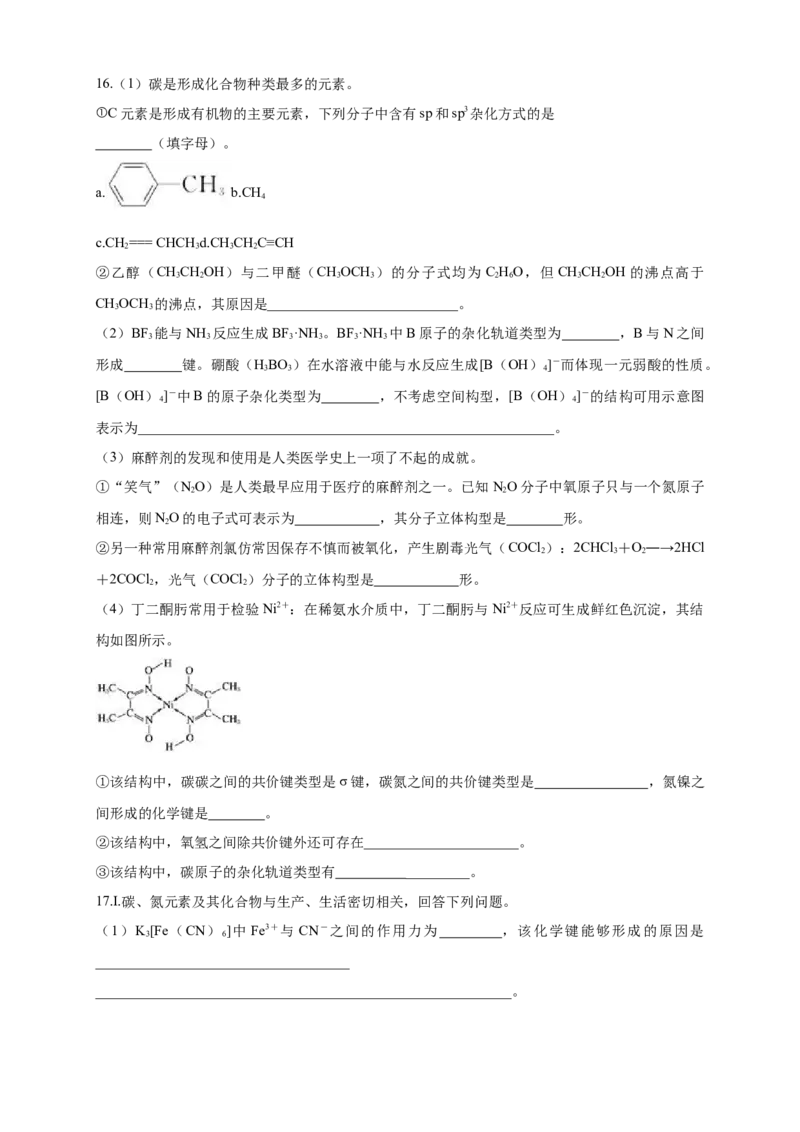
二、填空题16.(1)碳是形成化合物种类最多的元素。
①C元素是形成有机物的主要元素,下列分子中含有sp和sp3杂化方式的是
(填字母)。
a. b.CH
4
c.CH === CHCH d.CH CHC≡CH
2 3 3 2
②乙醇(CHCHOH)与二甲醚(CHOCH )的分子式均为 C HO,但 CHCHOH的沸点高于
3 2 3 3 2 6 3 2
CHOCH 的沸点,其原因是___________________________。
3 3
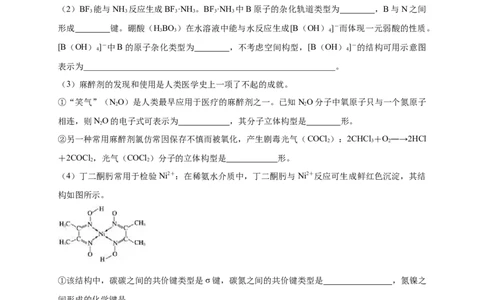
(2)BF 能与NH 反应生成BF·NH 。BF·NH 中B原子的杂化轨道类型为 ,B与N之间
3 3 3 3 3 3
形成 键。硼酸(HBO )在水溶液中能与水反应生成[B(OH) ]-而体现一元弱酸的性质。
3 3 4
[B(OH) ]-中B的原子杂化类型为 ,不考虑空间构型,[B(OH) ]-的结构可用示意图
4 4
表示为___________________________________________________________。
(3)麻醉剂的发现和使用是人类医学史上一项了不起的成就。
①“笑气”(NO)是人类最早应用于医疗的麻醉剂之一。已知NO分子中氧原子只与一个氮原子
2 2
相连,则NO的电子式可表示为 ,其分子立体构型是 形。
2
②另一种常用麻醉剂氯仿常因保存不慎而被氧化,产生剧毒光气(COCl ):2CHCl +O―→2HCl
2 3 2
+2COCl ,光气(COCl )分子的立体构型是 形。
2 2
(4)丁二酮肟常用于检验Ni2+:在稀氨水介质中,丁二酮肟与Ni2+反应可生成鲜红色沉淀,其结
构如图所示。
①该结构中,碳碳之间的共价键类型是σ键,碳氮之间的共价键类型是 ,氮镍之
间形成的化学键是 。
②该结构中,氧氢之间除共价键外还可存在______________________。
③该结构中,碳原子的杂化轨道类型有 _________。
17.Ⅰ.碳、氮元素及其化合物与生产、生活密切相关,回答下列问题。
(1)K[Fe(CN) ]中 Fe3+与 CN-之间的作用力为 ,该化学键能够形成的原因是
3 6
____________________________________
___________________________________________________________。(2)某有机物的结构简式为 。该有机物分子是 (填“极
性”或“非极性”)分子,该有机物分子中采取sp3杂化的原子对应元素的电负性由大到小的顺序
为 。
(3)乙二胺(HNCH CHNH )分子中氮原子杂化类型为 ,乙二胺和三甲胺[N(CH ) ]
2 2 2 2 3 3
均 属 于 胺 , 但 乙 二 胺 比 三 甲 胺 的 沸 点 高 很 多 , 原 因 是
___________________________________________________________
___________________________________________________________。
(4)NH Cl中阳离子中心原子的价层电子对数为 ,该物质中不含有 。
4
A.离子键 B.极性共价键
C.非极性共价键 D.配位键
E.σ键 F.π键
(5)NCl 的立体构型为 ,其中心原子的杂化轨道类型为 。
3
Ⅱ.叠氮化合物是一类重要的化合物,其中氢叠氮酸(HN )是一种弱酸,其分子结构可表示为H—
3
N===N≡N,肼(NH )被亚硝酸氧化时便可得到氢叠氮酸(HN ),发生的反应为 NH +
2 4 3 2 4
HNO===2HO+HN 。HN 的酸性和醋酸相近,可微弱电离出H+和N 。试回答下列问题:
2 2 3 3
(1)下列有关说法正确的是 (填序号)。
A.HN 中含有5个σ键
3
B.HN 中的三个氮原子均采用sp2杂化
3
C.HN、HNO、HO、NH 都是极性分子
3 2 2 2 4
D.肼(NH)的沸点高达113.5 ℃,说明肼分子间可形成氢键
2 4
(2)叠氮酸根能与许多金属离子等形成配合物,如[Co(N )(NH ) ]SO ,在该配合物中钴显
3 3 5 4
价;根据价层电子对互斥理论判断SO 的空间构型为 。
(3)与N 互为等电子体的分子有 (写两种即可)。
18.回答下列问题。
( 1 ) 次 氯 酸 、 亚 硝 酸 、 硫 酸 、 高 溴 酸 4 种 含 氧 酸 的 酸 性 由 强 到 弱 的 顺 序 是
___________________________________________________________。
(2)磷与砷元素同主族,HPO (亚磷酸)和HAsO (亚砷酸)的分子组成相似,但它们的酸性
3 3 3 3
差别很大,HPO 是中强酸,HAsO 既有弱酸性又有弱碱性。由此可推出它们的结构式分别为①
3 3 3 3
,②___________________________________________________________。
HPO 和 HAsO 与 过 量 的 NaOH 溶 液 反 应 的 化 学 方 程 式 分 别 是
3 3 3 3①___________________________________________________________,
②___________________________________________________________。
19.(1)配合物[Cr(HO)]3+中,与Cr3+形成配位键的原子是 (填元素符号)。
2 6
(2)NH BF(氟硼酸铵)是合成氮化硼纳米管的原料之一。1 mol NH BF 含有 mol配位
4 4 4 4
键。
(3)Cu2+的水合离子中,提供孤电子对的原子是 。将Cu单质的粉末加入NH 的浓溶液中,
3
通 入 O , 充 分 反 应 后 溶 液 呈 深 蓝 色 , 该 反 应 的 离 子 方 程 式 是
2
_____________________________________。
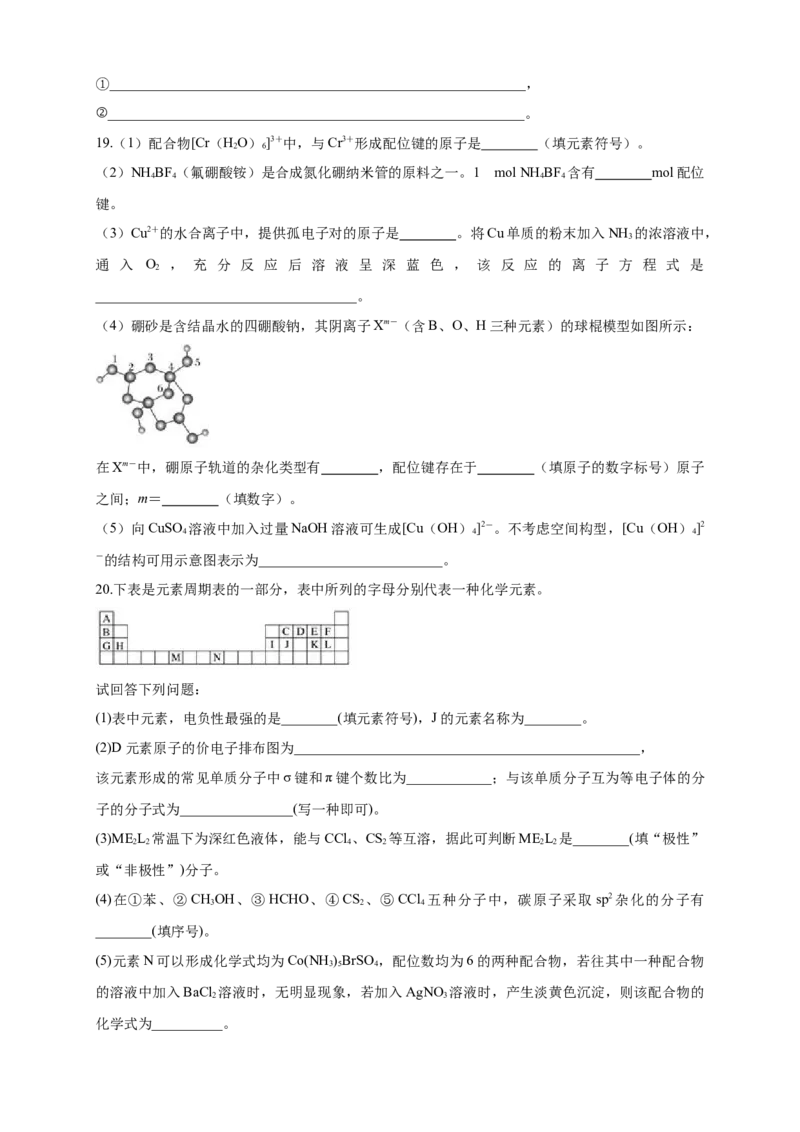
(4)硼砂是含结晶水的四硼酸钠,其阴离子Xm-(含B、O、H三种元素)的球棍模型如图所示:
在Xm-中,硼原子轨道的杂化类型有 ,配位键存在于 (填原子的数字标号)原子
之间;m= (填数字)。
(5)向CuSO 溶液中加入过量NaOH溶液可生成[Cu(OH) ]2-。不考虑空间构型,[Cu(OH) ]2
4 4 4
-的结构可用示意图表示为__________________________。
20.下表是元素周期表的一部分,表中所列的字母分别代表一种化学元素。
试回答下列问题:
(1)表中元素,电负性最强的是________(填元素符号),J的元素名称为________。
(2)D元素原子的价电子排布图为_________________________________________________,
该元素形成的常见单质分子中σ键和π键个数比为____________;与该单质分子互为等电子体的分
子的分子式为________________(写一种即可)。
(3)ME L 常温下为深红色液体,能与CCl 、CS 等互溶,据此可判断ME L 是________(填“极性”
2 2 4 2 2 2
或“非极性”)分子。
(4)在①苯、②CHOH、③HCHO、④CS 、⑤CCl 五种分子中,碳原子采取 sp2杂化的分子有
3 2 4
________(填序号)。
(5)元素N可以形成化学式均为Co(NH )BrSO ,配位数均为6的两种配合物,若往其中一种配合物
3 5 4
的溶液中加入BaCl 溶液时,无明显现象,若加入AgNO 溶液时,产生淡黄色沉淀,则该配合物的
2 3
化学式为__________。21.周期表中前四周期元素R、W、X、Y、Z的原子序数依次增大。R基态原子中,电子占据的最高
能层符号为L,最高能级上只有两个自旋方向相同的电子。工业上通过分离液态空气获得X单质。
Y原子的最外层电子数与电子层数之积等于R、W、X三种元素的原子序数之和。Z基态原子的最
外能层只有一个电子,其他能层均已充满电子。请回答下列问题:
(1)YX 的立体构型是____________;与YX 互为等电子体的一种分子为________(填化学式);
HYX 酸性比HYX 强,其原因是_____________________________________________。
4 2
(2)结构简式为RX(WH ) 的化合物中R原子的杂化轨道类型为____________;1 mol RX(WH ) 分子
2 2 2 2
中含有σ键数目为______________。(H为氢元素,下同)
(3)往Z的硫酸盐溶液中通入过量的WH,可生成[Z(WH )]SO ,下列说法正确的是________。
3 3 4 4
A.[Z(WH )]SO 中所含的化学键有离子键、极性键和配位键
3 4 4
B.在[Z(WH )]2+中Z2+给出孤电子对,WH 提供空轨道
3 4 3
C.[Z(WH )]SO 组成元素中第一电离能最大的是氧元素
3 4 4