文档内容
第二章 章末测试(提升)
满分100分,考试用时75分钟
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的
1.(2022·浙江 )下列有关化学及应速率的说法中错误的是
A.决定化学反应速率的主要因素是反应物本身的性质
B.同一化学反应,用不同物质的浓度变化所表示的化学反应速率的数值不一定相同
C.某些反向选用适当的催化剂,能降低反应所需活化能,可以降低反应所需的温度
D.对于反应 单位时间内的化学反应速率有
【答案】D
【解析】A.化学反应速率的大小首先由反应物本身的性质决定,浓度、温度等外界条件能影响化学反应
速率,A正确;
B. 同一化学反应,用不同物质的浓度变化所表示的化学反应速率的数值不一定相同,但是数值之比等于
化学计量数之比,B正确;
C.适当的催化剂,能降低反应所需活化能、能大幅度增加化学反应速率,因此可以降低反应所需的温度,
C正确;
D. 结合选项B、对于反应 单位时间内的化学反应速率有 ,D不正确;
答案选D。
2.(2022·辽宁·铁岭市清河高级中学 )可逆反应 (a为正整数)。反应过程中,
当其他条件不变时,C的百分含量与温度(T)和压强(P)的关系如图所示。下列说法不正确的是
A.若 ,则A为非气体
B.该反应的正反应为放热反应C. ,
D.其他条件不变时,增加B的物质的量,平衡向正反应方向移动,化学平衡常数K增大
【答案】D
【解析】根据“先拐先平数值大”,可以判断出: , ;在T 下C的百分含量较小,说明升高
2
温度,C的百分含量降低,平衡向逆反应方向移动,说明该反应的正反应是放热反应,增大压强,C的百
分含量减小,平衡向逆反应方向移动,故气体反应物的化学计量数之和小于气体生成物的化学计量数之和,
由此分析。A.由C的百分含量与压强的关系图,可以确定 ,增大压强,C的百分含量减小,平衡向
逆反应方向移动,故气体反应物的化学计量数之和小于气体生成物的化学计量数之和,若 ,则A为非
气体,故A正确;
B.由C的百分含量与温度的关系图,可以确定 ,升高温度,C的百分含量降低,平衡向逆反应方
向移动,说明该反应的正反应是放热反应,即∆H<0,故B正确;
C.根据“先拐先平数值大”判断出: , ,故C正确;
D.其他条件不变时,增加B的物质的量,平衡向正反应方向移动,但温度不改变,则化学平衡常数K不
变,故D错误;答案选D。
3.(2022·辽宁·铁岭市清河高级中学 )在一定温度下的恒容容器中,当下列物理量不再发生变化时,能
证明反应 已达到平衡状态的是
①混合气体的压强 ②混合气体的密度 ③ 的物质的量浓度 ④混合气体的总物质的量 ⑤混合气体的平
均相对分子质量 ⑥ 与 的比值 ⑦混合气体的总质量 ⑧混合气体的总体积 ⑨ 、 的分子数
之比为
A.①③④⑤ B.①③④⑤⑧⑨ C.①②③④⑤⑦ D.①②③④⑤⑥⑦⑧
【答案】A
【解析】①该反应为反应前后气体体积减小的反应,压强为变量,当混合气体的压强不变时,说明各组分
的浓度不再变化,该反应达到平衡状态,正确;
②该反应的反应物和生成物都是气体,混合气体总质量不变,容器容积不变,则密度为定值,不能根据混
合气体的密度判断平衡状态,错误;③B物质的量浓度不变时,说明正、逆反应速率相等,该反应达到平衡状态,正确;
④该反应为气体体积减小的反应,混合气体的总物质的量为变量,当其不变时,说明各组分的浓度不再变
化,该反应达到平衡状态,正确;
⑤混合气体的总质量不变,总物质的量为变量,则混合气体的平均相对分子质量为变量,当其不变时,说
明各组分的浓度不再变化,该反应达到平衡状态,正确;
⑥未说明两物质反应速率的方向,则根据 与 的比值始终不变,不能说明各组分的浓度不再变化,
则无法判断平衡状态,错误;
⑦该反应的反应物和生成物都是气体,混合气体的总质量始终不变,不能根据混合气体的总质量判断平衡
状态,错误;
⑧容器容积不变,则混合气体的总体积为定值,不能根据混合气体总体积判断平衡状态,错误;
⑨C、D的分子数之比为 ,无法判断各组分的浓度是否发生变化,则无法判断平衡状态,错误;故选
A。
4.(2021·全国·高二单元测试)升高温度时,化学反应速率加快,主要原因是
A.该化学反应的过程是吸热的
B.反应物分子能量增加,活化分子百分数增大,有效碰撞次数增多
C.该化学反应的过程是放热的
D.分子运动速率加快,使反应物分子间的碰撞机会增多
【答案】B
【解析】升高温度时,反应物分子吸收能量,能量增加,会使活化分子的百分含量增加,单位体积内活化
分子数增加,有效碰撞的次数增加,导致反应速率增大,而与反应过程是吸热还是放热无关,故B正确。
故选:B。
5.(2022广东)在25 ℃时,密闭容器中X+3Y 2Z三种气体的初始浓度和平衡浓度如表,下列说法错误
的是 ⇌
物质 X Y Z
初始浓度/molL-1 0.1 0.2 0
平衡浓度/mol ⋅ L-1 0.05 0.05 0.1
A.反应达到平⋅ 衡时,X的转化率为50%
B.改变温度可以改变此反应的平衡常数
C.增大压强使平衡向生成Z的方向移动,平衡常数增大
D.降低温度,正逆反应速率都减小
【答案】C【解析】A.平衡时Δc(X)=0.1mol/L-0.05mol/L=0.05mol/L,转化率为 ×100%=50%,A正确;
B.平衡常数只受温度影响,改变温度会改变平衡常数,B正确;
C.平衡常数只受温度影响,增大压强平衡常数不变,C错误;
D.降低温度,活化分子百分数减小,正逆反应速率都减小,D正确;
综上所述答案为C。
6.(2022·辽宁·铁岭市清河高级中学 )在容积一定的密闭容器中,置入一定量的一氧化氮和足量碳发生
化学反应:C(s)+2NO(g) CO(g)+N(g),平衡时c(NO)与温度T的关系如图所示,则下列说法正确的是
2 2
( )
A.该反应的ΔH>0
B.若该反应在T℃、T℃时的平衡常数分别为K 、K ,则K <K
1 2 1 2 1 2
C.在T℃时,若反应体系处于状态D,则此时υ >υ
2 正 逆
D.若状态B、C、D的压强分别为p(B)、p(C)、p(D),则p(C)=p(D)>p(B)
【答案】C
【解析】A.升高温度,NO浓度增大,平衡逆向移动,逆向是吸热个,正向为放热反应,故A错误;
B.该反应是放热反应,升高温度,平衡逆向移动,平衡常数减小,因此K <K ,故B错误;
2 1
C.在T℃时,若反应体系处于状态D,D向平衡方向移动,浓度减低,则为正向移动,因此υ >υ ,故
2 正 逆
C正确;
D.该反应是等体积反应,B、D温度相同,物质的量相同,因此p(D)=p(B),C、D物质的量相等,温度C
大于D点,因此压强p(C)>p(D),故D错误。
综上所述,答案为C。
7.(2022·浙江·杭州市富阳区第二中学高二阶段练习)在1100℃,一定容积的密闭容器中发生反应:
FeO(s)+CO(g) Fe(s)+CO (g) H=a kJ/mol(a >0),该温度下K=0.263,下列有关该反应的说法正确的是
2
A.若生成1 m⇌ol Fe,则吸收的△热量小于a kJ
B.若升高温度,则正反应速率加快,逆反应速率加快,化学平衡逆向移动C.若容器内压强不随时间变化,则可以判断该反应已达到化学平衡状态
D.达到化学平衡状态时,若c(CO)=0.100 mol/L,则c(CO)=0.0263 mol/L
2
【答案】D
【解析】A.焓变大于0为吸热反应,根据热化学方程式可知生成1 mol Fe,则吸收的热量为a kJ,A错误;
B.该反应为吸热反应,升高温度平衡正向移动,B错误;
C.该反应是反应前后气体体积相等的反应,在任何时刻都存在容器内压强不随时间变化,因此压强不变
不能作为判断该反应达到化学平衡状态的标志,C错误;
D.该反应平衡常数K= ,所以c(CO)=0.100 mol/L,则c(CO)=Kc(CO)= 0.263×0.1mol/L=0.0263
2
mol/L,D正确。
故选D。
8.(2022·吉林·吉化第一高级中学校 )实验室用 粒与稀盐酸反应制备 时反应速率太慢,为了加快
反应速率,下列方法可行的是
A.加入浓 B.加入
C.使 粒过量 D.滴入几滴 溶液
【答案】D
【解析】A.加入浓 会产生的NO 气体,故A错误;
2
B.加水稀释,氢离子浓度减小,反应速率减慢,故B错误;
C.为了加快反应速率,滴加浓盐酸,使氢离子浓度变大,使 粒过量无法改变速率,故C错误;
D.滴加硫酸铜后,Cu2+会先于氢离子与锌反应,置换出的铜与锌粒形成原电池,加快反应速率,故D正
确;
故答案为D。
9.(2022·广东·高一期中)向绝热恒容密闭容器中通入SO 和NO ,一定条件下使反应
2 2
达到平衡,正反应速率随时间变化的示意图如下所示。下列叙述正确
的是A.反应在c 点达到平衡状态
B.反应物浓度: 点小于 点
C.反应物的总能量低于生成物的总能量
D. 时,SO 的转化率: 段小于 段
2
【答案】D
【解析】A、化学平衡状态的实质是正反应速率等于逆反应速率,c点对应的正反应速率还在改变,未达平
衡,错误;
B、a到b时正反应速率增加,反应物浓度随时间不断减小,错误;
C、从a到c正反应速率增大,之后正反应速率减小,说明反应刚开始时温度升高对正反应速率的影响大于
浓度减小对正反应速率的影响,说明该反应为放热反应,即反应物的总能量高于生成物的总能量,错误;
D、随着反应的进行,正反应速率增大, t= t 时,SO 的转化率:a~b段小于b~c段,正确;
1 2 2
答案选D。 △ △
10.实验室中模拟合成氨反应: 在恒容密闭容器中,初始投入量相等的条件下,
得到三组实验数据如表所示:
浓度( )
实验序号 温度( )
1 300 2.00 1.70 1.50 1.36 1.25 1.20 1.20
2 300 2.00 1.50 1.28 1.20 1.20 1.20 1.20
3 200 2.00 1.60 1.39 1.29 1.27 1.27 1.27
下列有关说法不正确的是
A.当容器内的压强不再改变时,说明该可逆反应已达到化学平衡状态
B.实验2中,前 内以 的浓度变化表示的化学反应速率为
C.比较实验1和2,说明实验2使用了更高效的催化剂D.实验3中, 时向容器中充入一定量 ,则正反应速率 不变
【答案】B
【解析】A.根据反应方程式可知,该反应前后气体的分子数不同,在反应过程中体系的压强随着分子数
的变化而变化,故当容器内的压强不再改变时,说明该可逆反应已达到化学平衡状态,A正确;
B.实验2中,前20min内以H 的浓度变化表示的化学反应速率为 =0.036mol•L-1•min-1,
2
NH 的浓度变化表示的化学反应速率为0.024mol•L-1•min-1,B错误;
3
C.催化剂只能加快反应速率,不能影响平衡移动。比较实验1和2,实验2更快达到了与实验1相同的化
学平衡状态,说明实验2使用了更高效的催化剂C正确;
D.恒容容器中通入氦气,反应混合物中各组分的深度保持不变,故反应速率不变,D正确;
故选B。
11.(2022·辽宁·铁岭市清河高级中学 )下列叙述与图对应的是
A.对于达到平衡状态的反应:N(g)+3H(g) 2NH (g),图①表示在t 时刻充入了一定量的NH ,平衡逆向
2 2 3 0 3
移动 ⇌
B.由图②可知,P>P、T>T 满足反应:2A(g)+B(g) 2C(g) ΔH<0
2 1 1 2
C.图③表示的反应方程式为:2A=B+3C ⇌
D.对于反应2X(g)+3Y(g) 3Z(g) ΔH<0,图④y轴可以表示Y的百分含量
【答案】B ⇌
【解析】A.对于达到平衡状态的反应:N(g)+3H(g) 2NH (g),图①表示在t 时刻v 、v 都增大,v 增
2 2 3 0 正 逆 逆
大的多,化学平衡逆向移动,应该是升高温度使平衡逆⇌向移动导致。若是充入了一定量的NH ,则v 增大,
3 逆
v 瞬间不变,这与图像不吻合,A不符合题意;
正
B.增大压强反应速率加快,达到平衡所需时间缩短;升高温度反应速率加快,达到平衡所需时间缩短。
则根据图像可知:压强:P>P;温度:T>T。增大压强,平衡向气体体积减小的方向移动,C含量增大,
2 1 1 2
说明正反应是气体体积减小的反应;升高温度,C含量减小,说明平衡逆向移动,逆反应为吸热反应,则
正反应为放热反应,故该反应的正反应是气体体积减小的放热反应,故满足反应:2A(g)+B(g) 2C(g) ΔH
<0,B正确; ⇌C.该反应是可逆反应,应该用可逆号“ ”,不能用等号“=”表示,C错误;
D.在压强不变时,升高温度,化学平衡⇌向吸热的逆反应方向移动,表示Y的含量应该增大,但图象显示
y轴数值减小,因此图④y轴不可以表示Y的百分含量,D错误;
故合理选项是B。
12.(2022·吉林·吉化第一高级中学校 )一定条件下,体积为2 L的密闭容器中,2 mol X和3 mol Y进行
反应:X(g)+Y(g) Z(g),经12 s达到平衡,生成0.6 mol Z。下列说法正确的是
A.以X浓度变化⇌表示的反应速率为0.05 mol/(L•s)
B.其他条件不变,增大X的浓度,平衡右移,X的转化率增大
C.其他条件不变,12 s后将容器体积扩大为10 L,Z的平衡浓度变为0.06 mol/L
D.12 s达平衡时Y的转化率为20%
【答案】D
【解析】A.反应进行到12 s时产生0.6 mol Z,根据物质反应转化关系可知会同时消耗0.6 mol的X,则以
X浓度变化表示的反应速率v(X)= =0.025 mol/(L•s),A错误;
B.其他条件不变,增大X的浓度,平衡右移,但平衡移动的趋势是微弱的,最终达到平衡水X的转化率
减小,B错误;
C.其他条件不变,12 s后将容器体积扩大为10 L,若平衡不移动,Z的浓度应为0.06 mol/L。但该反应的
正反应是气体体积减小的反应,将容器的容积扩大,容器内气体的压强减小,化学平衡逆向移动,导致Z
的平衡浓度小于0.06 mol/L,C错误;
D.反应开始时n(Y)=3 mol,反应到12 s时产生Z的物质的量是0.6 mol,同时会消耗0.6 mol Y,则12 s反
应达平衡时Y的转化率为 ,D正确;
故合理选项是D。
13.下列说法正确的是
A.H(g)+I(g) 2HI(g),其他条件不变,缩小反应容器体积,正逆反应速率不变
2 2
B.C(s)+H
2
O(g)⇌ H
2
(g)+CO(g),碳的质量不再改变说明反应已达平衡
C.若压强不再随时⇌间变化能说明反应2A(?)+B(g) 2C(?)已达平衡,则A、C不能同时是气体
D.1 mol N
2
和3 mol H
2
反应达到平衡时H
2
转化率为⇌10%,放出的热量为Q
1
;在相同温度和压强下,当2
mol NH 分解为N 和H 的转化率为10%时,吸收的热量为Q,Q 不等于Q
3 2 2 2 2 1
【答案】B【解析】A.该可逆反应的反应前后气体计量数不发生变化,当缩小反应容器体积,相当于加压,正逆反应
速率同等程度增加,A项错误;
B.在建立平衡前,碳的质量不断改变,达到平衡时,质量不变,因而碳的质量不再改变说明反应已达平衡,
B项正确;
C.即使A,C物质均为气体,反应前后气体体积也会发生变化,当压强不随时间变化时,仍能说明反应达
到平衡,C项错误;
D.易知N(g)+3H(g) 2NH (g) ΔH,合成氨气实际参与反应n(H )=3×10%=0.3mol,因而Q=0.3/3×|ΔH|=0.1|
2 2 3 2 1
ΔH|,分解氨气时实际⇌消耗的n(NH )=2×10%=0.2mol,Q=0.2/2×|ΔH|=0.1|ΔH|,则Q=Q ,D项错误。
3 2 1 2
故答案选B。
14.(2022·陕西·西北农林科技大学附中高二期末)在3种不同条件下,分别向容积为2 L的恒容密闭容器
中充入2 mol A和1 mol B,发生反应:2A (g)+B (g) 2C (g) H=Q kJ/mol,相关条件和数据
△
见表:
实验编号 实验I 实验II 实验III
反应温度/℃ 700 700 750
达平衡时间/min 40 5 30
平衡时n(C) /mol 1.5 1.5 1
化学平衡常数 K K K
1 2 3
下列说法正确的是( )
A.K<K<K
1 2 3
B.升高温度能加快反应速率的原因是降低了反应的活化能
C.实验II比实验I达平衡所需时间小的可能原因是使用了催化剂
D.实验Ⅲ达平衡后,恒温下再向容器中通入1 mol A和1 mol C,平衡正向移动
【答案】C
【解析】A.反应为 ,比较实验I和III,温度升高,平衡时C的量减少,化学平衡
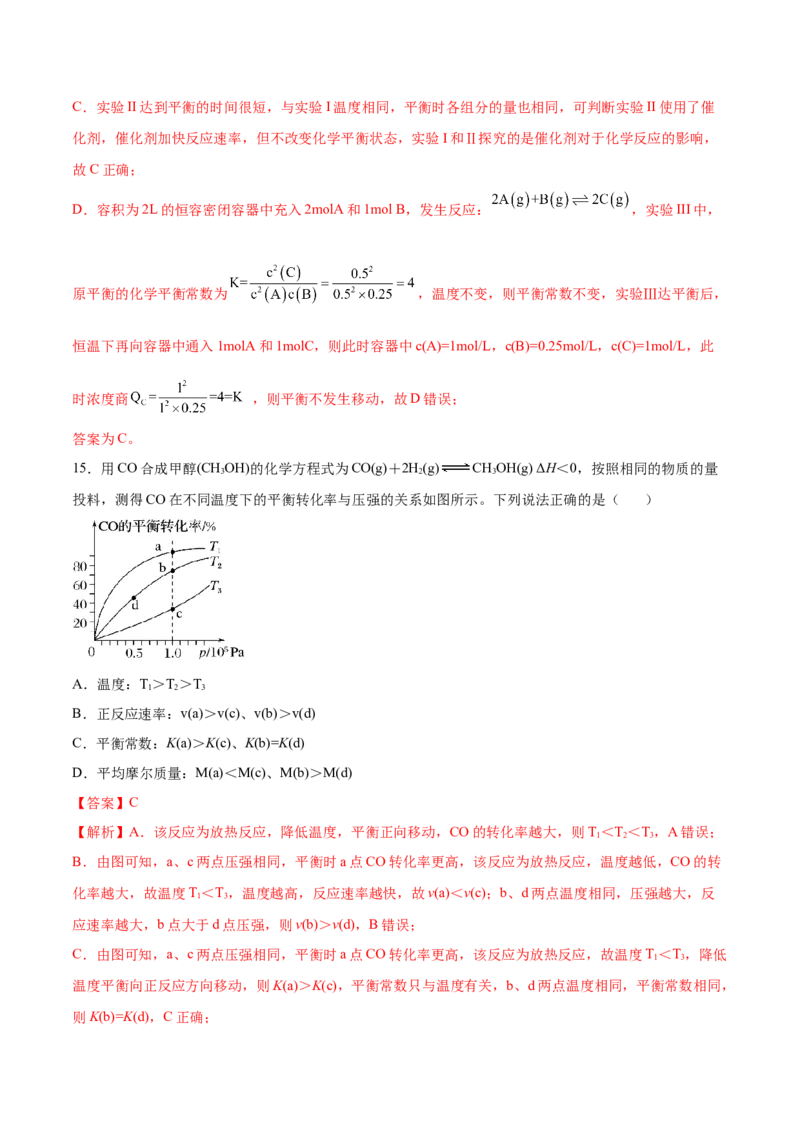
向逆反应方向移动,正反应为放热反应,Q<0,则KM(c),M(b)>M(d),D错误;
答案选C。
16.(2021·全国·高二单元测试)如图,I是恒压密闭容器,II是恒容密闭容器。其它条件相同时,在I、II
中分n别加入2molX和2molY,起始时容器体积均为VL,发生如下反应并达到平衡(X、Y状态未知):
2X(?)+Y(?) aZ(g)。此时I中X、Y、Z的物质的量之比为1∶3∶2,则下列说法一定正确的是
⇌
A.若X、Y均为气态,则平衡时气体平均摩尔质量:II>I,
B.若X、Y不均为气态,则平衡时气体平均摩尔质量:I>II
C.若X为固态,Y为气态,则I、II中从起始到平衡所需时间相同
D.平衡时I容器的体积小于VL
【答案】C
【解析】
达到平衡时,I中X、Y、Z的物质的量之比为1∶3∶2,则 ,n=0.8, ,a=1。
A.X、Y均为气态,II和I相比,相当于减压,平衡逆向移动,气体物质的量II>I,平衡时气体平均摩尔
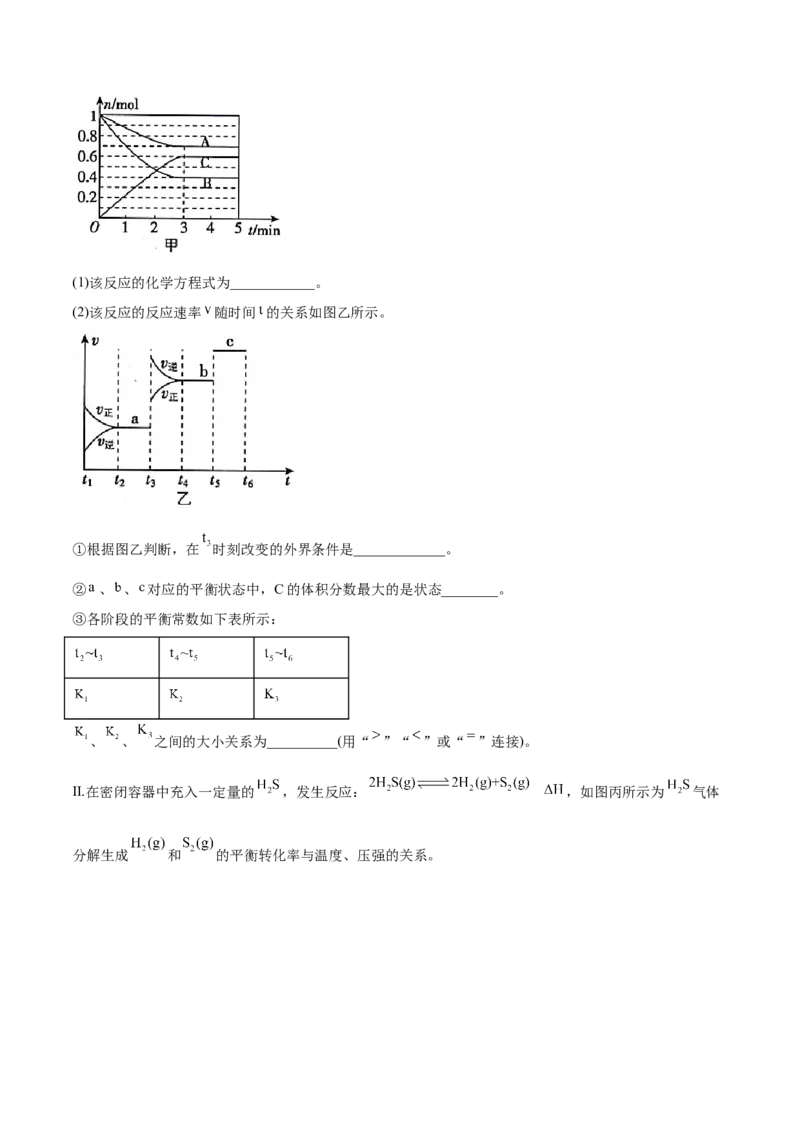
质量:II”“=”或“<”)。
②10min反应达平衡,氢气的转化率为_______。当反应达平衡后,维持温度和压强不变,改变其它条件
使反应速率增大,采取的措施_______(写一条即可)
③在其他条件不变的情况下,将体系体积压缩到原来的二分之一,下列有关该体系的说法正确的是
_______
A.氢气的浓度减小 B.正反应速率增大 C.逆反应速率减小 D.达到平衡的时间不会
改变
【答案】(1)BD
(2) 0.5mol/(L•min) > 75% 使用催化剂或增加反应物浓度(其它答案合理均可) B
【解析】(1)条件改变对反应速率的影响有如下几条:升温、增压、增浓、加有效催化剂、增加固体表面积,
均能提高反应速率,由此,本问应选填“BD”;
(2)①根据题目所给数据信息,3分钟时,CO 消耗了1.00mol/L-0.50mol/L= 0.50mol/L,所以H 消耗浓度是
2 23×0.50mol/L=1.50mol/L,那么H 在0~3分钟的平均速率是 ;
2
由于反应物继续减少,反应向正向进行,并未达到平衡,所以正反应速率大于逆反应速率,本问第二空应
填“>”;
②利用题目所给数据信息,建立平衡时的三段式,
氢气的转化率为 ;增大反应速率的方法可以通过:升温、增压、
增浓、加有效催化剂、增大固体表面积等方法,题目中限定温度压强不变,且反应体系内物质均为气态,
所以只能考虑恒容增加CO 或者H 的物质的量,或者增加更优质催化剂两个角度增大速率;
2 2
③在其他条件不变的情况下,将体系体积压缩到原来的二分之一,使得反应起始容器内压强翻倍,反应物
起始浓度翻倍,所以达到新平衡时,反应速率均比未压缩前增大,反应物消耗量比之前平衡更大,但达不
到原平衡消耗的一倍,所以新平衡时反应物平衡浓度会大于上一个平衡时的平衡浓度,反应速率增大,同
时反应物转化率上升,故达到平衡的时间不能确定是否比原平衡达到时间长还是短;综上,本小问只有B
选项符合题意。
19.(2022·云南省楚雄彝族自治州民族中学高二阶段练习)(16分) 、 、 均为大气污染物,
它们在一定条件下可以转化为其他物质,以减少对环境的污染。
(1)一定条件下,将 与 置于恒容密闭容器中发生反应 ,下列
状态能说明该反应达到化学平衡的是_____(填序号)。
A.混合气体的密度保持不变
B. 的转化率保持不变
C. 和 的物质的量之比保持不变
D. 的消耗速率和 的消耗速率相等
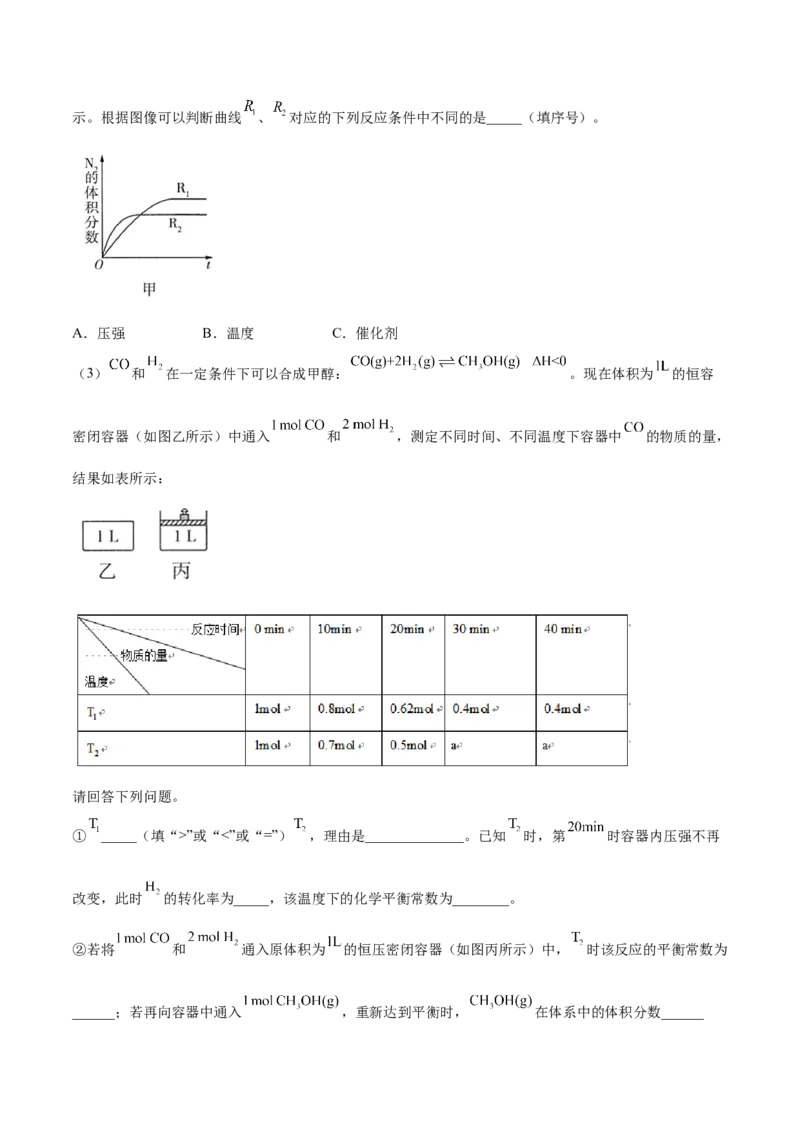
(2)已知反应 ,在不同条件时 的体积分数随时间 的变化如图甲所示。根据图像可以判断曲线 、 对应的下列反应条件中不同的是_____(填序号)。
A.压强 B.温度 C.催化剂
(3) 和 在一定条件下可以合成甲醇: 。现在体积为 的恒容
密闭容器(如图乙所示)中通入 和 ,测定不同时间、不同温度下容器中 的物质的量,
结果如表所示:
请回答下列问题。
① _____(填“>”或“<”或“=”) ,理由是______________。已知 时,第 时容器内压强不再
改变,此时 的转化率为_____,该温度下的化学平衡常数为________。
②若将 和 通入原体积为 的恒压密闭容器(如图丙所示)中, 时该反应的平衡常数为
______;若再向容器中通入 ,重新达到平衡时, 在体系中的体积分数______(填“变大”“变小”或“不变”)。
【答案】 (1)B
(2) B
(3)①< 相同时间内, 时 的减少量大于 时 的减少量 50% 1.0
(4)1.0 不变
【解析】(1)A. 、 和 都是气体,恒容条件下反应时混合气体的密度始终不变,A项不能说明反应
达到化学平衡;
B.反应正向进行, 的转化率增大,反应逆向进行, 的转化率减小,故 的转化率保持不变,说明
该反应达到平衡状态,B项能说明反应达到化学平衡
D.起始加入 和 的物质的量之比为 ,与其化学计量数之比相等,则二者的物质的量之比始终等于
,C项不能说明反应达到化学平衡;
D. 的消耗速率与 的消耗速率之比为 时,说明该反应达到平衡状态,D项不能说明反应达到化学
平衡;
故选B;
(2)由图甲可知,曲线 代表的反应比曲线 代表的反应先达到平衡状态;
A项,改变压强,平衡不移动, 的体积分数不变,与图象不符合;
B项,该反应的 ,由题图知曲线 代表的反应温度高于曲线 ,升高温度,平衡逆向移动, 的
体积分数减小,与图象符合;
C项,使用催化剂,只能改变反应速率,但平衡不移动, 的体积分数不变,与图象不符合;
故选B;
(3)①由表中数据可知,未达到平衡之前,相同时间内, 时 的减少量大于 时 的减少量,说明
时化学反应速率快,而温度越高,反应速率越快,故 , 时,第 时容器内压强不再改变,则
反应达到平衡状态,此时 ,则有:故 时 的转化率为 ,该温度下化学平衡常数
,故答案为:<;相同时间内, 时 的减少量大于 时 的减少量;
50%;1;
②若将 和 通入原体积为 的恒压密闭容器中,由于温度不变,化学平衡常数不变,则
时该反应的平衡常数为1.0。若再向容器中通入 ,由于是恒压条件,该平衡与之前的平衡等
效,故重新达到平衡时, 在体系中的体积分数不变,故答案为:1.0;不变。
20.(14分)研究氮氧化物之间的转化具有重要意义。
(1)已知:NO(g) 2NO (g)ΔH>0将一定量NO 充入恒容密闭容器中,控制反应温度为T。
2 4 2 2 4 1
①下列可以作为反⇌应达到平衡的判据是___。
A.气体的压强不变
B.v (N O)=2v (NO )
正 2 4 逆 2
C.K不变
D.容器内气体的密度不变
E.容器内颜色不变
②t时刻反应达到平衡,混合气体平衡总压强为P,NO 气体的平衡转化率为75%,则反应的
2 4
NO(g) 2NO (g)的平衡常数K =___(对于气相反应,用某组分B的平街压强P(B)代替物质的量浓度c(B)也
2 4 2 p
可表示平⇌衡常数,记作K ,如P(B)= P∙x(B),P为平衡总压强,x(B)为平衡系统中B的物质的量分数)。
P
③温度T 时,c(N O)随t(时间)变化曲线如图1,画出0~t,时段,c(NO )随t变化曲线。保持其它条件不变,
1 2 4 2
改变温度为T(T>T),再次画出0~t 时段,c(NO )随t变化趋势的曲线___。
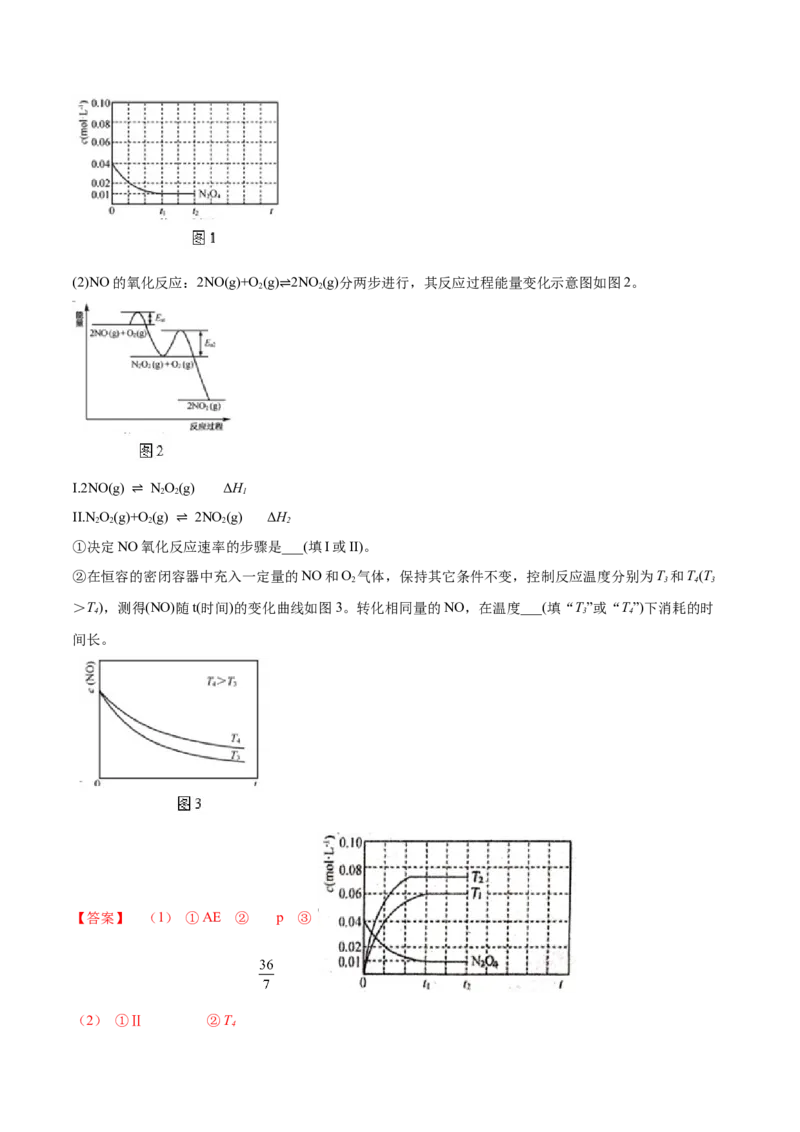
2 2 1 2 2(2)NO的氧化反应:2NO(g)+O (g) 2NO (g)分两步进行,其反应过程能量变化示意图如图2。
2 2
⇌
I.2NO(g) NO(g) ΔH
2 2 1
II.N
2
O
2
(g)+⇌O
2
(g) 2NO
2
(g) ΔH
2
①决定NO氧化反⇌应速率的步骤是___(填I或II)。
②在恒容的密闭容器中充入一定量的NO和O 气体,保持其它条件不变,控制反应温度分别为T 和T(T
2 3 4 3
>T),测得(NO)随t(时间)的变化曲线如图3。转化相同量的NO,在温度___(填“T”或“T”)下消耗的时
4 3 4
间长。
【答案】 (1) ①AE ② p ③
(2) ①Ⅱ ②T
4【解析】(1)①A.该反应是一个气体体积减小的反应,气体的压强不变说明各物质浓度保持不变,反应达
到化学平衡状态,故A符合题意;
B.v (N O)=2v (NO )说明正逆反应速率不相等,反应没有达到化学平衡状态,故B不符合题意;
正 2 4 逆 2
C.温度不变,化学平衡常数K不变,则K不变不能说明反应达到化学平衡状态,故C不符合题意;
D.由质量守恒定律可知,反应前后气体质量不变,恒容容器的体积不变,则密度始终不变,则密度不变
不能说明反应达到化学平衡状态,故D不符合题意;
E.容器内颜色不变说明各物质浓度保持不变,反应达到化学平衡状态,故E符合题意;
故答案为AE;
②设起始NO 的物质的量为1mol,NO 气体的平衡转化率为75%,由题给数据建立如下三段式:
2 4 2 4
由三段式数据可知NO 的平衡分压为 ×P= ,NO 的平衡分压为 ×P= ,则平衡常数K =
2 4 2 p
= ;
③由图可知,t 时反应消耗NO 的浓度为(0.04—0.01)mol/L,由方程式可得反应生成NO 的浓度为0.03
1 2 4 2
mol/L×2=0.06 mol/L;该反应为吸热反应,升高温度,平衡向正反应方向移动,NO 的浓度增大,则0~t
2 2
时段,NO 的浓度c(NO )随t变化趋势的曲线为 ;
2 2
(2)①由图可知,反应Ⅰ的活化能小于反应Ⅱ的活化能,活化能越大,反应速率越慢,则化学反应速率反应
Ⅰ快于反应Ⅱ,化学反应取决于反应速率较慢的一步,则决定NO氧化反应速率的步骤是反应Ⅱ;
②由图可知,转化相同量的NO,在温度T 下消耗的时间较长,原因是反应Ⅰ为放热反应,温度升高,反
4应Ⅰ平衡逆移,c(N O)减小,浓度降低的影响大于温度对反应Ⅱ速率的影响,导致转化相同量的NO,在
2 2
温度较高的T 下消耗的时间较长。
4倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育