文档内容
第二章 章末测试(基础)
满分100分,考试用时75分钟
一、选择题:本题共16小题,共44分。第1~10小题,每小题2分;第11~16小题,每小题4分。在每小
题给出的四个选项中,只有一项是符合题目要求的
1.(2022·湖北·鄂州市教学研究室高二期末)向一个密闭容器中充入1mol 和3mol H,在一定条件下使
2
其发生反应生成 。达到平衡时,下列说法中正确的是
A. 、H 和 的物质的量浓度之比为1:3:2
2
B. 完全转化为
C.正反应速率和逆反应速率都为零
D.单位时间内消耗amol ,同时消耗2amol
2.(2021·河南洛阳·高二期中)下列事实不能用勒夏特列原理解释的是
A.开启啤酒瓶后,马上泛起大量泡沫
B.合成氨工厂通常采用高温条件(N (g)+3H(g) 2NH (g) H<0)
2 2 3
C.实验室中常用排饱和食盐水的方法收集氯气⇌ △
D.工业上生产硫酸的过程中使用过量的空气以提高二氧化硫的利用率
3.(2022·广东茂名·高二期末)下列不属于自发进行的变化是
A.红墨水加到清水使整杯水变红 B.冰在室温下融化成水
C.电解饱和食盐水 D.铁器在潮湿的空气中生锈
4.(2021·山东·微山县第二中学高二阶段练习)一定温度下,在固定体积的密闭容器中发生下列反应:
2HI(g) H(g)+I (g)。若c(HI)由0.1 mol·L-1降到0.08 mol·L-1时,需要20s,那么c(HI)由0.08mol·L-1降到
2 2
0.07 m⇌ol·L-1时,所需反应的时间为
A.等于5 s B.等于10 s C.大于10 s D.小于10 s
5.(2021·黑龙江·农垦佳木斯学校高二阶段练习)对已达平衡的下列反应:3A(g)+B(g) 2C(g)+2D(g),若
增大压强,则所产生的影响正确的是 ⇌
A.正反应速率增大,逆反应速率减小,平衡向正反应方向移动
B.正、逆反应速率都增大,平衡不发生移动
C.正反应速率减小,逆反应速率增大,平衡向逆反应方向移动D.正、逆反应速率都增大,平衡向正反应方向移动
6.下列有关化学反应速率的说法正确的是
A.用铁片和稀硫酸反应制取氢气时,改用98%的浓硫酸可以加快产生氢气的速率
B.100mL2mol/L的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C.在一定温度下固定容积的容器中,发生SO 的催化氧化反应,增大容器内压强,反应速率不一定改变。
2
D.NH 的催化氧化是一个放热的反应,所以,升高温度,反应的速率减慢
3
7.利用反应2NO(g)+2CO(g) 2CO(g)+N(g) ΔH=-746.8 kJ·mol-1,可净化汽车尾气,如果要同时提高
2 2
该反应的速率和NO的转化率,⇌采取的措施是
A.升高温度 B.增大压强
C.向容器中通入NO D.及时将CO 和N 从反应体系中移走
2 2
8.在一定条件下,某反应达到平衡时,平衡常数K= 。恒容时,若温度适当降低,D的浓度增
加。下列说法正确的是
A.减低温度,逆反应速率增大 B.该反应的焓变为正值
C.若增大c(A)、c(B),K值增大 D.该反应的化学方程式为:A(g)+B(g) C(g)+D(g)
9.(2021·辽宁·辽河油田第二高级中学高二期中)80℃时,2 L密闭容器中充入0.40 mol NO,发生反应
2 4
NO 2NO ΔH=+Q kJ·mol-1(Q>0),获得如表数据:
2 4 2
时间/⇌s 0 20 40 60 80 100
c(NO )/mol·L-1 0.00 0.12 0.20 0.26 0.30 0.30
2
下列判断正确的是
A.当温度不变时增大压强,该反应的平衡常数K减小
B.0~40 s内,NO 的平均反应速率为0.005mol·L-1·s-1
2 4
C.反应达平衡时,吸收的热量为0.30Q kJ
D.100s后升高温度,体系颜色变浅
10.(2022·江苏·盐城市伍佑中学高二期中)关于平衡常数,下列说法正确的是
A.使用催化剂能使化学反应速率加快,平衡常数增大
B.平衡常数随温度的改变而改变
C.化学平衡发生移动,平衡常数必发生变化
D.对于3Fe(s)+4H O(g) Fe O(s)+4H(g),反应的化学平衡常数的表达式K=
2 3 4 211.(2022·广西·南宁市第五十六中学高二期末)在2A+B=3C+4D反应中,表示该反应速率最快的是
A.v(A)=0.5mol·L-1·s-1 B.v(B)=0.3mol·L-1·s-1
C.v(C)=0.8mol·L-1·s-1 D.v(D)=1mol·L-1·s-1
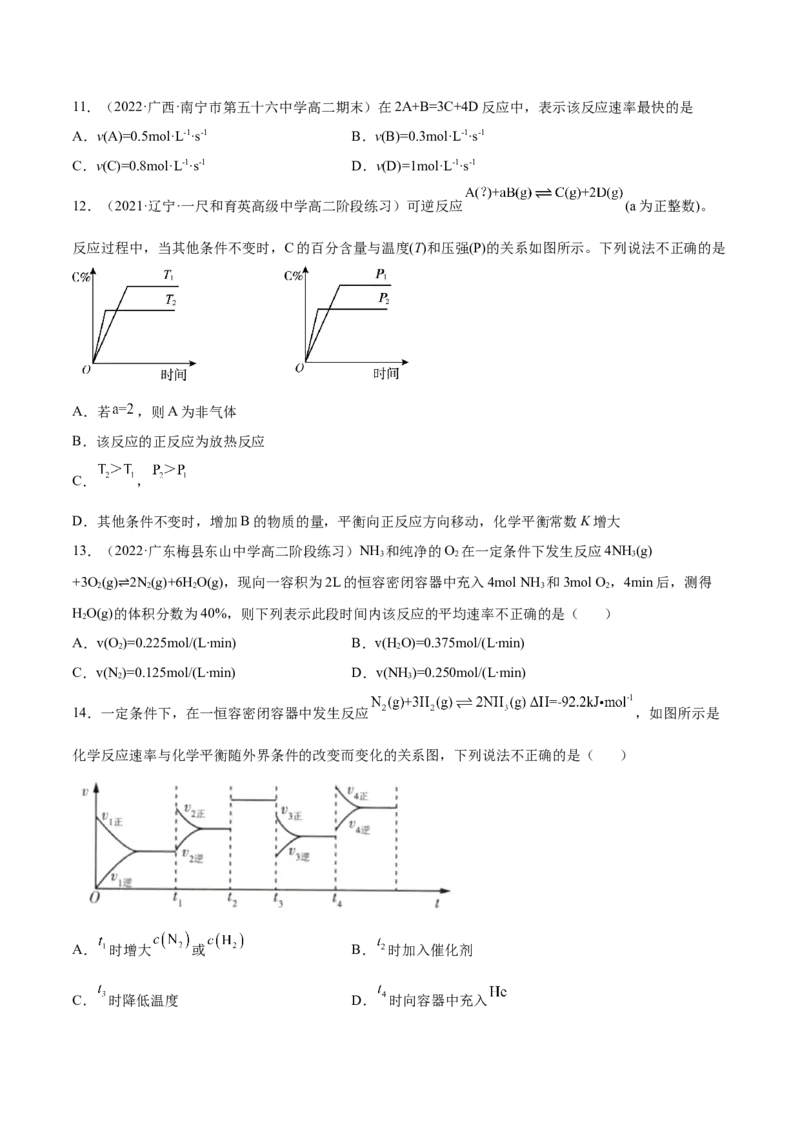
12.(2021·辽宁·一尺和育英高级中学高二阶段练习)可逆反应 (a为正整数)。
反应过程中,当其他条件不变时,C的百分含量与温度(T)和压强(P)的关系如图所示。下列说法不正确的是
A.若 ,则A为非气体
B.该反应的正反应为放热反应
C. ,
D.其他条件不变时,增加B的物质的量,平衡向正反应方向移动,化学平衡常数K增大
13.(2022·广东梅县东山中学高二阶段练习)NH 和纯净的O 在一定条件下发生反应4NH (g)
3 2 3
+3O (g) 2N(g)+6HO(g),现向一容积为2L的恒容密闭容器中充入4mol NH 和3mol O,4min后,测得
2 2 2 3 2
HO(g)的⇌体积分数为40%,则下列表示此段时间内该反应的平均速率不正确的是( )
2
A.v(O )=0.225mol/(L∙min) B.v(H O)=0.375mol/(L∙min)
2 2
C.v(N )=0.125mol/(L∙min) D.v(NH )=0.250mol/(L∙min)
2 3
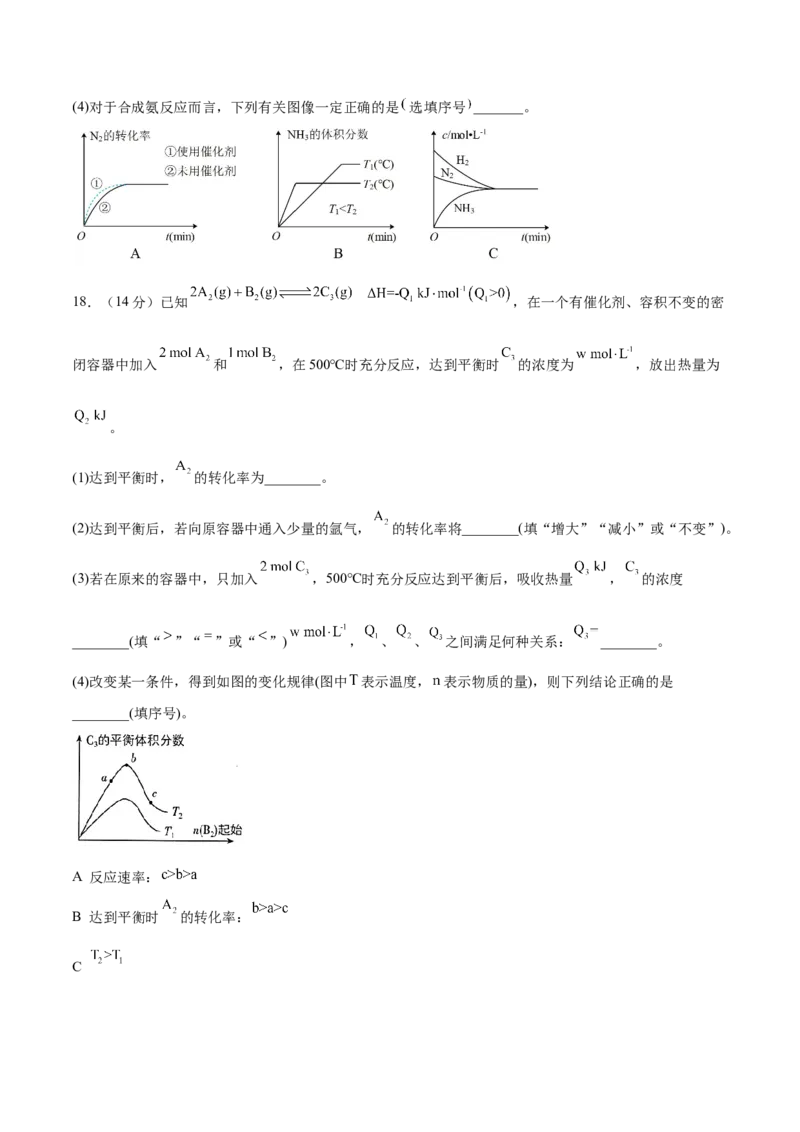
14.一定条件下,在一恒容密闭容器中发生反应 ,如图所示是
化学反应速率与化学平衡随外界条件的改变而变化的关系图,下列说法不正确的是( )
A. 时增大 或 B. 时加入催化剂
C. 时降低温度 D. 时向容器中充入15.例1 气体和 气体在一容积可变的密闭容器中发生反应 。反应达到
平衡时,测得X的转化率为50%,且在同温同压下还测得反应前混合气体的密度是反应后混合气体密度的
,则a和b的数值可能是( )
A. B. C. D.
【解析】16.在一定温度下的恒容容器中,当下列物理量不再发生变化时,能证明反应
已达到平衡状态的是
①混合气体的压强 ②混合气体的密度 ③ 的物质的量浓度 ④混合气体的总物质的量 ⑤混合气体的平
均相对分子质量 ⑥ 与 的比值 ⑦混合气体的总质量 ⑧混合气体的总体积 ⑨ 、 的分子数
之比为
A.①③④⑤ B.①③④⑤⑧⑨ C.①②③④⑤⑦ D.①②③④⑤⑥⑦⑧
二、非选择题:共56分。
17.(10分)合成氨工业对国民经济和社会发展具有重要的意义。其原理为:N 2NH
;据此回答以下问题:
(1)该反应的化学平衡常数表达式为 _______。
(2)根据温度对化学平衡的影响规律可知,对于该反应温度越高,其化学平衡常数的值_______。(填“越
大”、“越小”或“不变”)
(3)某温度下,若把 与 置于体积为 的密闭容器内,反应达到平衡状态时,测得混合气
体的压强变为开始时的 ,则平衡时氢气的转化率 =_______ (用百分数表示 。能说明该反应达到化学平
衡状态的是_______ 填字母 。
a.容器内的密度保持不变
b.容器内压强保持不变
c.v (N )=2v (NH )
正 2 逆 3
d.混合气体中c(NH )不变
3(4)对于合成氨反应而言,下列有关图像一定正确的是 选填序号 _______。
18.(14分)已知 ,在一个有催化剂、容积不变的密
闭容器中加入 和 ,在500℃时充分反应,达到平衡时 的浓度为 ,放出热量为
。
(1)达到平衡时, 的转化率为________。
(2)达到平衡后,若向原容器中通入少量的氩气, 的转化率将________(填“增大”“减小”或“不变”)。
(3)若在原来的容器中,只加入 ,500℃时充分反应达到平衡后,吸收热量 , 的浓度
________(填“ ”“ ”或“ ”) , 、 、 之间满足何种关系: ________。
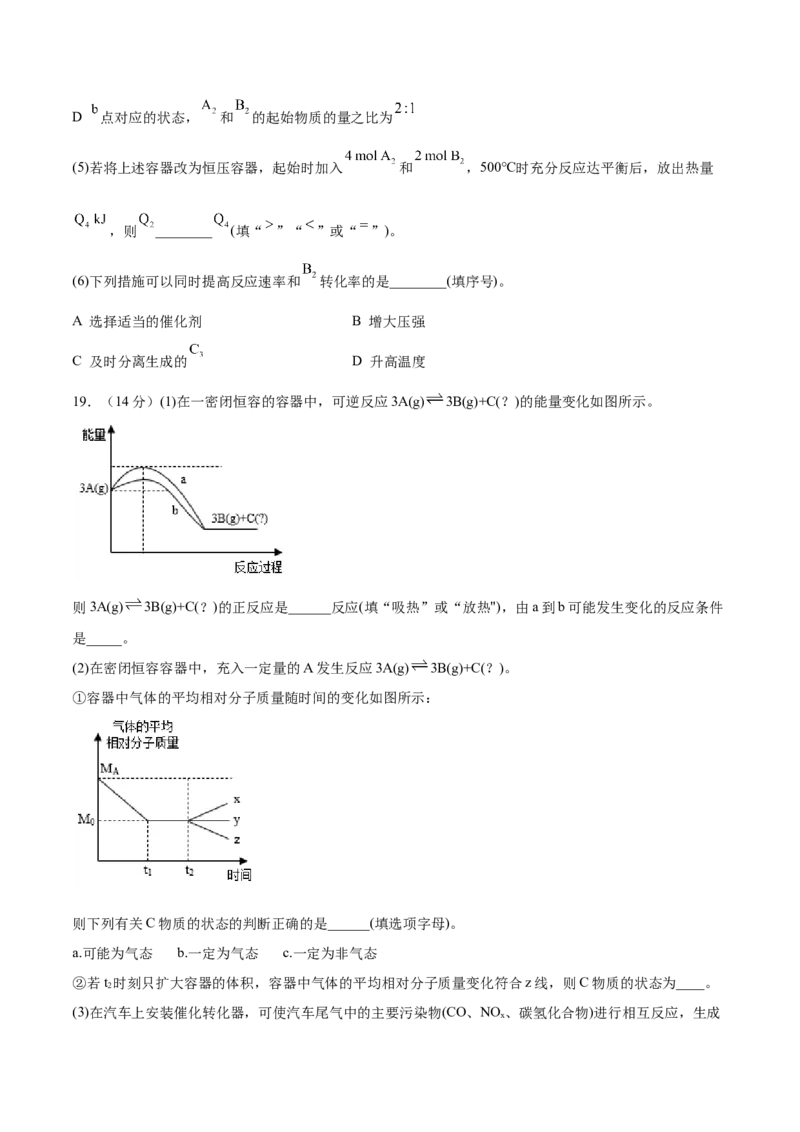
(4)改变某一条件,得到如图的变化规律(图中 表示温度, 表示物质的量),则下列结论正确的是
________(填序号)。
A 反应速率:
B 达到平衡时 的转化率:
CD 点对应的状态, 和 的起始物质的量之比为
(5)若将上述容器改为恒压容器,起始时加入 和 ,500℃时充分反应达平衡后,放出热量
,则 ________ (填“ ”“ ”或“ ”)。
(6)下列措施可以同时提高反应速率和 转化率的是________(填序号)。
A 选择适当的催化剂 B 增大压强
C 及时分离生成的 D 升高温度
19.(14分)(1)在一密闭恒容的容器中,可逆反应3A(g) 3B(g)+C(?)的能量变化如图所示。
则3A(g) 3B(g)+C(?)的正反应是______反应(填“吸热”或“放热"),由a到b可能发生变化的反应条件
是_____。
(2)在密闭恒容容器中,充入一定量的A发生反应3A(g) 3B(g)+C(?)。
①容器中气体的平均相对分子质量随时间的变化如图所示:
则下列有关C物质的状态的判断正确的是______(填选项字母)。
a.可能为气态 b.一定为气态 c.一定为非气态
②若t 时刻只扩大容器的体积,容器中气体的平均相对分子质量变化符合z线,则C物质的状态为____。
2
(3)在汽车上安装催化转化器,可使汽车尾气中的主要污染物(CO、NO 、碳氢化合物)进行相互反应,生成
x无害物质,减少污染。
已知:N(g)+O(g)=2NO(g) H=+180.5 kJ·mol-1
2 2
2C(s)+O
2
(g)=2CO(g) H=-22△1.0 kJ·mol-1
C(s)+O
2
(g)=CO
2
(g) △H=-393.5 kJ·mol-1
试计算尾气转化的反△应之一:2NO(g)+2CO(g) N
2
(g)+2CO
2
(g)的 H=_____。此反应的化学平衡常数表达
式为K=____,随着温度的升高,K值将____(填“增大”“减小”△或“不变”)。
20.(2022·云南省楚雄彝族自治州民族中学高二阶段练习)(18分) 、 、 均为大气污染物,
它们在一定条件下可以转化为其他物质,以减少对环境的污染。
(1)一定条件下,将 与 置于恒容密闭容器中发生反应 ,下列
状态能说明该反应达到化学平衡的是_____(填序号)。
A.混合气体的密度保持不变
B. 的转化率保持不变
C. 和 的物质的量之比保持不变
D. 的消耗速率和 的消耗速率相等
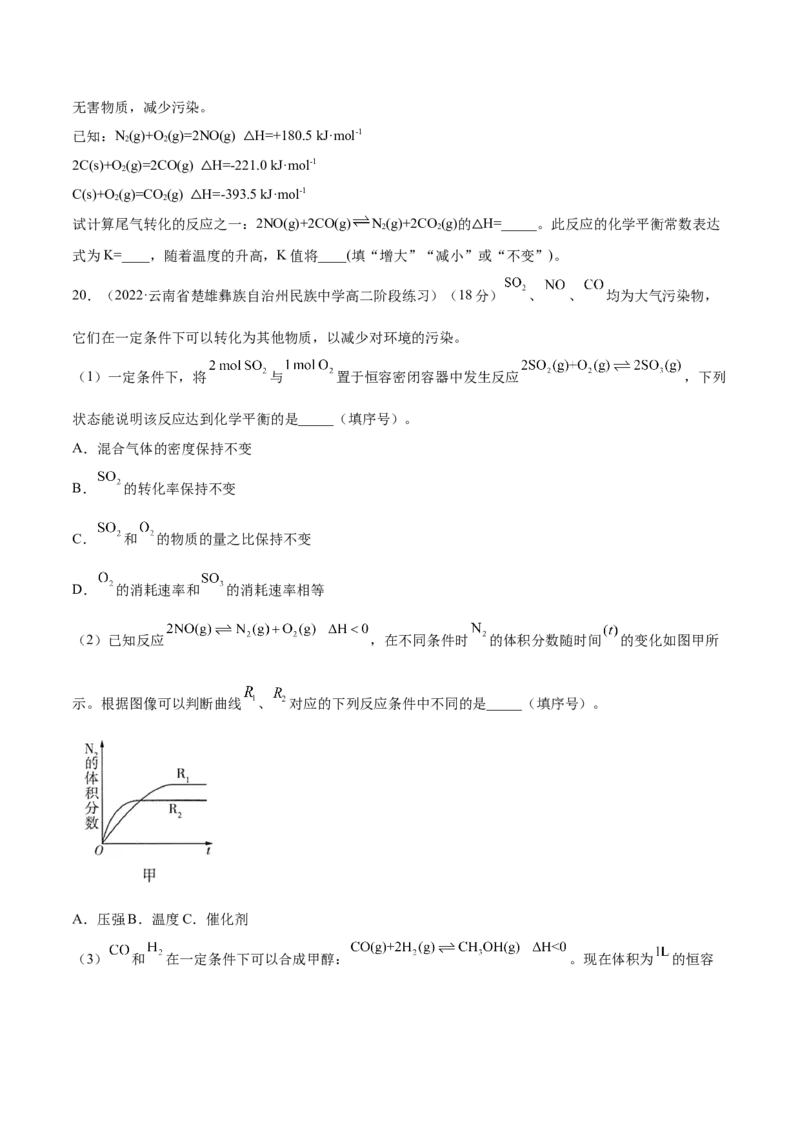
(2)已知反应 ,在不同条件时 的体积分数随时间 的变化如图甲所
示。根据图像可以判断曲线 、 对应的下列反应条件中不同的是_____(填序号)。
A.压强B.温度C.催化剂
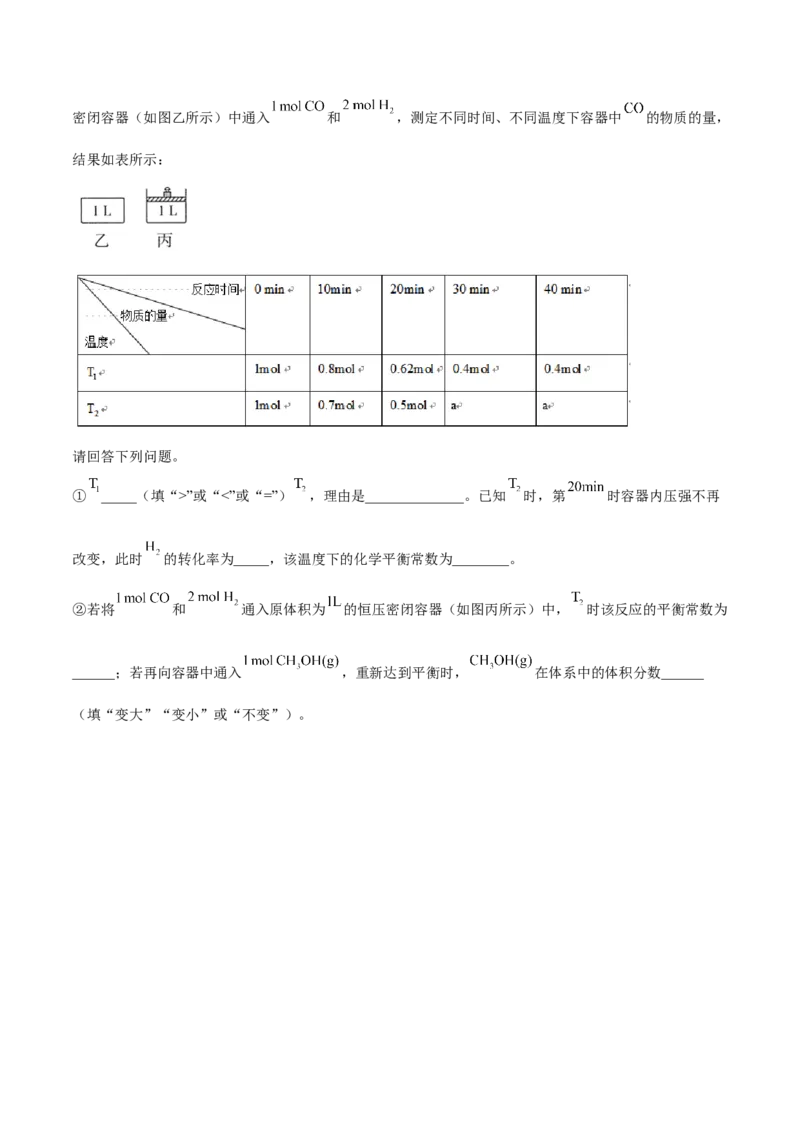
(3) 和 在一定条件下可以合成甲醇: 。现在体积为 的恒容密闭容器(如图乙所示)中通入 和 ,测定不同时间、不同温度下容器中 的物质的量,
结果如表所示:
请回答下列问题。
① _____(填“>”或“<”或“=”) ,理由是______________。已知 时,第 时容器内压强不再
改变,此时 的转化率为_____,该温度下的化学平衡常数为________。
②若将 和 通入原体积为 的恒压密闭容器(如图丙所示)中, 时该反应的平衡常数为
______;若再向容器中通入 ,重新达到平衡时, 在体系中的体积分数______
(填“变大”“变小”或“不变”)。倒卖拉黑,关注更新免费领取,淘宝唯一每月更新店铺:知二教育