文档内容
第二章 章末测试
注意事项:
1.答题前填写好自己的姓名、班级、考号等信息
2.请将答案正确填写在答题卡上
一、单选题(每题4分,共14题,56分)
1.(2020·全国课时练习)配制250mL 0.2mol/L的KNO 溶液,需量取4mol/L KNO 溶液的体积为
3 3
( )
A.125mL B.12.5mL C.50mL D.75mL
【答案】B
【解析】根据稀释前后溶质的物质的量相等,可得 ,
解得 ;故选B。
2.(2020·商水县实验高级中学月考)下列关于0.5molNa SO 的说法正确的是( )
2 4
A.含有3.01×1023个SO B.含有0.5个NaSO
2 4
C.含有0.5molNa+ D.含有1mol氧原子
【答案】A
【解析】A.0.5mol Na SO 含有0.5mol ,即 个 ,故A正确;
2 4
B.0.5mol Na SO 含有0.5mol ,1mol Na+,而不是0.5个NaSO ,故B错误;
2 4 2 4
C.含有Na+物质的量为0.5mol×2=1mol,故C错误;
D.0.5mol Na SO 含有氧原子物质的的量为0.5mol×4=2mol,故D错误。
2 4
综上所述,答案为A。
3.(2020·全国课时练习)下列关于氯水的说法正确的( )
A.新制氯水呈浅黄绿色,是因为氯水中含有HClO
B.新制氯水在光照的条件下,可以产生气体,该气体是氯气
C.新制氯水中滴加硝酸银溶液,没有任何现象
D.新制氯水中滴加石蕊试液,变红后褪色
【答案】D
【解析】A选项,新制氯水呈浅黄绿色,是因为氯水中含有氯气分子而显浅黄绿色,故A错误;B选项,新制氯水在光照的条件下,可以产生气体,该气体是氧气,故B错误;
C选项,新制氯水中滴加硝酸银溶液,生成氯化银沉淀,故C错误;
D选项,新制氯水中滴加石蕊试液,氢离子使石蕊先变红,次氯酸使红色又褪色,故D正确;
综上所述,答案为D。
4.(2020·全国课时练习)实验室欲用 晶体配制 的 溶液,下列
说法正确的是
A.要完成实验需称取 晶体
B.本实验需用到的仪器有天平、药匙、玻璃棒、烧杯、 容量瓶
C.配制时若容量瓶不干燥,含有少量蒸馏水会导致溶液浓度偏低'
D.定容时俯视刻度线会导致溶液浓度偏高
【答案】D
【解析】A. 配制 的 溶液,需要 晶体的质量
,A项错误;
B. 配制一定物质的量浓度溶液的步骤:计算、称量或量取、溶解、移液、洗涤、定容等,用到的仪器有天
平、药匙、玻璃棒、烧杯、 容量瓶、胶头滴管等,B项错误;
C. 定容时,需要向容量瓶中加入蒸馏水,所以配制时若容量瓶不干燥,含有少量蒸馏水对溶液浓度无影响,
C项错误;
D. 定容时俯视刻度线,导致溶液体积偏小,依据 可知溶液浓度偏高,D项正确;
故选D。
5.(2020·马尾·福建师大二附中期末)有NaCl、KSCN、NaOH、AgNO 四种溶液,只用一种试剂就把它
3
们鉴别开来,这种试剂是( )
A.盐酸 B.NaCO 溶液 C.氯水 D.FeCl 溶液
2 3 3
【答案】D
【解析】A.盐酸只能鉴别硝酸银溶液,A错误;
B.碳酸钠溶液只能鉴别硝酸银溶液,B错误;C.氯水和氢氧化钠溶液反应,氯水褪色,和硝酸银反应产生白色沉淀,但不能鉴别氯化钠和KSCN,C错
误;
D.FeCl 溶液与NaCl没有明显现象、与KSCN溶液显血红色、与NaOH生成红褐色沉淀、与AgNO 生成白
3 3
色沉淀,可以鉴别,D正确。答案选D。
6.(2020·全国课时练习)如图所示,两圆圈相交的部分表示圆圈内的物质相互发生的反应。已知钠及其
氧化物的物质的量均为0.1 mol,水的质量为100 g。下列说法正确的是( )
A.NaO 中阴阳离子数目之比为1∶1
2 2
B.反应①的离子方程式为Na+2HO===Na++2OH-+H↑
2 2
C.①、②、③充分反应后所得溶液中溶质的质量分数:①>②>③
D.反应③转移电子的物质的量为0.1mol
【答案】C
【解析】A、过氧化钠中阴离子是O2-,所以阴阳离子数目之比为1:2,错误;
2
B、反应①的离子方程式为:2Na+2HO=2Na++2OH-+H ↑,错误;
2 2
C、反应方程式为:2NaO+2H O=4NaOH+O ↑转移电子2e-,则0.1mol过氧化钠反应最多能转移0.1 mol电
2 2 2 2
子,正确;
D、钠、氧化钠、过氧化钠和水反应的方程式分别如下:
Na+1/2H O=NaOH+1/2H ↑,溶液增加的质量=m(Na)-m(H)=2.3g-0.1g=2.2g;NaO+HO=2NaOH,溶
2 2 2 2 2
液增加的质量=m(NaO)=0.1mol×62g/mol=6.2g;NaO+H O=2NaOH+1/2O ↑,溶液增加的质量=m
2 2 2 2 2
(NaO)-m(O)=m(NaO)=6.2g,所以溶液增加的质量大小顺序为:钠<氧化钠=过氧化钠,根据钠原
2 2 2 2
子守恒知,0.1mol的钠、氧化钠、过氧化钠、溶于水所得氢氧化钠的物质的量分别为:0.1mol、0.2mol、
0.2mol,通过以上分析可知,0.1mol的钠、氧化钠、过氧化钠、分别溶于水所得溶液的质量分数分别为:
4/(100+2.2)×100%、8/(100+6.2)×100%、8/(100+6.2)×100%,所以①、②、③充分反应后所得溶液的质量分
数从大到小:①<②=③,错误;答案选C。
7.(2020·全国课时练习)由NaCl和BaCl 组成的混合溶液100 mL,分为两等份,向其中一份中加入50mL
2
0.60 mol·L-1的AgNO 溶液可使溶液中的Cl-沉淀完全;向另一份溶液中加入50 mL 0.20 mol·L-1的稀硫酸可使
3Ba2+刚好沉淀完全。则原溶液中c(Na+)(单位:mol·L-1)为( )
A.0.1 B.0.2 C.0.4 D.0.02
【答案】B
【解析】根据Ba2+ + SO 2-= BaSO↓可知:n(Ba2+) = n(SO 2-) =0.2mol/L × 0.05L = 0.01mol,根据反应
4 4 4
Ag+ + Cl- ═ AgCl↓,则:n(Cl-) = n(AgNO) =0.6mol/L × 0.05L = 0.03mol,每份溶液中含有:n
3
(Ba2+) = 0.01molmol,n(Cl-) = 0.03mol,由混合溶液分成2等份,则原溶液中钡离子的浓度为:
=0.2mol/L,氯离子的浓度为: =0.6mol/L,根据溶液不显电性,设原混合溶液中
钠离子物质的量浓度为x,则:0.2 mol/L × 2 + x × 1 =0.6mol/L × 1,解得:x =0.2mol/L,所以B正确;故选
B。
8.(2020·全国课时练习)设 为阿伏加德罗常数的值,下列说法正确的是( )
A.1mol 与 个 分子中所含的氧原子数相等
B.含 个O的 的物质的量为1mol
C.1mol NaCl所含的分子数为
D.分子总数为 的 和 混合气体中所含的原子数为
【答案】A
【解析】A.1mol 中含氧原子数为 , 个 分子中含氧原子数为 ,两者所含的氧原
子数相等,故A正确;
B.氧气是双原子分子,含 个O原子的 的物质的量为0.5mol,故B错误;
C.NaCl是离子化合物,化合物中只含钠离子与氯离子,故C错误;
D. 和 都是三原子分子,分子总数为 的 和 的物质的量为1mol,则混合气体中所含
的原子数为 ,故D错误;故选A。
9.(2020·全国课时练习)将0.4g NaOH和1.06g Na CO 混合并配成溶液,向溶液中滴加0.1mol·L-1稀盐酸。
2 3下列图像能正确表示加入盐酸的体积和生成CO 的物质的量的关系的是( )
2
A. B.
C. D.
【答案】C
【解析】0.4g NaOH的物质的量为0.4g÷40g·mol-1=0.01mol和1.06gNa CO 的物质的量为
2 3
1.06g÷106g·mol-1=0.01mol,则
A、0.1L盐酸与氢氧化钠反应没有气体生成,但碳酸钠与盐酸反应生成碳酸氢钠时也没有气体生成,则图
象与反应不符,故A错误;
B、图象中开始反应即有气体生成,与反应不符,故B错误;
C、向NaOH和NaCO 混合溶液中滴加盐酸时,首先和NaOH反应生成水和氯化钠,当滴入0.1L时,两者
2 3
恰好反应完全;继续滴加时,盐酸和NaCO 开始反应,首先发生HCl+Na CO=NaHCO+NaCl,不放出气
2 3 2 3 3
体,当再加入0.1L时,此步反应进行完全;继续滴加时,发生反应:NaHCO +HCl=NaCl+H O+CO↑;此
3 2 2
时开始放出气体,正好与图象相符,故C正确;
D、因碳酸钠与盐酸的反应分步完成,则碳酸钠与盐酸先反应生成碳酸氢钠和氯化钠,此时没有气体生成,
则图象与反应不符,故D错误;
故选C。
10.(2020·全国课时练习)下列反应中,氯气既作氧化剂又作还原剂的是( )
A.
B.
C.D.
【答案】C
【解析】A.由方程式可知,反应中氯元素化合价降低被还原,氯气是反应的氧化剂,故A不符合题意;
B.由方程式可知,反应中氯元素部分化合价升高被氧化,氯气即是氧化产物又是还原产物,故B不符合题
意;
C.由方程式可知,反应中氯元素化合价即降低被还原,又升高被氧化,氯气既作氧化剂又作还原剂,故C
符合题意;
D.由方程式可知,反应中氯元素化合价降低被还原,氯气是反应的氧化剂,故D不符合题意;
故选C。
11.(2021·郁南县蔡朝焜纪念中学高三月考)配制一定物质的量浓度的溶液是一个重要的定量实验,下列
有关说法正确的是( )
A.容量瓶用蒸馏水洗净后,可不经干燥直接用于配制溶液
B.配制一定物质的量浓度的稀盐酸时,用量筒量取9.82 mL浓盐酸
C.配制1 L 0.1 mol·L-1的NaCl溶液时,用托盘天平称量5.85 g NaCl固体
D.定容时,为防止液滴飞溅,胶头滴管紧贴容量瓶内壁
【答案】A
【解析】A.容量瓶用蒸馏水洗净后,不需要干燥,因定容时还需要加水,故A正确;B.量筒的感量为
0.1mL,可量取9.8mL浓盐酸,故B错误;C.托盘天平的感量为0.1g,可称量5.8g固体,故C错误;D.
定容时,胶头滴管要悬空正放,不能紧贴容量瓶内壁,故D错误;故选A。
12.(2020·全国高一单元测试)设N 为阿伏加德罗常数的值。下列说法不正确的是( )
A
A.22.4L(标准状况)氩气含有的质子数为18N
A
B.标准状况下,2.24LCO 和O 的混合气体中分子数为0.2N
2 2 A
C.1molK Cr O 被还原为Cr3+转移的电子数为6N
2 2 7 A
D.120gNaHSO 和KHSO 的固体混合物中含有的阳离子数为N
4 3 A
【答案】B
【解析】A.22.4L(标准状况)氩气的物质的量为1mol,氩气是单原子分子,1mol氩气含有的质子数是
18N ,故A正确;
A
B.标准状况下,2.24L CO 和O 的混合气体的物质的量为0.1mol,所含分子数为0.1N ,故B错误;
2 2 A
C.1molK Cr O 被还原为Cr3+,每个Cr降低3个价态,因此转移的电子数为 ,故C正确;
2 2 7
D.NaHSO 和KHSO 的摩尔质量均为120 g∙mol−1,含有的阳离子分别为Na+、K+,故120gNaHSO 和
4 3 4KHSO 的混合物的物质的量为1mol,含有阳离子的物质的量为1mol,故D正确。
3
综上所述,答案为B。
13.(2020·全国高一单元测试)实验室制备Cl 的反应为MnO +4HCl(浓) Mn2++Cl↑+2H O。下列说法
2 2 2 2
错误的是( )
A.该反应中HCl作还原剂,MnO 作氧化剂
2
B.每生成1molCl ,转移2mol电子
2
C.每消耗1molMnO ,有4molHCl被氧化
2
D.利用该反应制备的Cl 粗产品中,除含有水蒸气外,还含有HCl气体
2
【答案】C
【解析】A. Mn元素化合价降低,得电子,则 作氧化剂,Cl元素化合价升高,失电子,则 作还
原剂,故A正确;
B. 作还原剂, 中Cl元素化合价从-1价升高为Cl 中的0,失电子,则每生成 ,转移
2
电子,故B正确;
C. 该反应每消耗 ,同时消耗 ,其中有 被氧化,另外 表现酸性,
故C错误;
D. 浓盐酸具有挥发性,因此得到的 气体中,除含有水蒸气外,还含有HCl气体,故D正确;
故选C。
14.(2020·黑龙江郊区· 佳木斯一中高三开学考试)下列叙述中不正确的是
A.NaO 是淡黄色固体, Na O 是白色固体, 二者都能与水反应生成 NaOH
2 2 2
B.Na和O 在加热时反应生成 NaO,在常温下反应生成 NaO
2 2 2 2
C.NaO与CO 发生化合反应生成NaCO,NaO 与CO 发生置换反应生成 O
2 2 2 3 2 2 2 2
D.2 g H 充分燃烧后产物被NaO 完全吸收,NaO 固体增重2g
2 2 2 2 2
【答案】C
【解析】A.NaO 是淡黄色固体,与水反应生成氢氧化钠和氧气,NaO 是白色固体,与水反应生成
2 2 2
NaOH,故A正确;
B.Na和O 在加热时反应生成 NaO,在常温下反应生成 NaO,故B正确;
2 2 2 2C.NaO 与CO 反应生成 O 的反应不属于置换反应,故C错误;
2 2 2 2
D.2 g H 充分燃烧生成18g水,18g水被NaO 完全吸收放出氧气,NaO 固体增重2g,故D正确;
2 2 2 2 2
故选C。
二、填空题(共44分)
15.(7分)(2020·全国课时练习)某兴趣小组的同学制备了氯气并探究其性质。试回答下列问题:
Ⅰ.写出实验室制取氯气的化学方程式:_______________________。
Ⅱ.甲同学设计如图所示装置研究氯气能否与水发生反应,气体a是含有少量空气和水蒸气的氯气。请回
答下列问题:
(1)浓硫酸的作用是__________________________。
(2)证明氯气和水反应的实验现象为___________________________。
(3)ICl的性质与 类似,写出ICl与水反应的化学方程式_________________________________。
(4)若将氯气通入石灰乳制取漂白粉,反应的化学方程式是__________________________________。
(5)漂白粉溶于水后,遇到空气中的 ,即产生漂白、杀菌作用,反应的化学方程式是________。
【答案】I:
II (1)干燥
(2)干燥的有色布条不褪色,湿润的有色布条褪色
(3)
(4)
(5)
【解析】Ⅰ.实验室制取 的反应原理: 与浓盐酸在加热条件下反应生成 、 和 ;故答案为: 。
Ⅱ.(1)浓 具有吸水性,常用作干燥剂;故答案为:干燥 。
(2)干燥的 不具有漂白性, 和 反应生成HCl和HClO,HClO具有漂白性,能使有色布条褪色;
故答案为:干燥的有色布条不褪色,湿润的有色布条褪色。
(3)ICl的性质与 类似,其中I的非金属性弱于Cl,I显+1价,Cl显-1价,ICl与 反应生成HIO和
HCl;故答案为: 。
(4) 和石灰乳反应生成 、 和 ;故答案为:
。
(5)漂白粉溶于水后,遇到空气中的 ,反应产生HClO,即产生漂白、杀菌作用,反应的化学方程式是
;故答案为:
。
16.(8分)(2020·全国课时练习)Ⅰ.如图所示为常见仪器的部分结构。
(1)写出下列仪器的名称:
A____________,B____________,C____________。
(2)仪器B上标有____________(填标号)。
①质量 ②温度 ③刻度线 ④浓度 ⑤容积
Ⅱ.现用质量分数为98%的浓硫酸(密度为 )来配制220 mL 0.2 的稀硫酸。有关操作:①计算所需浓硫酸的体积;②量取一定体积的浓硫酸;③稀释、冷却;④转移、洗涤;⑤定容;
⑥摇匀。
(3)用量筒量取的浓硫酸的体积是___________mL。
(4)第③步中稀释浓硫酸的操作是_______________________________________。
(5)将所配制的稀硫酸进行测定,发现实际浓度大于 。会引起所配溶液浓度偏大的操作有
______________(填标号)。
A.用量筒量取浓硫酸时,仰视量筒的刻度线
B.容量瓶未干燥就用来配制溶液
C.浓硫酸在烧杯中稀释后,未冷却就立即转移到容量瓶中,并进行定容
D.烧杯中稀溶液往容量瓶中转移时,有少量液体溅出
E.定容时俯视容量瓶刻度线
F.定容后塞上瓶塞反复摇匀,静置后,液面不到刻度线,再加水至刻度线
【答案】(1)量筒 容量瓶 温度计
(2)②③⑤
(3)2.7
(4)将浓硫酸沿烧杯内壁慢慢加入水中,边加边用玻璃棒搅拌
(5)ACE
【解析】Ⅰ.(1)根据仪器形状、刻度及数值变化确定仪器类型,A是量筒,B是容量瓶(有刻度线),C是
温度计(“0”在中间位置);
(2)容量瓶上标有刻度线、温度和容积,故选②③⑤;
Ⅱ.(3)质量分数为98%的浓硫酸的物质的量浓度
,根据“大而近”原则,配制220mL
溶液需要选用250mL容量瓶,根据稀释定律有 ,解得
,即用量筒量取的浓硫酸的体积为2.7mL;
(4)稀释浓硫酸时,应将浓硫酸沿烧杯内壁慢慢加入水中,边加边用玻璃棒搅拌;
(5)A. 用量筒量取浓硫酸时,仰视量筒的刻度线,量取浓硫酸的体积偏大,溶质偏多,溶液浓度偏大,A
项符合;B. 容量瓶未干燥就用来配制溶液,对所配溶液浓度无影响,B项不符合;
C. 浓硫酸在烧杯中稀释后,未冷却就立即转移到容量瓶中,并进行定容,冷却后溶液的体积变小,溶液浓
度偏大,C项符合;
D. 将烧杯中稀溶液往容量瓶中转移时,有少量液体溅出,溶质有损失,溶液浓度偏小,D项不符合;
E. 定容时俯视容量瓶刻度线,造成容量瓶内溶液的体积偏小,溶液浓度偏大,E项符合;
F. 定容后塞上瓶塞反复摇匀,静置后,液面低于刻度线,再加水至刻度线,导致溶液的体积偏大,溶液浓
度偏小,F项不符合;故选ACE。
17.(10分)(2019·全国高一课时练习)氯气是一种重要的化工原料,氯气及其化合物在自来水的消毒、
农药的生产、药物的合成等领域都有着重要的应用。
Ⅰ.(1)NaClO中Cl的化合价为___________________,NaClO具有较强的___________________(填“氧
化”或“还原”)性,是常用的消毒剂和漂白剂的有效成分。
(2)黄色气体ClO 可用于污水杀菌和饮用水净化。
2
①KClO 与SO 在强碱性溶液中反应可制得ClO ,SO 被氧化为 ,该反应的离子方程式为
3 2 2 2
______________________________________。
②ClO 可将废水中的Mn2+氧化为MnO 而除去,本身被还原为Cl-,该反应过程中氧化剂与还原剂的物质
2 2
的量之比为_____________。
Ⅱ.某学生设计如图所示的实验装置,利用氯气与潮湿的消石灰反应制取少量漂白粉(该反应为放热反应),
回答下列问题:
(1)在A装置中用固体二氧化锰与浓盐酸在加热条件下反应制取氯气,写出该反应的化学方程式
_______________________________。
(2)C装置的作用是________________________。
(3)此实验所得漂白粉的有效成分偏低,该学生经分折并查阅资料发现,主要原因是在U形管中还存在两个
副反应。
①温度较高时氯气与消石灰反应生成Ca(ClO ),为避免此副反应的发生,可采取的措施是_____________。
3 2
②另一个副反应是2HCl+Ca(OH)=CaCl +2H O,为避免此副反应的发生,装置的改进措施为
2 2 2_______________________________。
【答案】I(1)+1 氧化 (2)① ② II(1)
(2)吸收未反应完的氯气,防止污染空气
(3)①将 装置放在冷水浴中 ②在 、 之间连接一个装有饱和 溶液的洗气瓶
【解析】I.(1)NaClO中Na为+1价,O为-2价,则NaClO中Cl为+1价;+1价的Cl容易转化为-1价的
Cl,因此次氯酸钠具有较强的氧化性,故答案为:+1;氧化;
(2)①KClO 与SO 在强酸性溶液中反应可制得ClO ,SO 被氧化为 ,根据得失电子守恒、原子守恒和
3 2 2 2
电荷守恒,反应的离子方程式为 ,故答案为:
;
②ClO 可将废水中的Mn2+转化为MnO 而除去,本身被还原为Cl-,反应中ClO 为氧化剂,Cl元素化合价
2 2 2
由+4价降低为-1价,Mn2+为还原剂,Mn元素化合价由+2价升高到+4价,氧化剂和还原剂得失电子数目相
等,则氧化剂和还原剂的物质的量之比为2∶5,故答案为:2∶5;
Ⅱ.(1)在加热条件下,二氧化锰与浓盐酸反应生成氯化锰、氯气和水,反应的化学方程式为
,故答案为: ;
(2)氯气是有毒气体,要进行尾气处理,则装置C中的氢氧化钠溶液是用于吸收未反应完的氯气,防止污染
空气,故答案为:吸收未反应完的氯气,防止污染空气;
(3)①因温度较高时发生副反应生成Ca(ClO ),则可将B装置冷却来避免该副反应的发生,故答案为:将B
3 2
装置冷却(或将B装置放在冷水浴中);
②因浓盐酸易挥发,为了防止另一个副反应的发生,需要除去氯气中的HCl,可以在A、B之间接一个盛
有饱和NaCl溶液的洗气瓶除去HCl,故答案为:在A、B之间接一个盛有饱和NaCl溶液的洗气瓶。
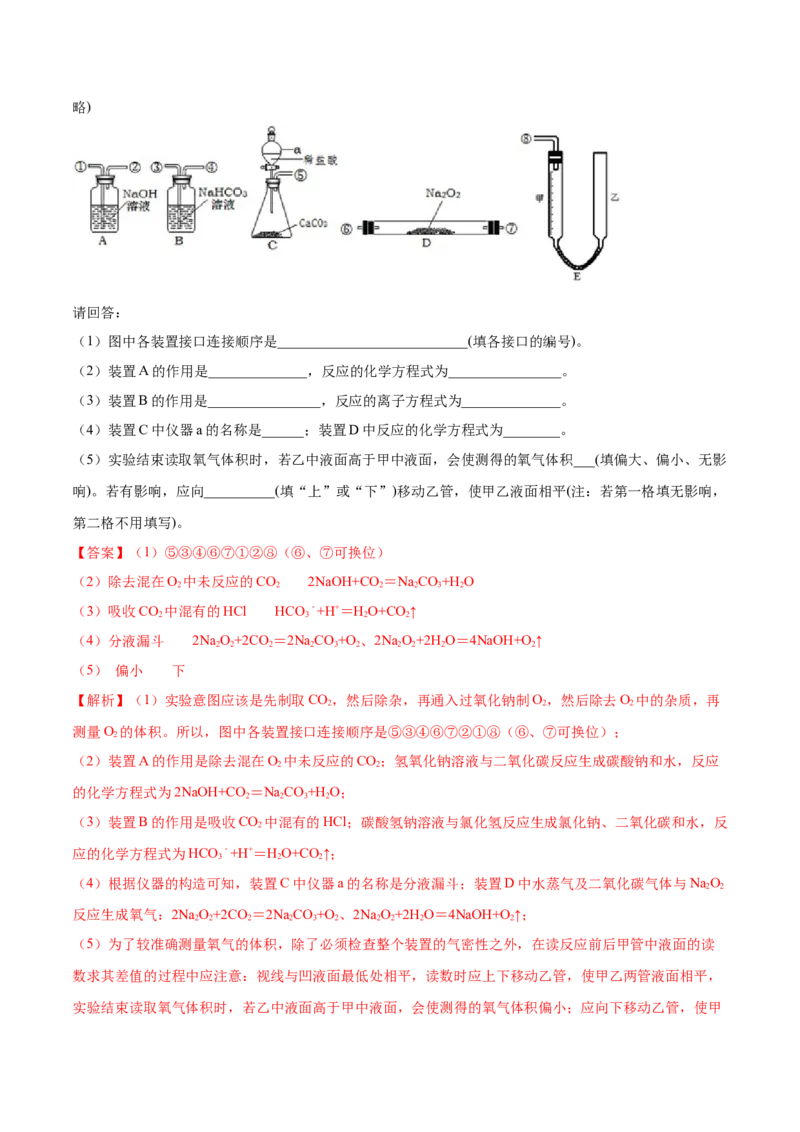
18.(10分)(2020·全国课时练习)某研究性学习小组模拟呼吸面具中的有关反应原理,设计用图所示
的仪器来制取氧气并测量氧气的体积。图中量气装置E由甲、乙两根玻璃管组成,它们由橡皮管连通,并
装入适量水。甲管有刻度(0 50mL)供量气用,乙管可上下移动调节液面高低。(连接胶管及夹持装置均省
∼略)
请回答:
(1)图中各装置接口连接顺序是___________________________(填各接口的编号)。
(2)装置A的作用是______________,反应的化学方程式为________________。
(3)装置B的作用是________________,反应的离子方程式为______________。
(4)装置C中仪器a的名称是______;装置D中反应的化学方程式为________。
(5)实验结束读取氧气体积时,若乙中液面高于甲中液面,会使测得的氧气体积___(填偏大、偏小、无影
响)。若有影响,应向__________(填“上”或“下”)移动乙管,使甲乙液面相平(注:若第一格填无影响,
第二格不用填写)。
【答案】(1)⑤③④⑥⑦①②⑧(⑥、⑦可换位)
(2)除去混在O 中未反应的CO 2NaOH+CO =NaCO+H O
2 2 2 2 3 2
(3)吸收CO 中混有的HCl HCO ﹣+H+=HO+CO↑
2 3 2 2
(4)分液漏斗 2NaO+2CO =2NaCO+O 、2NaO+2H O=4NaOH+O ↑
2 2 2 2 3 2 2 2 2 2
(5) 偏小 下
【解析】(1)实验意图应该是先制取CO,然后除杂,再通入过氧化钠制O,然后除去O 中的杂质,再
2 2 2
测量O 的体积。所以,图中各装置接口连接顺序是⑤③④⑥⑦②①⑧(⑥、⑦可换位);
2
(2)装置A的作用是除去混在O 中未反应的CO;氢氧化钠溶液与二氧化碳反应生成碳酸钠和水,反应
2 2
的化学方程式为2NaOH+CO =NaCO+H O;
2 2 3 2
(3)装置B的作用是吸收CO 中混有的HCl;碳酸氢钠溶液与氯化氢反应生成氯化钠、二氧化碳和水,反
2
应的化学方程式为HCO ﹣+H+=HO+CO↑;
3 2 2
(4)根据仪器的构造可知,装置C中仪器a的名称是分液漏斗;装置D中水蒸气及二氧化碳气体与NaO
2 2
反应生成氧气:2NaO+2CO =2NaCO+O 、2NaO+2H O=4NaOH+O ↑;
2 2 2 2 3 2 2 2 2 2
(5)为了较准确测量氧气的体积,除了必须检查整个装置的气密性之外,在读反应前后甲管中液面的读
数求其差值的过程中应注意:视线与凹液面最低处相平,读数时应上下移动乙管,使甲乙两管液面相平,
实验结束读取氧气体积时,若乙中液面高于甲中液面,会使测得的氧气体积偏小;应向下移动乙管,使甲乙液面相平。
19.(9分)(2020·全国高一单元测试)微型化学实验能有效减少污染,节约药品。如图,某学生在衬有
一张白纸的玻璃片上放置表面皿,在表面皿上的不同位置分别滴加浓度均为0.1 的 、 (含
淀粉)、 (含酚酞)、 (含 )溶液各1滴,在表面皿中心处放置2小粒 晶体,并滴
加一滴浓盐酸,立即将表面皿盖好。可见 晶体很快溶解,并产生气体。
已知 能与 反应生成红色络合物 。
(1)①写出化学实验室中用 制取 的化学方程式:____。
②完成本实验中制取 的化学方程式:___ ____ ____ ___ ____
____,如该反应中消耗还原剂的物质的量为8 ,则转移电子数目为______。
(2)b处的实验现象为______。c处的实验现象为_______。
(3)d处反应的离子方程式为____。
(4)通过该实验能比较 、 、 三种物质氧化性的强弱,其氧化性由强到弱的顺序是_____。
【答案】(1)①
② 2 16 2 2 5
(2)溶液变蓝色 溶液红色褪去(3) 、
(4)
【解析】(1) ①实验室中用 和浓盐酸在加热条件下反应制备 ,化学方程式为
;故答案为:
;
②反应中, 中 元素化合价由+7价降低为 中+2价,共降低5价, 中部分 元素
化合价由-1价升高为 中0价,共升高2价,化合价最小公倍数为10,故 的系数为2、 的系
数为5,根据 原子守恒可知 的系数为2,由K原子守恒可知 的系数为2,根据 原子守恒
可知 的系数为16,再由H原子守恒可知产物中还有水,系数为8,故配平后为
;反应中 中 元素化合价降低,
作氧化剂, 中部分 元素化合价升高, 作还原剂,还有一部分 表现酸性,当消耗
作还原剂的 的物质的量为8 时,生成4 ,转移 电子,个数为 ;
故答案为:2、16、2、2、5、 ; ;
(2) (含淀粉)溶液中的 会被氯气氧化成碘单质,淀粉溶液遇碘单质变蓝,故b处溶液变蓝色;c处滴有
酚酞的氢氧化钠溶液呈红色, 与 发生反应: ,消耗,溶液碱性减弱,且 水解生成的 具有漂白性,溶液红色褪去;故答案为:溶液变蓝
色;溶液红色褪去;
(3)氯气通入 (含 )溶液中,会把亚铁离子氧化成铁离子,铁离子和硫氰化钾反应生成红色的络
合物,离子方程式为 、 ;故答案为:
、 ;