文档内容
第二章 海水中的重要元素——钠和氯
第三节 物质的量
物质的量是化学专有的计量方式,也是高中化学定量计算的核心,当然也是学习的难点,能不能过
去这一关,可能会影响你的选科决定,这部分内容概念多,又抽象,看不见摸不着的,确实让人着急,
所以为了让更多的人能通过这一关,我专门多设置了几个点,以便分散大家的学习压力,本节总共找
出来13个点,可能一时半会儿看不完,你就分开看,或者打印出来慢慢看!
一、物质的量的概念理解
(1)“物质的量”四个字是一个整体,不能添字、漏字或换字。
(2)使用摩尔作单位时,须用微粒符号或化学式或名称指明粒子的种类;摩尔计量的对象只能是微观粒子,不能是
宏观物体。
对点练习1
(2020·西藏昌都市第四高级中学高一期中)下列对于“摩尔”理解正确的是( )
A.1mol任何物质所含有的原子数都相同
B.摩尔是物质的量的单位,简称摩
C.摩尔可以把宏观物质的数量与微观粒子的数量联系起来
D.32g 和32g 中所含氧原子的个数比是2:3
二、摩尔质量概念的理解
(1)等值性:摩尔质量以g·mol-1作单位时,在数值上与其相对分子质量或相对原子质量相等。
(2)确定性:对于指定的物质来说,其摩尔质量的值是一个定值,不随物质的物质的量的多少而改变。
对点练习2
(2020·定边县职业教育中心高一月考)下列说法正确的是( )
A.1molH SO 的质量为98g·mol-1
2 4
B.HSO 的摩尔质量为98g
2 4
C.98gHSO 含有6.02×1023个HSO 分子
2 4 2 4
D.1个HSO 分子的质量是98g
2 4三、物质的量计算微粒数目
(1)物质的质量与微粒数目相互计算时,一般先转换成物质的量,再计算。
(2)物质的化学式表示构成微粒之间物质的量的关系。
如HSO ~2H~S~4O。
2 4
对点练习3
(1)6.02×1023个氢氧根离子的物质的量是________mol,
其摩尔质量为________。
(2)3.01×1023个HO的物质的量为________mol,其中所有原子的物质的量为________mol,所含电子的物质的量为
2
________mol。
(3)1.204×1023个NH +的物质的量为________mol,质量为________g。
4
四、气体摩尔体积
(1)气体摩尔体积只适用于单一气体或混合气体。标准状况下固体或液体的摩尔体积不是22.4 L·mol-1。
(2)气体摩尔体积与压强和温度有关。常温常压下气体摩尔体积不是22.4 L·mol-1,非标准状况下,气体摩尔体积
有可能为22.4 L·mol-1。
对点练习4
(2020·江西南昌十中高一期中)下列有关气体摩尔体积的描述中正确的是( )
A.相同条件下,气体物质的量越大,气体摩尔体积越大
B.通常状况下的气体摩尔体积大于22.4L/mol
C.非标准状况下的气体摩尔体积不可能为22.4L/mol
D.在标准状况下,气体的气体摩尔体积22.4L
五、 正确地理解阿伏加德罗定律及其推论
(1)适用范围:适用于任何气体(单一气体或混合气体),不适用于液体或固体。
(2)“三同定一同”:同温、同压、同体积和同分子数,只要有三“同”成立,则另一“同”就必定成立。
对点练习5
(2020·浙江高一期中)等体积等温度等压强的两容器,A中盛N2,B中盛NH3和H2,A与B比较,下列结论正确的
是( )
A.氢原子个数比为2:5 B.原子个数比为1:2
C.质量比为28:17 D.分子总数比为1:1六、气体摩尔质量的计算方法
(1)定义式法:M=。
(2)标准状况下气体密度法:
M=V ρ =22.4 L·mol-1×ρ (ρ 的单位是g·L-1)。
m 标 标 标
(3)气体相对密度法:M=MD 即==D ,
1 相对 相对
其中D 又叫相对密度。
相对
对点练习6
现有21.6g由CO和CO 组成的混合气体,在标况下其体积为13.44L。回答下列问题:
2
(1)该混合气体的平均摩尔质量为
(2)混合气体中碳原子的质量为
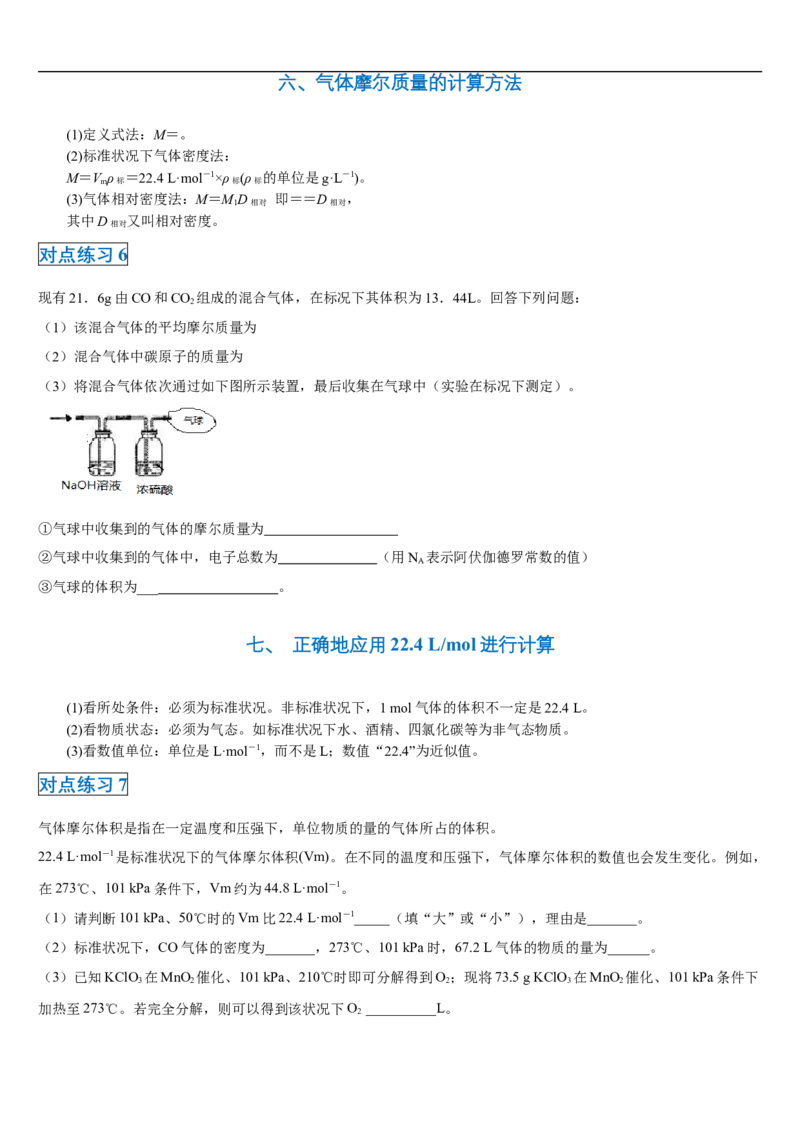
(3)将混合气体依次通过如下图所示装置,最后收集在气球中(实验在标况下测定)。
①气球中收集到的气体的摩尔质量为
②气球中收集到的气体中,电子总数为 (用N 表示阿伏伽德罗常数的值)
A
③气球的体积为___ 。
七、 正确地应用22.4 L/mol进行计算
(1)看所处条件:必须为标准状况。非标准状况下,1 mol气体的体积不一定是22.4 L。
(2)看物质状态:必须为气态。如标准状况下水、酒精、四氯化碳等为非气态物质。
(3)看数值单位:单位是L·mol-1,而不是L;数值“22.4”为近似值。
对点练习7
气体摩尔体积是指在一定温度和压强下,单位物质的量的气体所占的体积。
22.4 L·mol-1是标准状况下的气体摩尔体积(Vm)。在不同的温度和压强下,气体摩尔体积的数值也会发生变化。例如,
在273℃、101 kPa条件下,Vm约为44.8 L·mol-1。
(1)请判断101 kPa、50℃时的Vm比22.4 L·mol-1_____(填“大”或“小”),理由是_______。
(2)标准状况下,CO气体的密度为_______,273℃、101 kPa时,67.2 L气体的物质的量为______。
(3)已知KClO 在MnO 催化、101 kPa、210℃时即可分解得到O;现将73.5 g KClO 在MnO 催化、101 kPa条件下
3 2 2 3 2
加热至273℃。若完全分解,则可以得到该状况下O __________L。
2七、物质的量浓度的计算方法
(1)正确判断溶液的溶质并确定其物质的量
①与水发生反应生成的新的物质为溶质,如Na、NaO、NaO――→NaOH,SO ――→HSO 等。
2 2 2 3 2 4
②含结晶水的物质如CuSO ·5H O溶于水,CuSO 为溶质。
4 2 4
③特殊物质:如NH 溶于水后溶质为NH ·H O,但计算浓度时是以NH 分子作为溶质。
3 3 2 3
(2)正确确定溶液的体积
①物质的量浓度表达式中,V代表溶液体积,而不代表溶剂体积。
②在用物质的量浓度进行计算时要注意V的单位为L。
③浓度较大的溶液与水混合,所得溶液的体积不是水和原溶液的体积之和。
对点练习8
若求一定体积溶液中溶质的物质的量,还必须知道溶液的组成。溶液的组成常用物质的量浓度来表示。
(1)物质的量浓度是用来表示___溶液里所含溶质B的___的物理量,其符号是________。
(2)物质的量浓度常用单位是____________。
(3)溶液的体积用V表示,溶质B的物质的量用n 表示,物质的量浓度(c )的表达式__________。
B B
(4)将20 g氢氧化钠溶于水,配制成500 mL溶液,氢氧化钠溶液的物质的量浓度是__。
九、物质的量浓度与其他浓度的换算
(1)万能公式n====cV(溶液)。
(2)若已知某溶液的密度为ρ g·cm-3(摩尔质量为M g·mol-1的V L气体溶于1 L水形成的溶液),c=== mol·L-
1。
(3)已知溶质B的摩尔质量为M g·mol-1,溶液密度为ρ g·mol-1,溶质的质量分数为w,设其体积为1 L,c ==
B
= mol·L-1。
对点练习9
标况下 VL 氨气溶于 1L 水中制得密度为d g/cm3 的氨水,为计算氨水的物质的量浓度,完成下列空格(要有计算过
程)。
①氨水的体积_______L。
②氨水的物质的量浓度______mol/L。
十、容量瓶的使用——“一查五忌一原则”
一查:使用前检查容量瓶是否漏水。检验程序:
注水→盖塞→倒立→观察→正立→塞旋180°→倒立→观察。
五忌:一忌用容量瓶溶解固体;二忌用容量瓶稀释浓溶液;三忌给容量瓶加热;四忌把容量瓶当作反应容器;五
忌用容量瓶长期存放溶液。
一原则:选择容量瓶应遵循“大而近”的原则。例如配制950 mL 1 mol·L-1 NaCl溶液,应选择1000 mL的容量
瓶,计算NaCl的质量时也应按1000 mL溶液计算。对点练习10
下列关于容量瓶使用方法的叙述中,正确的是
①使用容量瓶前检查是否漏水;
②在容量瓶中溶解氢氧化钠固体;
③容量瓶用蒸馏水洗净后残留少量水即使用;
④溶液需冷却至室温方可注入容量瓶;
⑤加水定容时,不小心超出刻度线,用滴管吸出多余液体.
A.①②③ B.①③④ C.③④⑤ D.①④⑤
十一、配制一定物质的量浓度溶液时的注意事项
(1)配制一定物质的量浓度的溶液时,若加水超过刻度线,不能用胶头滴管吸出过量水的方式进行弥补,而要重新配
制。
(2)容量瓶不能用来配制任意体积的溶液,选择容量瓶时,应遵循“大而近”的原则。
(3)不能在容量瓶中溶解固体药品或稀释浓溶液。
(4)向容量瓶中转移液体前要冷却至室温。
(5)向容量瓶中转移溶液用玻璃棒引流。
(6)液面接近刻度线1~2 cm时,改用胶头滴管滴加蒸馏水 (7)称量NaOH固体时,应把NaOH样品放在小烧杯中
称量。
对点练习11
(2020·山东新泰市第一中学高一期中)下列有关溶液配制说法错误的是( )
A.称取12.5g胆矾[CuSO ·5H O]溶于水中,并加水稀释至500mL,所得溶液物质的量浓度为0.1mol•L-1
4 2
B.取58.5gNaCl固体放入1L水中充分溶解,所得溶液中NaCl的物质的量浓度为1mol·L-1
C.将100g5%的食盐水加热蒸发掉50g水后(没有晶体析出),所得溶液中NaCl的质量分数为10%
D.将浓度为2mol•L-1硫酸钠溶液10mL加水稀释至200mL,所得溶液浓度为0.1mol•L-1
对点练习12
下列与实验相关的叙述中正确的是
A.欲配制1.00 L 1.00 mol·L−1的NaCl溶液,可将58.5 g NaCl溶解在水中配成1.00 L溶液
B.配制溶液时,若加水超过容量瓶刻度线,应用胶头滴管将多余的溶液吸出C.用量筒取5.00 mL 1.00 mol·L−1的盐酸于50 mL容量瓶中,加水稀释至刻度线,可配制0.100 mol·L−1 的盐酸
D.如图所示操作为进行一定物质的量浓度溶液配制时的定容操作
十二、配制一定物质的量浓度溶液的误差分析
(1)由c=可进行误差分析:若n偏小,V准确,则c偏小;若n准确,V偏小,则c偏大;若n偏大,V准确,则c
偏大;若n准确,V偏大,则c偏小。
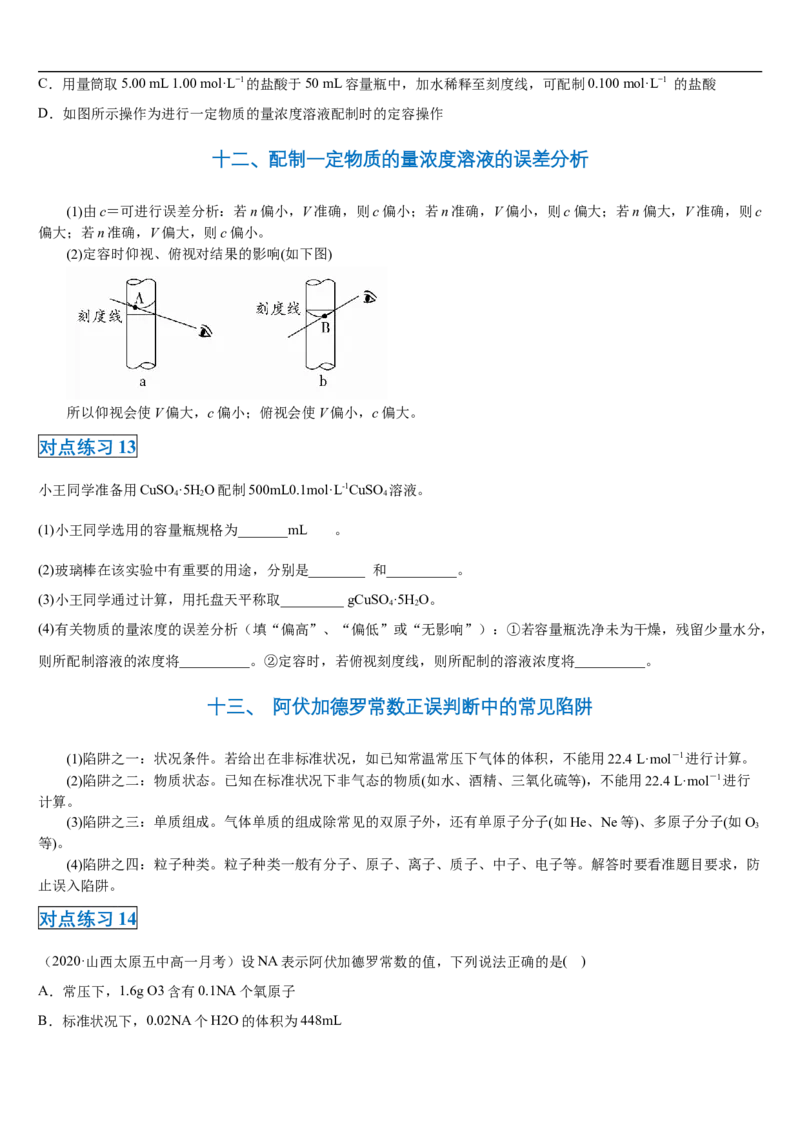
(2)定容时仰视、俯视对结果的影响(如下图)
所以仰视会使V偏大,c偏小;俯视会使V偏小,c偏大。
对点练习13
小王同学准备用CuSO ·5H O配制500mL0.1mol·L-1CuSO 溶液。
4 2 4
(1)小王同学选用的容量瓶规格为_______mL 。
(2)玻璃棒在该实验中有重要的用途,分别是________ 和__________。
(3)小王同学通过计算,用托盘天平称取_________ gCuSO ·5H O。
4 2
(4)有关物质的量浓度的误差分析(填“偏高”、“偏低”或“无影响”):①若容量瓶洗净未为干燥,残留少量水分,
则所配制溶液的浓度将__________。②定容时,若俯视刻度线,则所配制的溶液浓度将__________。
十三、 阿伏加德罗常数正误判断中的常见陷阱
(1)陷阱之一:状况条件。若给出在非标准状况,如已知常温常压下气体的体积,不能用22.4 L·mol-1进行计算。
(2)陷阱之二:物质状态。已知在标准状况下非气态的物质(如水、酒精、三氧化硫等),不能用22.4 L·mol-1进行
计算。
(3)陷阱之三:单质组成。气体单质的组成除常见的双原子外,还有单原子分子(如He、Ne等)、多原子分子(如O
3
等)。
(4)陷阱之四:粒子种类。粒子种类一般有分子、原子、离子、质子、中子、电子等。解答时要看准题目要求,防
止误入陷阱。
对点练习14
(2020·山西太原五中高一月考)设NA表示阿伏加德罗常数的值,下列说法正确的是( )
A.常压下,1.6g O3含有0.1NA个氧原子
B.标准状况下,0.02NA个H2O的体积为448mLC.NA个氢气分子与NA个氧气分子的质量比为1:8
D.0.4mol·L-1KNO3溶液中含有0.4NA个NO
对点练习15
阿伏加德罗常数用N 表示,气体摩尔体积用V 表示,物质的质量用m表示,请回答下列问题:
A m
(1)n= = = ,①②③处分别补充为___、___、___。
(2)一个铜原子的质量为m’g,铜的相对原子质量为M’,则阿伏加德罗常数N =___mol-1。(列出表达式,下同)
A
(3)常温下20滴水约为1mL,水的密度为1g·mL-1,每滴水中约含a个水分子,则阿伏加德罗常数N =___mol-1。
A
(4)bgH 中含N个氢分子,则阿伏加德罗常数N =___mol-1。
2 A
(5)在标准状况下,VLO 中含有N个氧原子,则阿伏加德罗常数N =___mol-1。
2 A
本节跟踪练习
1.(2020·吉林油田高级中学高一开学考试)下列说法和理解正确的是( )
A.阿伏加德罗常数是指1mol任何物质所含的粒子数,其数值约等于6.02×1023
B.摩尔质量在数值上等于它的相对原子质量
C.摩尔既能用来计量纯净物,又能用来计量混合物
D.国际上规定,0.012kg碳原子所含有的碳原子数目为1摩
2.下列对物质的量的理解正确的是( )
A.物质的量是物质所含微粒的数目
B.物质的量就是物质的质量
C.物质的量就是1mol物质的质量
D.物质的量是一种基本物理量
3.(2020·宁夏固原一中高三月考)N 是阿伏加德罗常数的值。下列说法正确的是( )
A
A.10 g质量分数为34%的HO 溶液含有的氢原子数为0.2N
2 2 A
B.0.1 molNa O 和NaO的混合物中含有的离子总数等于0.4N
2 2 2 A
C.标准状况下,22.4 L氯气通入足量氢氧化钠溶液中充分反应后转移电子数为N
A
D.100 mL 0.1 mol/L醋酸中含有的醋酸分子数是0.01N
A
4.下列关于摩尔质量的说法正确的是( )
A.水和冰的摩尔质量都是18g
B.任何物质的摩尔质量都等于它的相对分子质量或相对原子质量C.2 mol氧气的摩尔质量是1 mol氧气摩尔质量的2倍
D.铜的摩尔质量是氢气摩尔质量的32倍
5.(2020·浙江高一期中)草酸(分子式为HC O,沸点:150℃)是生物体的一种代谢产物,广泛分布于植物、动物和
2 2 4
真菌体中。下列有关判断不正确的是
A.草酸的摩尔质量是90 g·mol-1
B.1 mol草酸中含有6.02 ×1023个分子
C.45 g草酸中含有1.204 ×1024 个氧原子
D.1 mol草酸在标准状况下的体积约为22.4L
6.(2020·莆田擢英中学高一期中)下列物质中,摩尔质量最大的是( )
A.1 g CaCO B.0.8 mol HSO C.10 mL H O D.54 g Al
3 2 4 2
7.(2019·陕西西北工业大学附属中学高一期末)在常温常压下,向一个密闭容器中通入aL NO和bL O 会发生反应:
2
2NO+O =2NO,2NO NO 反应后容器内氮原子和氧原子个数之比为( )
2 2 2 2 4
A.a:b ⇌B.a:2b C.a:(a+2b) D.a:2(a+b)
8.下列有关气体摩尔体积的描述中,正确的是( )
A.单位物质的量的气体所占的体积就是气体摩尔体积
B.气体摩尔体积一定是22.4L·mol-1
C.1 mol气体体积为22.4L,则一定是标准状况
D.相同物质的量的气体摩尔体积也相同
9.下列有关阿伏伽德罗定律的说法不正确的是
A.同温同压下,相同质量的NO和C2H4(气体)体积相同
B.同温同压下,气体的密度之比等于摩尔质量之比
C.同温同压下,相同体积的H2和CO2的原子数之比为2:3
D.同温同体积的气体,若物质的量相同则压强相同
10.(2020·四川省广元市川师大万达中学高一期中)下列溶液中溶质的物质的量浓度为1mol·L-1的是( )
A.将标况下 22.4LHCl气体配成 1 L溶液
B.将含有 6.02×1022个 SO 分子的 SO 溶于水并配成 1 L溶液
3 3
C.将 58.5gNaCl溶解于 1 L水中配成的溶液
D.K+为2mol的KSO 溶液
2 4
11.(2019·陕西西北工业大学附属中学高一期末)根据阿伏加德罗定律的相关内容,下列说法错误的是( )
A.温度相同,体积相同的O 和N 分子数不一定相同
2 2
B.常温常压下,SO 与CO 的密度之比等于16∶11
2 2
C.温度和容积相同的两容器中,分别盛有5 mol O 和2 mol N ,则压强之比等于5∶2
2 2
D.标准状况下,SO 与O 的体积之比等于物质的量之比
3 212.(2020·山西大附中高一期中)下列两种气体的原子数一定相等的是( )
A.质量相等、密度不等的N 和C H
2 2 4
B.等温、等体积的O 和Cl
2 2
C.等体积、等密度的C H 和C H
2 4 3 6
D.等压、等体积的NH 和CO
3 2
13.(2020·浙江高一期中)设N 代表阿伏加德罗常数,下列说法正确的是( )
A
A.0°C、101kPa下,11.2LN 和O 的混合气体中所含原子数为N
2 2 A
B.18gHO在标况下的体积为22.4L
2
C.物质的量浓度为2mol/L的BaCl 溶液中,含有Cl-个数为4N
2 A
D.22.4L氨气溶于水制得1L氨水,氨水的物质的量浓度为1mol·L-1
14.(2020·浙江温州中学高一期中)下列溶液中的c(Cl-)与50mL 1mol/L MgCl 溶液中的c(Cl-)相等的是( )
2
A.100mL 1mol/L NaCl溶液 B.75mL 2mol/L CaCl 溶液
2
C.100mL 2mol/L KCl溶液 D.75mL 1mol/L AlCl 溶液
3
15.(2020·山东高一期中)浓度均为0.1mol·L-1的NaCl、CaCl 溶液等体积混合,下列说法错误的是( )
2
A.Na+和Ca2+混合前后的数目均不变
B.混合前CaCl 溶液中c(Cl-)为0.2mol·L-1
2
C.混合后溶液中c(Cl-)为0.3mol·L-1
D.混合前NaCl、CaCl 溶液中c(Cl-)之比为1∶2
2
16.(2020·东台市创新学校高一月考)在标准状况下,所占体积最大的是( )
A.2 mol I B.35.5 g Cl C.36 g HO D.6.02×1022个HF分子
2 2 2
17.(2020·湖南高一期中)下列说法正确的是
A.将0.5 mol NaOH溶于500 mL水中,所得溶液的物质的量浓度为1 mol·L-1
B.从500mL 1 mol·L-1的NaOH溶液中取出一半,则剩余溶液的物质的量浓度为0.5 mol·L-1
C.要配制250 mL 1 mol·L-1的NaOH溶液,需称取NaOH的质量为10 g
D.已知100 mL 1 mol·L-1的NaOH溶液的质量为40 g,则该溶液中溶质的质量分数为10%
18.(2020·平罗中学高一期中)实验室需0.5mol/L的NaOH溶液230mL,配制时应选用容量瓶的规格和称取NaOH
的质量分别是( )
A.240mL,4.8g B.250mL,5.0g C.500mL,10.0g D.任意规格,4.8g
19.(2020·定州市第二中学高一月考)(1)等质量的O 和O 所含的原子个数之比是___________。
2 3
(2)含有相同碳原子数的CO和CO,其质量比为___________。
2
(3)若1g CO 中含有x个原子,则阿伏加德罗常数可表示为__________。
2
(4)4.9g HSO 能和________mol NaOH完全反应。
2 4
(5)标准状况下,10 mL N 气体恰好与30 mL H 完全反应生成20 mL气体A,则A的分子式为_________。
2 2(6)将34.2g Al(SO ) 固体溶于水配成100mL溶液从该溶液中取出10mL,稀释到100mL,稀释后溶液中溶质Al
2 4 3 2
(SO ) 的物质的量浓度为___________。
4 3
20.(2020·福建高一期中)I.(1)10.8 g水与________mol硫酸所含的分子数相等,它们所含氧原子数之比是_____,
氢原子数之比是________。
(2)质量相等的CO和CO 中,同温同压下所占的体积比为______,原子总数之比为___。
2
(3)4.0g某气体X中含有的分子数约为3.01×1022,则气体X的摩尔质量为______。
Ⅱ.某化学实验需要450mL0.10mol·L—1NaCO 溶液,某同学选用NaCO·10H O晶体进行配制,简要回答下列问题:
2 3 2 3 2
(4)该实验应选择____ 容量瓶;需称取NaCO ·10H O晶体的质量为_____g。
2 3 2
(5)下列操作对溶液浓度有何影响(填“偏高”、“偏低”或“无影响”)。
①若容量瓶中有检漏时残留的少量蒸馏水,会使所配溶液浓度__________;
②配制过程中未洗涤烧杯和玻璃棒,会使所配溶液浓度__________;
③定容时必须使凹液面最低处与刻度线相切,若仰视会使所配溶液浓度__________;
④摇匀后,发现容量瓶中液面低于刻度线,会使所配溶液浓度__________。
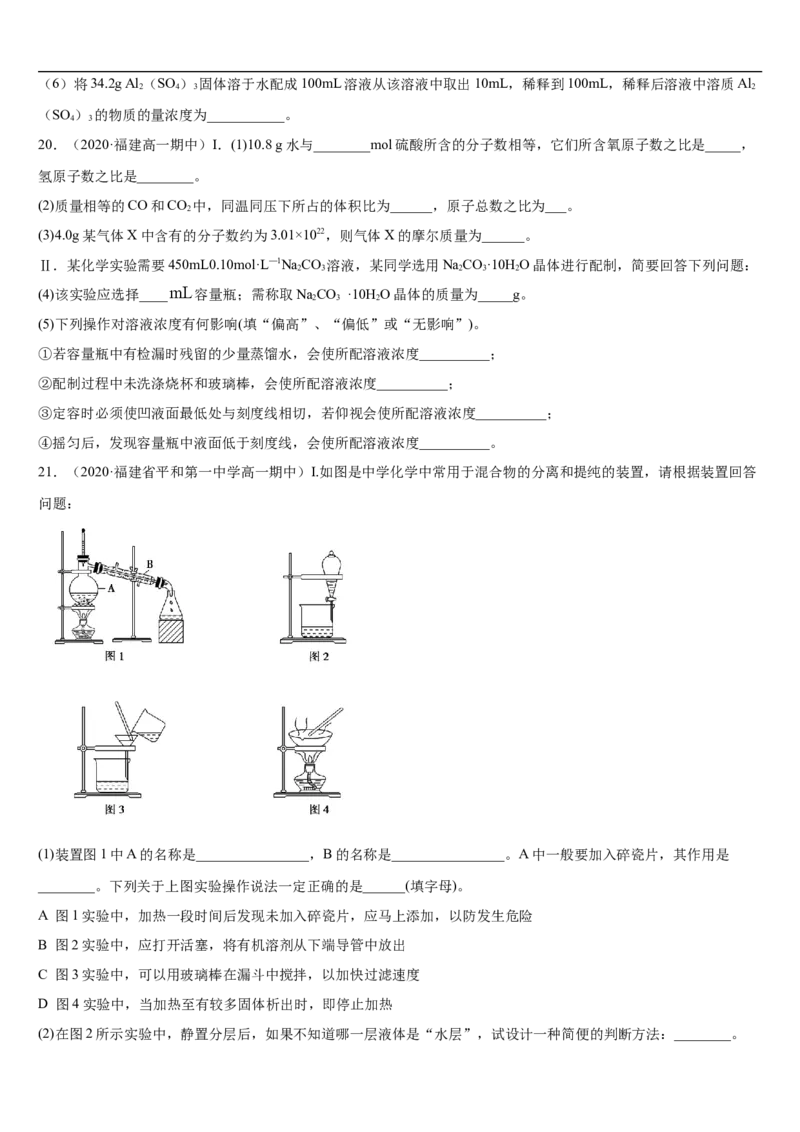
21.(2020·福建省平和第一中学高一期中)I.如图是中学化学中常用于混合物的分离和提纯的装置,请根据装置回答
问题:
(1)装置图1中A的名称是________________,B的名称是________________。A中一般要加入碎瓷片,其作用是
________。下列关于上图实验操作说法一定正确的是______(填字母)。
A 图1实验中,加热一段时间后发现未加入碎瓷片,应马上添加,以防发生危险
B 图2实验中,应打开活塞,将有机溶剂从下端导管中放出
C 图3实验中,可以用玻璃棒在漏斗中搅拌,以加快过滤速度
D 图4实验中,当加热至有较多固体析出时,即停止加热
(2)在图2所示实验中,静置分层后,如果不知道哪一层液体是“水层”,试设计一种简便的判断方法:________。II.现用质量分数为98%、密度为1.84 g·cm-3的浓硫酸来配制480 mL 0.2 mol·L-1的稀硫酸。可供选择的仪器有:①玻璃
棒 ②烧杯 ③胶头滴管 ④量筒,
请回答下列问题:
(1)上述仪器中,在配制稀硫酸时还需要用到的仪器有_____(填名称)。
(2)经计算,浓硫酸物质的量的浓度________________;需用量筒量取浓硫酸的体积为 _________;现有①10 mL、
②50mL、③100 mL三种规格的量筒,应选用的量筒是_______(填代号)。
(3)在配制过程中,下列操作中会引起稀硫酸物质的量浓度偏低的有_______(填代号)。
①洗涤量取浓硫酸后的量筒,并将洗涤液转移到容量瓶中
②未等稀释后的硫酸溶液冷却至室温就转移到容量瓶中
③定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
④转移前,容量瓶中含有少量蒸馏水
⑤量取浓硫酸时,俯视刻度线