文档内容
《化学生产中的重要非金属元素》检测题(含答案)
一、单选题
1.下列说法不正确的是
A.浓硝酸、硝酸银、氯水均用棕色试剂瓶保存
B.氨气能使湿润的蓝色石蕊试纸变红
C.硝酸与FeO反应生成 ,表明硝酸具有氧化性
D.等量的铜与足量 完全反应,硝酸的浓度越大,消耗的 越多
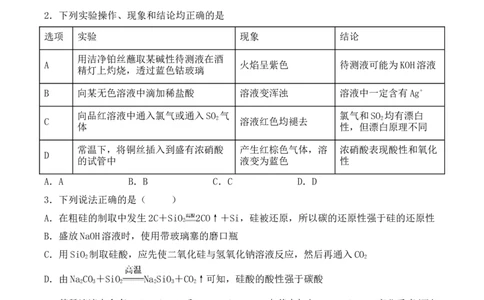
2.下列实验操作、现象和结论均正确的是
选项 实验 现象 结论
用洁净铂丝蘸取某碱性待测液在酒
A 火焰呈紫色 待测液可能为KOH溶液
精灯上灼烧,透过蓝色钴玻璃
B 向某无色溶液中滴加稀盐酸 溶液变浑浊 溶液中一定含有Ag+
向品红溶液中通入氯气或通入SO 气 氯气和SO 均有漂白
C 2 溶液红色均褪去 2
体 性,但漂白原理不同
常温下,将铜丝插入到盛有浓硝酸 产生红棕色气体,溶 浓硝酸表现酸性和氧化
D
的试管中 液变为蓝色 性
A.A B.B C.C D.D
3.下列说法正确的是( )
A.在粗硅的制取中发生2C+SiO 2CO↑+Si,硅被还原,所以碳的还原性强于硅的还原性
2
B.盛放NaOH溶液时,使用带玻璃塞的磨口瓶
C.用SiO 制取硅酸,应先使二氧化硅与氢氧化钠溶液反应,然后再通入CO
2 2
D.由Na CO +SiO Na SiO +CO ↑可知,硅酸的酸性强于碳酸
2 3 2 2 3 2
4.某稀溶液中含有3.5 mol KNO 和2.2 mol H SO ,向其中加入1.2 mol Fe,充分反应(已知
3 2 4
NO 被还原为NO)。下列说法正确的是
A.反应过程中转移的电子数3N
A
B.反应后生成NO的体积为24.64 L
C.所得溶液中c(Fe2+)∶c(Fe3+)=1∶3
D.所得溶液中c(NO -)=2.4 mol·L-1
3
5.下列各组物质的各步转化均可以通过一步反应完成的是A.S→SO →H SO →SO B.Al→Al O →Al(OH) →AlCl
3 2 4 2 2 3 3 3
C.Si→SiO →H SiO →Na SiO D.Fe→FeCl →Fe(OH) →Fe(OH)
2 2 3 2 3 2 2 3
6.三氟化氮(NF )常用于微电子工业,可用以下反应制备:4NH +3F =NF +3NH F,下列说法
3 3 2 3 4
中,正确的是( )
A.NF 的电子式为
3
B.NH F分子中仅含离子键
4
C.在制备NF 的反应中,NH 表现出还原性
3 3
D.在制备NF 的反应方程式中,各物质均为共价化合物
3
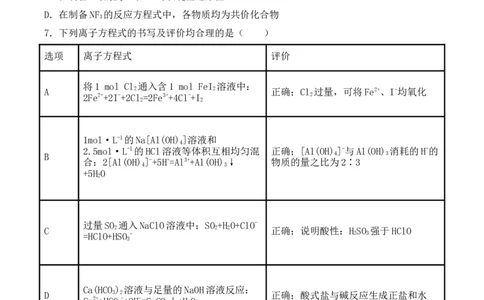
7.下列离子方程式的书写及评价均合理的是( )
选项 离子方程式 评价
将1 mol Cl 通入含1 mol FeI 溶液中:
A 2 2 正确;Cl 过量,可将Fe2+、I-均氧化
2Fe2++2I-+2Cl =2Fe3++4Cl-+I 2
2 2
1mol·L-1的Na[Al(OH) ]溶液和
4
2.5mol·L-1的HCl溶液等体积互相均匀混 正确;[Al(OH) ]-与Al(OH) 消耗的H+的
B 4 3
合:2[Al(OH) ]-+5H+=Al3++Al(OH) ↓ 物质的量之比为2∶3
4 3
+5H O
2
过量SO 通入NaClO溶液中:SO +H O+ClO-
C 2 2 2 正确;说明酸性:H SO 强于HClO
=HClO+HSO - 2 3
3
Ca(HCO ) 溶液与足量的NaOH溶液反应:
D 3 2 正确;酸式盐与碱反应生成正盐和水
Ca2++HCO -+OH-=CaCO ↓+H O
3 3 2
A.A B.B C.C D.D
8.下列气体中有毒且有颜色的是( )
A.Cl B.O C.N D.CO
2 2 2
9.下列物质不能通过化合反应制得的是( )
A.CO B.FeCl C.Fe(OH) D.H SiO
2 2 3 2 310.下列物质的保存方法正确的是
A.氢氧化钠溶液保存在玻璃塞的玻璃瓶中
B.漂白粉露置于空气中
C.浓硝酸、氯水保存在棕色细口玻璃瓶中
D.钠保存在盛有水的试剂瓶中
11.化学无处不在,下列有关说法正确的是
A.在“雾霾” 等空气污染的治理方面,化学不能发挥作用
B.常温下,可以用铁罐贮存浓硝酸,说明铁与浓硝酸不反应
C.用豆浆可以制作出美味可口的豆腐,运用化学知识可以解释其原理
D.氯气、明矾是水处理过程中常用的两种化学试剂,均可用于自来水消毒
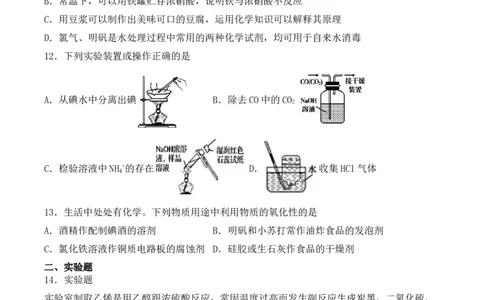
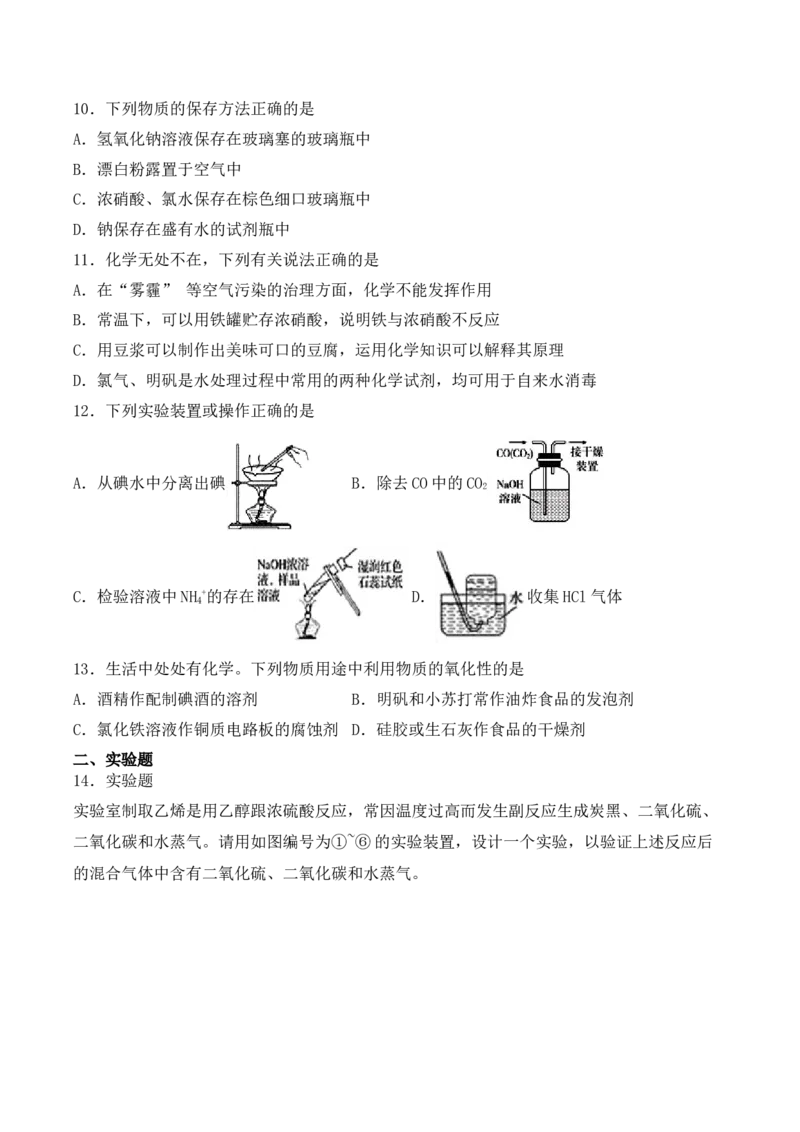
12.下列实验装置或操作正确的是
A.从碘水中分离出碘 B.除去CO中的CO
2
C.检验溶液中NH +的存在 D. 收集HCl气体
4
13.生活中处处有化学。下列物质用途中利用物质的氧化性的是
A.酒精作配制碘酒的溶剂 B.明矾和小苏打常作油炸食品的发泡剂
C.氯化铁溶液作铜质电路板的腐蚀剂 D.硅胶或生石灰作食品的干燥剂
二、实验题
14.实验题
实验室制取乙烯是用乙醇跟浓硫酸反应,常因温度过高而发生副反应生成炭黑、二氧化硫、
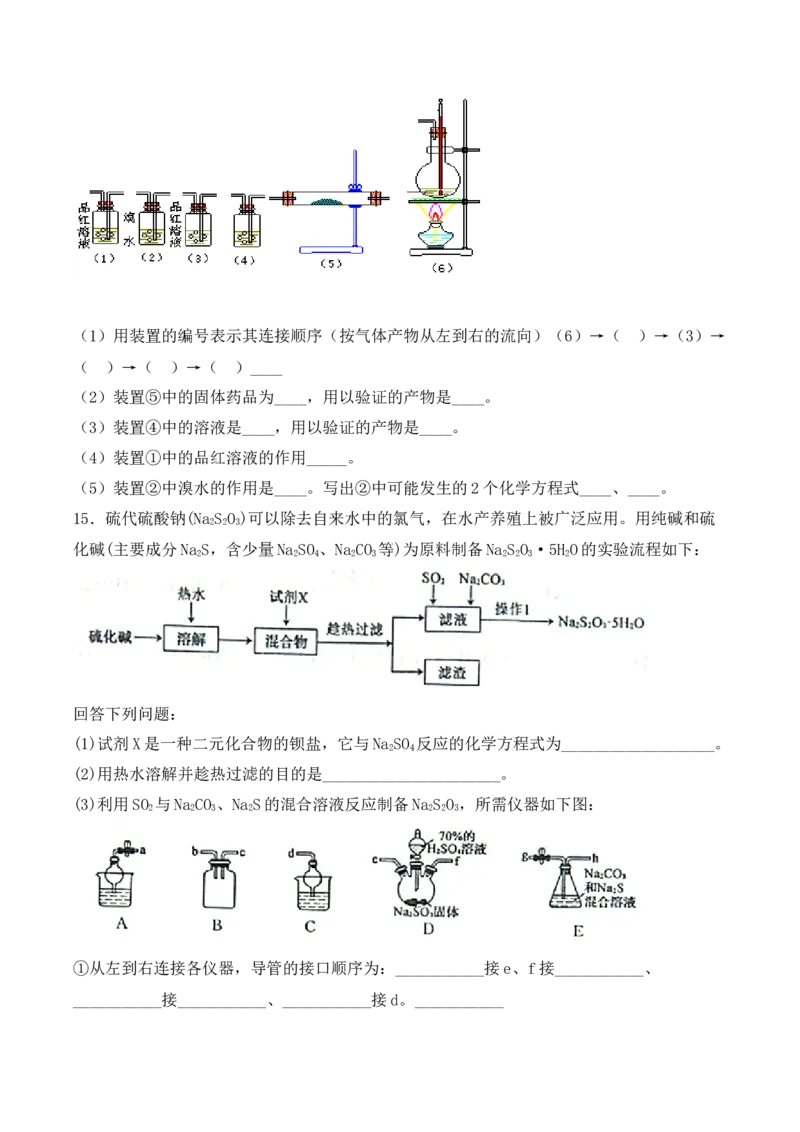
二氧化碳和水蒸气。请用如图编号为①~⑥的实验装置,设计一个实验,以验证上述反应后
的混合气体中含有二氧化硫、二氧化碳和水蒸气。(1)用装置的编号表示其连接顺序(按气体产物从左到右的流向)(6)→( )→(3)→
( )→( )→( )____
(2)装置⑤中的固体药品为____,用以验证的产物是____。
(3)装置④中的溶液是____,用以验证的产物是____。
(4)装置①中的品红溶液的作用_____。
(5)装置②中溴水的作用是____。写出②中可能发生的2个化学方程式____、____。
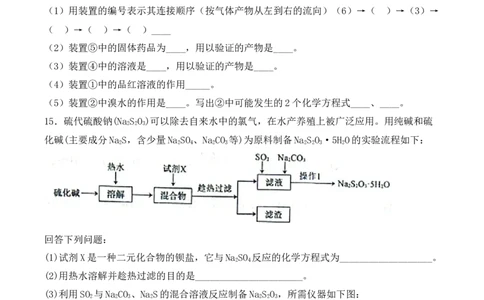
15.硫代硫酸钠(Na S O )可以除去自来水中的氯气,在水产养殖上被广泛应用。用纯碱和硫
2 2 3
化碱(主要成分Na S,含少量Na SO 、Na CO 等)为原料制备Na S O ·5H O的实验流程如下:
2 2 4 2 3 2 2 3 2
回答下列问题:
(1)试剂X是一种二元化合物的钡盐,它与Na SO 反应的化学方程式为___________________。
2 4
(2)用热水溶解并趁热过滤的目的是______________________。
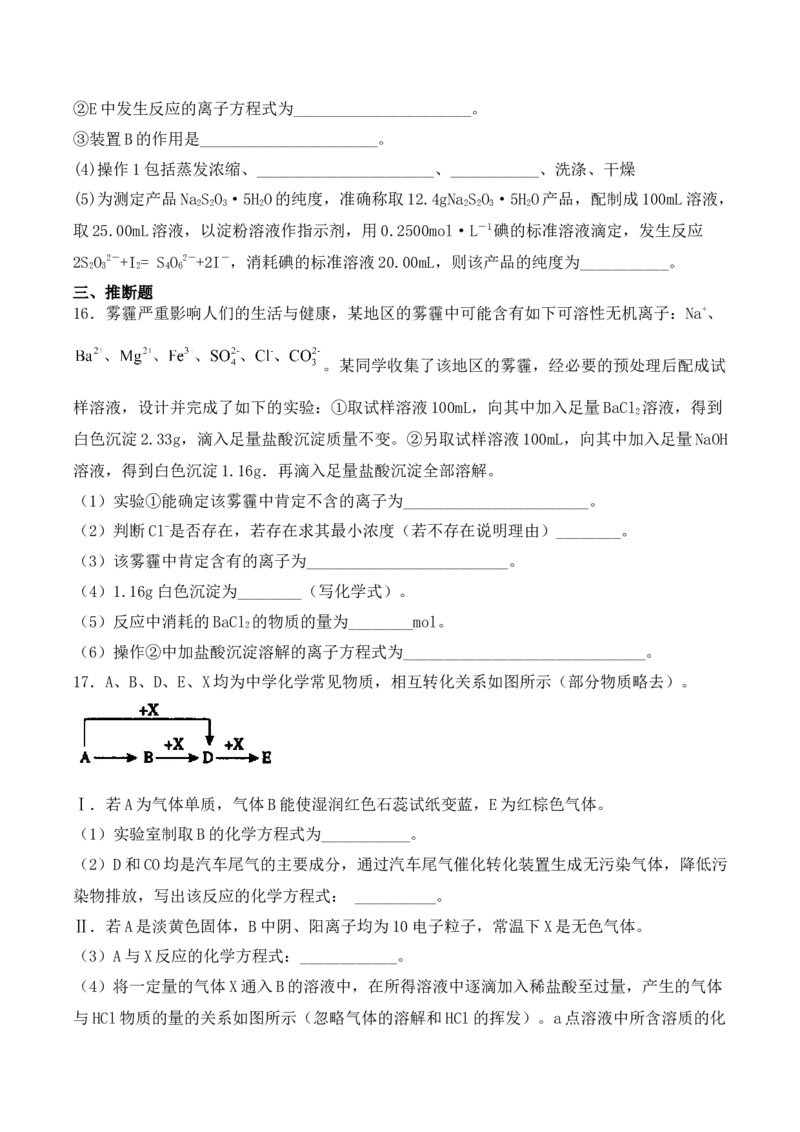
(3)利用SO 与Na CO 、Na S的混合溶液反应制备Na S O ,所需仪器如下图:
2 2 3 2 2 2 3
①从左到右连接各仪器,导管的接口顺序为:___________接e、f接___________、
___________接___________、___________接d。___________②E中发生反应的离子方程式为______________________。
③装置B的作用是______________________。
(4)操作1包括蒸发浓缩、______________________、___________、洗涤、干燥
(5)为测定产品Na S O ·5H O的纯度,准确称取12.4gNa S O ·5H O产品,配制成100mL溶液,
2 2 3 2 2 2 3 2
取25.00mL溶液,以淀粉溶液作指示剂,用0.2500mol·L-1碘的标准溶液滴定,发生反应
2S O 2-+I = S O 2-+2I-,消耗碘的标准溶液20.00mL,则该产品的纯度为___________。
2 3 2 4 6
三、推断题
16.雾霾严重影响人们的生活与健康,某地区的雾霾中可能含有如下可溶性无机离子:Na+、
。某同学收集了该地区的雾霾,经必要的预处理后配成试
样溶液,设计并完成了如下的实验:①取试样溶液100mL,向其中加入足量BaCl 溶液,得到
2
白色沉淀2.33g,滴入足量盐酸沉淀质量不变。②另取试样溶液100mL,向其中加入足量NaOH
溶液,得到白色沉淀1.16g.再滴入足量盐酸沉淀全部溶解。
(1)实验①能确定该雾霾中肯定不含的离子为_______________________。
(2)判断Cl-是否存在,若存在求其最小浓度(若不存在说明理由)________。
(3)该雾霾中肯定含有的离子为_________________________。
(4)1.16g白色沉淀为________(写化学式)。
(5)反应中消耗的BaCl 的物质的量为________mol。
2
(6)操作②中加盐酸沉淀溶解的离子方程式为______________________________。
17.A、B、D、E、X均为中学化学常见物质,相互转化关系如图所示(部分物质略去)。
Ⅰ.若A为气体单质,气体B能使湿润红色石蕊试纸变蓝,E为红棕色气体。
(1)实验室制取B的化学方程式为___________。
(2)D和CO均是汽车尾气的主要成分,通过汽车尾气催化转化装置生成无污染气体,降低污
染物排放,写出该反应的化学方程式: __________。
Ⅱ.若A是淡黄色固体,B中阴、阳离子均为10电子粒子,常温下X是无色气体。
(3)A与X反应的化学方程式:____________。
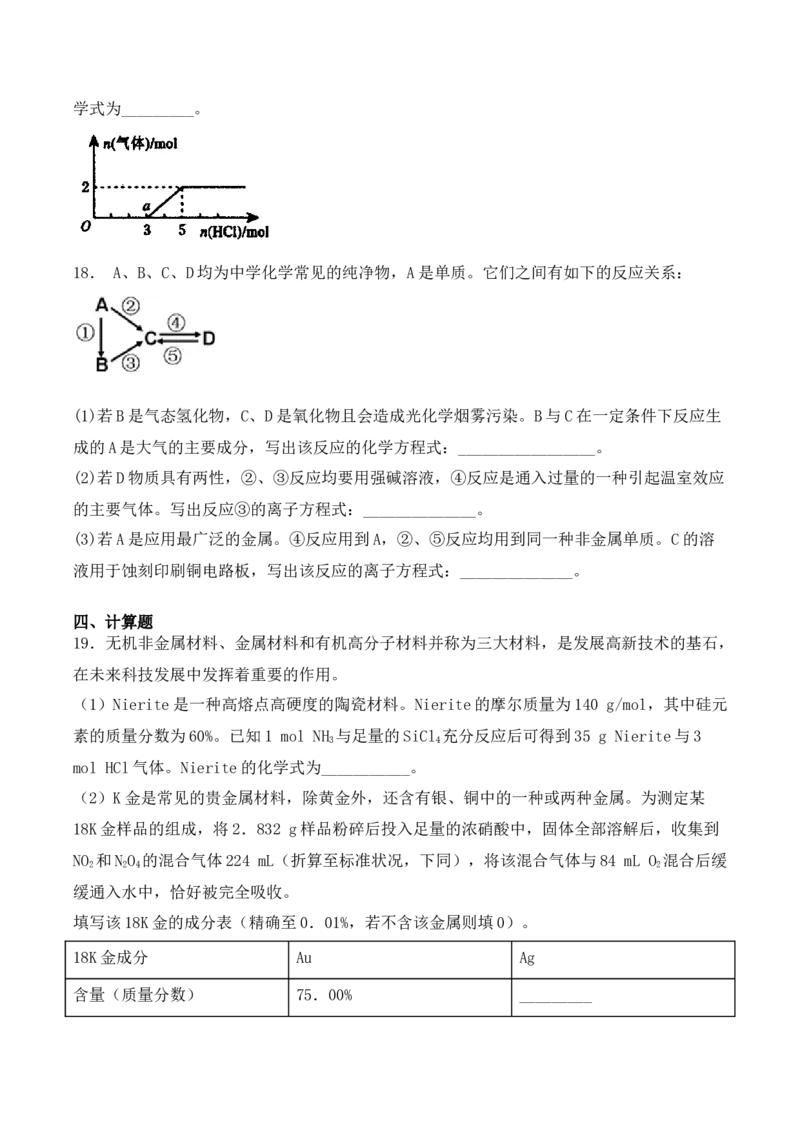
(4)将一定量的气体X通入B的溶液中,在所得溶液中逐滴加入稀盐酸至过量,产生的气体
与HCl物质的量的关系如图所示(忽略气体的溶解和HCl的挥发)。a点溶液中所含溶质的化学式为_________。
18. A、B、C、D均为中学化学常见的纯净物,A是单质。它们之间有如下的反应关系:
(1)若B是气态氢化物,C、D是氧化物且会造成光化学烟雾污染。B与C在一定条件下反应生
成的A是大气的主要成分,写出该反应的化学方程式:_________________。
(2)若D物质具有两性,②、③反应均要用强碱溶液,④反应是通入过量的一种引起温室效应
的主要气体。写出反应③的离子方程式:______________。
(3)若A是应用最广泛的金属。④反应用到A,②、⑤反应均用到同一种非金属单质。C的溶
液用于蚀刻印刷铜电路板,写出该反应的离子方程式:______________。
四、计算题
19.无机非金属材料、金属材料和有机高分子材料并称为三大材料,是发展高新技术的基石,
在未来科技发展中发挥着重要的作用。
(1)Nierite是一种高熔点高硬度的陶瓷材料。Nierite的摩尔质量为140 g/mol,其中硅元
素的质量分数为60%。已知1 mol NH 与足量的SiCl 充分反应后可得到35 g Nierite与3
3 4
mol HCl气体。Nierite的化学式为___________。
(2)K金是常见的贵金属材料,除黄金外,还含有银、铜中的一种或两种金属。为测定某
18K金样品的组成,将2.832 g样品粉碎后投入足量的浓硝酸中,固体全部溶解后,收集到
NO 和N O 的混合气体224 mL(折算至标准状况,下同),将该混合气体与84 mL O 混合后缓
2 2 4 2
缓通入水中,恰好被完全吸收。
填写该18K金的成分表(精确至0.01%,若不含该金属则填0)。
18K金成分 Au Ag
含量(质量分数) 75.00% _________20. 向400mL某浓度的稀硝酸中加入Wg铁粉(还原产物只有NO),充分反应后,铁粉减少
16.8 g且铁粉有剩余,继续向容器中加入足量的稀硫酸,会产生气体A。回答下列问题:
(1)稀硝酸的物质的量浓度是_____________ mol·L−1
(2)气体A中若含有H ,则W的值一定要大于__________g.
2参考答案
1.B2.A3.C4.C5.D6.C7.B8.A9.D10.C11.C12.B13.C
14.(6)→(5)→(3)→(2)→(1→(4) 无水硫酸铜粉末 H O
2
澄清石灰水 CO 检验SO 是否被除尽 除出CO 中的SO
2 2 2 2
SO +Br +2H O=H SO +2HBr CH =CH +Br →BrCH CH Br
2 2 2 2 4 2 2 2 2 2
15.BaS+Na SO = BaSO +Na S 更快更多溶解硫化碱,并防止过滤时,因降温
2 4 4 2
而析出Na S,造成损失 a b c g h CO 2-+2 S2-+SO =3S O 2-+CO
2 3 2 2 3 2
作安全瓶,防止E中溶液倒吸入D中 冷却结晶 过滤 80%
16.Ba2+、Fe3+、CO 2- 0.2mol/L Mg2+、SO 2-、Cl- Mg(OH) 0.01mol
3 4 2
17.Ca(OH) + 2NH Cl== CaCl + 2NH ↑ + 2H O 2CO + 2NO N + 2CO
2 4 2 3 2 2 2
2CO + 2Na O =2Na CO + O NaHCO 、 NaCl
2 2 2 2 3 2 3
18.4NH +6NO 5N +6H O Al O +2OH-=2AlO -+H O 2Fe3++Cu=2Fe2++Cu2+
3 2 2 2 3 2 2
19.Si N 11.44%
3 4
20.2 67.2