文档内容
第五章 化工生产中的重要非金属元素
单元测试卷
(考试时间:90分钟 试卷满分:100分)
第Ⅰ卷(选择题 44 分)
一、选择题:本题包括22小题,每小题只有以个选项符合题意,每小题2分,共44分。
1.下列有关酸雨及形成的说法正确的是( )
A.pH小于7的降雨通常称为酸雨
B.酸雨的形成和空气中CO 含量增多有直接关系
2
C.大量含硫化石燃料燃烧是形成酸雨的主要原因
D.植被破坏、水土流失、生态环境破坏导致了酸雨形成
2.化学知识与科技、生产、生活有密切的关系。下列叙述中错误的是( )
A.“天宫二号”空间运行的动力源泉——太阳能电池帆板,其核心材料为晶体硅
B.“天问一号”火星车使用的保温材料——纳米气凝胶,具有丁达尔效应
C.三星堆二号祭祀坑出土商代的铜人铜像填补了我国考古学、青铜文化史上的诸多空白。青铜器的出土
表明我国商代已经掌握冶炼铜技术
D.“北斗系统”组网成功,北斗芯片中的半导体材料为二氧化硅
3.下列说法正确的是( )
A.硫质脆,微溶于酒精和二硫化碳
B.硫与氢气反应,体现了硫的还原性
C.硫与铁粉和铜粉分别反应,都可生成二价金属硫化物
D.从硫的化合价角度分析,硫单质既可作氧化剂又可作还原剂
4.下列说法正确的是( )
A.浓硫酸具有强氧化性,常温下可与铁单质剧烈反应
B.SO 能杀菌消毒防腐,常用作食品添加剂
2
C.氨气因有刺激性气味,因此不用来作制冷剂
D.所有铵盐受热均可以分解,产物均有NH
3
5.我国具有独立知识产权的电脑芯片“龙芯一号”的问世,填补了我国计算机制造史上的一项空白。下
列对硅及其化合物的有关叙述正确的是( )
A.二氧化硅既能与烧碱溶液反应又能与氢氟酸反应,所以二氧化硅是两性氧化物B.晶体硅的化学性质不活泼,常温下不与任何物质发生反应
C.晶体硅是一种良好的半导体材料,但是它的提炼工艺复杂,价格极高
D.晶体硅和金刚石的硬度都很大
6.下列关于氮及其化合物的说法错误的是( )
A.NO 和水反应,NO 既做了氧化剂又做了还原剂
2 2
B.NO、NO 均为大气污染气体,在大气中均可稳定存在
2
C.可用浓盐酸检测输送NH 的管道是否发生泄漏
3
D.HNO 具有强氧化性,可溶解铜、银等不活泼金属
3
7.大气污染物SO 易溶于水,通常表现出较强的还原性,对人体的呼吸系统和中枢神经系统等均有毒性作
2
用。认识和利用SO 的性质可有效防治 对环境的污染,并实现SO 的综合利用。实验室通过下列实验
2 2
探究SO 的性质。
2
实验 实验操作和现象
用充有80mLSO 的针筒吸入 蒸馏水,用橡皮塞堵住针筒前端,充分振荡,
1 2
针筒内几乎没有气体剩余
2 取5mL实验1中的溶液,滴入几滴紫色石蕊试液,溶液显红色
3 取5mL实验1中的溶液,加入5mL3%的HO 溶液,观察不到实验现象
2 2
4 取5mL实验1中的溶液,通入HS气体,出现淡黄色浑浊
2
下列有关说法正确的是( )
A.实验1说明SO 与水发生了化学反应
2
B.实验2中发生了以下过程:SO +HO HSO 、HSO ==2H++SO
2 2 2 3 2 3
C.实验3中可能发生了反应SO +HO==H SO
2 2 2 2 4
D.实验4说明SO 水溶液具有还原性
2
8.由下列实验事实得出的结论正确的是( )
A.由SiO 不能与水反应生成硅酸可知,SiO 不是酸性氧化物
2 2
B.CO 通入NaSiO 溶液产生白色沉淀,可知酸性HCO>HSiO
2 2 3 2 3 2 3
C.由SiO+2C \o(\s\up6(_____)Si+2CO↑,可知碳的非金属性大于硅
2
D.SiO 可与NaOH溶液反应,也可与氢氟酸反应,可知SiO 为两性氧化物
2 2
9.物质的类别和核心元素的化合价是研究物质化学性质的两个重要角度。某短周期元素的单质及其部分
化合物的价类二维图如图所示。下列推断合理的是( )
A.a到b、c、d、e、f均可直接转化B.标准状况下,1molb和c的混合物体积为22.4L
C.可先加盐酸,再加氯化钡溶液检验e的钠盐是否变质
D.f的水溶液在空气中放置,不易被氧化
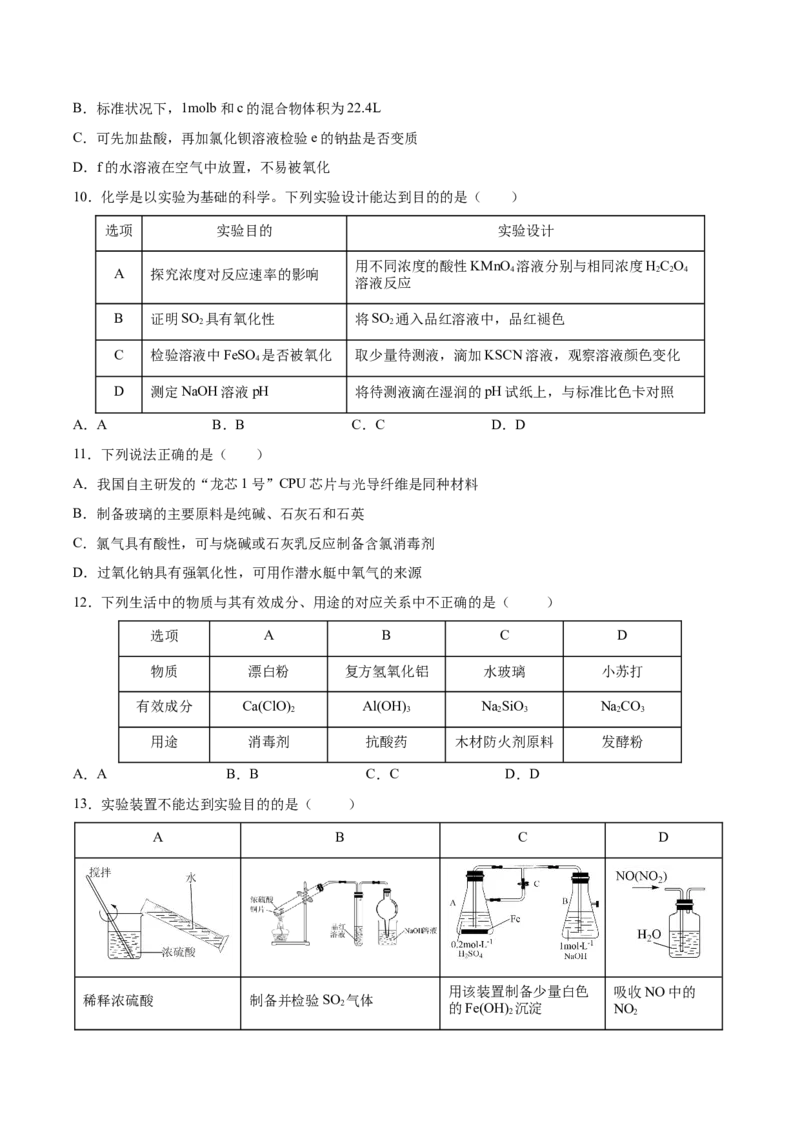
10.化学是以实验为基础的科学。下列实验设计能达到目的的是( )
选项 实验目的 实验设计
用不同浓度的酸性KMnO 溶液分别与相同浓度HC O
A 探究浓度对反应速率的影响 4 2 2 4
溶液反应
B 证明SO 具有氧化性 将SO 通入品红溶液中,品红褪色
2 2
C 检验溶液中FeSO 是否被氧化 取少量待测液,滴加KSCN溶液,观察溶液颜色变化
4
D 测定NaOH溶液pH 将待测液滴在湿润的pH试纸上,与标准比色卡对照
A.A B.B C.C D.D
11.下列说法正确的是( )
A.我国自主研发的“龙芯1号”CPU芯片与光导纤维是同种材料
B.制备玻璃的主要原料是纯碱、石灰石和石英
C.氯气具有酸性,可与烧碱或石灰乳反应制备含氯消毒剂
D.过氧化钠具有强氧化性,可用作潜水艇中氧气的来源
12.下列生活中的物质与其有效成分、用途的对应关系中不正确的是( )
选项 A B C D
物质 漂白粉 复方氢氧化铝 水玻璃 小苏打
有效成分 Ca(ClO) Al(OH) NaSiO NaCO
2 3 2 3 2 3
用途 消毒剂 抗酸药 木材防火剂原料 发酵粉
A.A B.B C.C D.D
13.实验装置不能达到实验目的的是( )
A B C D
用该装置制备少量白色 吸收NO中的
稀释浓硫酸 制备并检验SO 气体
2 的Fe(OH) 沉淀 NO
2 2A.A B.B C.C D.D
14.对下列有关事实的解释,其中错误的是 ( )
A.常温下,浓硝酸可以用铝槽贮存,说明铝与浓硝酸不能反应
B.浓硝酸在光照条件下其颜色变黄,说明浓硝酸不稳定见光容易分解
C.在蔗糖固体中加入适量浓硫酸后出现发黑现象,说明浓硫酸具有脱水性
D.反应:CuSO +HS===CuS↓+HSO 能够进行,说明硫化铜既不溶于水,也不溶于稀硫酸
4 2 2 4
15.纯二氧化硅可用下列流程制得。下列说法不正确的是( )
A.X可用作木材防火剂
B.步骤Ⅱ的反应是NaSiO+HSO =H SiO↓+NaSO
2 3 2 4 2 3 2 4
C.步骤Ⅱ中的Y生成可用SiO 与水反应代替
2
D.步骤 Ⅲ若在实验室完成,一般在坩埚中进行
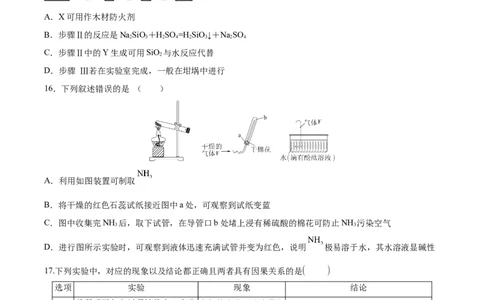
16.下列叙述错误的是 ( )
A.利用如图装置可制取
B.将干燥的红色石蕊试纸接近图中a处,可观察到试纸变蓝
C.图中收集完NH 后,取下试管,在导管口b处堵上浸有稀硫酸的棉花可防止NH 污染空气
3 3
D.进行图所示实验时,可观察到液体迅速充满试管并变为红色,说明 极易溶于水,其水溶液显碱性
17.下列实验中,对应的现象以及结论都正确且两者具有因果关系的是( )
选项 实验 现象 结论
将稀硝酸加入过量铁粉中,充分 有气体生成,溶液呈红
A 稀硝酸将Fe氧化为Fe3+
反应后滴加KSCN溶液 色
将铜粉加入1.0mol/LFe (SO ) 溶 溶液变蓝、有黑色固体
2 4 3
B 金属铁比铜活泼
液中 出现
C 向少许待测液中滴加稀盐酸 有刺激性气味气体放出 待测液中一定含有SO
NH Cl固体受热分解,产生氨气和氯化
4
D 加热盛有NH Cl固体的试管 试管底部固体消失
4
氢气体常温下重新结合成N H Cl
4
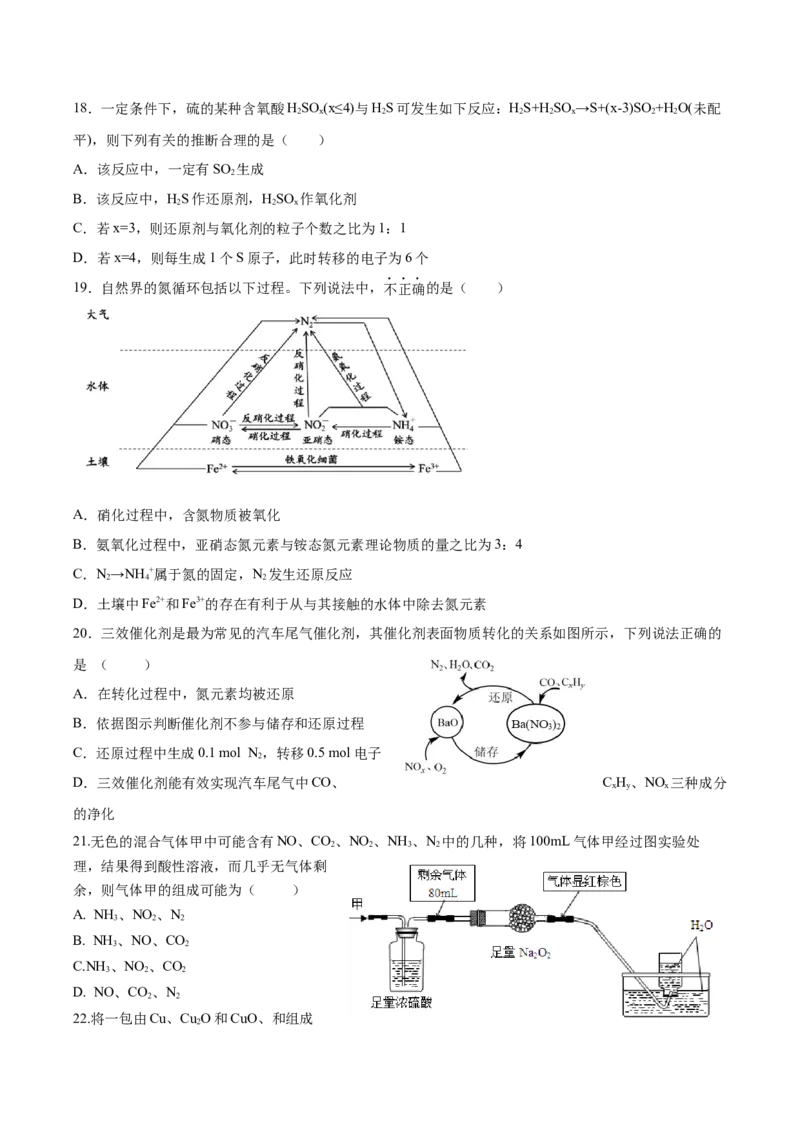
A. A B. B C. C D. D18.一定条件下,硫的某种含氧酸HSO (x≤4)与HS可发生如下反应:HS+HSO →S+(x-3)SO +H O(未配
2 x 2 2 2 x 2 2
平),则下列有关的推断合理的是( )
A.该反应中,一定有SO 生成
2
B.该反应中,HS作还原剂,HSO 作氧化剂
2 2 x
C.若x=3,则还原剂与氧化剂的粒子个数之比为1:1
D.若x=4,则每生成1个S原子,此时转移的电子为6个
19.自然界的氮循环包括以下过程。下列说法中,不正确的是( )
A.硝化过程中,含氮物质被氧化
B.氨氧化过程中,亚硝态氮元素与铵态氮元素理论物质的量之比为3:4
C.N→NH +属于氮的固定,N 发生还原反应
2 4 2
D.土壤中Fe2+和Fe3+的存在有利于从与其接触的水体中除去氮元素
20.三效催化剂是最为常见的汽车尾气催化剂,其催化剂表面物质转化的关系如图所示,下列说法正确的
是 ( )
A.在转化过程中,氮元素均被还原
B.依据图示判断催化剂不参与储存和还原过程
C.还原过程中生成0.1 mol N,转移0.5 mol电子
2
D.三效催化剂能有效实现汽车尾气中CO、 C H、NO 三种成分
x y x
的净化
21.无色的混合气体甲中可能含有NO、CO、NO 、NH 、N 中的几种,将100mL气体甲经过图实验处
2 2 3 2
理,结果得到酸性溶液,而几乎无气体剩
余,则气体甲的组成可能为( )
A. NH 、NO 、N
3 2 2
B. NH 、NO、CO
3 2
C.NH 、NO 、CO
3 2 2
D. NO、CO、N
2 2
22.将一包由Cu、Cu O和CuO、和组成
2的混合物均分成两份:一份混合物在加热条件下与H 充分反应,将固体全部转化成铜粉时固体质量减少了
2
6.4g;向另一份混合物中加入800mLHNO 溶液恰好完全反应生成Cu(NO ) 和NO(假设不产生其他还原产
3 3 2
物),这些NO和3.36LO (标准状况)混合并通入足量水中,气体全部被吸收生成HNO 。则该硝酸的物质
2 3
的量浓度为( )
A. 1.0mol/L B. 2.0mol/L C. 30mol/L D. 4.0mol/L
第 II 卷(非选择题 共 56 分)
二、非选择题:本题共5个小题,共56分。
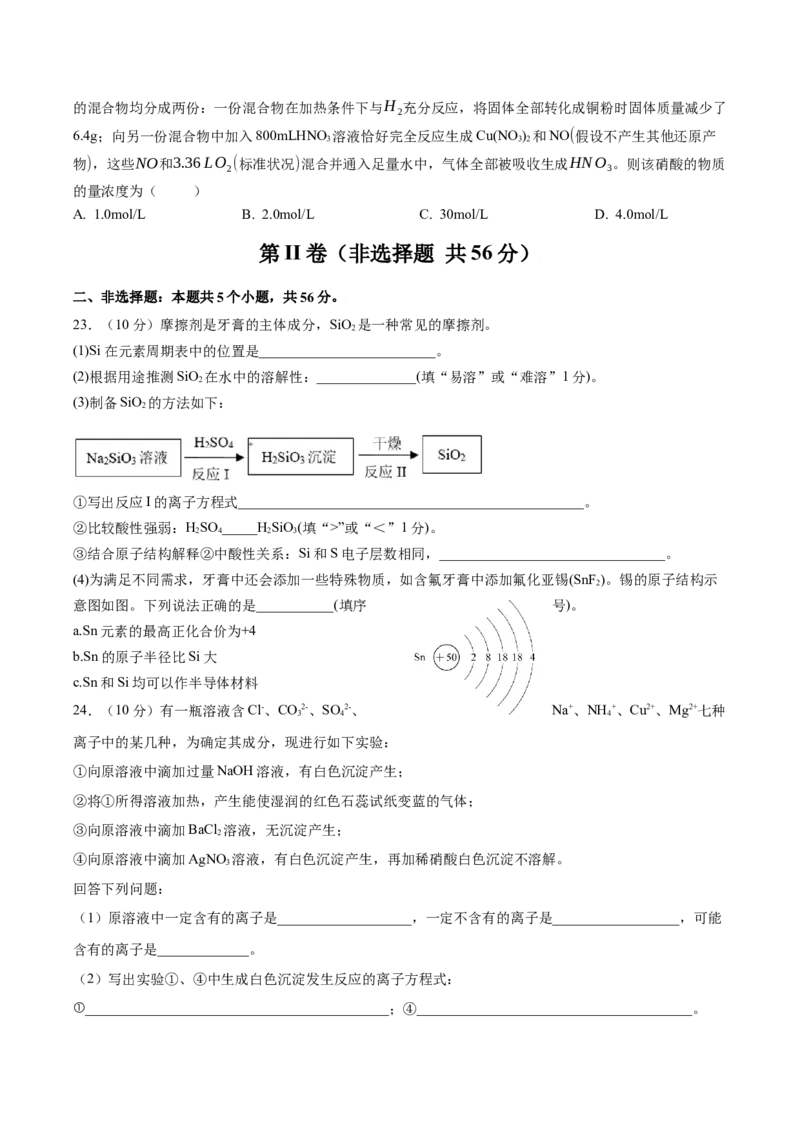
23.(10分)摩擦剂是牙膏的主体成分,SiO 是一种常见的摩擦剂。
2
(1)Si在元素周期表中的位置是_________________________。
(2)根据用途推测SiO 在水中的溶解性:______________(填“易溶”或“难溶”1分)。
2
(3)制备SiO 的方法如下:
2
①写出反应I的离子方程式_________________________________________________。
②比较酸性强弱:HSO _____HSiO(填“>”或“<”1分)。
2 4 2 3
③结合原子结构解释②中酸性关系:Si和S电子层数相同,________________________________。
(4)为满足不同需求,牙膏中还会添加一些特殊物质,如含氟牙膏中添加氟化亚锡(SnF )。锡的原子结构示
2
意图如图。下列说法正确的是___________(填序 号)。
a.Sn元素的最高正化合价为+4
b.Sn的原子半径比Si大
c.Sn和Si均可以作半导体材料
24.(10分)有一瓶溶液含Cl-、CO2-、SO 2-、 Na+、NH +、Cu2+、Mg2+七种
3 4 4
离子中的某几种,为确定其成分,现进行如下实验:
①向原溶液中滴加过量NaOH溶液,有白色沉淀产生;
②将①所得溶液加热,产生能使湿润的红色石蕊试纸变蓝的气体;
③向原溶液中滴加BaCl 溶液,无沉淀产生;
2
④向原溶液中滴加AgNO 溶液,有白色沉淀产生,再加稀硝酸白色沉淀不溶解。
3
回答下列问题:
(1)原溶液中一定含有的离子是___________________,一定不含有的离子是__________________,可能
含有的离子是_____________。
(2)写出实验①、④中生成白色沉淀发生反应的离子方程式:
①___________________________________________;④_______________________________________。(3)有同学认为实验④可以省略,你认为呢? ______________________(填“可以”或“不可以”),并
说明理由
________________________________________________________________________________________。
25.(12分)A、B、C、D均为中学化学常见的纯净物且都含有一种相同元素,A是单质,B是A的氧化
物。它们有如图反应关系:
(1)若B是淡黄色固体,②③的反应中均有一种相同的反应物且摩尔质
量为18g/mol,D俗称小苏打。则C的化学式为___________,写出物质B
与 反应的化学方程式________________________________,由D和澄清石灰水可得到C,写出该反应
的离子方程式_______________________________________。
(2)若B是制作光导纤维的材料,②③的反应物中均有烧碱,D为酸。用氧化物表示C的组成
___________,反应①②③④⑤中,属于氧化还原反应的有___________(填序号),写出D转化为C的离子
方程式________________________________________________。
(3)若B是红棕色固体,反应③在盐酸中完成,则反应②中加入物质的化学式为___________;若C、D
组成元素相同,则C转化为D的离子方程式为__________________________________,在D中滴入氢氧化
钠溶液,一段时间内观察到的现象是_________________________________________。
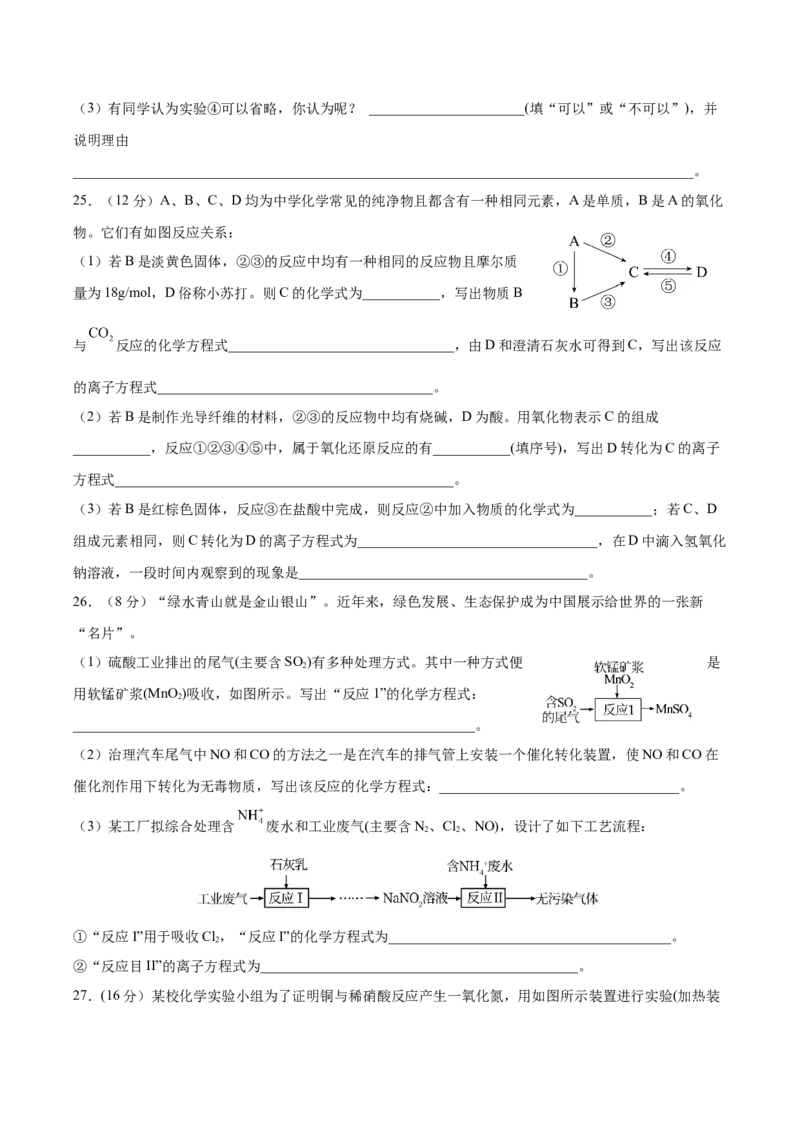
26.(8分)“绿水青山就是金山银山”。近年来,绿色发展、生态保护成为中国展示给世界的一张新
“名片”。
(1)硫酸工业排出的尾气(主要含SO )有多种处理方式。其中一种方式便 是
2
用软锰矿浆(MnO )吸收,如图所示。写出“反应1”的化学方程式:
2
_________________________________________________________。
(2)治理汽车尾气中NO和CO的方法之一是在汽车的排气管上安装一个催化转化装置,使NO和CO在
催化剂作用下转化为无毒物质,写出该反应的化学方程式:__________________________________。
(3)某工厂拟综合处理含 废水和工业废气(主要含N、Cl、NO),设计了如下工艺流程:
2 2
①“反应I”用于吸收Cl,“反应I”的化学方程式为________________________________________。
2
②“反应目II”的离子方程式为_____________________________________________。
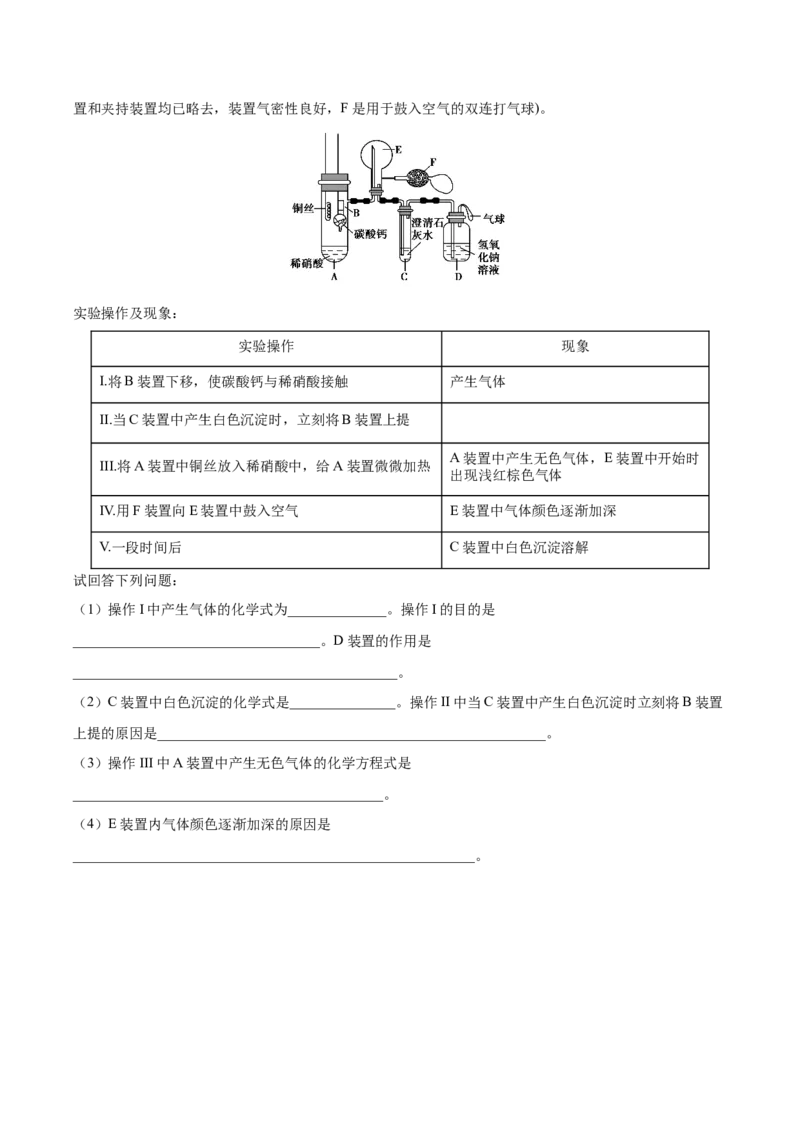
27.(16分)某校化学实验小组为了证明铜与稀硝酸反应产生一氧化氮,用如图所示装置进行实验(加热装置和夹持装置均已略去,装置气密性良好,F是用于鼓入空气的双连打气球)。
实验操作及现象:
实验操作 现象
I.将B装置下移,使碳酸钙与稀硝酸接触 产生气体
II.当C装置中产生白色沉淀时,立刻将B装置上提
A装置中产生无色气体,E装置中开始时
III.将A装置中铜丝放入稀硝酸中,给A装置微微加热
出现浅红棕色气体
IV.用F装置向E装置中鼓入空气 E装置中气体颜色逐渐加深
V.一段时间后 C装置中白色沉淀溶解
试回答下列问题:
(1)操作I中产生气体的化学式为______________。操作I的目的是
___________________________________。D装置的作用是
______________________________________________。
(2)C装置中白色沉淀的化学式是_______________。操作II中当C装置中产生白色沉淀时立刻将B装置
上提的原因是_______________________________________________________。
(3)操作III中A装置中产生无色气体的化学方程式是
____________________________________________。
(4)E装置内气体颜色逐渐加深的原因是
_________________________________________________________。