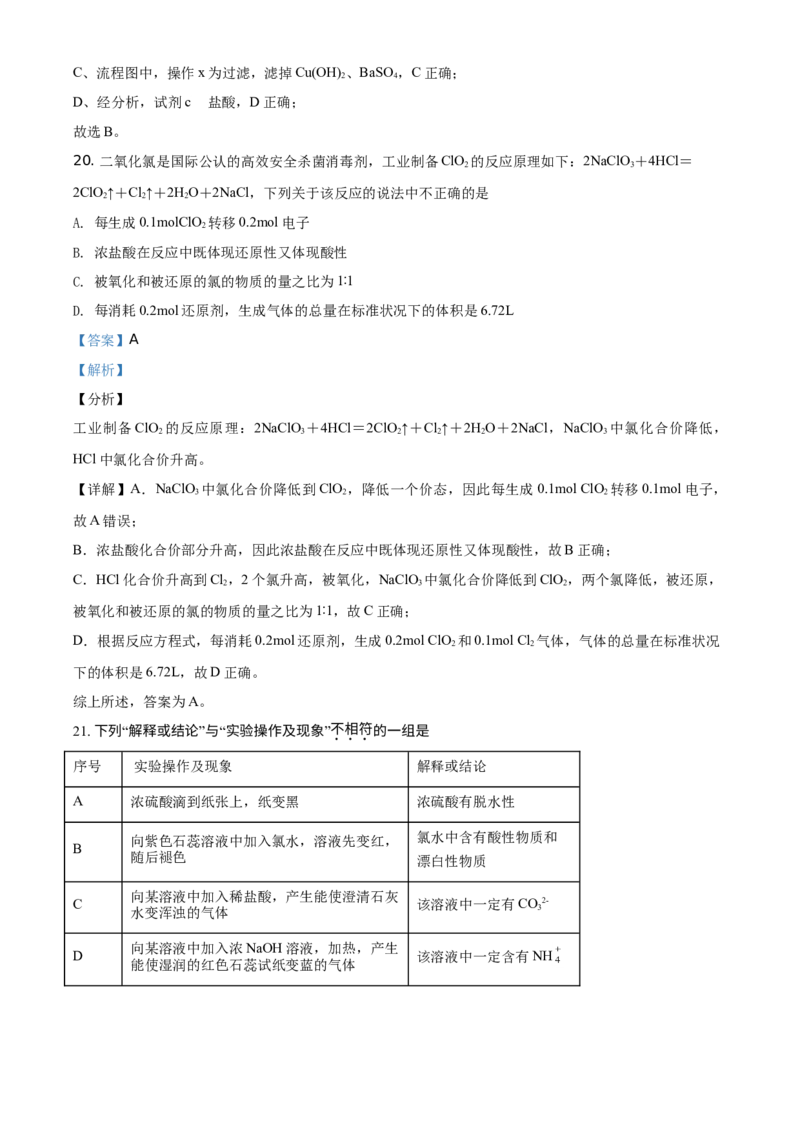文档内容
人大附中朝阳学校 2019~2020 年度第二学期高一年级阶段练习
化学试题(选考班)
考生须知:
1.本试卷分为Ⅰ、Ⅱ两卷,共有26题,考试时间为90分钟,满分为100分。
2.第Ⅱ卷各题均须用黑色签字笔按规定要求在答题纸上作答。
3.请将个人信息完整填写在密封线内。
4.客观题用手机登陆网页,对应输入选项(题号选项要对应);主观题拍照,上传照片(拍照时
务必保证手机竖立并与试卷平行且为同一方向)。
可能用到的相对原子质量:H-1 N-14 O-16 Na-23 Si-28 S-32 Fe-56 Cu-64
第Ⅰ卷 (共42分)
一、选择题(本题包括21小题,每小题2分,共42分。每小题只有一个选项符合题意。网上
作答)
1. 下列设备工作时,将化学能转化为电能的是
A B C D
铅蓄电池 硅太阳能电池 燃气灶 电烤箱
A. A B. B C. C D. D
【答案】A
【解析】
【详解】A.铅蓄电池放电时是原电池,可以把化学能转化为电能,故A正确;
B.硅太阳能电池是将光能转化为电能的装置,故B错误;
C.燃气灶为化学能转化为热能的装置,故C错误;
D.电烤箱是电能转化为热能的装置,故D错误;
故选A。
2. 下列物质属于电解质的是
A. Zn B. NaOH C. HSO 溶液 D. MgCl 溶液
2 4 2【答案】B
【解析】
【分析】
在水中或者熔融状态下能电离的化合物是电解质。
【详解】A、Zn是单质,不属于电解质的研究范畴,A错误;
B、NaOH在水中或者熔融状态下可以电离,该物质是电解质,B正确;
C、HSO 溶液是混合物,不属于电解质的研究范畴,C错误;
2 4
D、MgCl 溶液是混合物,不属于电解质的研究范畴,D错误;
2
故选B。
【点睛】根据定义,电解质和非电解质的研究对象都是化合物,故单质和溶液都不属于电解质和非电解质
的研究范畴。
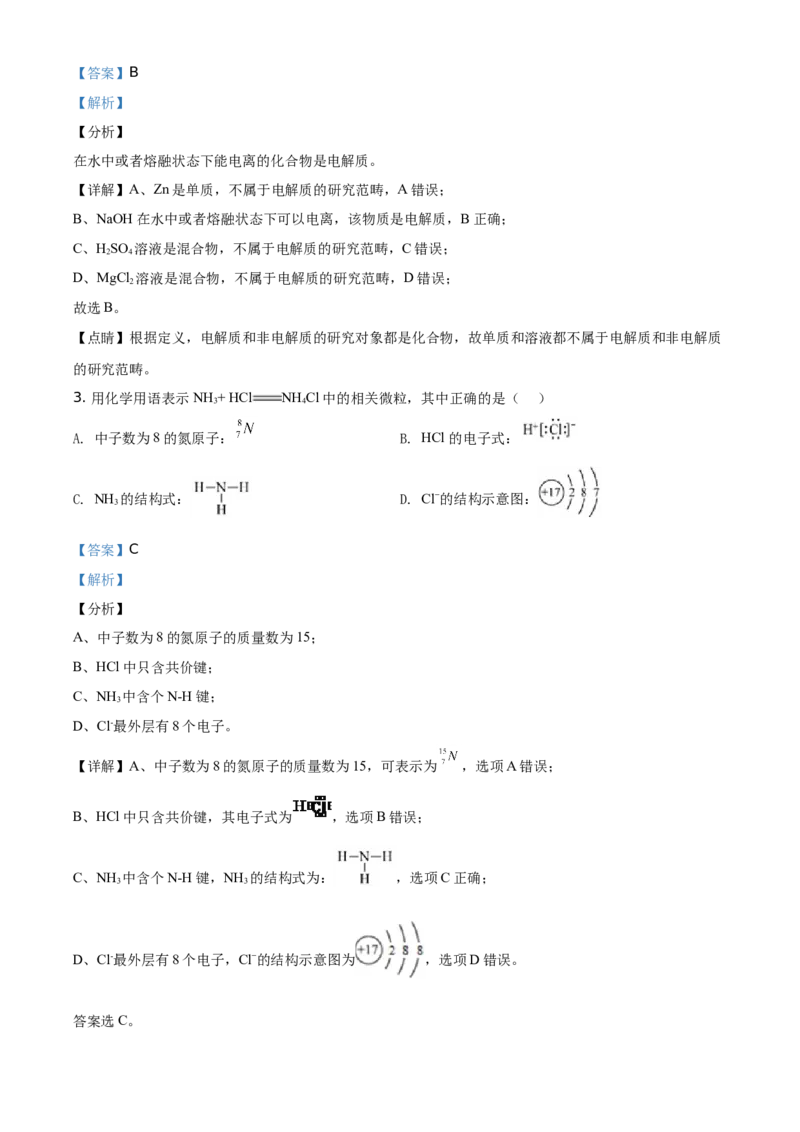
3. 用化学用语表示 NH + HCl NH Cl中的相关微粒,其中正确的是( )
3 4
A. 中子数为8的氮原子: B. HCl 的电子式:
C. NH 的结构式: D. Cl−的结构示意图:
3
【答案】C
【解析】
【分析】
A、中子数为8的氮原子的质量数为15;
B、HCl中只含共价键;
C、NH 中含个N-H键;
3
D、Cl-最外层有8个电子。
【详解】A、中子数为8的氮原子的质量数为15,可表示为 ,选项A错误;
B、HCl中只含共价键,其电子式为 ,选项B错误;
C、NH 中含个N-H键,NH 的结构式为: ,选项C正确;
3 3
D、Cl-最外层有8个电子,Cl−的结构示意图为 ,选项D错误。
答案选C。【点睛】本题考查化学用语,侧重考查原子结构、离子结构示意图、电子式和结构式,注意它们之间的区
别是解题的关键,如原子结构示意图与离子结构示意图的区别、共价化合物和离子化合物的区别、电子式
与结构式的区别等。
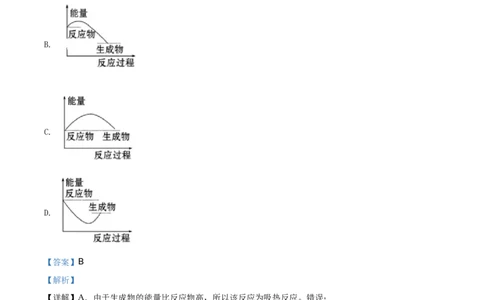
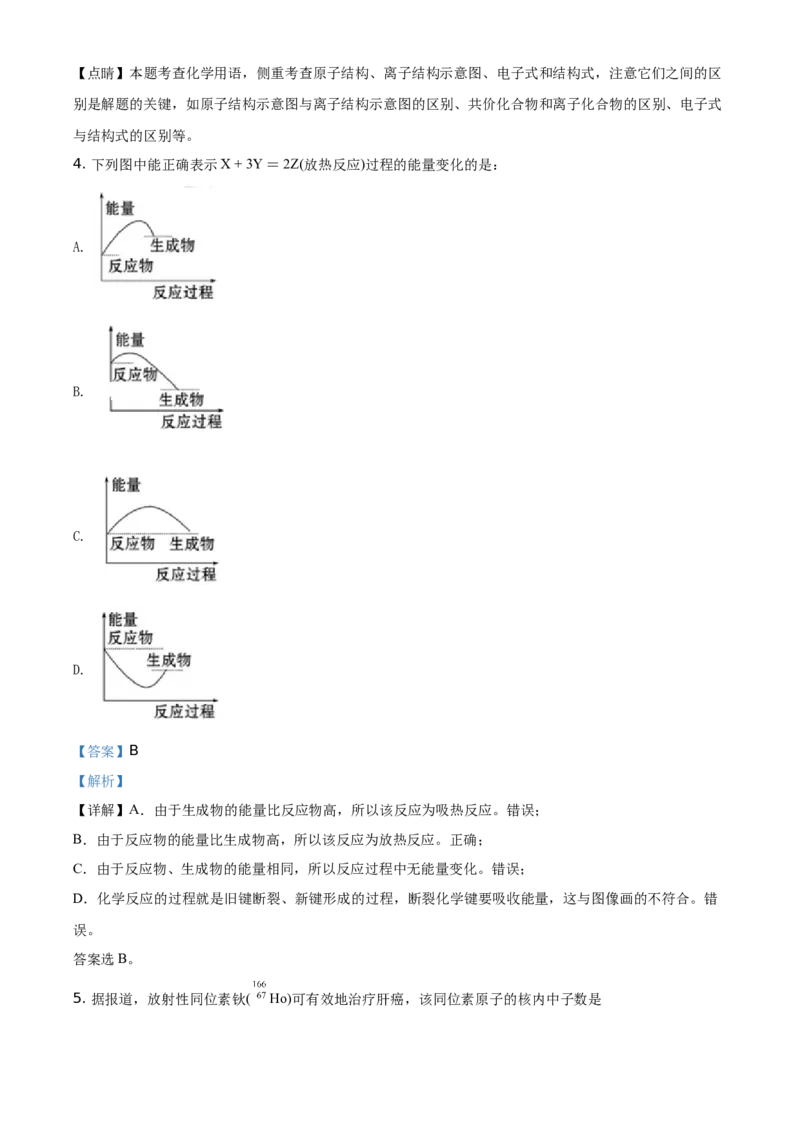
4. 下列图中能正确表示X + 3Y = 2Z(放热反应)过程的能量变化的是:
A.
B.
C.
D.
【答案】B
【解析】
【详解】A.由于生成物的能量比反应物高,所以该反应为吸热反应。错误;
B.由于反应物的能量比生成物高,所以该反应为放热反应。正确;
C.由于反应物、生成物的能量相同,所以反应过程中无能量变化。错误;
D.化学反应的过程就是旧键断裂、新键形成的过程,断裂化学键要吸收能量,这与图像画的不符合。错
误。
答案选B。
5. 据报道,放射性同位素钬( Ho)可有效地治疗肝癌,该同位素原子的核内中子数是A. 166 B. 67 C. 99 D. 32
【答案】C
【解析】
【详解】中子数=质量数-质子数=166-67=99,故C符合题意。
综上所述,答案为C。
6. 下列变化过程不涉及氧化还原反应的是
A B C D
将铁片放入冷 向 FeCl 溶液中滴加 KSCN 向 NaSO 固体 向包有 NaO 粉末的
2 2 3 2 2
的浓硫酸中无 溶液,不变色,滴加氯水 中加入硫酸, 脱脂棉上滴几滴蒸馏
明显现象 后溶液显红色 生成无色气体 水,脱脂棉燃烧
.
A A B. B C. C D. D
【答案】C
【解析】
【详解】A. 铁遇冷的浓硫酸发生钝化,铁被氧化生成致密的氧化层薄膜,属于氧化还原反应,故A错误;
B. 向 FeCl 溶液中滴加 KSCN溶液,溶液不变色,滴加氯水后,氯化亚铁被氯气氧化生成氯化铁,氯化铁
2
与硫氰化钾溶液反应,溶液显红色,属于氧化还原反应,故B错误;
C.亚硫酸钠与硫酸发生复分解反应生成硫酸钠、二氧化硫和水,反应前后没有化合价改变,不属于氧化还
原反应,故C正确;
D.过氧化钠与水反应生成氢氧化钠和氧气,反应放出大量的热,放出的热量使氧气和脱脂棉反应,使脱脂
棉燃烧,属于氧化还原反应,故D错误;
故选C。
【点睛】氧化还原反应的特征是元素化合价的升降,结合反应的特点以及元素化合价的角度判断反应是否
为氧化还原反应是解答关键。
7. 下列说法中,正确的是
A. 0.5 mol∙L−1NaCl溶液中含有0.5molNa+
B. 1molCl 中含有的氯原子数约为6.02×1023
2
C. 36gHO的物质的量为2mol
2
D. 常温常压下,1molN 的体积是22.4L
2
【答案】C
【解析】
【详解】A.0.5 mol∙L−1NaCl溶液,无溶液体积,无法计算物质的量,故A错误;B.1mol Cl 中含有的氯原子物质的量为2mol,氯原子数为2N ,约为1.204×1024,故B错误;
2 A
C.36gHO的物质的量 ,故C正确;
2
D.常温常压下,气体摩尔体积是24.5 L∙mol −1,因此1mol N 的体积是24.5L,故D错误。
2
综上所述,答案为C。
8. 能正确表示下列反应的离子方程式是
A. 稀硫酸滴在铜片上:Cu+2H+=Cu2++H ↑
2
B. 澄清石灰水与稀盐酸反应:Ca(OH) +2H+=Ca2++2H O
2 2
C. 碳酸钡溶于稀盐酸中: +2H+=HO+CO↑
2 2
D. 氧化铁与稀盐酸混合:Fe O+6H+=2Fe3++3H O
2 3 2
【答案】D
【解析】
【详解】A.稀硫酸滴在铜片上,铜与稀硫酸不反应,故A错误;
B.澄清石灰水与稀盐酸反应:OH-+H+=HO,故B错误;
2
C.碳酸钡溶于稀盐酸中:BaCO +2H+=HO+CO↑+Ba2+,故C错误;
3 2 2
D.氧化铁与稀盐酸混合:Fe O+6H+=2Fe3++3HO,故D正确。
2 3 2
答案为D。
9. 关于下图装置的叙述,正确的是( )
A. 铜是负极,铜片上有气泡产生
B. 铜片质量逐渐减少
C. 电流从锌片经导线流向铜片
D. 氢离子在铜片表面被还原后生成H
2
【答案】D
【解析】
【分析】
根据题中装置图可知,本题考查原电池的工作原理,运用原电池的工作原理分析。
【详解】A. Cu−Zn−稀硫酸原电池放电时,较活泼的金属锌作负极,故A错误;
B. Cu−Zn−稀硫酸原电池放电时,较活泼的金属锌作负极,铜作正极,氢离子从铜片获得电子被还原成氢气,铜片质量不变,故B错误;
C. 原电池放电时,电流从正极铜沿导线流向负极锌,故C错误;
D. Cu−Zn−稀硫酸原电池放电时,较活泼的金属锌作负极,铜作正极,氢离子从铜片获得电子被还原成氢
气,故D正确;
。
答案选D
10. 下列有关性质的比较,不能用元素周期律解释的是
A. 酸性;H SO >H PO
2 4 3 4
B. 非金属性:Cl>Br
.
C 碱性:NaOH>Mg(OH)
2
D. 热稳定性:NaCO>NaHCO
2 3 3
【答案】D
【解析】
【详解】A. 元素的非金属性越强,对应的最高价氧化物的水化物的酸性越强,非金属性:S>P,则酸性:
HSO >H PO ,能用元素周期律解释,故A错误;
2 4 3 4
B. 同主族元素从上到下非金属性依次减弱,则非金属性:Cl>Br,能用元素周期律解释,故B错误;
C. 元素的金属性越强,对应的最高价氧化物的水化物的碱性越强,金属性:Na>Mg,则碱性:
NaOH>Mg(OH) ,能用元素周期律解释,故C错误;
2
D. 碳酸氢盐易分解,碳酸盐难分解,所以热稳定性:NaCO>NaHCO,不能用元素周期律解释,故D正
2 3 3
确。
故答案选:D。
11. 下列各组离子在给定条件的溶液中不能大量共存的是
A. 使酚酞溶液变红的溶液:Na+、Cl-、
B. 无色透明溶液中K+、 、H+
C. 可与铝反应放出氢气的溶液中:Fe3+、Cl-、
D. 使pH试纸变蓝的溶液中:Ba2+、Na+、Cl-
【答案】C
【解析】
【详解】A.使酚酞溶液变红的溶液,说明溶液显碱性,OH-、Na+、Cl-、 都大量共存,故A不符
合题意;B.无色透明溶液中K+、 、H+都大量共存,故B不符合题意;
C.可与铝反应放出氢气的溶液,可能为酸性,可能为碱性,Fe3+与OH-反应,不共存,H+与 反应,
不共存,故C符合题意;
D.使pH试纸变蓝的溶液,说明溶液显碱性,OH-、Ba2+、Na+、Cl-都大量共存,故D不符合题意。
综上所述,答案为C。
12. 以不同类别物质间的转化为线索,认识钠及其化合物。
下列分析不正确的是
A. 反应③表明CO 具有酸性氧化物的性质
2
B. 反应④说明NaHCO 的稳定性强于NaCO
3 2 3
C. 反应⑤、⑥可用于潜水艇中氧气的供给
D. 上述转化中发生的反应有分解反应、化合反应、置换反应
【答案】B
【解析】
【详解】A. 反应③发生2NaOH+CO=Na CO +HO,NaOH为碱,NaCO 为盐,因此CO 具有酸性氧化
2 2 3 2 2 3 2
物的性质,故A说法正确;
B. 反应④是2NaHCO NaCO+CO↑+HO,说明NaCO 比NaHCO 稳定,故B说法错误;
3 2 3 2 2 2 3 3
C. 反应⑤⑥分别是2NaO+2HO=4NaOH+O↑、2NaO+2CO=2Na CO+O,因此反应⑤⑥可用于潜
2 2 2 2 2 2 2 2 3 2
水艇中氧气的供给,故C说法正确;
D. 反应④为分解反应,反应①为化合反应,反应②为置换反应,故D说法正确;
答案为B。
13. 2019年是元素周期表发表150周年,期间科学家为完善周期表做出了不懈努力。中国科学院院士张青
莲教授曾主持测定了铟( In)等9种元素相对原子质量的新值,被采用为国际新标准。铟与铷( Rb)同
49 37
周期。下列说法不正确的是
A. In是第五周期第ⅢA族元素
B. 115 In 的中子数与电子数的差值为17
49
C. 原子半径:In>AlD. 碱性:In(OH) >RbOH
3
【答案】D
【解析】
【分析】
A.根据原子核外电子排布规则,该原子结构示意图为 ,据此判断该元素在周期表中的位
置;
B.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数,原子的质子数=电子数;
C.同主族元素的原子,从上到下,电子层数逐渐增多,半径逐渐增大;
D.同周期元素,核电荷数越大,金属性越越弱,最高价氧化物对应水化物的碱性越弱;
【详解】A.根据原子核外电子排布规则,该原子结构示意图为 ,因此In位于元素周期表
第五周期第IIIA族,故A不符合题意;
B.质量数=质子数+中子数,元素符号的左上角为质量数、左下角为质子数,因此该原子的质子数=电子数
=49,中子数为115-49=66,所以中子数与电子数之差为66-49=17,故B不符合题意;
C.Al位于元素周期表的三周期IIIA族,In位于元素周期表第五周期IIIA族,同主族元素的原子,从上到下,
电子层数逐渐增多,半径逐渐增大,因此原子半径In>Al,故C不符合题意;
D.In位于元素周期表第五周期,铷(Rb)位于元素周期表第五周期第IA族,同周期元素,核电荷数越大,
金属性越越弱,最高价氧化物对应水化物的碱性越弱,因此碱性:In(OH) <RbOH,故D符合题意;
3
综上所述,本题应选D。
【点睛】本题考查原子结构与元素性质,题目难度不大,明确原子结构与元素周期律的关系为解答关键,
注意掌握原子构成及表示方法,试题培养了学生的分析能力及灵活应用能力。
14. 一个原电池的总反应的离子方程式是:Zn+Cu2+=Zn2++Cu,该反应的原电池的正确组成是
正极 负极 电解质溶液
A Zn Cu CuCl
2B Zn Cu ZnCl
2
C Cu Zn CuSO
4
D Cu Zn ZnSO
4
A. A B. B C. C D. D
【答案】C
【解析】
【详解】根据反应:Zn+Cu2+=Zn2++Cu知,锌失电子,发生氧化反应,作原电池的负极,电极反应式为
Zn-2e-==Zn2+;铜离子得电子发生还原反应,在原电池的正极发生反应,电极反应式为Cu2++2e-==Cu,电解
质溶液中含有铜离子;故答案选C。
15. 短周期元素W、X、Y、Z的原子序数依次增大。W的气态氢化物遇湿润的红色石蕊试纸变蓝色,X是
地壳中含量最高的元素,Y在同周期主族元素中原子半径最大,Z与Y形成的化合物的化学式为YZ。下列
说法不正确的是()
A. W在元素周期表中的位置是第二周期第VA族
B. 同主族中Z的气态氢化物稳定性最强
C. X与Y形成的两种常见的化合物中,阳离子和阴离子的个数比均为2∶1
D. 用电子式表示YZ的形成过程为:
【答案】B
【解析】
【分析】
短周期元素W、X、Y、Z 的原子序数依次增大。W 的气态氢化物遇湿润的红色石蕊试纸变蓝色,说明该
氢化物溶于水后显碱性,故该氢化物为氨气,则W为N元素;X 是地壳中含量最高的元素,则X为O元
素;Y 在同周期主族元素中原子半径最大,说明Y在第IA族,其原子序数大于O,则Y为Na元素;Z 与
Y 形成的化合物的化学式为YZ,Y为Na元素,化合价为+1价,则Z为-1价,所以Z为Cl元素,据此分
析解答。
【详解】根据以上分析可知,短周期元素W、X、Y、Z分别为N、O、Na、Cl四种元素。
A.N的原子序数为7,有两个电子层,最外层有5个电子,位于元素周期表第二周期第VA族,A正确;
B.Cl位于第VIIA族,非金属性F>Cl,则气态氢化物稳定性HF>HCl,B错误;
C.X 与Y 分别是O、Na, 形成的化合物为NaO和NaO,二者都是离子化合物,阳离子都是钠离子
2 2 2
(Na+),阴离子分别是氧离子(O2-)和过氧根离子(O 2-),则NaO和NaO 中阳离子和阴离子的个数比均为
2 2 2 22∶1,C正确;
D.YZ为NaCl,属于离子化合物,阴阳离子之间以离子键构成化合物,用电子式表示形成过程为:
,D正确。
答案选B。
【点睛】本题考查原子结构与元素周期律的应用,解答关键是推断元素,注意掌握元素周期律内容以及元
素周期表的结构,另外对常见元素及物质的特殊性质要有准确的记忆。
16. 对于反应A+3B=2C+2D,下列数据表示不同条件的反应速率,其中反应进行得最快的是
A. υ(A)=0.15mol/(L·s) B. υ(B)=0.3mol/(L·s)
C. υ(C)=0.2mol/(L·s) D. υ(D)=2mol/(L·min)
【答案】A
【解析】
【详解】A.υ(A)=0.15mol/(L·s),转化成B的速率υ(B)= 3υ(A)=3×0.15mol/(L·s)=0.45 mol/(L·s);
B.υ(B)=0.3mol/(L·s);
C.υ(C)=0.2mol/(L·s),转化成B的速率υ(B)=1.5υ(C)=1.5×0.2mol/(L·s)=0.3 mol/(L·s);
D.υ(D)=2mol/(L·min) = mol/(L·min)= mol/(L·min),转化成B的速率υ(B)=1.5υ(D)=1.5×
mol/(L·s)=0.05 mol/(L·s);
根据上述数据可知,反应进行最快的是υ(B)= 0.45 mol/(L·s),故A符合题意。
答案为A。
17. 已知断裂1molH—H键吸收的能量为436kJ,断裂1molH—N键吸收的能量为391kJ,根据化学方程式:
N(g)+3H(g)⇌2NH (g),生成2molNH (g)放出热量为92.4kJ,则断裂1molN≡N键吸收的能量是
2 2 3 3
A. 431kJ B. 945.6kJ C. 649kJ D. 869kJ
【答案】B
【解析】
【详解】断裂1molH—H键吸收的能量为436kJ,断裂1molH—N键吸收的能量为391kJ,根据化学方程式:
N(g)+3H(g)⇌2NH (g),生成2molNH (g)放出热量为92.4kJ,说明反应是放热,成键放出的热量大于断键
2 2 3 3
吸收的热量,设断裂 1molN≡N 键吸收的能量是 akJ,则有 391kJ×6-436kJ×3-a kJ=92.4kJ,解得 a
=945.6kJ,故B符合题意。
综上所述,答案为B。18. 汽车的启动电源常用铅蓄电池,放电时的电池反应:PbO +Pb+2H SO 2PbSO +2H O,根据此反应
2 2 4 4 2
判断下列叙述中正确的是
A. PbO 是电池的负极 B. 电子从Pb极流出
2
C. PbO 得电子,被氧化 D. 电池放电时,溶液酸性增强
2
【答案】B
【解析】
【详解】A.PbO 中Pb化合价降低,得到电子,是原电池的正极,故A错误;
2
B.Pb化合价升高,失去电子,是原电池负极,PbO 中Pb化合价降低,得到电子,是原电池正极,电子
2
从负极即Pb极流出,流入到正极即PbO 极,故B正确;
2
C.PbO 中Pb化合价降低,得到电子,被还原,故C错误;
2
D.根据总反应PbO +Pb+2H SO 2PbSO +2H O,电池放电时,硫酸不断消耗,因此溶液酸性减弱,故
2 2 4 4 2
D错误。
综上所述,答案为B。
19. 某工业废水中存在大量的Na+、Cl-、Cu2+、SO 2-,欲除去其中的Cu2+、SO 2-,设计工艺流程如图所示:
4 4
下列说法不正确的是
A. NaOH的作用是除去Cu2+ B. 试剂a 为NaCO,试剂b为BaCl
2 3 2
C. 流程图中,操作x为过滤 D. 试剂c为盐酸
【答案】B
【解析】
【分析】
加入NaOH后,废水中含有Na+、Cl-、OH-、SO 2-;再加入试剂a BaCl 除去SO 2-,此时废水中含有Na+、
4 2 4
Cl-、Ba2+;再加入稍过量的试剂b Na CO 除去Ba2+,此时废水中含有Na+、Cl-、CO2-;再加入试剂c盐酸,
2 3 3
至不再产生气泡即可。
【详解】A、废水中,只有Cu2+可以和NaOH反应,故NaOH的作用是除去Cu2+,A正确;
B、经分析,试剂a为BaCl ,试剂b为NaCO,B错误;
2 2 3C、流程图中,操作x为过滤,滤掉Cu(OH) 、BaSO,C正确;
2 4
D、经分析,试剂c 为盐酸,D正确;
故选B。
20. 二氧化氯是国际公认的高效安全杀菌消毒剂,工业制备ClO 的反应原理如下:2NaClO+4HCl=
2 3
2ClO ↑+Cl↑+2HO+2NaCl,下列关于该反应的说法中不正确的是
2 2 2
A. 每生成0.1molClO 转移0.2mol电子
2
B. 浓盐酸在反应中既体现还原性又体现酸性
C. 被氧化和被还原的氯的物质的量之比为1∶1
D. 每消耗0.2mol还原剂,生成气体的总量在标准状况下的体积是6.72L
【答案】A
【解析】
【分析】
工业制备ClO 的反应原理:2NaClO +4HCl=2ClO ↑+Cl↑+2HO+2NaCl,NaClO 中氯化合价降低,
2 3 2 2 2 3
HCl中氯化合价升高。
【详解】A.NaClO 中氯化合价降低到ClO ,降低一个价态,因此每生成0.1mol ClO 转移0.1mol电子,
3 2 2
故A错误;
B.浓盐酸化合价部分升高,因此浓盐酸在反应中既体现还原性又体现酸性,故B正确;
C.HCl化合价升高到Cl,2个氯升高,被氧化,NaClO 中氯化合价降低到ClO ,两个氯降低,被还原,
2 3 2
被氧化和被还原的氯的物质的量之比为1∶1,故C正确;
D.根据反应方程式,每消耗0.2mol还原剂,生成0.2mol ClO 和0.1mol Cl 气体,气体的总量在标准状况
2 2
下的体积是6.72L,故D正确。
综上所述,答案为A。
21. 下列“解释或结论”与“实验操作及现象”不相符的一组是
序号 实验操作及现象 解释或结论
A 浓硫酸滴到纸张上,纸变黑 浓硫酸有脱水性
向紫色石蕊溶液中加入氯水,溶液先变红, 氯水中含有酸性物质和
B
随后褪色 漂白性物质
向某溶液中加入稀盐酸,产生能使澄清石灰
C 该溶液中一定有CO2-
水变浑浊的气体 3
向某溶液中加入浓NaOH溶液,加热,产生
D 该溶液中一定含有NH
能使湿润的红色石蕊试纸变蓝的气体A. A B. B C. C D. D
【答案】C
【解析】
【详解】A、浓硫酸具有强脱水性,遇到有机物后,“强行”以HO的形式脱去有机物中的H、O元素,从
2
而使有机物碳化变黑,A正确;
B、氯水中含有HCl和HClO,HCl使石蕊变红,HClO再氧化石蕊成无色物质,氯水的酸性主要靠HCl体
现,漂白性靠HClO体现,B正确;
C、能使澄清石灰水变浑浊的气体不一定是CO,还可能是SO ,故该溶液中的离子可能是CO2-、HCO -、
2 2 3 3
SO 2-、HSO -中的一种或者几种,C错误;
3 3
D、能使湿润的红色石蕊试纸变蓝的气体是NH ,NH +和强碱溶液在加热的条件下,可以反应产生NH ,D
3 4 3
正确;
故选C。
【点睛】能使澄清石灰水变浑浊的气体,一般认为是CO,和酸反应产生CO 的离子有CO2-、HCO -,在
2 2 3 3
分析时,这两种离子都要考虑到;此外,SO 也能使澄清石灰水变浑浊,故若题中没有说明,也要考虑到
2
SO ,相应的,和酸反应产生SO 的离子有SO 2-、HSO -。
2 2 3 3
第Ⅱ卷 (非选择题部分共58分)
二、填空题(本题包括5小题)
22. 四种常见的短周期非金属元素在周期表中的相对位置如图所示,其中乙元素原子核外最外层电子数是
其电子层数的3倍。
甲 乙
丙 丁
请用化学用语回答:
(1)丙在元素周期表中的位置是______。
(2)丁单质的电子式是______(用化学用语回答,下同)
(3)乙的两种常见单质分别是______。
(4)甲、丙、丁的气态氢化物水溶液显酸性的是______。
(5)氢元素与甲和丁可以组成一种既有离子键、又有共价键的化合物,其化学式是______。
(6)已知丁的非金属性比丙强,原因是______(从原子结构角度解释)。【答案】 (1). 第三周期第VIA族 (2). (3). O 、O (4). HS,HCl (5). NH NO
2 3 2 4 3
(6). S原子最外层有6个电子,Cl原子最外层有7个电子,Cl比S易得到电子,因此Cl非金属比S强
【解析】
【分析】
乙元素原子核外最外层电子数是其电子层数的3倍,则乙为O,甲为N,丙为S,丁为Cl。
【详解】(1)丙在元素周期表中的位置是第三周期第VIA族;故答案为:第三周期第VIA族。
(2)丁单质是氯气,其电子式是: ;故答案为: 。
(3)乙的两种常见单质分别是O、O;故答案为:O、O。
2 3 2 3
(4)甲的气态氢化物为NH ,水溶液显碱性,丙的气态氢化物HS,水溶液显酸性,丁的气态氢化物HCl,
3 2
水溶液显酸性,因此气态氢化物水溶液显酸性的是HS,HCl;故答案为:HS,HCl。
2 2
(5)氢元素与甲和丁可以组成一种既有离子键、又有共价键的化合物,则为铵盐,其化学式是NH NO ;故
4 3
答案为:NH NO 。
4 3
(6)已知丁的非金属性比丙强,原因是S原子最外层有6个电子,Cl原子最外层有7个电子,Cl比S易得到
电子,因此Cl非金属比S强;故答案为:S原子最外层有6个电子,Cl原子最外层有7个电子,Cl比S易
得到电子,因此Cl非金属比S强。
【点睛】非金属元素能形成离子化合物一般是铵盐,两种非金属元素形成的离子化合物则为NH H,气态
4
氢化物水溶液显碱性的为NH 。
3
23. 人类农业生产离不开氮肥,科学合理使用氮肥,不仅能提高化肥的使用率,而且能够更好地保护环境,
请回答下列问题:
(1)将N 转化为含氮化合物的过程称为固氮
2
① 人工固氮,将N→NH , N 发生_________反应
2 3 2
② 自然界固氮,可将少量N 转化为Ca(NO ) 等氮肥,转化途径如下(转化所需试剂及条件已略去):
2 3 2
N NO NO HNO Ca(NO ) 写出NO→NO →HNO 的化学方程式__________、__________。将
2 2 3 3 2。 2 3
→ → →
HNO 转化为Ca(NO ),列举三种不同类别的化合物M_______(写化学式)。
3 3 2
(2)科学合理地保存、施用氮肥
① NHHCO 需阴凉处保存,原因是__________(写化学方程式)。
4 3
② 铵态氮肥不能与碱性肥料混合使用,以NH Cl为例写出发生反应的离子方程式________。
4
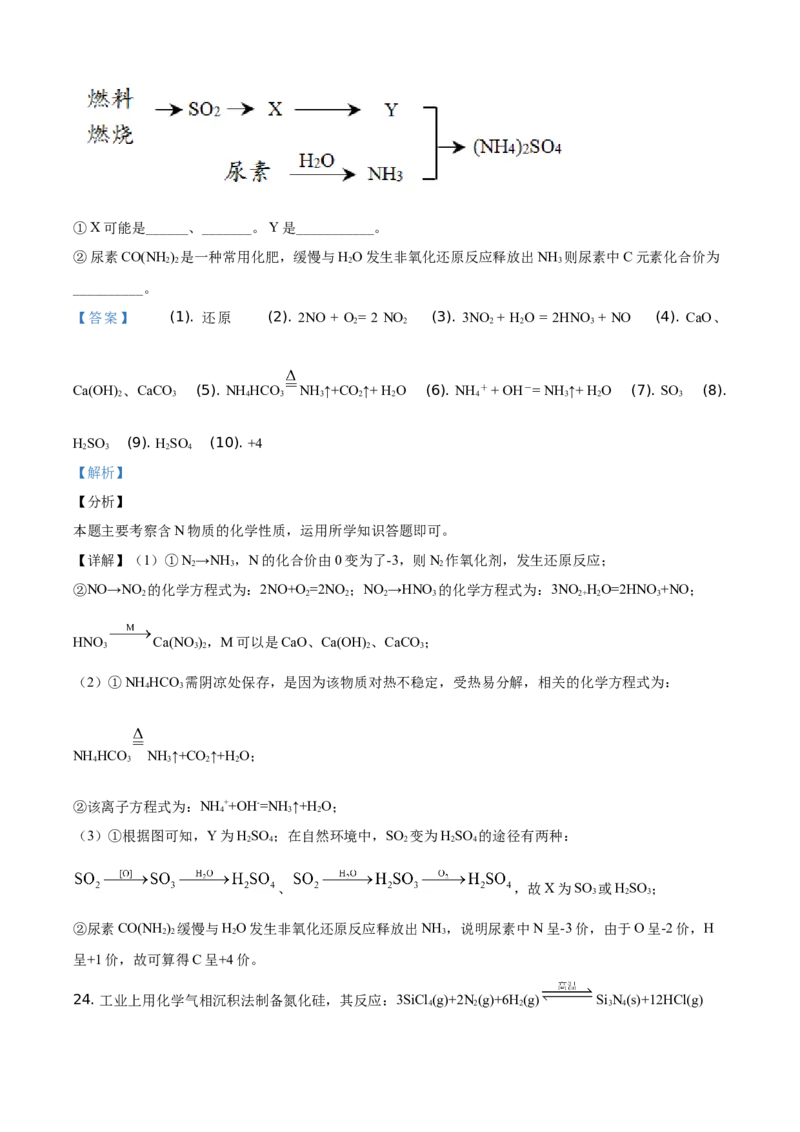
(3)过渡施用氮肥将导致大气中NH 含量增高,加剧雾霾的形成。(NH )SO 是雾霾的成分之一,其形成过
3 4 2 4
程如下图所示(转化所需试剂及条件已略去):① X可能是______、_______。 Y是___________。
② 尿素CO(NH) 是一种常用化肥,缓慢与HO发生非氧化还原反应释放出NH 则尿素中C元素化合价为
2 2 2 3
__________。
【答案】 (1). 还原 (2). 2NO + O = 2 NO (3). 3NO + H O = 2HNO + NO (4). CaO、
2 2 2 2 3
Ca(OH) 、CaCO (5). NH HCO NH ↑+CO ↑+ H O (6). NH + + OH-= NH ↑+ H O (7). SO (8).
2 3 4 3 3 2 2 4 3 2 3
HSO (9). HSO (10). +4
2 3 2 4
【解析】
【分析】
本题主要考察含N物质的化学性质,运用所学知识答题即可。
【详解】(1)①N→NH ,N的化合价由0变为了-3,则N 作氧化剂,发生还原反应;
2 3 2
②NO→NO 的化学方程式为:2NO+O =2NO;NO →HNO 的化学方程式为:3NO HO=2HNO +NO;
2 2 2 2 3 2+ 2 3
HNO Ca(NO ),M可以是CaO、Ca(OH) 、CaCO ;
3 3 2 2 3
(2)①NH HCO 需阴凉处保存,是因为该物质对热不稳定,受热易分解,相关的化学方程式为:
4 3
NH HCO NH ↑+CO ↑+H O;
4 3 3 2 2
②该离子方程式为:NH ++OH-=NH↑+H O;
4 3 2
(3)①根据图可知,Y为HSO ;在自然环境中,SO 变为HSO 的途径有两种:
2 4 2 2 4
、 ,故X为SO 或HSO ;
3 2 3
②尿素CO(NH) 缓慢与HO发生非氧化还原反应释放出NH ,说明尿素中N呈-3价,由于O呈-2价,H
2 2 2 3
呈+1价,故可算得C呈+4价。
24. 工业上用化学气相沉积法制备氮化硅,其反应:3SiCl (g)+2N(g)+6H(g) Si N(s)+12HCl(g)
4 2 2 3 4△H<0。某温度和压强条件下,分别将0.3mol SiCl (g)、0.2mol N (g)、0.6mol H (g)充入2L密闭容器内,
4 2 2
进行上述反应,5min所得Si N(s)的质量是5.60g(Si N 的摩尔质量为140g/mol)。
3 4 3 4
(1)H 的平均反应速率是______。
2
(2)5min时容器内N 的浓度是______。
2
(3)5min时容器内HCl的物质的量分数是______。
(4)5min时SiCl (g)的转化率是______。
4
(5)5min时容器内的压强是原来的______倍。
【答案】 (1). (2). (3). 42% (4). 40% (5). 0.95
【解析】
【分析】
计算出5min所得Si N(s)的物质的量,再建立“三段式”,再通过各种关系进行计算速率、浓度、物质的
3 4
量分数、转化率等。
【 详 解 】 5min 所 得 Si N(s) 的 物 质 的 量 为 ,
3 4
(1)H 的平均反应速率是 ;故答案为:
2
。
(2)5min时容器内N 的浓度是 ;故答案为: 。
2
(3)5min时容器内HCl的物质的量分数是 ;
故答案为:42%。(4)5min时SiCl (g)的转化率是 ;故答案为:40%。
4
(5)根据压强之比等于物质的量之比, ,
P(后)=0.95P(前),因此5min时容器内的压强是原来的0.95倍;故答案为:0.95。
【点睛】化学反应速率及三段式”建立是常考题型,主要考查“三段式”建立、化学反应速率、物质的量
分数、压强、浓度等。
25. 某兴趣小组为了探究铝电极在电池中的作用,设计并进行了以下系列实验,实验结果记录如下:
编号 电极材料 电解质溶液 电流计指针偏转方向
1 Mg、Al 稀盐酸 偏向Al
2 Al、Cu 稀盐酸 偏向Cu
3 Al、C(石墨) 稀盐酸 偏向石墨
4 Mg、Al NaOH溶液 偏向Mg
5 Al、Cu 浓硝酸 偏向Al
注:①实验均为常温下完成;②电流计指针偏转方向为正极方向。试根据表中实验现象完成下列问题:
(1)实验1、2中Al所作的电极(指正极或负极)______(填“相同”或“不同”)。
(2)对实验3完成下列填空:
①Al为______极,电极反应式为______。
②石墨为______极,电极反应式为______。
③电池总反应式为______
(3)实验4中Al作______极,理由是______。
(4)解释实验5中电流计偏向Al的原因______。
(5)根据实验结果总结出影响铝在电池中作正极或负极的因素有______。
【答案】 (1). 不同 (2). 负 (3). Al-3e-=Al3+ (4). 正 (5). 2H++2e-=H↑ (6). 2Al
2
+6HCl=2AlCl +3H↑ (7). 负 (8). Mg和NaOH溶液不反应,Al和NaOH溶液反应,因此Al为负
3 2
极 (9). Al与浓硝酸发生钝化 (10). 金属活泼性和电解质溶液
【解析】
【分析】
根据金属活泼性与电解质溶液反应,若两种金属都反应,则活泼性强的为负极,若两种金属中只有一种金属与电解质溶液反应,则反应的金属为负极。
【详解】(1)实验1中Mg、Al都与稀盐酸反应,Mg活泼性强,因此Mg作负极,Al作正极,实验2中Al
和盐酸反应,Al作负极,Cu作正极,因此实验1、2中Al所作的电极不同;故答案为:不同。
(2)①实验3中Al和稀盐酸反应,C和稀盐酸不反应,因此Al为负极,电极反应式为Al-3e-=Al3+;故答
案为:负;Al-3e-=Al3+。
②石墨为正极,电极反应式为2H++2e-=H↑;故答案为:正;2H++2e-=H↑。
2 2
③电池总反应式为2Al+6HCl=2AlCl +3H↑;故答案为:2Al+6HCl=2AlCl +3H↑。
3 2 3 2
(3)根据上面总结出电流计指针偏向的极为正极,因此实验4中Mg为正极,Al作负极,Mg和NaOH溶液
不反应,Al和NaOH溶液反应,因此Al为负极;故答案为:负;Mg和NaOH溶液不反应,Al和NaOH
溶液反应,因此Al为负极。
(4)实验5中电流计偏向Al,则Al为正极,Cu为负极,Cu与浓硝酸反应,而Al与浓硝酸发生钝化;故答
案为:Al与浓硝酸发生钝化。
(5)根据实验结果总结出影响铝在电池中作正极或负极的因素,根据实验1、2、3得出主要因素是金属活泼
性,实验4、5得出的因素是电解质溶液;故答案为:金属活泼性和电解质溶液。
【点睛】判断原电池正负极时要根据金属活泼性强弱和电解质溶液综合判断,不能只根据金属活泼性来判
断原电池的正负极。
26. 长期放置的FeSO 溶液易被氧化而变质,某兴趣小组进行了如下实验:
4
(1)设计实验检验FeSO 溶液的变质程度
4
实验方案 实验现象 实验结论
步骤1 取待检测液于试管中,向其中滴加KSCN溶液 ________
FeSO 溶液部分变质
4
步骤2 _____ _________
① 将上述方案补充完整
② 若要使部分变质的FeSO 复原,方法是__________。(写离子反应方程式)
4
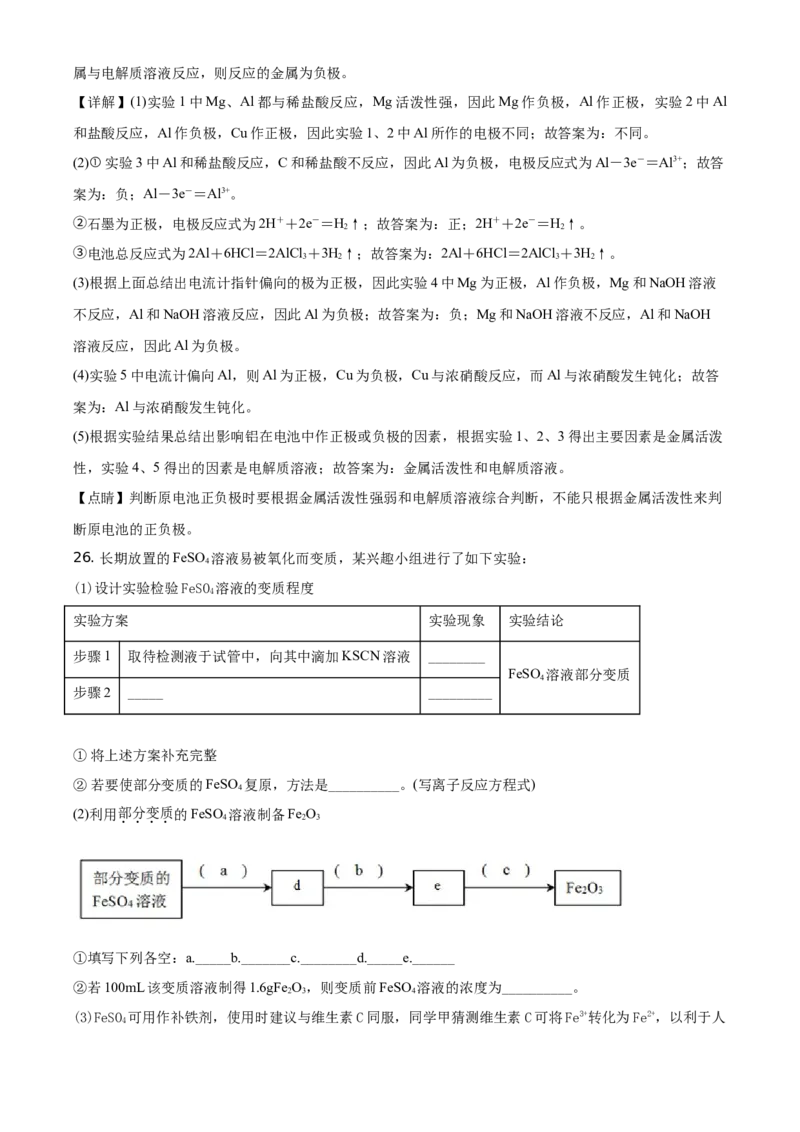
(2)利用部分变质的FeSO 溶液制备Fe O
4 2 3
①填写下列各空:a._____b._______c.________d._____e.______
②若100mL该变质溶液制得1.6gFe O,则变质前FeSO 溶液的浓度为__________。
2 3 4
(3)FeSO 可用作补铁剂,使用时建议与维生素C同服,同学甲猜测维生素C可将Fe3+转化为Fe2+,以利于人
4体吸收。为了验证这一猜想,设计了如下实验:
实验方案 实验现象
取适量 Fe (SO ) 溶液于试管中,加入维生素C片,振荡溶解后,滴加酸性高锰酸钾溶液。 紫色褪去
2 4 3
由上述实验能否得出“维生素C可将Fe3+转化为Fe2+”的结论?请说明理由_______。
【答案】 (1). 溶液变红 (2). 取待检测液于试管中,向其中滴加少量酸性高锰酸钾溶液 (3). 紫
色褪去 (4). 2Fe3++ Fe = 3Fe2+ (5). HO (6). NaOH (7). (8). Fe3+ (9). Fe(OH) (10).
2 2 3
0.2mol/L (11). 不能,维生素C可能过量,也可使高锰酸钾溶液褪色∆,则无法说明一定有Fe2+生成
【解析】
【分析】
(1)①要想证明FeSO 溶液部分变质,需要证明溶液中含有Fe3+和Fe2+;
4
②若要使变质的FeSO 溶液复原,可以向溶液中加入过量的Fe粉,再经过滤除去剩余的Fe粉即可;
4
(2)①利用部分变质的FeSO 溶液制备Fe O 的路线为:
4 2 3
;
②根据Fe元素守恒进行计算;
(3)Fe2+和维生素C都具有还原性,若维生素C过量,也可使高锰酸钾溶液褪色,则无法说明一定有
Fe2+生成。
【详解】(1)①要想证明FeSO 溶液部分变质,需要证明溶液中含有Fe3+和Fe2+;步骤1中,向待测液中
4
加入KSCN溶液,溶液变为血红色,说明溶液中含有Fe3+;步骤2中,向待测液中加入酸性KMnO 溶液,
4
酸性KMnO 溶液褪色,说明溶液中含有Fe2+;
4
②若要使变质的FeSO 溶液复原,可以向溶液中加入过量的Fe粉,再经过滤除去剩余的Fe粉即可,反应
4
的离子方程式为2Fe3++Fe=3Fe2+;
(2)①利用部分变质的FeSO 溶液制备Fe O 的路线为:
4 2 3
,故a为HO,b为
2 2
Fe (SO )、c为NaOH、d为Fe(OH) ,e为△;
2 4 3 3
②n(Fe O)= =0.01mol,则变质前,100mL FeSO 溶液中,n(FeSO )=0.02mol,故c(FeSO )=
2 3 4 4 4=0.2mol/L;
(3)该实验现象不能验证猜想,因为维生素C也具有还原性,若维生素C过量,也可使高锰酸钾溶液褪
色,则无法说明一定有Fe2+生成。