文档内容
北京 101 中学 2019-2020 学年上学期高一年级期中考试化学试卷
可能用到的相对原子质量:H 1 Li 7 C 12 N 14 O 16 S 32 Cl 35.5 Na 23 C 64 Ca 40
U
I卷 选择题(共42分)
1.下列物质属于电解质的是
A. 硝酸钾 B. 酒精 C. 铁 D. 稀硫酸
2.关于容量瓶上标有的内容不正确的是
A. 容积 B. 温度 C. 一条刻度线 D. 两条刻度线
3.下列电离方程式正确的是
A. NaCO=Na ++CO 2- B. Fe (SO )=Fe3++SO2-
2 3 2 3 2 4 3 4
C. NH ·HO NH ++OH- D. HCl H++Cl-
3 2 4
4.下列化合物中,不能由单质之间直接化合生成的是
A. Fe O B. Na O C. CuCl D. FeCl
3 4 2 2 2 2
5.下列关于物质用途的说法中,不正确的是
A. 钠可用于制造高压钠灯 B. 氯气可用于制备漂白粉
C. Na O 可用于呼吸面具供给氧气 D. 碳酸钠可用于治疗胃酸过多
2 2
6.下表中关于物质的分类正确的是
酸 碱 盐 碱性氧化物 酸性氧化物
A HSO NaOH BaCO CO CO
2 4 3 2
B HClO KOH NaHCO CaO SO
3 2
C CHCOOH NaCO CaCl NaO SO
3 2 3 2 2 3
D NaHSO NH ·H O NaCl NaO CO
4 3 2 2 2
A. A B. B C. C D. D
7.下列实验现象的描述正确的是
A. 钠在空气中燃烧,发出黄色火焰,生成白色固体
B. 氢气在氯气中燃烧,发出苍白色火焰,瓶口上方有白色烟雾
C. 铜在氯气中燃烧,产生棕黄色烟,产物溶于水,溶液呈蓝绿色D. 铁丝在氯气中燃烧,产生红棕色烟,产物溶于水,溶液呈浅绿色
8.下列说法正确的是
A. O 的摩尔质量是32g
2
B. 11.2L H 的物质的量为0.5 mol
2
C. 将25g 胆矾固体(CuSO ·5HO)溶解在1L水中,可配制0.1 mol/L的硫酸铜溶液
4 2
D. 将10 mL 10 mol/L的盐酸加水稀释成100 mL,所得盐酸的物质的量浓度为1 mol/L
9.与100mL 0.2mol/L CaCl 溶液中Cl-浓度相同的是
2
A. 50mL 0.1 mol/L FeCl 溶液 B. 200 mL 0.4 mol/L NaCl溶液
3
C. 200 mL 0.1 mol/L MgCl 溶液 D. 200mL 0.2 mol/L KCl溶液
2
10.下列化学方程式不能用H++OH-=H O表示的是
2
A. KOH+HCl=KCl+H O
2
B. Ba(OH)+2HCl=BaCl +2H O
2 2 2
C. 2NaOH+H SO =Na SO +2H O
2 4 2 4 2
.
D Cu(OH)+2HNO =Cu(NO )+2H O
2 3 3 2 2
11.下列能大量共存的离子组是
A. Na+、Ag+、Cl-、OH- B. K+、OH-、HCO -、NO -
3 3
C. Na+、H+、Cl-、CO2- D. Na+、K+、OH-、Cl-
3
12.下列离子方程式 的书写正确的是
A. 氯化镁溶液与氢氧化钠溶液混合:Mg2++2OH-=Mg(OH)↓
2
B. 碳酸钠溶液与稀盐酸混合:NaCO+2H+=2Na++H O+CO↑
2 3 2 2
C. 金属钠放入硫酸铜溶液中:2Na+Cu2+=2Na++Cu
D. 金属钠放入水中:2Na+2H+=2Na++H ↑
2
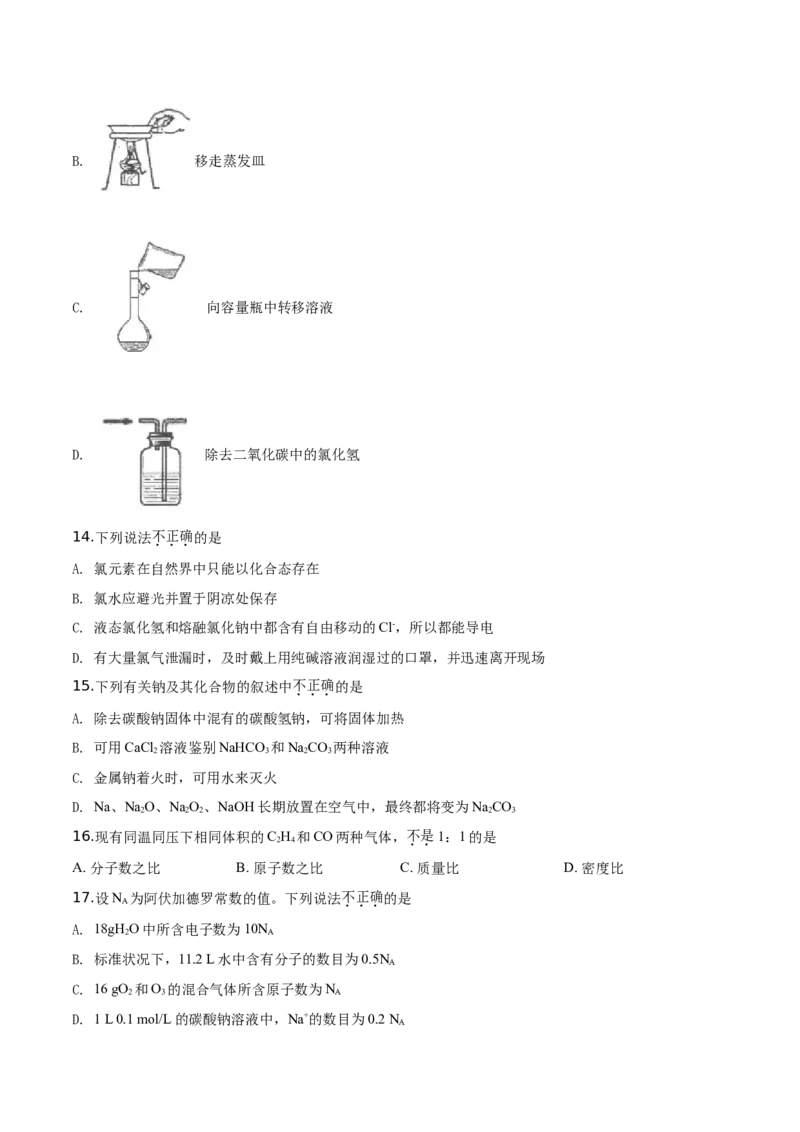
13.下列装置或实验操作正确的是
A. 除去食盐水中的泥沙B. 移走蒸发皿
C. 向容量瓶中转移溶液
D. 除去二氧化碳中的氯化氢
14.下列说法不正确的是
A. 氯元素在自然界中只能以化合态存在
B. 氯水应避光并置于阴凉处保存
C. 液态氯化氢和熔融氯化钠中都含有自由移动的Cl-,所以都能导电
D. 有大量氯气泄漏时,及时戴上用纯碱溶液润湿过的口罩,并迅速离开现场
15.下列有关钠及其化合物的叙述中不正确的是
A. 除去碳酸钠固体中混有的碳酸氢钠,可将固体加热
B. 可用CaCl 溶液鉴别NaHCO 和NaCO 两种溶液
2 3 2 3
C. 金属钠着火时,可用水来灭火
D. Na、NaO、NaO、NaOH长期放置在空气中,最终都将变为NaCO
2 2 2 2 3
16.现有同温同压下相同体积的C H 和CO两种气体,不是1:1的是
2 4
A. 分子数之比 B. 原子数之比 C. 质量比 D. 密度比
17.设N 为阿伏加德罗常数的值。下列说法不正确的是
A
A. 18gHO中所含电子数为10N
2 A
B. 标准状况下,11.2 L水中含有分子的数目为0.5N
A
C. 16 gO 和O 的混合气体所含原子数为N
2 3 A
D. 1 L 0.1 mol/L 的碳酸钠溶液中,Na+的数目为0.2 N
A18.某研究性学习小组在国庆期间进行了研究膨松剂的蒸馒头实验。他们取一定量的面粉和水,和好面后
分成六等份,按照下表加入对应物质后充分揉面,做成6个馒头放在同一个蒸锅里蒸制。实验完成后,他
们比较6个馒头的大小和颜色,下列有关结论或解释不正确的是
编号 1 2 3 4 5 6
1g 1g 2g 1g NaHCO 适量
3
所加物质 无
NaCO NaHCO NaHCO 和适量食醋 酵母
2 3 3 3
A. 1、2号馒头外形最小,且2号馒头呈黄色带碱味,说明NaCO 不能单独做膨松剂
2 3
B. 4号馒头会比3号馒头外形较大、颜色较深
C. 3号馒头比5号馒头外形较小、颜色较深,说明等量的NaHCO 受热分解时比与酸反应时产生的气体较
3
多、残留有碱性较强的物质
D. 6号馒头中的酵母属于生物膨松剂,馒头蒸制过程中发生了化学反应
19.2019年诺贝尔化学奖授予约翰·古迪纳夫(97岁的Mr.Goodenough)、斯坦利·惠廷厄姆和吉野彰,
以表彰他们在锂离子电池研发领域作出的贡献。已知金属锂的化学性质与金属钠相似;金属锂的密度是
0.534g/cm3,金属钠的密度是0.97g/cm3,煤油的密度约为0.80g/cm3。下列有关金属锂的说法不正确的是
A. 金属锂也可保存在煤油中
B. 7g Li中所含质子的物质的量为3mol
C. 金属锂可能会与氧气、氯气、水发生反应
D. 金属锂与金属钠的性质有相似又有不同,体现了分类法和比较法
20.下列说法正确的是
A. 取少量待测液,加入稀盐酸,产生无色无味并能使澄清石灰水变浑浊的气体,则原溶液中一定有CO2-
3
B. 取少量待测液,加入BaCl 溶液,产生白色沉淀,再加稀盐酸,沉淀不消失,则原溶液中一定有SO 2-
2 4
C. 取少量待测液,加入AgNO 溶液,产生白色沉淀,再加稀盐酸,沉淀不消失,则原溶液中一定有Cl-
3
D. 可用稀盐酸一种试剂将NaCO、NaCl、AgNO 三种溶液区别开来
2 3 3
21.在无土栽培时,需用0.5 mol·L-1 NHCl、0.16 mol·L-1 KCl、0.24 mol·L-1 K SO 配制而成的营养液。若用
4 2 4
KCl、NH Cl和(NH )SO 三种固体来配制1 L营养液,则需此三种固体物质的量分别为
4 4 2 4
A. 0.4 mol、0.5 mol、0.12 mol B. 0.66 mol、0.5 mol、0.24 mol
C. 0.64 mol、0.5 mol、0.24 mol D. 0.64 mol、0.02 mol、0.24 mol
II卷 非选择题(共58分)
22.7.8g Na O 投入200mL水中,充分反应。
2 2(1)该反应的化学方程式为________。
(2)生成的气体在标准状况下的体积为________L。
(3)反应后溶液中溶质的物质的量浓度为________mol/L。(忽略反应前后溶液体积变化)
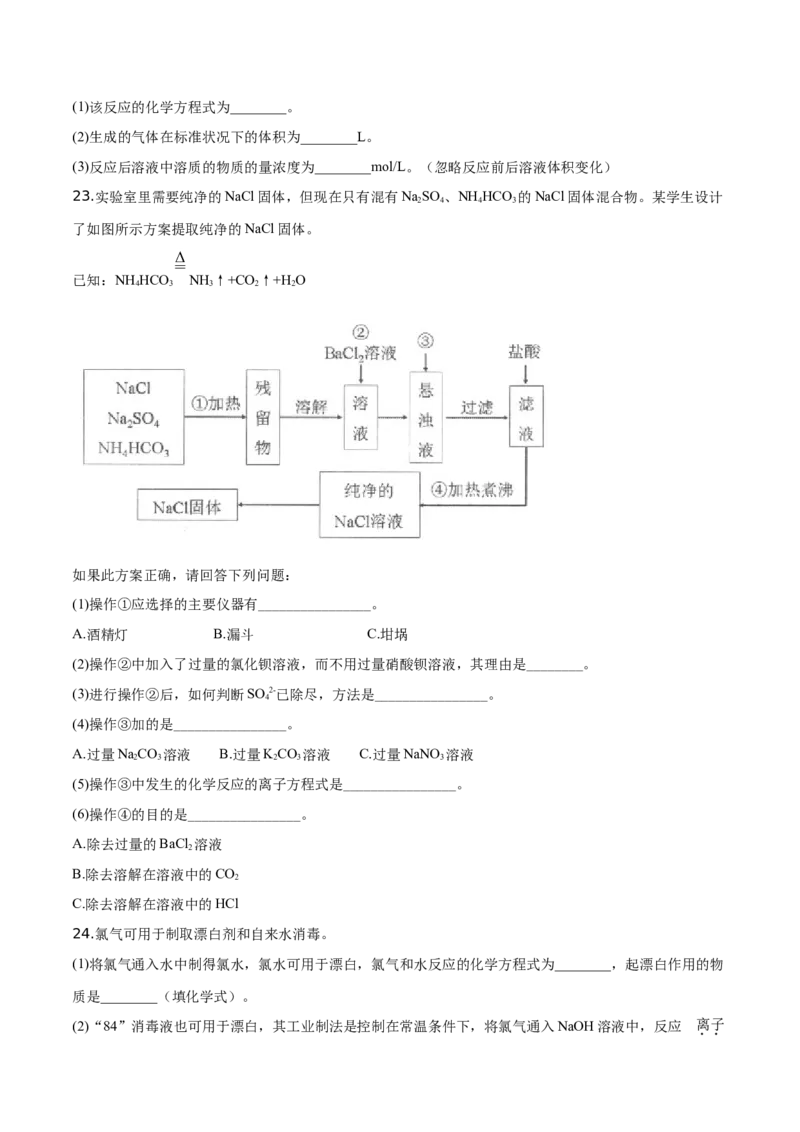
23.实验室里需要纯净的NaCl固体,但现在只有混有NaSO 、NH HCO 的NaCl固体混合物。某学生设计
2 4 4 3
了如图所示方案提取纯净的NaCl固体。
已知:NH HCO NH ↑+CO ↑+H O
4 3 3 2 2
如果此方案正确,请回答下列问题:
(1)操作①应选择的主要仪器有________________。
A.酒精灯 B.漏斗 C.坩埚
(2)操作②中加入了过量的氯化钡溶液,而不用过量硝酸钡溶液,其理由是________。
(3)进行操作②后,如何判断SO 2-已除尽,方法是________________。
4
(4)操作③加的是________________。
A.过量NaCO 溶液 B.过量KCO 溶液 C.过量NaNO 溶液
2 3 2 3 3
(5)操作③中发生的化学反应的离子方程式是________________。
(6)操作④的目的是________________。
A.除去过量的BaCl 溶液
2
B.除去溶解在溶液中的CO
2
C.除去溶解在溶液中的HCl
24.氯气可用于制取漂白剂和自来水消毒。
(1)将氯气通入水中制得氯水,氯水可用于漂白,氯气和水反应的化学方程式为________,起漂白作用的物
质是________(填化学式)。
(2)“84”消毒液也可用于漂白,其工业制法是控制在常温条件下,将氯气通入NaOH溶液中,反应 的离子方程式为__________。
(3)同学们探究“84”消毒液在不同pH下使红纸褪色的情况,做了如下实验:
步骤1:将5 mL 市售“84”消毒液稀释100倍,测得稀释后溶液的pH=12;
步骤2:将稀释后溶液各20 mL分别加入3个洁净的小烧杯中;
步骤3:用HSO 溶液将3个烧杯内溶液的pH分别调至10、7和4。
2 4
(溶液体积变化忽略不计)
步骤4:在3个烧杯中分别放入大小相同的红纸,观察现象,记录如下:
烧杯 溶液的pH 现象
a 10 10 min后,红纸基本不褪色;4 h后红纸褪色
b 7 10 min后,红纸颜色变浅;4 h后红纸褪色
c 4 10 min后,红纸颜色变得更浅;4 h后红纸褪色
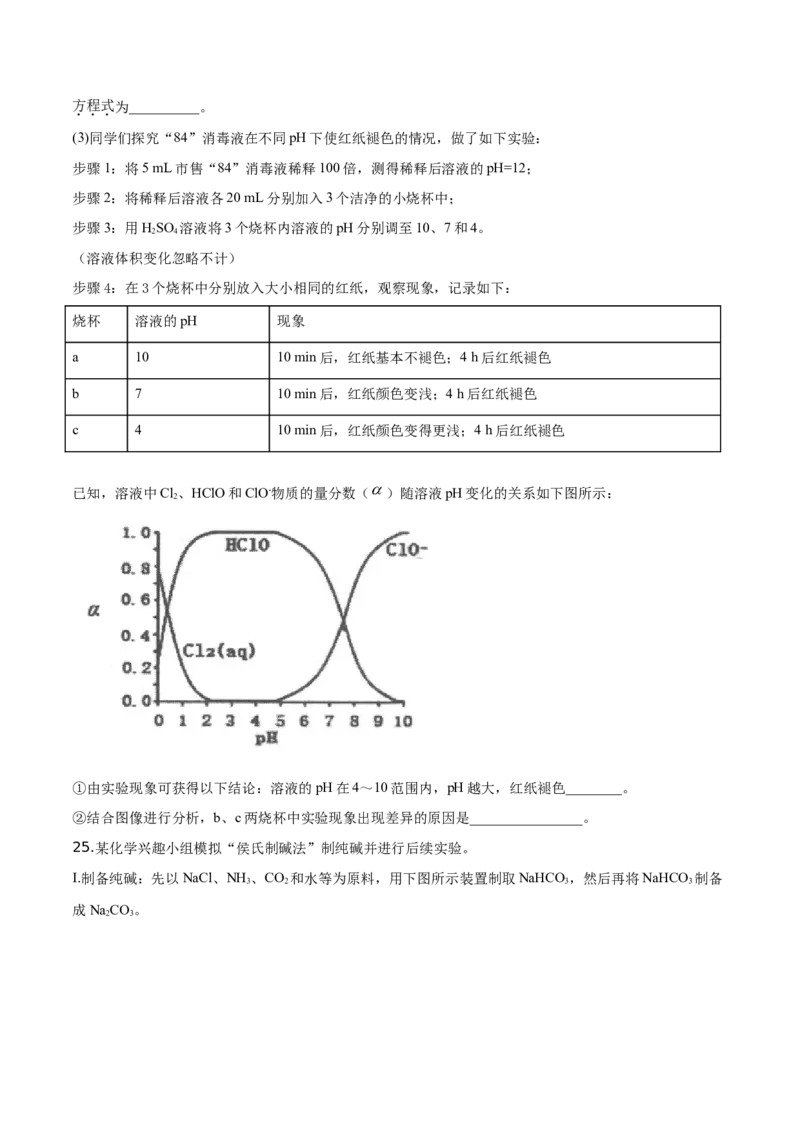
已知,溶液中Cl、HClO和ClO-物质的量分数( )随溶液pH变化的关系如下图所示:
2
①由实验现象可获得以下结论:溶液的pH在4~10范围内,pH越大,红纸褪色________。
②结合图像进行分析,b、c两烧杯中实验现象出现差异的原因是________________。
25.某化学兴趣小组模拟“侯氏制碱法”制纯碱并进行后续实验。
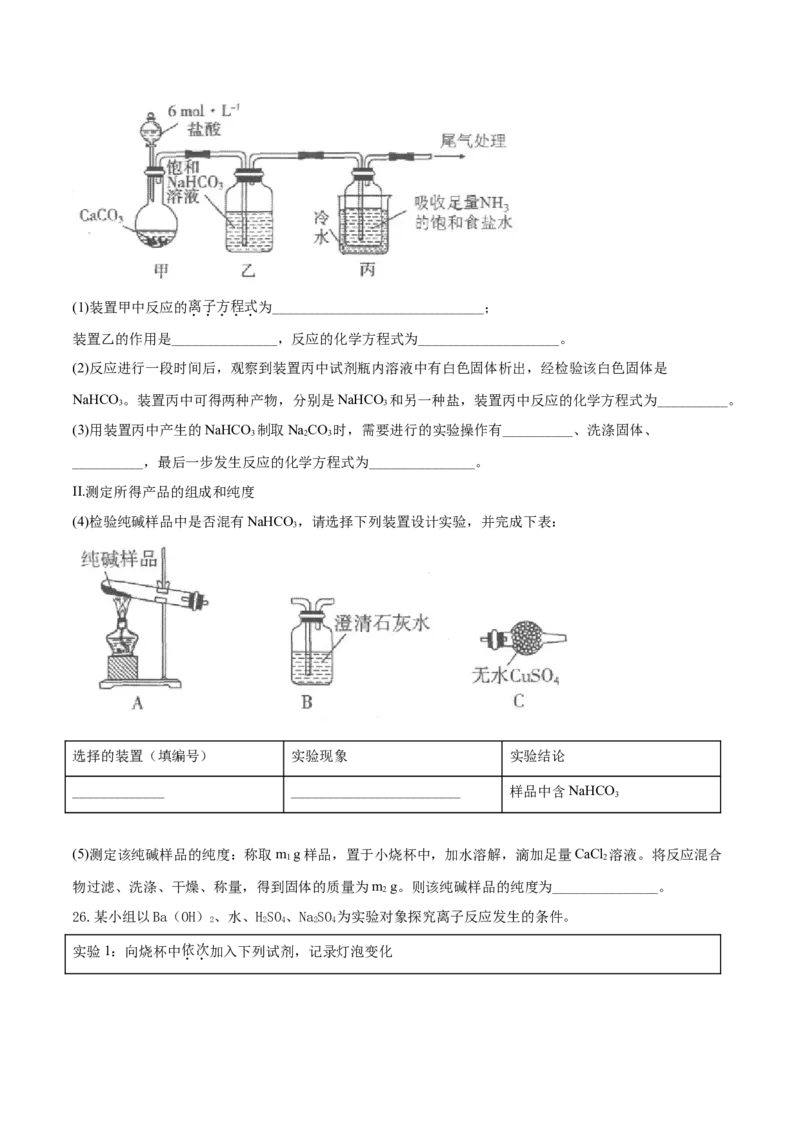
I.制备纯碱:先以NaCl、NH 、CO 和水等为原料,用下图所示装置制取NaHCO ,然后再将NaHCO 制备
3 2 3 3
成NaCO。
2 3(1)装置甲中反应的离子方程式为______________________________;
装置乙的作用是_______________,反应的化学方程式为____________________。
(2)反应进行一段时间后,观察到装置丙中试剂瓶内溶液中有白色固体析出,经检验该白色固体是
NaHCO 。装置丙中可得两种产物,分别是NaHCO 和另一种盐,装置丙中反应的化学方程式为__________。
3 3
(3)用装置丙中产生的NaHCO 制取NaCO 时,需要进行的实验操作有__________、洗涤固体、
3 2 3
__________,最后一步发生反应的化学方程式为_______________。
II.测定所得产品的组成和纯度
(4)检验纯碱样品中是否混有NaHCO ,请选择下列装置设计实验,并完成下表:
3
选择的装置(填编号) 实验现象 实验结论
_____________ ________________________ 样品中含NaHCO
3
(5)测定该纯碱样品的纯度:称取m g样品,置于小烧杯中,加水溶解,滴加足量CaCl 溶液。将反应混合
1 2
物过滤、洗涤、干燥、称量,得到固体的质量为m g。则该纯碱样品的纯度为_______________。
2
26.某小组以Ba(OH)、水、HSO、NaSO 为实验对象探究离子反应发生的条件。
2 2 4 2 4
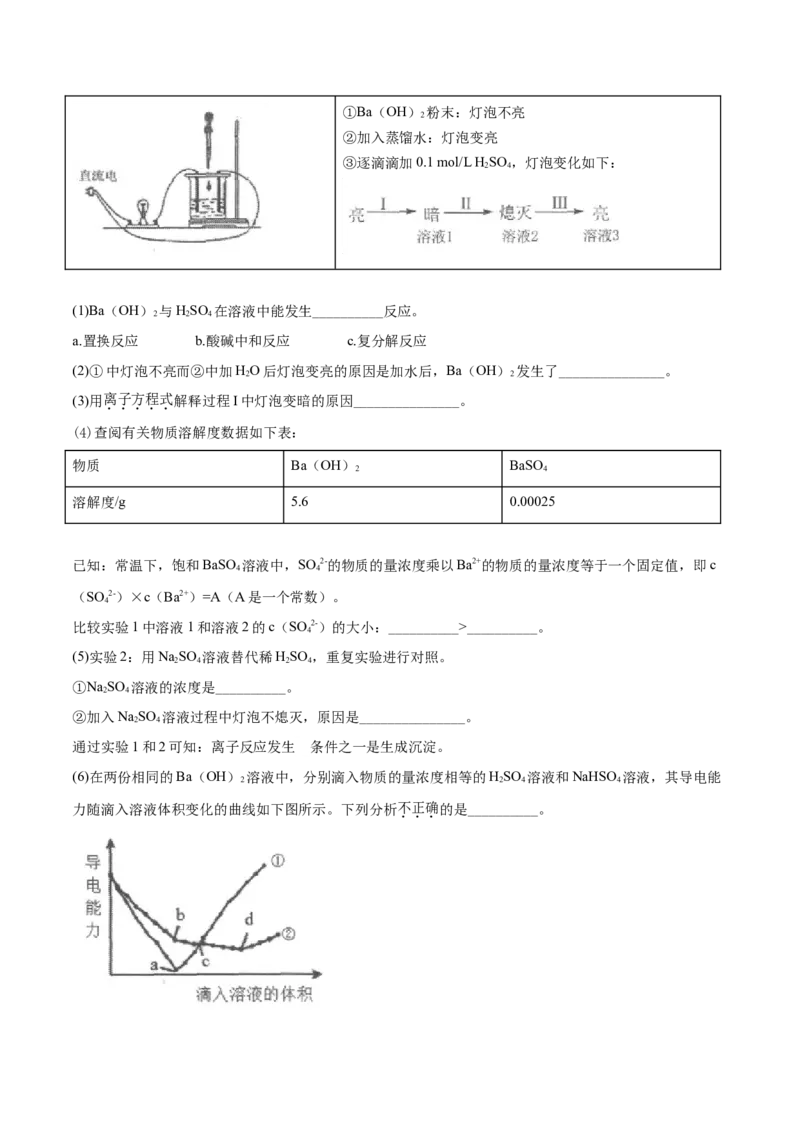
实验1:向烧杯中依次加入下列试剂,记录灯泡变化①Ba(OH) 粉末:灯泡不亮
2
②加入蒸馏水:灯泡变亮
③逐滴滴加0.1 mol/L H SO ,灯泡变化如下:
2 4
(1)Ba(OH) 与HSO 在溶液中能发生__________反应。
2 2 4
a.置换反应 b.酸碱中和反应 c.复分解反应
(2)①中灯泡不亮而②中加HO后灯泡变亮的原因是加水后,Ba(OH) 发生了_______________。
2 2
(3)用离子方程式解释过程I中灯泡变暗的原因_______________。
(4)查阅有关物质溶解度数据如下表:
物质 Ba(OH) BaSO
2 4
溶解度/g 5.6 0.00025
已知:常温下,饱和BaSO 溶液中,SO 2-的物质的量浓度乘以Ba2+的物质的量浓度等于一个固定值,即c
4 4
(SO 2-)×c(Ba2+)=A(A是一个常数)。
4
比较实验1中溶液1和溶液2的c(SO 2-)的大小:__________>__________。
4
(5)实验2:用NaSO 溶液替代稀HSO ,重复实验进行对照。
2 4 2 4
①NaSO 溶液的浓度是__________。
2 4
②加入NaSO 溶液过程中灯泡不熄灭,原因是_______________。
2 4
通过实验1和2可知:离子反应发生 的条件之一是生成沉淀。
(6)在两份相同的Ba(OH) 溶液中,分别滴入物质的量浓度相等的HSO 溶液和NaHSO 溶液,其导电能
2 2 4 4
力随滴入溶液体积变化的曲线如下图所示。下列分析不正确的是__________。A.①代表滴加HSO 溶液的变化曲线
2 4
B.b点,溶液中大量存在的离子是Na+、OH-、SO 2-
4
C.c点,两份溶液中含有相同量的OH-
D.a、d两点对应的溶液均显中性