文档内容
北京市西城区第二学期阶段性试卷
高一化学
本试卷共8页,共100分。考试时长90分钟。考生务必将答案写在答题卡上,在试卷上作答
无效。
可能用到的相对原子质量: H 1 C 12 N 14 O 16 Cu 64
第一部分(选择题 共50分)
每小题只有一个选项符合题意(1 ~ 10小题,每小题2分;11 ~ 20小题,每小题3分)
1.十八大以来,我国科学技术迅猛发展。下列设备工作时,将化学能转化为电能的是
A. 锂离子电池 B. 风力发电机
C. 偏二甲肼燃烧 D. 太阳能集热器
2.下列营养物质中,属于高分子的是
A. 蔗糖 B. 油脂 C. 蛋白质 D. 葡萄糖
3.下列各组物质的相互关系描述正确的是
A. H、D 和T 互为同位素 B. 和 互为同分异构体
2 2 2
C. 金刚石、C 、石墨互为同系物 D. (CH)CHC H 和CHCHCH(CH ) 属于同种物质
60 3 2 2 5 3 2 3 2
4.下列气体呈红棕色的是
A. Cl B. SO C. NO D. CO
2 2 2 2
5.下列有机物中,不属于烃的是
A. CH = CH B. C. CHCHCH D. CH COOH
2 2 3 2 3 3
6.下列说法不正确的是
A. 纯净的乙酸称为冰醋酸 B. 乙醇能与水以任意比互溶
C. 乙酸是比碳酸更弱的酸 D. 用食醋清除暖瓶中的水垢7.下列试剂不能用来鉴别乙醇和乙酸的是
A. 酸性高锰酸钾溶液 B. 碳酸钠溶液
C. 紫色石蕊溶液 D. 蒸馏水
8.安徽宣城所产的宣纸、宣笔、徽墨、宣砚举世闻名。做宣笔常用羊、兔等动物的毛,其主要成分是
.
A 蛋白质 B. 纤维素 C. 糖类 D. 油脂
9.常温下,下列物质可用铁罐车装运的是
A. 浓硫酸 B. 浓盐酸 C. 稀盐酸 D. 稀硝酸
10.下列物质能使酸性高锰酸钾溶液褪色的是
A. 聚乙烯 B. 甲烷 C. 苯 D. 乙烯
11.下列化学用语表达正确的是
A. N 的电子式: B. Cl-离子的结构示意图:
2
C. CH 分子的比例模型: D. 质子数为92、中子数为146的铀(U)原子符号:
4
12.下列物质中能使湿润的红色石蕊试纸变蓝的是
A. NH B. SO C. HCl D. NO
3 3 2
13.下列有关物质用途的说法中,不正确的是
A. NH 常用作制冷剂 B. Al O 做耐火坩埚
3 2 3
C. 用Al(OH) 治疗胃酸过多 D. 用SO 漂白馒头
3 2
14.如右图所示,将SO 通入下列不同溶液中,实验现象与所得结论不正确的是
2
溶液 现象 结论
A 品红溶液 红色溶液褪色 SO 有漂白性
2
B HS溶液 产生黄色沉淀 SO 有氧化性
2 2
C 酸性KMnO 溶液 紫色溶液褪色 SO 有漂白性
4 2
SO 的水溶液呈酸
D 滴有酚酞的NaOH溶液 红色溶液褪色 2
性
A. A B. B C. C D. D15.下列说法正确的是
A. 石油分馏是化学变化
B. 石油裂解得到的汽油是纯净物
C. 天然气是一种清洁的化石燃料
D. 水煤气是通过煤的液化得到的气体燃料
16.在一定温度下的密闭容器中,可逆反应N + 3H 2NH 达到平衡状态的标志是
2 2 3
A. N、H、NH 在容器中共存
2 2 3
B. 混合气体的总物质的量不再发生变化
C. 单位时间内生成n mol N ,同时生成3n mol H
2 2
D. 单位时间内消耗n mol N ,同时消耗n mol NH
2 3
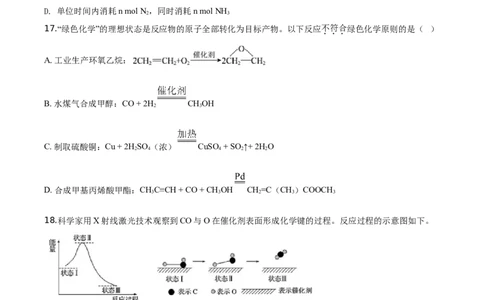
17.“绿色化学”的理想状态是反应物的原子全部转化为目标产物。以下反应不符合绿色化学原则的是( )
A. 工业生产环氧乙烷:
B. 水煤气合成甲醇:CO + 2H CHOH
2 3
C. 制取硫酸铜:Cu + 2H SO (浓) CuSO + SO↑+ 2H O
2 4 4 2 2
D. 合成甲基丙烯酸甲酯:CHC≡CH + CO + CH OH CH=C(CH)COOCH
3 3 2 3 3
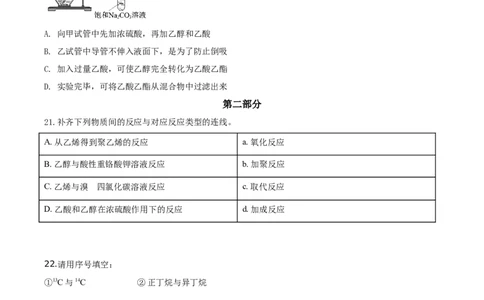
18.科学家用X射线激光技术观察到CO与O在催化剂表面形成化学键的过程。反应过程的示意图如下。
下列说法不正确的是
A. CO 含有极性共价键 B. 上述过程表示CO和O生成CO
2 2
C. 上述过程中CO断键形成C和O D. 从状态Ⅰ到状态Ⅲ,有能量放出
19.向BaCl 溶液中通入SO 气体,溶液仍然澄清;若将BaCl 溶液分盛在两支试管中,一只试管加稀HNO,
2 2 2 3
另一只加NaOH溶液,然后再通入SO 气体,结果两支试管都有白色沉淀产生。由此得出的下列结论中不合
2
理的是A. SO 是酸性氧化物、SO 具有还原性
2 2
B. 两支试管中的白色沉淀不是同种物质
C. BaCl 既能跟强酸、又能跟强碱反应,具有两性
2
D. 升高pH时,SO 水溶液中SO2-浓度增大
2 3
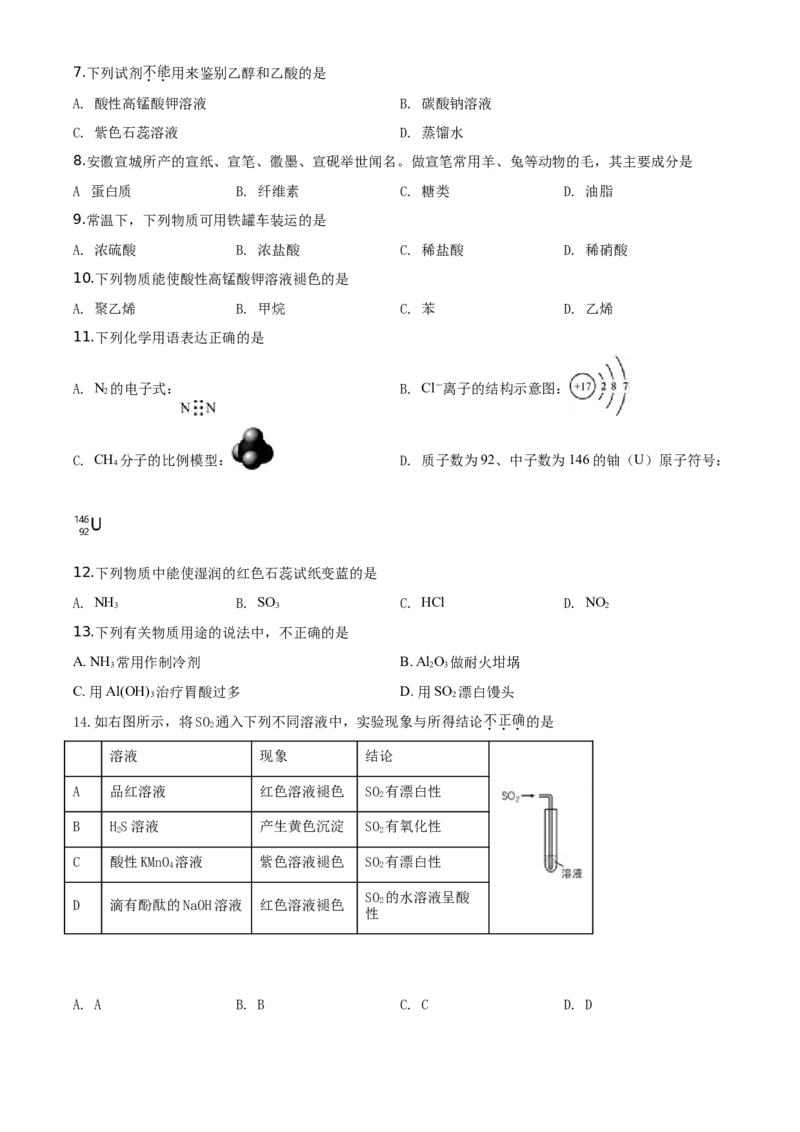
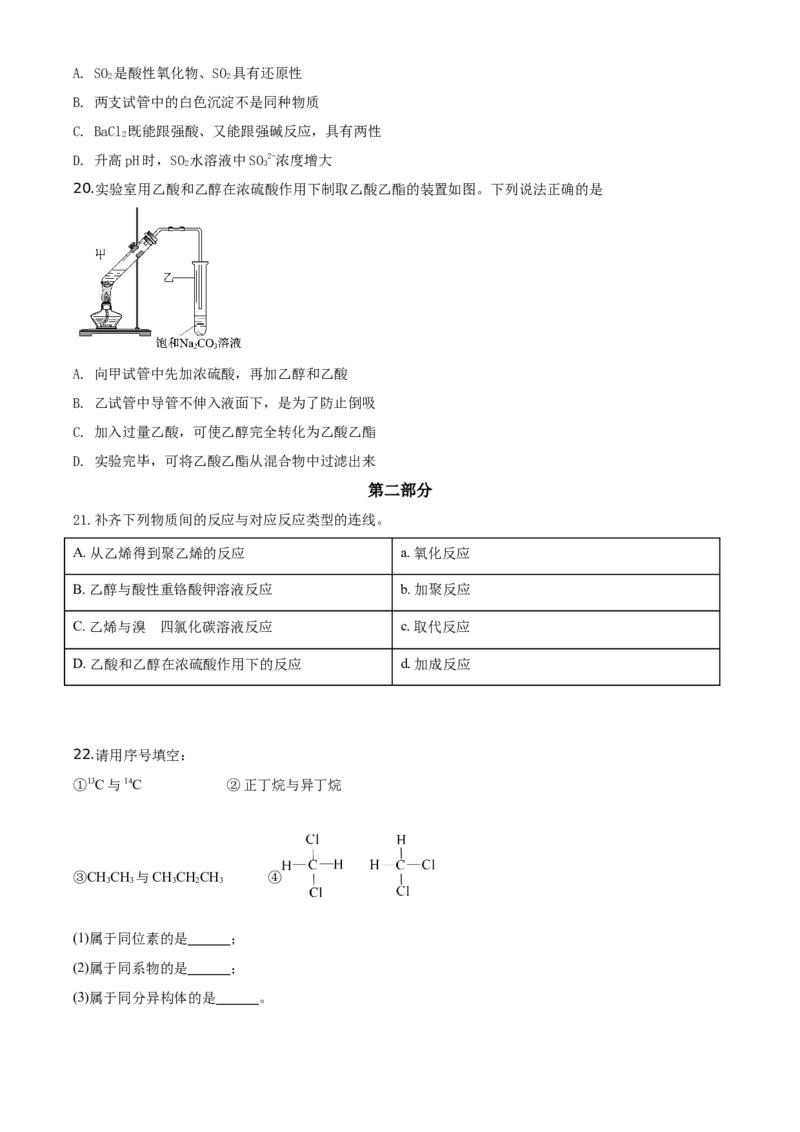
20.实验室用乙酸和乙醇在浓硫酸作用下制取乙酸乙酯的装置如图。下列说法正确的是
A. 向甲试管中先加浓硫酸,再加乙醇和乙酸
B. 乙试管中导管不伸入液面下,是为了防止倒吸
C. 加入过量乙酸,可使乙醇完全转化为乙酸乙酯
D. 实验完毕,可将乙酸乙酯从混合物中过滤出来
第二部分
21.补齐下列物质间的反应与对应反应类型的连线。
A. 从乙烯得到聚乙烯的反应 a. 氧化反应
B. 乙醇与酸性重铬酸钾溶液反应 b. 加聚反应
C. 乙烯与溴 的四氯化碳溶液反应 c. 取代反应
D. 乙酸和乙醇在浓硫酸作用下的反应 d. 加成反应
22.请用序号填空:
①13C与14C ②正丁烷与异丁烷
③CHCH 与CHCHCH ④
3 3 3 2 3
(1)属于同位素的是______;
(2)属于同系物的是______;
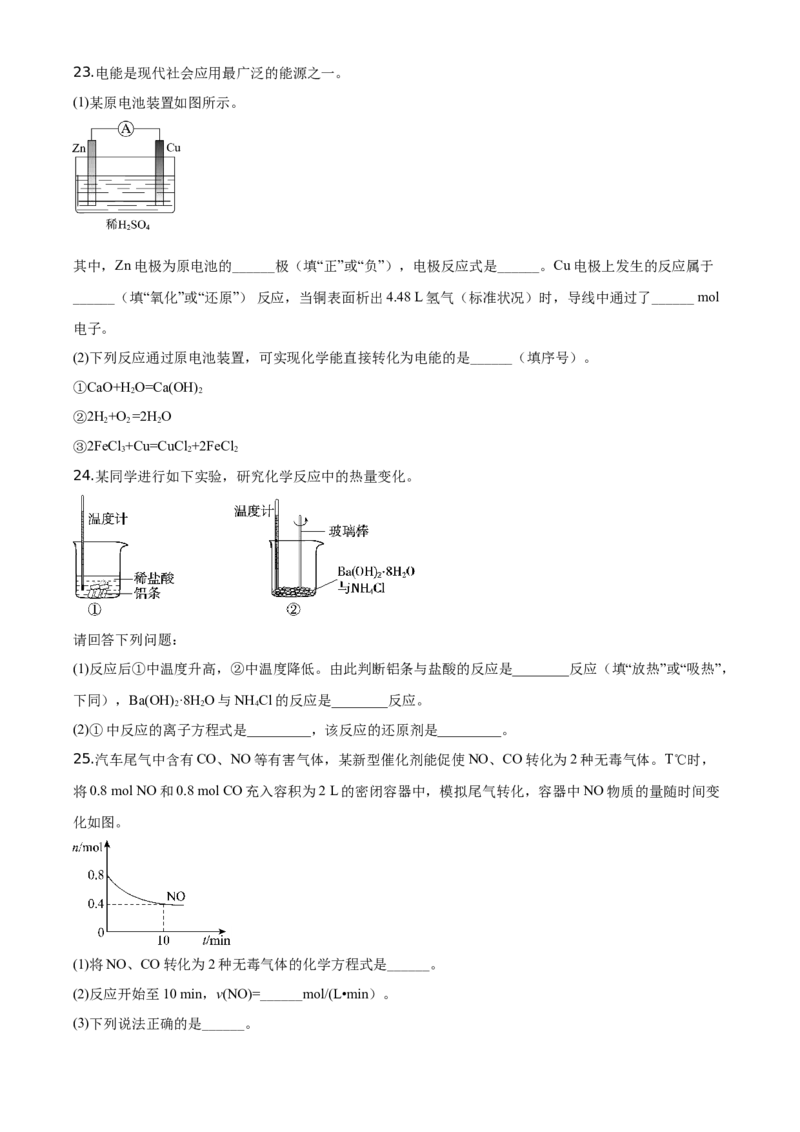
(3)属于同分异构体的是______。23.电能是现代社会应用最广泛的能源之一。
(1)某原电池装置如图所示。
其中,Zn电极为原电池的______极(填“正”或“负”),电极反应式是______。Cu电极上发生的反应属于
______(填“氧化”或“还原”) 反应,当铜表面析出4.48 L氢气(标准状况)时,导线中通过了______ mol
电子。
(2)下列反应通过原电池装置,可实现化学能直接转化为电能的是______(填序号)。
①CaO+H O=Ca(OH)
2 2
②2H+O =2H O
2 2 2
③2FeCl +Cu=CuCl +2FeCl
3 2 2
24.某同学进行如下实验,研究化学反应中的热量变化。
请回答下列问题:
(1)反应后①中温度升高,②中温度降低。由此判断铝条与盐酸的反应是________反应(填“放热”或“吸热”,
下同),Ba(OH) ·8H O与NH Cl的反应是________反应。
2 2 4
(2)①中反应的离子方程式是_________,该反应的还原剂是_________。
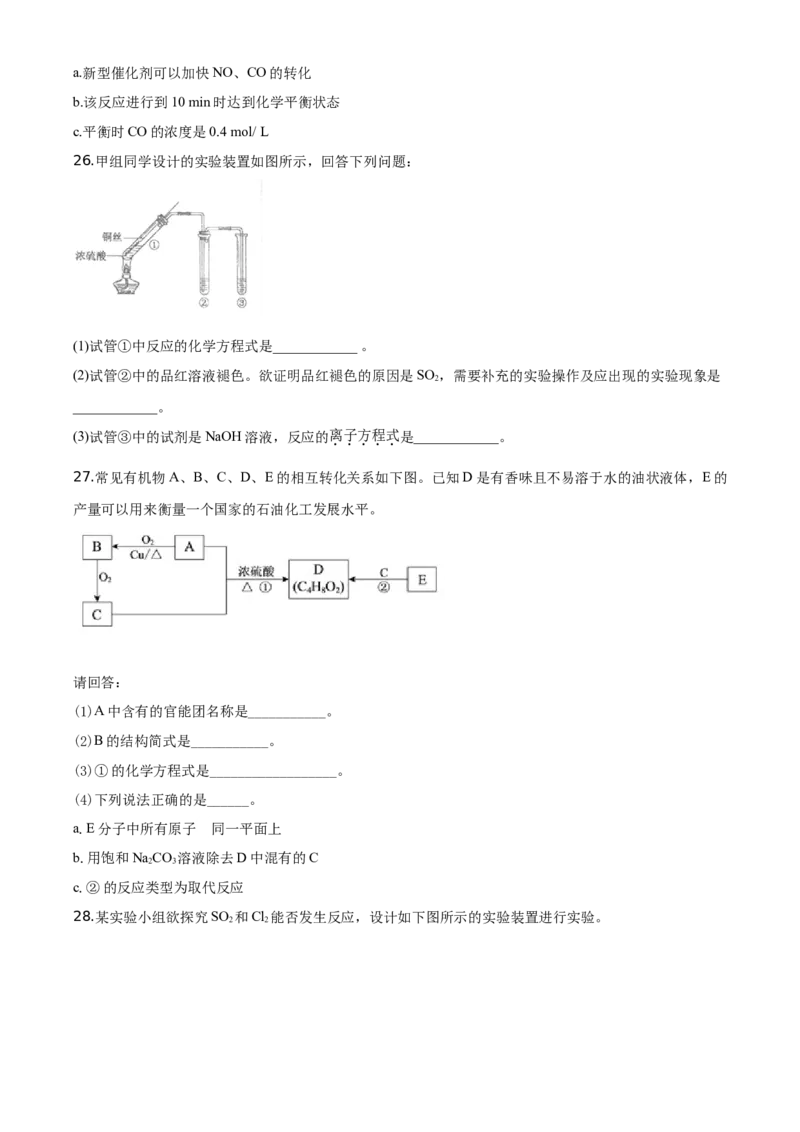
25.汽车尾气中含有CO、NO等有害气体,某新型催化剂能促使NO、CO转化为2种无毒气体。T℃时,
将0.8 mol NO和0.8 mol CO充入容积为2 L的密闭容器中,模拟尾气转化,容器中NO物质的量随时间变
化如图。
(1)将NO、CO转化为2种无毒气体的化学方程式是______。
(2)反应开始至10 min,v(NO)=______mol/(L•min)。
(3)下列说法正确的是______。a.新型催化剂可以加快NO、CO的转化
b.该反应进行到10 min时达到化学平衡状态
c.平衡时CO的浓度是0.4 mol/ L
26.甲组同学设计的实验装置如图所示,回答下列问题:
(1)试管①中反应的化学方程式是____________ 。
(2)试管②中的品红溶液褪色。欲证明品红褪色的原因是SO ,需要补充的实验操作及应出现的实验现象是
2
____________。
(3)试管③中的试剂是NaOH溶液,反应的离子方程式是____________。
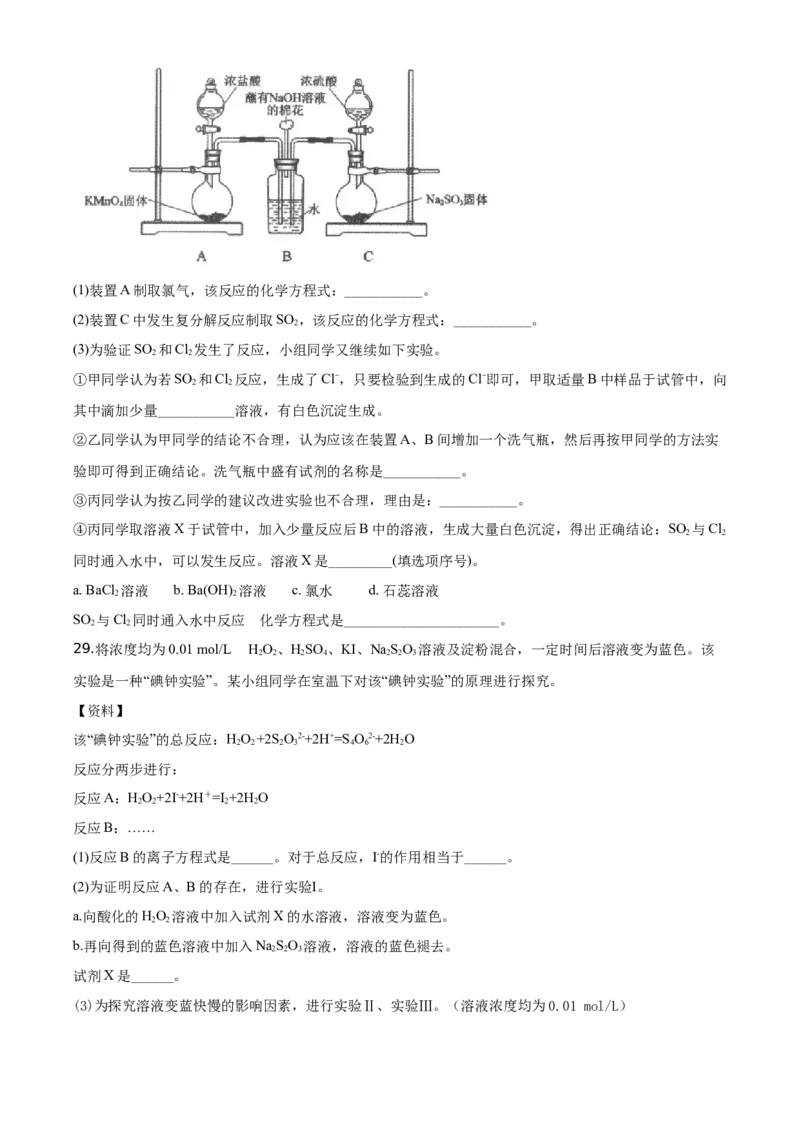
27.常见有机物 A、B、C、D、E的相互转化关系如下图。已知D 是有香味且不易溶于水的油状液体,E的
产量可以用来衡量一个国家的石油化工发展水平。
请回答:
(1)A中含有的官能团名称是___________。
(2)B的结构简式是___________。
(3)①的化学方程式是__________________。
(4)下列说法正确的是______。
a.E分子中所有原子 在同一平面上
b.用饱和NaCO 溶液除去D中混有的C
2 3
c.②的反应类型为取代反应
28.某实验小组欲探究SO 和Cl 能否发生反应,设计如下图所示的实验装置进行实验。
2 2(1)装置A制取氯气,该反应的化学方程式:___________。
(2)装置C中发生复分解反应制取SO ,该反应的化学方程式:___________。
2
(3)为验证SO 和Cl 发生了反应,小组同学又继续如下实验。
2 2
①甲同学认为若SO 和Cl 反应,生成了Cl-,只要检验到生成的Cl-即可,甲取适量B中样品于试管中,向
2 2
其中滴加少量___________溶液,有白色沉淀生成。
②乙同学认为甲同学的结论不合理,认为应该在装置A、B间增加一个洗气瓶,然后再按甲同学的方法实
验即可得到正确结论。洗气瓶中盛有试剂的名称是___________。
③丙同学认为按乙同学的建议改进实验也不合理,理由是:___________。
④丙同学取溶液X于试管中,加入少量反应后B中的溶液,生成大量白色沉淀,得出正确结论:SO 与Cl
2 2
同时通入水中,可以发生反应。溶液X是_________(填选项序号)。
a. BaCl 溶液 b. Ba(OH) 溶液 c. 氯水 d. 石蕊溶液
2 2
SO 与Cl 同时通入水中反应 的化学方程式是______________________。
2 2
29.将浓度均为0.01 mol/L 的HO、HSO 、KI、NaSO 溶液及淀粉混合,一定时间后溶液变为蓝色。该
2 2 2 4 2 2 3
实验是一种“碘钟实验”。某小组同学在室温下对该“碘钟实验”的原理进行探究。
【资料】
该“碘钟实验”的总反应:HO +2S O2-+2H+=S O2-+2H O
2 2 2 3 4 6 2
反应分两步进行:
反应A:HO+2I-+2H+=I +2H O
2 2 2 2
反应B:……
(1)反应B的离子方程式是______。对于总反应,I-的作用相当于______。
(2)为证明反应A、B的存在,进行实验Ⅰ。
a.向酸化的HO 溶液中加入试剂X的水溶液,溶液变为蓝色。
2 2
b.再向得到的蓝色溶液中加入NaSO 溶液,溶液的蓝色褪去。
2 2 3
试剂X是______。
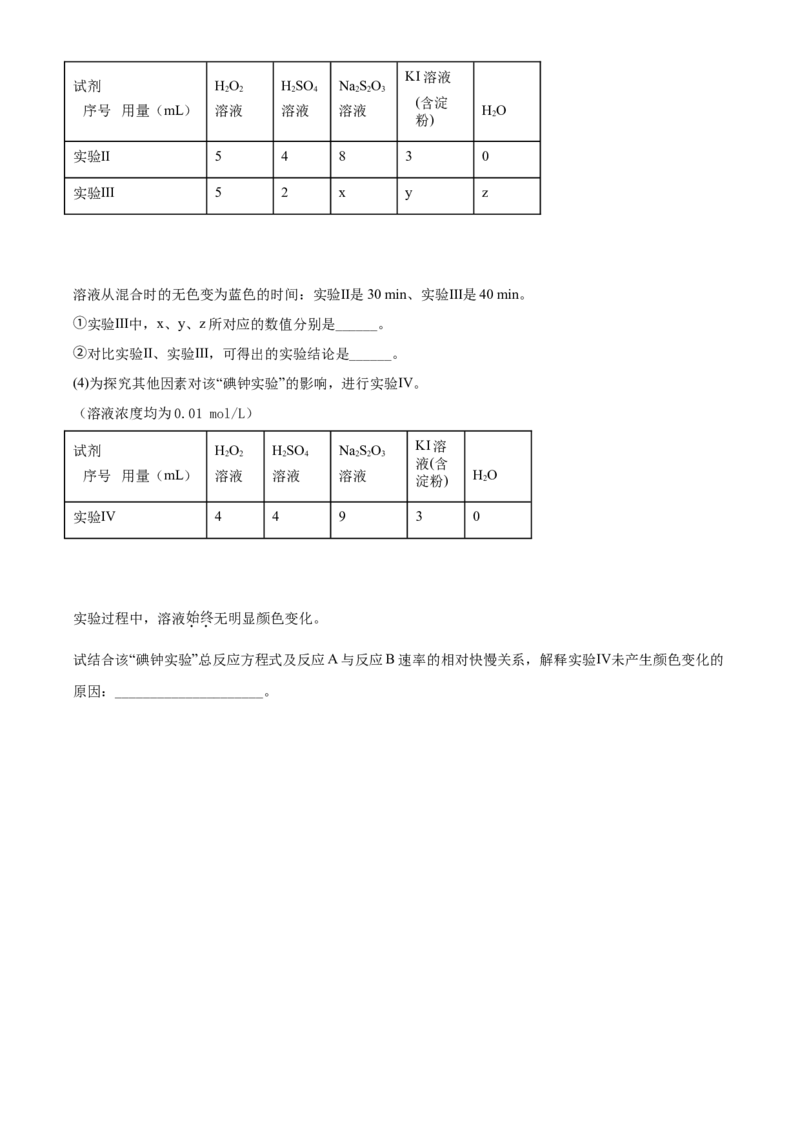
(3)为探究溶液变蓝快慢的影响因素,进行实验Ⅱ、实验Ⅲ。(溶液浓度均为0.01 mol/L)KI溶液
试剂 HO HSO NaSO
2 2 2 4 2 2 3
(含淀
序号 用量(mL) 溶液 溶液 溶液 HO
粉) 2
实验Ⅱ 5 4 8 3 0
实验Ⅲ 5 2 x y z
溶液从混合时的无色变为蓝色的时间:实验Ⅱ是30 min、实验Ⅲ是40 min。
①实验Ⅲ中,x、y、z所对应的数值分别是______。
②对比实验Ⅱ、实验Ⅲ,可得出的实验结论是______。
(4)为探究其他因素对该“碘钟实验”的影响,进行实验Ⅳ。
(溶液浓度均为0.01 mol/L)
KI溶
试剂 HO HSO NaSO
2 2 2 4 2 2 3
液(含
序号 用量(mL) 溶液 溶液 溶液 HO
淀粉) 2
实验Ⅳ 4 4 9 3 0
实验过程中,溶液始终无明显颜色变化。
试结合该“碘钟实验”总反应方程式及反应A与反应B速率的相对快慢关系,解释实验Ⅳ未产生颜色变化的
原因:_____________________。