文档内容
第五单元 化学方程式 单元测试题附答案
一、选择题。(每小题只有一个正确答案,请将其序号填入题后的括号内,30分。)
l. 化学反应遵循质量守恒定律,其原因是反应前后的( )
A. 分子种类没有改变 B.分子数目没有改变
C. 原子种类和数目没有改变 D.物质种类没有改变
2.下列现象不能用质量守恒定律来解释的是( )
A. 蜡烛燃烧后长度越来越短,最后消失 B. 高锰酸钾受热后固体质最减少
C. 铁丝在氧气中燃烧,固体质量增加 D.潮湿的衣服在阳光下晒干
3.下列关于质量守恒定律的说法正确的是( )
A. 10g水与10g酒精混合,得到20g液体,这个过程符合质量守恒定律
B.8g氢气与8g氧气混合反应仅得9g水,但这个过程符合质量守恒定律
C. 把10g双氧水放在锥形瓶中得到的水和氧气的质量一定等于10g
D.所有的变化都符合质量守恒定律
点燃
4.关于化学方程式2CO+O 2CO ,读法正确的是( )
2 2
A. 一氧化碳和氧气生成二氧化碳
B.一氧化碳加氧气点燃等于二氧化碳
C. 两个一氧化碳分子加一个氧气的分子等于两个二氧化碳分子
D.一氧化碳和氧气在点燃的条件下反应生成二氧化碳
5.化学变化可能会改变的是( )
① 分子的总数目 ② 原子的总数目 ③ 原子核中质子的总数目
④ 某种元素的原子核外电子数目
A.① ② B. ③ ④ C.② ③ D. ① ④
6.下列关于化学方程式的意义的叙述中错误的是( )
A. 化学方程式可以表示各种物理变化
B.化学方程式可以表示各反应物和各生成物之间的质量比
C. 化学方程式可以表示各反应物和各生成物之间的粒子(分子或原子)数目之比
D. 化学方程式可以表示反应物、生成物和反应条件
7.下列化学方程式正确的是( )
点燃 点燃
A.Mg+O MgO B.S+O ↑ SO
2 2 2
C.C+O 点 燃 CO ↑ D.2HO 通 电2 H↑ +O↑
2 2 2 2 2
8.化学方程式配平后,有时不需要在等号上方注明反应条件,这表明( )
A.此化学方程式不完整 B.此反应在通常状况下可以发生
C.此反应不能发生 D.此反应方程式不符合质量守恒定律
9.在化学反应C+0 点 燃 CO 中,若生成m个C0 分子,则参加反应的氧原子的个数
2 2 2
是( )
A. m B. 2m C. m/2 D. 4m
10.加热8gKMn0 一段时间后,称得剩余固体质量是7.4g,那么剩余物质是( )
4
A.Mn0 和KMn0 B.KMnO
2 2 4 2 4
C. KMn0 和KMn0 D.Mn0 、KMn0 和KMn0
4 2 4 2、 2 4 4
11. 下列对质量守恒定律的理解错误的是( )
A. 质量守恒定律只适用于化学反应,不适用于物理变化
1B.质量守恒定律研究的内容仅是指“质量”,不能推广到其它物理量
C.催化剂可以改变其它物质的化学反应速率,有催化剂参加的反应也遵守质量守恒
定律
D.蜡烛燃烧后质量减轻,不符合质量守恒定律
12. 现将A、B两种物质各10g混合加热,A完全反应,生成了8gC和4gD,则参加反应的
A与B的质量比为( )
A.1:1 B.2:1 C.4:1 D.5:1
13.图中四位同学正在讨论某一化学方程式表示的意义,他们所描述的化学方程式是( )
A.
B.
C.
D.
14. 在反应A+B=C+D中,已知20gA与一定质量的B恰好完全反应,生成5gC和40gD,
当15gB完全反应时,生成D的质量为( )
A.10g B.20g C.24g D.30g
15.在一个密闭容器中,有甲、乙、丙、丁四种物质在一定条件下充分反应后,测得反应
前后各物质的质量如下表:
物质 甲 乙 丙 丁
反应前质量/g 5 2 20 22
反应后质量/g 待测 11 28 5
下列说法错误的是( )
A.该反应是分解反应 B.甲可能是该反应的催化剂
C.乙、丙变化的质量比为9:8 D.反应后甲的质量为0g
二、填空题。(共50分)
16. 写出下列反应的化学方程式。
(1) 铁丝在氧气中燃烧 。
(2) 实验室加热高锰酸钾制取氧气 。
(3) 氢气在氯气里燃烧生成氯化氢 。
(4) 红磷在空气中燃烧 。
(5) 过氧化氢溶液与二氧化锰混合制氧气 。
其中 (填序号,下同)属于化合反应, 属于分解反应。
17.在铁路提速时,需将一些短铁轨焊接成长铁轨,以减少摩擦,增加速度。常用铝热剂
(铝和四氧化三铁混合物)在高温下反应,生成另一种氧化物和另一种金属单质,写
出该反应的化学方程式: .
18. 观察比较与归纳是学习化学的重要方法。对于以下三个化学方程式:
2Mg+O 2MgO,2H+O 2HO,2CO+O 2CO。
2 2 2 2 2 2
(1)通过比较,发现它们有许多共同点,请你写出其中两点:
① ;
② .
(2) 以上化学方程式也有许多不同之处,请你写出其中一个与另两个的一点不同之
2处: 。
(3)课外学习Cu(OH)CO 2CuO+HO+CO↑后,你会发现它和上述三个反
2 2 3 2 2
应相似,其相似之处是 。
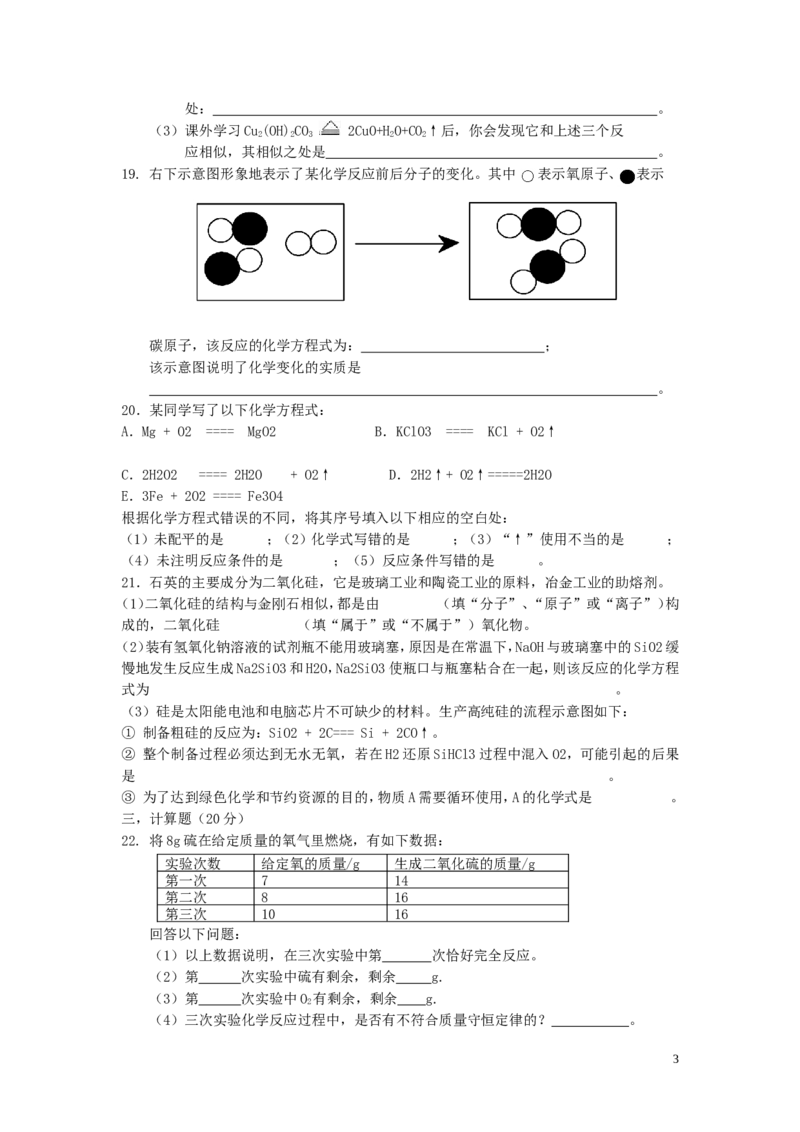
19. 右下示意图形象地表示了某化学反应前后分子的变化。其中 表示氧原子、 表示
碳原子,该反应的化学方程式为: ;
该示意图说明了化学变化的实质是
。
20.某同学写了以下化学方程式:
A.Mg + O2 ==== MgO2 B.KClO3 ==== KCl + O2↑
C.2H2O2 ==== 2H2O + O2↑ D.2H2↑+ O2↑=====2H2O
E.3Fe + 2O2 ==== Fe3O4
根据化学方程式错误的不同,将其序号填入以下相应的空白处:
(1)未配平的是 ;(2)化学式写错的是 ;(3)“↑”使用不当的是 ;
(4)未注明反应条件的是 ;(5)反应条件写错的是 。
21.石英的主要成分为二氧化硅,它是玻璃工业和陶瓷工业的原料,冶金工业的助熔剂。
(1)二氧化硅的结构与金刚石相似,都是由 (填“分子”、“原子”或“离子”)构
成的,二氧化硅 (填“属于”或“不属于”)氧化物。
(2)装有氢氧化钠溶液的试剂瓶不能用玻璃塞,原因是在常温下,NaOH与玻璃塞中的SiO2缓
慢地发生反应生成Na2SiO3和H2O,Na2SiO3使瓶口与瓶塞粘合在一起,则该反应的化学方程
式为 。
(3)硅是太阳能电池和电脑芯片不可缺少的材料。生产高纯硅的流程示意图如下:
① 制备粗硅的反应为:SiO2 + 2C=== Si + 2CO↑。
② 整个制备过程必须达到无水无氧,若在H2还原SiHCl3过程中混入O2,可能引起的后果
是 。
③ 为了达到绿色化学和节约资源的目的,物质A需要循环使用,A的化学式是 。
三,计算题(20分)
22. 将8g硫在给定质量的氧气里燃烧,有如下数据:
实验次数 给定氧的质量/g 生成二氧化硫的质量/g
第一次 7 14
第二次 8 16
第三次 10 16
回答以下问题:
(1)以上数据说明,在三次实验中第 次恰好完全反应。
(2)第 次实验中硫有剩余,剩余 g.
(3)第 次实验中O 有剩余,剩余 g.
2
(4)三次实验化学反应过程中,是否有不符合质量守恒定律的? 。
323.中国登山协会为了纪念我国首次攀登珠穆朗玛峰成功50周年,再次组织攀登珠峰
活动。阿旺扎西等一行登山运动员于前年5月21日13:40成功登顶。假如每名运
动员冲项时消耗自带的液氧4.8kg。求:
(1) 4.8kg氧在标准状况下的体积是多少L? (标况下,氧气的密度为1.43g/L)
(2) 若在实验室中用高锰酸钾为原料制取相同质量的氧气,需要多少kg高锰酸钾?
第五单元 化学方程式 单元测试题答案
一、选择题。
1,C(解析:从微观的角度讲:化学变化就是分子结构发生变化。但比分子更小的微粒(原子
等)的结构没变,小的微粒数总数不变,只是构成分子的微粒数和微粒种类发生了变化。)
2,D 3,B 4,D 5,D 6,A 7,D 8,B(化学方程式配平后,有时不需要在等号上
4方注明反应条件,这表示:该反应的反应物在常温常压下一接触就能反应了。如:
Fe+CuSO=FeSO+CuCaCO3+2HCl=CaCl2+HO+CO↑) 9,B 10,D 11,D 12,D
4 4 2 2
13,B 14,C 15,D(解析:该题主要考查的知识点为质量守恒定律.要做对该题可分
两步走,第一,先根据反应前后物质的总重量不变,求出待测处的数值即反应后甲的质量.
5+2+20+22═待测+11+28+5故待测的数值是5.第二:根据反应前后各物质质量的增减,知道
反应物是丁,生成物是乙和丙.) 二、填空题。
16. 略。 17. 8Al+3FeO 9Fe+4AlO
3 4 2 3
18. (1)反应条件都是加热 都是化合反应(答案合理均可) (2)镁与氧气反应是固体
与气体反应,另外两个是气体与气体间的反应(答案合理均可) (3)生成物都是氧化物
19. 2CO+ O2 =2CO2 原子发生了重新组合(或分子发生了变化)(析由图中可知,每2个
一氧化碳分子和1个氧分子反应生成2个二氧化碳分子.然后根据反应物和生成物及其质量
守恒定律可以正确的书写化学方程式,) 20.(1)B (2)A (3)D (4)E (5)C
21.(1)原子 属于
(2)2NaOH + SiO2 = Na2SiO3 + H2O
(3)硅被氧化得不到高纯硅,且发生爆炸 HCl
三、计算题。
22.(1)二 (2)一 1 (3)三 2 (4)没有 23. 3360L 57.4Kg
5