文档内容
“铝三角”的图像分析及计算
一、氢氧化铝沉淀的图象分析
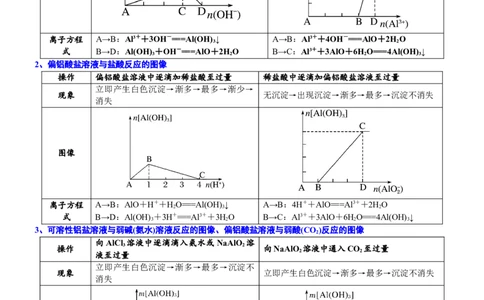
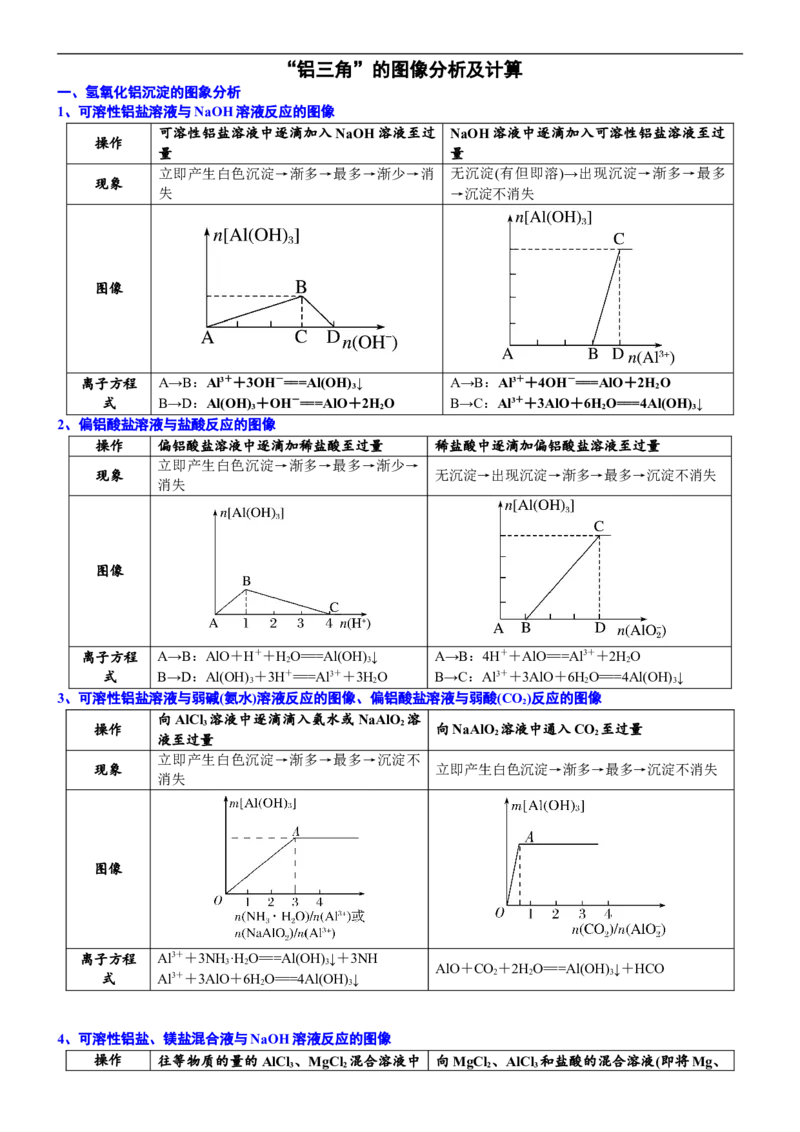
1、可溶性铝盐溶液与NaOH溶液反应的图像
可溶性铝盐溶液中逐滴加入NaOH溶液至过 NaOH溶液中逐滴加入可溶性铝盐溶液至过
操作
量 量
立即产生白色沉淀→渐多→最多→渐少→消 无沉淀(有但即溶)→出现沉淀→渐多→最多
现象
失 →沉淀不消失
图像
离子方程 A→B:Al3++3OH-===Al(OH) ↓ A→B:Al3++4OH-===AlO+2HO
3 2
式 B→D:Al(OH) +OH-===AlO+2HO B→C:Al3++3AlO+6HO===4Al(OH) ↓
3 2 2 3
2、偏铝酸盐溶液与盐酸反应的图像
操作 偏铝酸盐溶液中逐滴加稀盐酸至过量 稀盐酸中逐滴加偏铝酸盐溶液至过量
立即产生白色沉淀→渐多→最多→渐少→
现象 无沉淀→出现沉淀→渐多→最多→沉淀不消失
消失
图像
离子方程 A→B:AlO+H++HO===Al(OH) ↓ A→B:4H++AlO===Al3++2HO
2 3 2
式 B→D:Al(OH) +3H+===Al3++3HO B→C:Al3++3AlO+6HO===4Al(OH) ↓
3 2 2 3
3、可溶性铝盐溶液与弱碱(氨水)溶液反应的图像、偏铝酸盐溶液与弱酸(CO)反应的图像
2
向AlCl 溶液中逐滴滴入氨水或NaAlO 溶
操作 3 2 向NaAlO 溶液中通入CO 至过量
液至过量 2 2
立即产生白色沉淀→渐多→最多→沉淀不
现象 立即产生白色沉淀→渐多→最多→沉淀不消失
消失
图像
离子方程 Al3++3NH ·H O===Al(OH) ↓+3NH
3 2 3 AlO+CO+2HO===Al(OH) ↓+HCO
式 Al3++3AlO+6HO===4Al(OH) ↓ 2 2 3
2 3
4、可溶性铝盐、镁盐混合液与NaOH溶液反应的图像
操作 往等物质的量的AlCl 、MgCl 混合溶液中 向MgCl 、AlCl 和盐酸的混合溶液(即将Mg、
3 2 2 3Al溶于过量盐酸所得的溶液)中逐滴滴入NaOH
加入NaOH溶液至过量
溶液至过量
开始出现白色沉淀,后沉淀量增多,最后 先无沉淀,后出现白色沉淀,然后沉淀量增
现象
沉淀部分溶解 多,最后沉淀部分溶解
图像
O→A:H++OH-===H O
O→A:Al3++3OH-===Al(OH) ↓ 2
离子方程 3 A→B:Al3++3OH-===Al(OH) ↓
Mg2++2OH-===Mg(OH) ↓ 3
式 2 Mg2++2OH-===Mg(OH) ↓
A→B:Al(OH) +OH-===AlO+2HO 2
3 2 A→B:Al(OH) +OH-===AlO+2HO
3 2
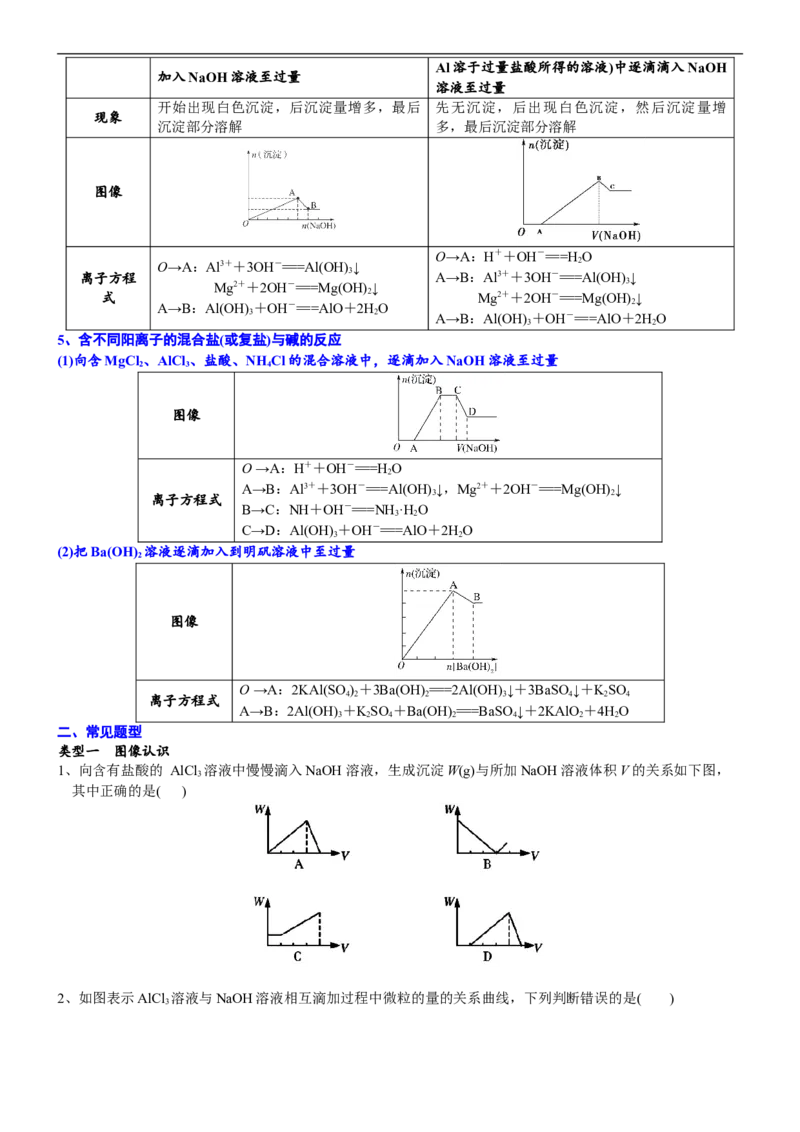
5、含不同阳离子的混合盐(或复盐)与碱的反应
(1)向含MgCl 、AlCl 、盐酸、NH Cl的混合溶液中,逐滴加入NaOH溶液至过量
2 3 4
图像
O →A:H++OH-===H O
2
A→B:Al3++3OH-===Al(OH) ↓,Mg2++2OH-===Mg(OH) ↓
离子方程式 3 2
B→C:NH+OH-===NH·H O
3 2
C→D:Al(OH) +OH-===AlO+2HO
3 2
(2)把Ba(OH) 溶液逐滴加入到明矾溶液中至过量
2
图像
O →A:2KAl(SO )+3Ba(OH) ===2Al(OH) ↓+3BaSO↓+KSO
离子方程式 4 2 2 3 4 2 4
A→B:2Al(OH) +KSO +Ba(OH) ===BaSO ↓+2KAlO +4HO
3 2 4 2 4 2 2
二、常见题型
类型一 图像认识
1、向含有盐酸的 AlCl 溶液中慢慢滴入NaOH 溶液,生成沉淀W(g)与所加NaOH 溶液体积V的关系如下图,
3
其中正确的是( )
2、如图表示AlCl 溶液与NaOH溶液相互滴加过程中微粒的量的关系曲线,下列判断错误的是( )
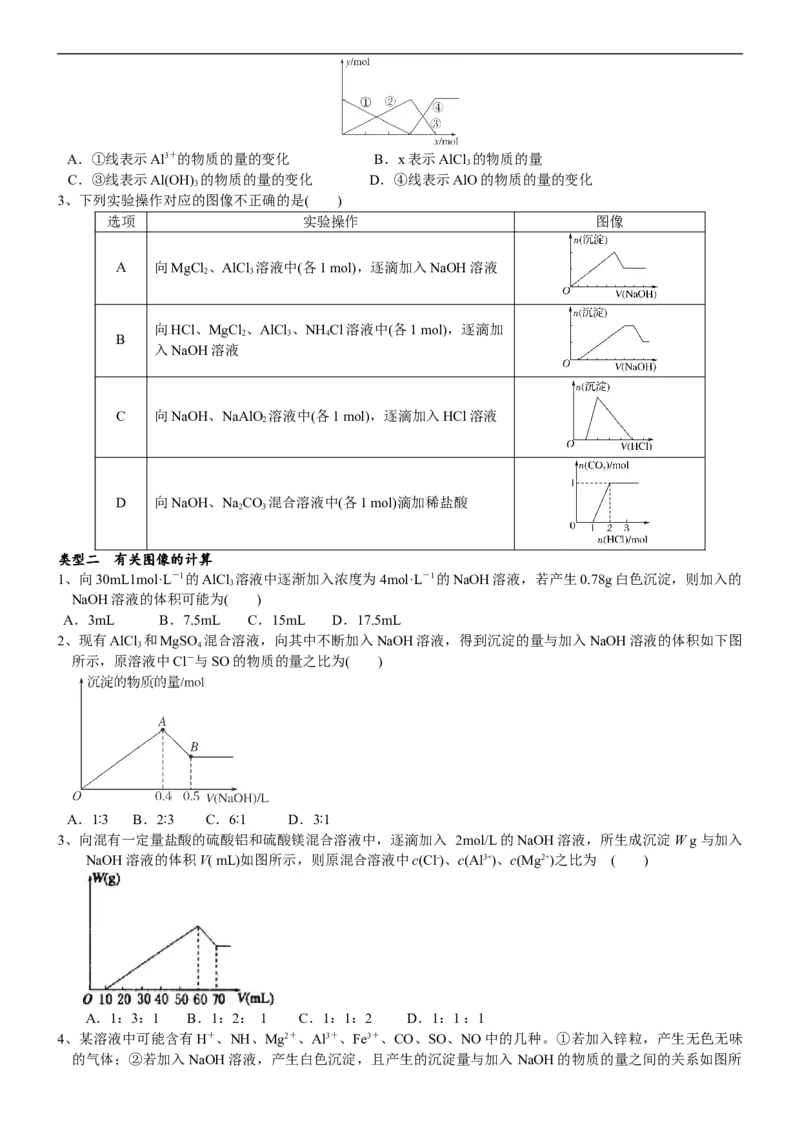
3A.①线表示Al3+的物质的量的变化 B.x表示AlCl 的物质的量
3
C.③线表示Al(OH) 的物质的量的变化 D.④线表示AlO的物质的量的变化
3
3、下列实验操作对应的图像不正确的是( )
选项 实验操作 图像
A 向MgCl 、AlCl 溶液中(各1 mol),逐滴加入NaOH溶液
2 3
向HCl、MgCl 、AlCl 、NH Cl溶液中(各1 mol),逐滴加
B 2 3 4
入NaOH溶液
C 向NaOH、NaAlO 溶液中(各1 mol),逐滴加入HCl溶液
2
D 向NaOH、NaCO 混合溶液中(各1 mol)滴加稀盐酸
2 3
类型二 有关图像的计算
1、向30mL1mol·L-1的AlCl 溶液中逐渐加入浓度为4mol·L-1的NaOH溶液,若产生0.78g白色沉淀,则加入的
3
NaOH溶液的体积可能为( )
A.3mL B.7.5mL C.15mL D.17.5mL
2、现有AlCl 和MgSO 混合溶液,向其中不断加入NaOH溶液,得到沉淀的量与加入NaOH溶液的体积如下图
3 4
所示,原溶液中Cl-与SO的物质的量之比为( )
A.1∶3 B.2∶3 C.6∶1 D.3∶1
3、向混有一定量盐酸的硫酸铝和硫酸镁混合溶液中,逐滴加入 2mol/L的NaOH 溶液,所生成沉淀W g 与加入
NaOH 溶液的体积V( mL)如图所示,则原混合溶液中c(Cl-)、c(Al3+)、c(Mg2+)之比为 ( )
A.1:3:1 B.1:2: 1 C.1:1:2 D.1:1 :1
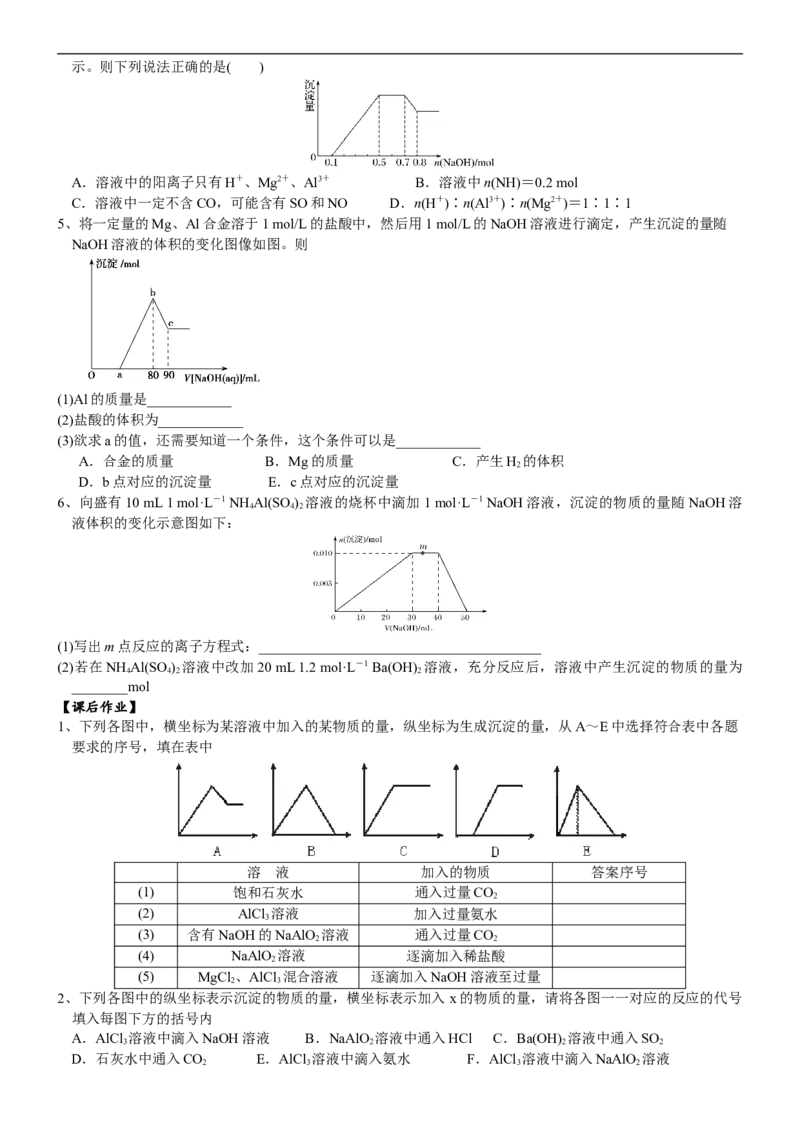
4、某溶液中可能含有H+、NH、Mg2+、Al3+、Fe3+、CO、SO、NO中的几种。①若加入锌粒,产生无色无味
的气体;②若加入NaOH溶液,产生白色沉淀,且产生的沉淀量与加入 NaOH的物质的量之间的关系如图所示。则下列说法正确的是( )
A.溶液中的阳离子只有H+、Mg2+、Al3+ B.溶液中n(NH)=0.2 mol
C.溶液中一定不含CO,可能含有SO和NO D.n(H+)∶n(Al3+)∶n(Mg2+)=1∶1∶1
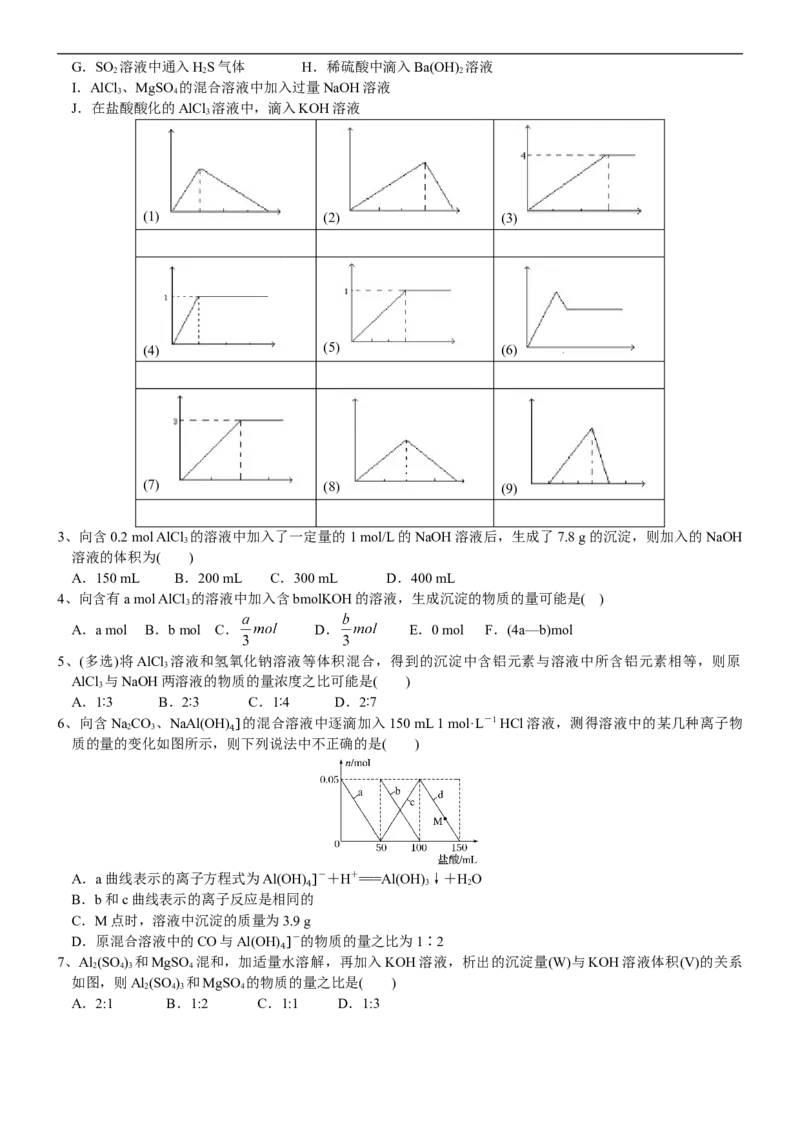
5、将一定量的Mg、Al合金溶于1 mol/L的盐酸中,然后用1 mol/L的NaOH溶液进行滴定,产生沉淀的量随
NaOH溶液的体积的变化图像如图。则
(1)Al的质量是____________
(2)盐酸的体积为____________
(3)欲求a的值,还需要知道一个条件,这个条件可以是____________
A.合金的质量 B.Mg的质量 C.产生H 的体积
2
D.b点对应的沉淀量 E.c点对应的沉淀量
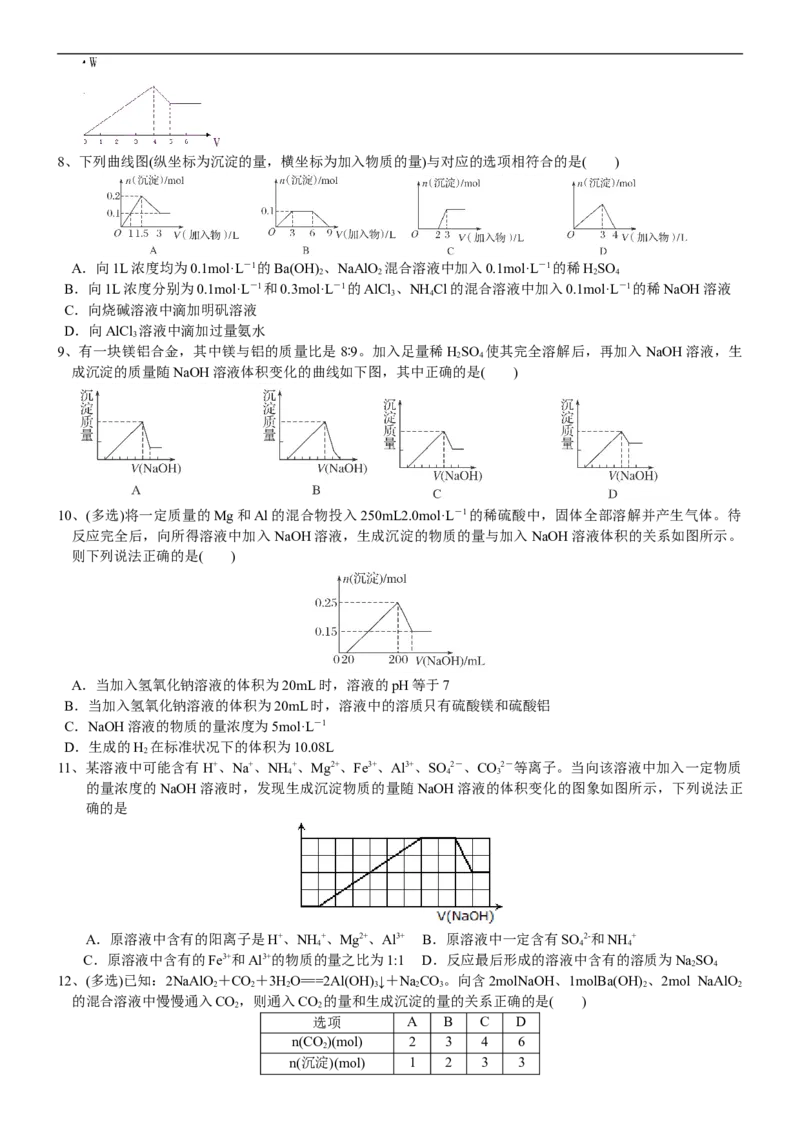
6、向盛有10 mL 1 mol·L-1 NHAl(SO ) 溶液的烧杯中滴加1 mol·L-1 NaOH溶液,沉淀的物质的量随NaOH溶
4 4 2
液体积的变化示意图如下:
(1)写出m点反应的离子方程式:________________________________________
(2)若在NH Al(SO ) 溶液中改加20 mL 1.2 mol·L-1 Ba(OH) 溶液,充分反应后,溶液中产生沉淀的物质的量为
4 4 2 2
________mol
【课后作业】
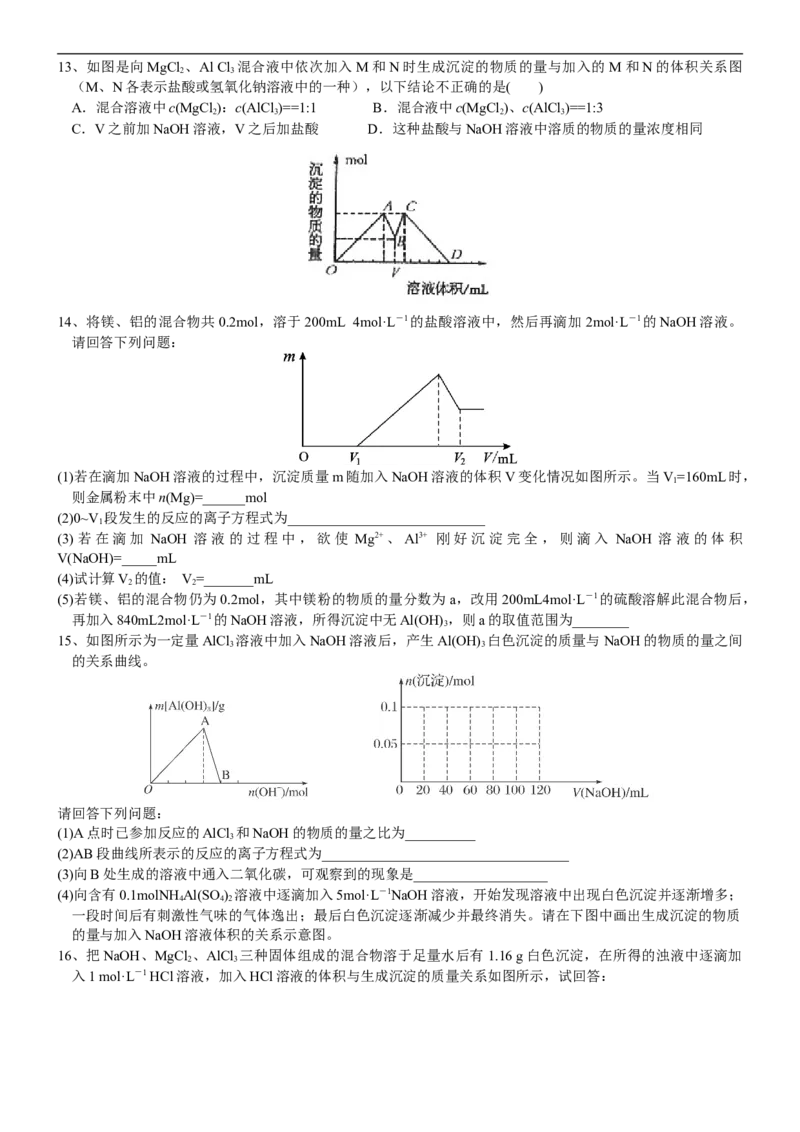
1、下列各图中,横坐标为某溶液中加入的某物质的量,纵坐标为生成沉淀的量,从A~E中选择符合表中各题
要求的序号,填在表中
溶 液 加入的物质 答案序号
(1) 饱和石灰水 通入过量CO
2
(2) AlCl 溶液 加入过量氨水
3
(3) 含有NaOH的NaAlO 溶液 通入过量CO
2 2
(4) NaAlO 溶液 逐滴加入稀盐酸
2
(5) MgCl 、AlCl 混合溶液 逐滴加入NaOH溶液至过量
2 3
2、下列各图中的纵坐标表示沉淀的物质的量,横坐标表示加入 x的物质的量,请将各图一一对应的反应的代号
填入每图下方的括号内
A.AlCl 溶液中滴入NaOH溶液 B.NaAlO 溶液中通入HCl C.Ba(OH) 溶液中通入SO
3 2 2 2
D.石灰水中通入CO E.AlCl 溶液中滴入氨水 F.AlCl 溶液中滴入NaAlO 溶液
2 3 3 2G.SO 溶液中通入HS气体 H.稀硫酸中滴入Ba(OH) 溶液
2 2 2
I.AlCl 、MgSO 的混合溶液中加入过量NaOH溶液
3 4
J.在盐酸酸化的AlCl 溶液中,滴入KOH溶液
3
(1) (2) (3)
(4) (5) (6)
(7) (8) (9)
3、向含0.2 mol AlCl 的溶液中加入了一定量的1 mol/L的NaOH溶液后,生成了7.8 g的沉淀,则加入的NaOH
3
溶液的体积为( )
A.150 mL B.200 mL C.300 mL D.400 mL
4、向含有a mol AlCl 的溶液中加入含bmolKOH的溶液,生成沉淀的物质的量可能是( )
3
A.a mol B.b mol C. D. E.0 mol F.(4a—b)mol
5、(多选)将AlCl 溶液和氢氧化钠溶液等体积混合,得到的沉淀中含铝元素与溶液中所含铝元素相等,则原
3
AlCl 与NaOH两溶液的物质的量浓度之比可能是( )
3
A.1∶3 B.2∶3 C.1∶4 D.2∶7
6、向含NaCO 、NaAl(OH) ]的混合溶液中逐滴加入150 mL 1 mol·L-1 HCl溶液,测得溶液中的某几种离子物
2 3 4
质的量的变化如图所示,则下列说法中不正确的是( )
A.a曲线表示的离子方程式为Al(OH) ]-+H+===Al(OH) ↓+HO
4 3 2
B.b和c曲线表示的离子反应是相同的
C.M点时,溶液中沉淀的质量为3.9 g
D.原混合溶液中的CO与Al(OH) ]-的物质的量之比为1∶2
4
7、Al (SO ) 和MgSO 混和,加适量水溶解,再加入KOH溶液,析出的沉淀量(W)与KOH溶液体积(V)的关系
2 4 3 4
如图,则Al (SO ) 和MgSO 的物质的量之比是( )
2 4 3 4
A.2:1 B.1:2 C.1:1 D.1:38、下列曲线图(纵坐标为沉淀的量,横坐标为加入物质的量)与对应的选项相符合的是( )
A.向1L浓度均为0.1mol·L-1的Ba(OH) 、NaAlO 混合溶液中加入0.1mol·L-1的稀HSO
2 2 2 4
B.向1L浓度分别为0.1mol·L-1和0.3mol·L-1的AlCl 、NH Cl的混合溶液中加入0.1mol·L-1的稀NaOH溶液
3 4
C.向烧碱溶液中滴加明矾溶液
D.向AlCl 溶液中滴加过量氨水
3
9、有一块镁铝合金,其中镁与铝的质量比是 8∶9。加入足量稀HSO 使其完全溶解后,再加入NaOH溶液,生
2 4
成沉淀的质量随NaOH溶液体积变化的曲线如下图,其中正确的是( )
10、(多选)将一定质量的Mg和Al的混合物投入250mL2.0mol·L-1的稀硫酸中,固体全部溶解并产生气体。待
反应完全后,向所得溶液中加入NaOH溶液,生成沉淀的物质的量与加入NaOH溶液体积的关系如图所示。
则下列说法正确的是( )
A.当加入氢氧化钠溶液的体积为20mL时,溶液的pH等于7
B.当加入氢氧化钠溶液的体积为20mL时,溶液中的溶质只有硫酸镁和硫酸铝
C.NaOH溶液的物质的量浓度为5mol·L-1
D.生成的H 在标准状况下的体积为10.08L
2
11、某溶液中可能含有H+、Na+、NH +、Mg2+、Fe3+、Al3+、SO 2-、CO2-等离子。当向该溶液中加入一定物质
4 4 3
的量浓度的NaOH溶液时,发现生成沉淀物质的量随NaOH溶液的体积变化的图象如图所示,下列说法正
确的是
A.原溶液中含有的阳离子是H+、NH +、Mg2+、Al3+ B.原溶液中一定含有SO 2-和NH +
4 4 4
C.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1 D.反应最后形成的溶液中含有的溶质为NaSO
2 4
12、(多选)已知:2NaAlO +CO+3HO===2Al(OH) ↓+NaCO。向含2molNaOH、1molBa(OH) 、2mol NaAlO
2 2 2 3 2 3 2 2
的混合溶液中慢慢通入CO,则通入CO 的量和生成沉淀的量的关系正确的是( )
2 2
选项 A B C D
n(CO)(mol) 2 3 4 6
2
n(沉淀)(mol) 1 2 3 313、如图是向MgCl 、Al Cl 混合液中依次加入M和N时生成沉淀的物质的量与加入的M和N的体积关系图
2 3
(M、N各表示盐酸或氢氧化钠溶液中的一种),以下结论不正确的是( )
A.混合溶液中c(MgCl ):c(AlCl )==1:1 B.混合液中c(MgCl )、c(AlCl )==1:3
2 3 2 3
C.V之前加NaOH溶液,V之后加盐酸 D.这种盐酸与NaOH溶液中溶质的物质的量浓度相同
14、将镁、铝的混合物共0.2mol,溶于200mL 4mol·L-1的盐酸溶液中,然后再滴加2mol·L-1的NaOH溶液。
请回答下列问题:
(1)若在滴加NaOH溶液的过程中,沉淀质量m随加入NaOH溶液的体积V变化情况如图所示。当V=160mL时,
1
则金属粉末中n(Mg)=______mol
(2)0~V 段发生的反应的离子方程式为____________________________
1
(3)若在滴加 NaOH 溶液的过程中,欲使 Mg2+、Al3+ 刚好沉淀完全,则滴入 NaOH 溶液的体积
V(NaOH)=_____mL
(4)试计算V 的值: V=_______mL
2 2
(5)若镁、铝的混合物仍为0.2mol,其中镁粉的物质的量分数为a,改用200mL4mol·L-1的硫酸溶解此混合物后,
再加入840mL2mol·L-1的NaOH溶液,所得沉淀中无Al(OH) ,则a的取值范围为________
3
15、如图所示为一定量AlCl 溶液中加入NaOH溶液后,产生Al(OH) 白色沉淀的质量与NaOH的物质的量之间
3 3
的关系曲线。
请回答下列问题:
(1)A点时已参加反应的AlCl 和NaOH的物质的量之比为__________
3
(2)AB段曲线所表示的反应的离子方程式为___________________________________
(3)向B处生成的溶液中通入二氧化碳,可观察到的现象是___________________
(4)向含有0.1molNH Al(SO ) 溶液中逐滴加入5mol·L-1NaOH溶液,开始发现溶液中出现白色沉淀并逐渐增多;
4 4 2
一段时间后有刺激性气味的气体逸出;最后白色沉淀逐渐减少并最终消失。请在下图中画出生成沉淀的物质
的量与加入NaOH溶液体积的关系示意图。
16、把NaOH、MgCl 、AlCl 三种固体组成的混合物溶于足量水后有 1.16 g白色沉淀,在所得的浊液中逐滴加
2 3
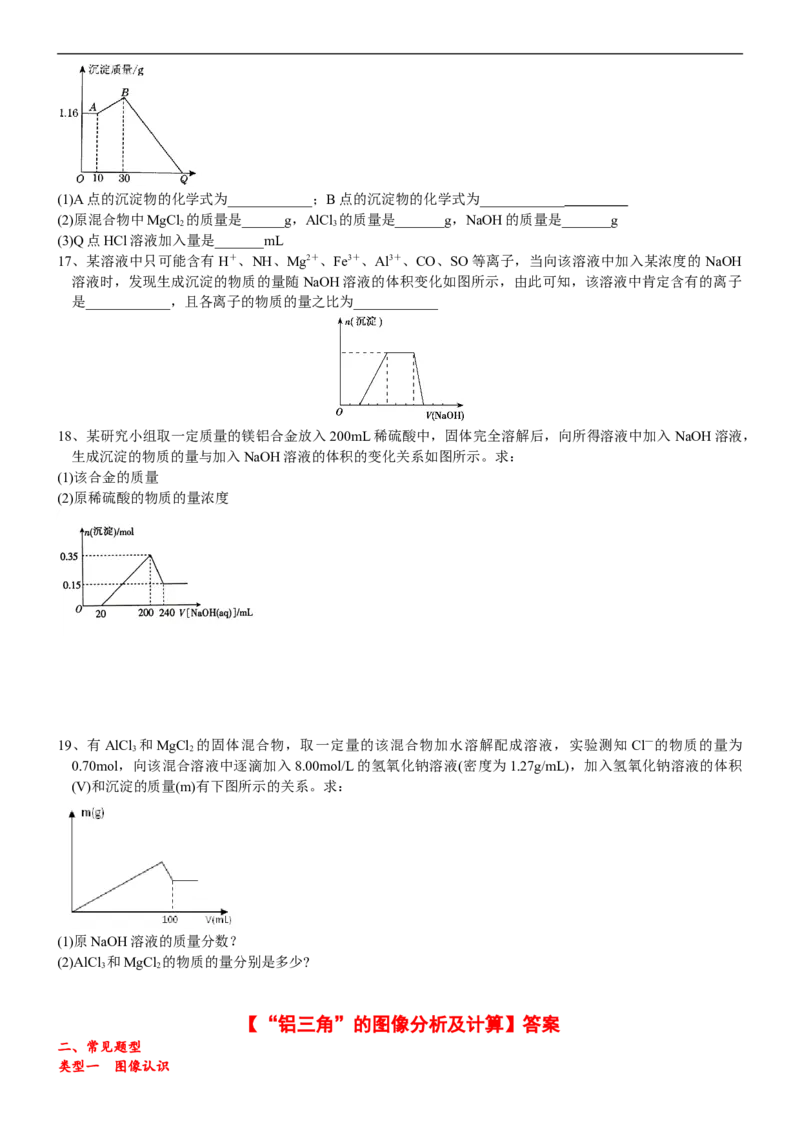
入1 mol·L-1 HCl溶液,加入HCl溶液的体积与生成沉淀的质量关系如图所示,试回答:(1)A点的沉淀物的化学式为____________;B点的沉淀物的化学式为____________
(2)原混合物中MgCl 的质量是______g,AlCl 的质量是_______g,NaOH的质量是_______g
2 3
(3)Q点HCl溶液加入量是_______mL
17、某溶液中只可能含有H+、NH、Mg2+、Fe3+、Al3+、CO、SO等离子,当向该溶液中加入某浓度的 NaOH
溶液时,发现生成沉淀的物质的量随NaOH溶液的体积变化如图所示,由此可知,该溶液中肯定含有的离子
是____________,且各离子的物质的量之比为____________
18、某研究小组取一定质量的镁铝合金放入200mL稀硫酸中,固体完全溶解后,向所得溶液中加入NaOH溶液,
生成沉淀的物质的量与加入NaOH溶液的体积的变化关系如图所示。求:
(1)该合金的质量
(2)原稀硫酸的物质的量浓度
19、有AlCl 和MgCl 的固体混合物,取一定量的该混合物加水溶解配成溶液,实验测知 Cl—的物质的量为
3 2
0.70mol,向该混合溶液中逐滴加入8.00mol/L的氢氧化钠溶液(密度为1.27g/mL),加入氢氧化钠溶液的体积
(V)和沉淀的质量(m)有下图所示的关系。求:
(1)原NaOH溶液的质量分数?
(2)AlCl 和MgCl 的物质的量分别是多少?
3 2
【“铝三角”的图像分析及计算】答案
二、常见题型
类型一 图像认识1、D
2、B。解析:AlCl 溶液与NaOH溶液混合有两种方式:向AlCl 溶液中缓慢滴加NaOH溶液,开始有沉淀生成
3 3
后沉淀溶解,且生成沉淀与沉淀溶解消耗的NaOH的物质的量之比为3∶1,显然符合题意,则x表示NaOH的物
质的量,B项错误;另一种方式是向NaOH溶液中缓慢滴加AlCl 溶液,开始没有沉淀,后有沉淀生成,与本题
3
图示情况不符。
3、D。解析:A项,向MgCl 、AlCl 溶液中加入NaOH溶液,会产生Al(OH) 、Mg(OH) 沉淀,当NaOH溶液
2 3 3 2
过量时,Al(OH) 沉淀又逐渐溶解,最后只剩余Mg(OH) 沉淀,图像与反应事实符合,正确;B项,向HCl、
3 2
MgCl 、AlCl 、NH Cl溶液中加入NaOH溶液,首先与HCl反应,无沉淀产生,然后产生Al(OH) 、Mg(OH) 沉
2 3 4 3 2
淀,再生成NH ·H O,最后Al(OH) 沉淀溶解,只有Mg(OH) 沉淀,图像与反应事实符合,正确;C项,向
3 2 3 2
NaOH、NaAlO 溶液中加入HCl溶液,首先与NaOH反应,没有沉淀生成,然后与AlO反应生成Al(OH) 沉淀,
2 3
HCl溶液过量后,Al(OH) 沉淀完全溶解,图像与反应事实符合,正确;D项,向NaOH、NaCO 混合溶液中滴
3 2 3
加稀盐酸,首先与NaOH反应,没有气体生成,后与NaCO 反应生成NaHCO ,没有气体生成,再与NaHCO
2 3 3 3
生成气体,图像与反应事实不符合,符合题意。
类型二 有关图像的计算
1、B。解析:解法一:把该题的信息转化为图像,用图像法求解,如图所示:
当生成沉淀0.01mol时需NaOH0.03mol或0.11mol,显然B项符合题意。
解法二:已知n(AlCl )=0.03mol,n[Al(OH) ]=0.01mol,由沉淀的物质的量小于氯化铝的物质的量可推知此题
3 3
可能有两个答案:一是氢氧化钠不足,二是氢氧化钠过量。
当碱的量不足时,则V(NaOH)=L=0.0075L=7.5mL;当碱过量时,则V(NaOH)=L=0.0275L=27.5mL。
2、C。解析:OA上升的直线表示Al(OH) 和Mg(OH) 一起沉淀,AB下降的直线表示Al(OH) 沉淀溶解,B点
3 2 3
表示Al(OH) 完全溶解。AB段完全溶解Al(OH) 消耗NaOH0.1L,则Al3+生成Al(OH) 消耗NaOH0.3L,沉淀
3 3 3
Mg2+消耗NaOH0.1L,因而n(AlCl )∶n(MgSO )=2∶1,所以,n(Cl-)∶n(SO)=6∶1。
3 4
3、D
4、B。解析:由①知溶液中一定含有H+,一定没有CO、NO,由②及图像知溶液中一定含有Mg2+、Al3+和
NH,且n(NH)=0.7 mol-0.5 mol=0.2 mol,n(H+)=0.1 mol,n(Al3+)=0.8 mol-0.7 mol=0.1 mol,沉淀Al3+、
Mg2+共消耗0.4 mol OH-,其中沉淀Al3+消耗0.3 mol OH-,沉淀Mg2+消耗0.1 mol OH-,根据Mg2+~2OH-,
可得n(Mg2+)=0.05 mol,故只有选项B正确。
5、(1)0.27g
(2)80ml
(3)ABDE
6、(1)NH+OH-===NH·HO
3 2
(2)0.022
解析:(2)因NH Al(SO ) 的物质的量为0.01 L×1 mol·L-1=0.01 mol,Ba(OH) 的物质的量为0.02 L×1.2 mol·L-1
4 4 2 2
=0.024 mol,产生沉淀的反应有两类,一是SO+Ba2+===BaSO ↓,n(SO)=0.01 mol×2=0.02 mol,0.02 mol<
4
0.024 mol,故n(BaSO)=0.02 mol;二是OH-参与的反应,
4
Al3+ + 3OH- === Al(OH) ↓
3
0.01 mol 0.03 mol 0.01 mol
OH-余0.024 mol×2-0.03 mol=0.018 mol,之后发生反应:NH+OH-===NH·H O,n(NH)=0.01 mol,再消耗
3 2
OH- 0.01 mol,则剩余OH-为0.018 mol-0.01 mol=0.008 mol,最后发生沉淀的溶解:Al(OH) +OH-===AlO
3
+2HO,OH-为0.008 mol,溶解Al(OH) 0.008 mol,则剩余Al(OH) 为0.01 mol-0.008 mol=0.002 mol。溶液
2 3 3
中产生沉淀的物质的量为0.02 mol+0.002 mol=0.022 mol。
【课后作业】
1、(1)B (2)C (3)D (4)E (5)A
2、(1)B (2)A (3)F (4)H (5)E (6)I (7)G (8)CD (9)J
3、C4、ACDEF
5、BD
6、D。解析:NaCO 、NaAl(OH) ]的混合溶液中加入HCl溶液,先发生反应:Al(OH) ]-+H+===Al(OH) ↓+
2 3 4 4 3
HO,a曲线表示Al(OH) ]-减少,Al(OH) ]-反应完毕后,发生反应:CO+H+===HCO,b曲线表示CO减少,c
2 4 4
曲线表示HCO增加,CO反应完毕后,发生反应:HCO+H+===CO ↑+HO,d曲线表示HCO减少,此阶段
2 2
Al(OH) 不参与反应,A、B项正确;加入盐酸50 mL时NaAl(OH) ]中铝元素全部转化为氢氧化铝沉淀,加50
3 4
mL盐酸之后CO反应,氢氧化铝沉淀不溶解,则M点沉淀的质量和加入盐酸50 mL时沉淀的质量相同,由
NaAl(OH))]+HCl===NaCl+Al(OH) ↓+HO知,nAl(OH) ]=n{NaAl(OH)) ]}=n(HCl)=0.05 mol,mAl(OH) ]=
4 3 2 3 4 3
0.05 mol×78 g·mol-1=3.9 g,C项正确;Al(OH)) ]-与CO消耗的盐酸的体积都是50 mL,所以消耗的氯化氢的
4
物质的量相等,依据反应Al(OH)) ]-+H+===Al(OH) ↓+HO、CO+H+===HCO可知CO与Al(OH) ]-的物质的
4 3 2 4
量之比为1∶1,但Al(OH))]-与CO都发生水解,水解程度不同导致无法判断原混合溶液中CO与Al(OH) ]-的物
4 4
质的量之比,D项错误。
7、C
8、A。解析:A项,Ba(OH) 和NaAlO 中加入HSO ,发生的反应依次为Ba2++2OH-+2H++SO===BaSO ↓+
2 2 2 4 4
2HO、AlO+H++HO===Al(OH) ↓、Al(OH) +3H+===Al3++3HO,所以加1LHSO 时,Ba(OH) 反应完,再
2 2 3 3 2 2 4 2
加 0.5LH SO 时 AlO 参加反应,再加 1.5LH SO 时,Al(OH) 全部溶解,A 正确;B 项,向 1L 浓度分别为
2 4 2 4 3
0.1mol·L-1和0.3mol·L-1的AlCl 、NH Cl的混合溶液中加入0.1mol·L-1的NaOH溶液,发生的反应依次是Al3+
3 4
+3OH-===Al(OH) ↓、OH-+NH===NH·H O、Al(OH) +OH-===AlO+2HO,所以沉淀Al3+和溶解Al(OH)
3 3 2 3 2 3
所用NaOH的量之比为3∶1,而图像上看到的是1∶1,B错误;C项,向烧碱溶液中滴加明矾溶液,发生的反应依
次是Al3++4OH-===AlO+2HO、Al3++3AlO+6HO===4Al(OH) ↓,C错误;D项,AlCl 溶液中滴加过量氨水,
2 2 3 3
沉淀不会溶解,D错误。
9、A。解析:镁与铝的质量比是 8∶9,则物质的量之比是 1∶1,NaOH溶液过量后 Al(OH) 完全溶解,只有
3
Mg(OH) ,B错;等物质的量的Mg(OH) 与Al(OH) 的质量之比是58∶78,即剩余的Mg(OH) 的质量小于沉淀最
2 2 3 2
大质量的,排除C、D,故选A。
10、CD。解析:从图像可以看出加入的 NaOH溶液先将过量的HSO 中和,此时溶液中的溶质为 MgSO 、
2 4 4
Al (SO ) 和NaSO ,但是此时因Al3+、Mg2+水解使溶液呈酸性,A、B项错误;当加入NaOH溶液的体积为
2 4 3 2 4
200mL时,此时溶质只有NaSO ,根据元素守恒,可得n(NaOH)=2n(H SO ),c(NaOH)×0.2L=2×2.0mol·L-
2 4 2 4
1×0.25L,则c(NaOH)=5mol·L-1,C项正确;用于生成氢气的硫酸的物质的量为0.18L×5mol·L-1÷2=0.45mol,
即H 的物质的量,标况下氢气的体积为0.45mol×22.4L·mol-1=10.08L,D项正确。
2
11、B
12、AC
解析:向含2molNaOH、1molBa(OH) 、2molNa[Al(OH) ]的混合溶液中慢慢通入CO 发生反应依次为
2 4 2
2NaOH +CO ―→ NaCO+HO
2 2 3 2
2mol1mol1mol
Ba(OH) + CO ―→ BaCO ↓+HO
2 2 3 2
1mol1mol1mol
2Na[Al(OH)]+CO―→2Al(OH) ↓+NaCO+HO
4 2 3 2 3 2
2mol1mol2mol1mol
NaCO+CO+HO―→2NaHCO
2 3 2 2 3
1mol1mol
BaCO +CO+HO―→Ba(HCO )
3 2 2 3 2
1mol1mol
当通入2molCO 时,生成1molBaCO 沉淀;
2 3
当通入3molCO 时,生成1molBaCO 沉淀和2molAl(OH) 沉淀;
2 3 3
当通入4molCO 时,生成1molBaCO 沉淀和2molAl(OH) 沉淀;
2 3 3
当通入5molCO 时,生成2molAl(OH) 沉淀;当通入6molCO 时,BaCO 已完全反应,Al(OH) 量不变,即仍为
2 3 2 3 3
2mol沉淀。
13、B
14、(1)0.12(2)H++OH-===H O
2
(3)400
(4)440
(5)0.6≤a<1
解析:在0~V 段没有沉淀生成,是NaOH溶液与过量的盐酸反应n(HCl)=n(NaOH)=0.16L3mol/L=0.32mol,那么
1
与镁、铝的混合物反应的盐酸的物质的量为:0.2L×4mol·L—1-0.32mol=0.48mol,(1)设镁、铝的物质的量分别为
xmol、ymol,根据:Mg +2 H+ =Mg 2+ +H ↑,2Al + 6H+ =Al3++ 3H ↑,
2 2
x 2x y 3y
则有:x+y=0.2 2x + 3y=0.48 得:x=0.12 mol y=0.08mol。(2)0~V 段是NaOH溶液与过量的盐酸反应,离子
1
方程式为:H++OH-=HO(3)Mg 2+ +2OH-=Mg(OH)2↓, Al3+ + 3 OH-=Al(OH) ↓, 0.12 mol 的Mg 2+和0.08mol的
2 3
Al3+刚好沉淀需要的NaOH物质的量为:0.12mol×2+0.08mol×3=0.48mol,总共需要的NaOH的物质的量为:
0.48mol+0.32mol=0.8mol,NaOH 溶液的体积为:0.8mol÷2mol·L=0.4L=400 mL;(4)继续加入 NaOH 溶液,
Al(OH) 发生溶解,0.08mol的Al(OH) 溶解需要0.08mol的NaOH物质的量为:0.08mol ,Al(OH) 刚好溶解消耗
3 3 3
的NaOH的物质的量为:0.8+0.08=0.88mol,体积为:0.88mol÷2mol·L=0.44L=440 mL;
15、(1)1∶3
(2)Al(OH) +OH-===AlO+2HO
3 2
(3)生成白色沉淀
(4)
16、(1)Mg(OH) Mg(OH) 和 Al(OH)
2 2 3
(2)1.90 2.67 5.20
(3)130
解析:由图像中当消耗10mL盐酸时沉淀的质量不变,确定原溶液中NaOH过量,A点时混合体系中存在Mg
(OH) 沉淀、NaOH和NaAlO 的混合液,且AB段的发生反应:AlO-+H++H O=Al(OH) ↓,所以B点时的沉
2 2 2 2 3
淀物为Mg(OH) 和 Al(OH) ;BQ段发生反应:Mg(OH) +2H+=Mg2++2H O和Al(OH) +3H+=Al3++3H O;
2 3 2 2 3 2
解题过程:1.16g沉淀为Mg(OH) ,n(Mg(OH) )=1.16g/58g/mol=0.02mol,原溶液中n(MgCl )=0.02mol,m
2 2 2
(MgCl )=n×M=0.02mol×95g/mol=1.90g;发生反应:Mg(OH) +2H+=Mg2++2H O时消耗n(HCl)=0.04mol,由
2 2 2
于AB段发生反应:AlO-+H++H O=Al(OH) ↓,消耗n(HCl)=c×V=1mol/L×(30-10)mL×10-3=0.02mol,而
2 2 3
且生成n(Al(OH) )=0.02mol,原溶液中n(AlCl )=0.02mol,m(AlCl )=n×M=0.02mol×133.5g/mol=2.67g;
3 3 3
当 发 生 反 应 : Al(OH) +3H+=Al3++3H O 时 消 耗 n ( HCl ) =0.06mol , 所 以 BQ 段 消 耗 n ( HCl )
3 2
=0.04+0.06=0.1mol,V=n/C=0.1mol/1mol/L=0.1L,即100mL,确定Q点时HCl的总加入量为100mL+30mL=130mL;
计算原溶液中n (OH-):原溶液中过量的n(OH-)为0.01mol,沉淀Mg2+消耗的n(OH-)= n(Mg(OH) )
总 2
×2=0.0.04mol ; 发 生 反 应 : Al3++4OH-=AlO2-+2H O 消 耗 n ( OH- ) =0.02×4=0.08mol , n ( OH- )
2 总
=0.01+0.04+0.08=0.13mol,m(NaOH)=n×M=0.13mol×40g/mol=5.20g.
17、H+、Al3+、NH、SO 2:1:3:4
18、(1)9g
(2)2.5mol/L
过程:(1)加入过量NaOH溶液,最终生成的沉淀只有Mg(OH) ,
2
故Mg(OH) 为0.15mol
2
∴生成的Al(OH) 最多为0.35mol-0.15mol=0.2mol
3
合金中含有0.15molMg和0.2molAl
合金的质量为
(2)由于加入200mL~240mLNaOH溶液时,发生反应:
NaOH+Al(OH) =NaAlO +2H O
3 2 2
得c(NaOH)=根据图示知:加入200mLNaOH溶液时,所得溶液中只含有NaSO 。
2 4
溶液中含有NaSO : ,即SO 2-为0.5mol
2 4 4
所以原稀硫酸中含HSO 0.5mol
2 4
c(HSO )=
2 4
答:合金的质量为9g;原稀硫酸的物质的量浓度为2.5mol/L
19、(1)25.2%
(2)0.1mol 0.2mol
解析:(1)根据 可知氢氧化钠溶液的质量分数= ,即质量分数是
25.2%。
(2)根据图像可知当加入100ml氢氧化钠溶液时沉淀质量不再发生变化,这说明此时所得沉淀是氢氧化镁,溶
液中的溶质是氯化钠和偏铝酸钠。根据氯离子守恒可知氯化钠是 0.7mol。氢氧化钠共计是0.8mol,所以根据钠
离子守恒可知偏铝酸钠是0.8mol—0.7mol=0.1mol,因此根据铝原子守恒可知氯化铝的物质的量是 0.1mol,所
以氯化镁的物质的量是(0.7mol—0.1mol×3)÷2=0.2mol。