文档内容
2018 年陕西省中考化学副题
可能用到的相对原子质量:H-1 O-16 Na-23 Mg-24 Al-27 Cl-35.5
一、选择题(共7小题,每小题2分,计14分。每小题只有一个选项是符合题意的)
1. 我国2018年世界环境日的主题是“美丽中国,行动有我”。下列做法不符合这一主题的是
A. 发展公共交通,提倡绿色出行 B. 积极植树造林,美化生态环境
C. 推行垃圾分类,回收利用资源 D. 就地焚烧秸杆,增加土壤肥效
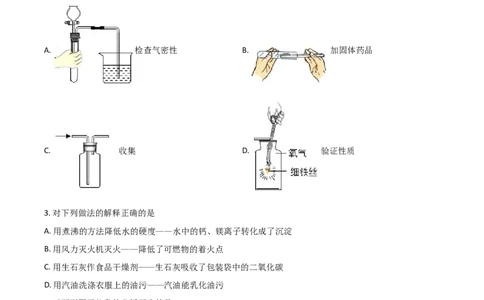
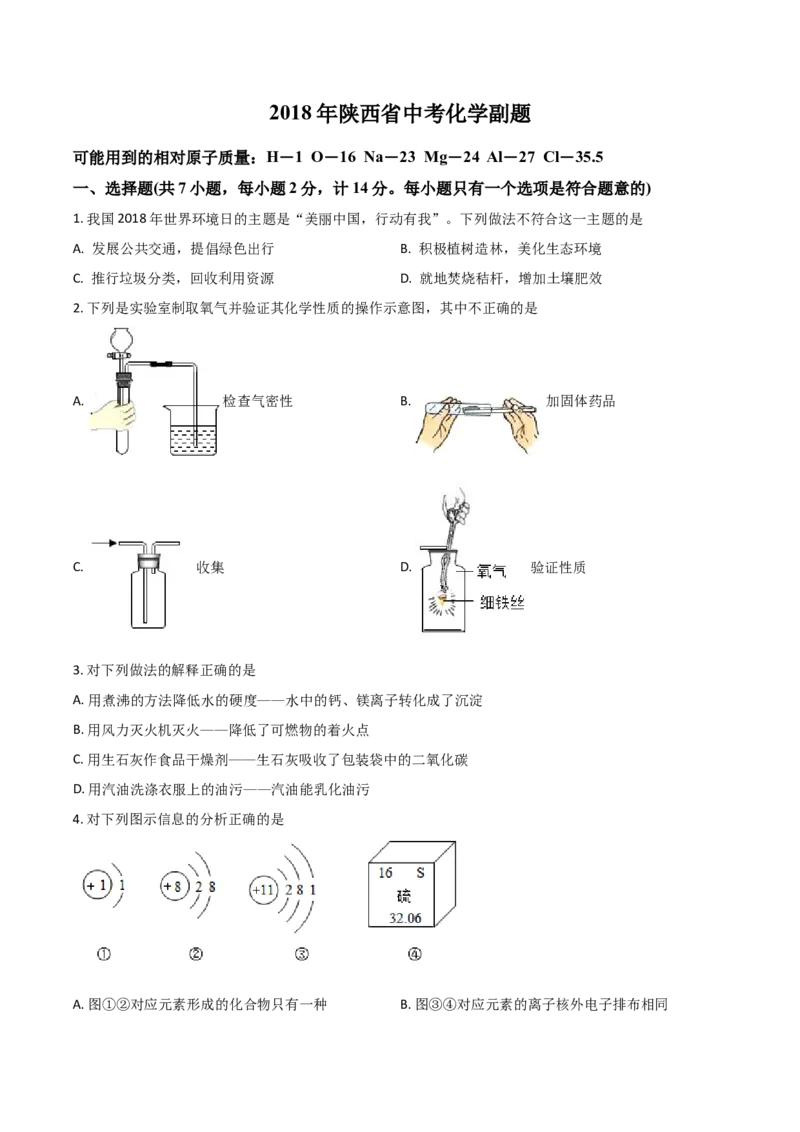
2. 下列是实验室制取氧气并验证其化学性质的操作示意图,其中不正确的是
A. 检查气密性 B. 加固体药品
C. 收集 D. 验证性质
3. 对下列做法的解释正确的是
A. 用煮沸的方法降低水的硬度——水中的钙、镁离子转化成了沉淀
B. 用风力灭火机灭火——降低了可燃物的着火点
C. 用生石灰作食品干燥剂——生石灰吸收了包装袋中的二氧化碳
D. 用汽油洗涤衣服上的油污——汽油能乳化油污
4. 对下列图示信息的分析正确的是
A. 图①②对应元素形成的化合物只有一种 B. 图③④对应元素的离子核外电子排布相同C. 图①③对应元素的化学性质相似 D. 图①②③对应的三种元素形成的化合物水溶液
pH>7
5. 纸质电池被称为“软电池”,总反应为 。该电池采用薄层纸片
作传导体,避免了传统电池带来的污染,使用后可作为一般废弃物处理。下列说法正确的是
A. MnO 是该电池反应的催化剂 B. 电池反应中锌元素化合价升高
2
C. 电池工作时将电能转化为化学能 D. 该反应属于复分解反应
的
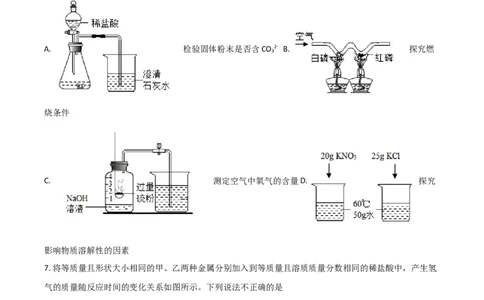
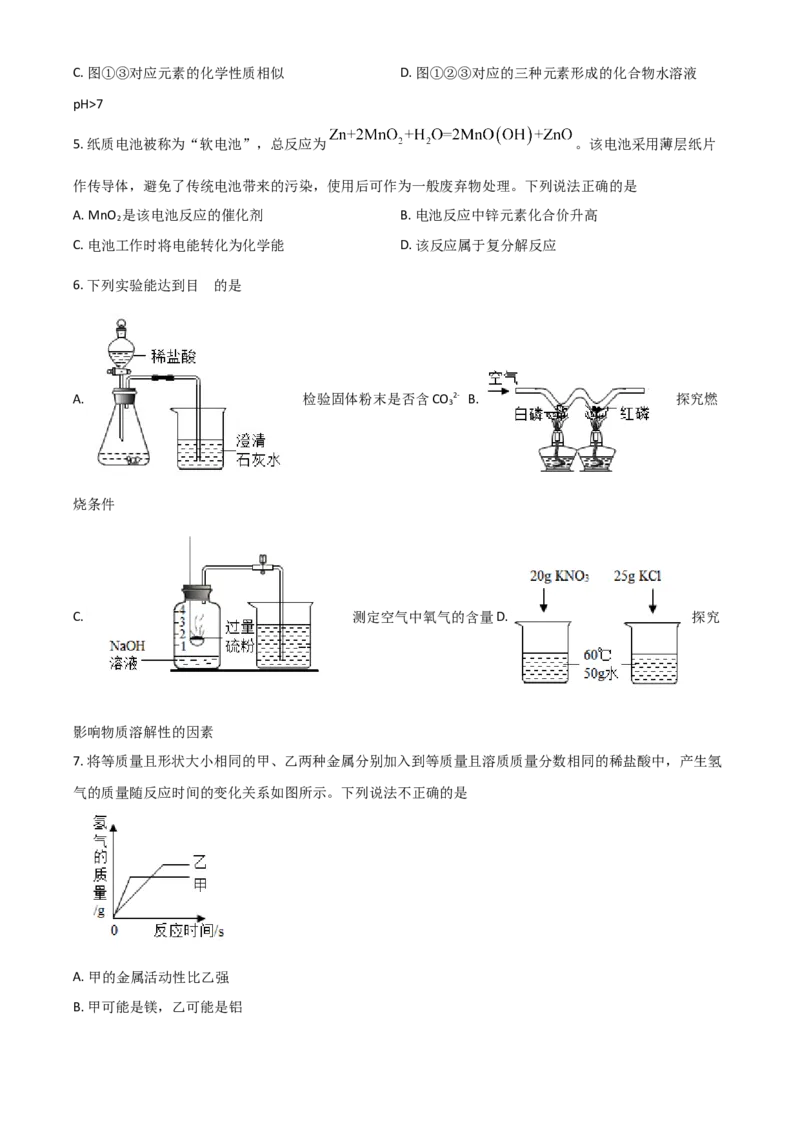
6. 下列实验能达到目 的是
A. 检验固体粉末是否含CO 2- B. 探究燃
3
烧条件
C. 测定空气中氧气的含量D. 探究
影响物质溶解性的因素
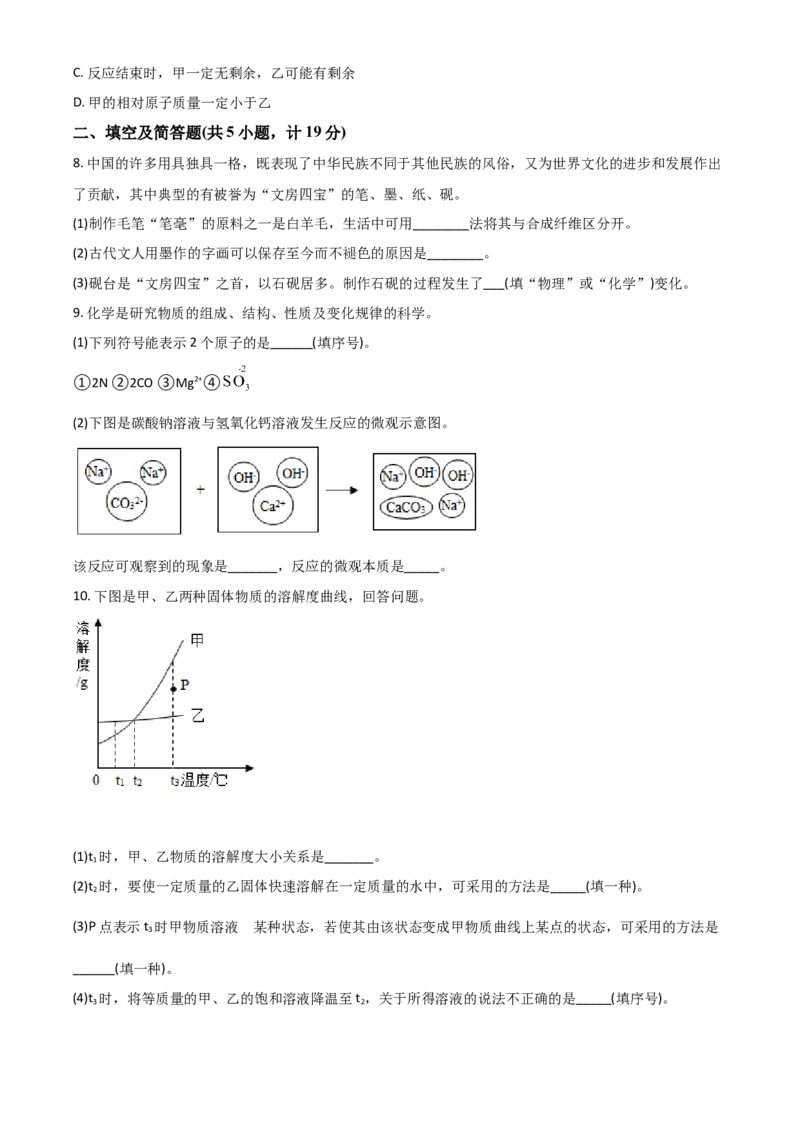
7. 将等质量且形状大小相同的甲、乙两种金属分别加入到等质量且溶质质量分数相同的稀盐酸中,产生氢
气的质量随反应时间的变化关系如图所示。下列说法不正确的是
A. 甲的金属活动性比乙强
B. 甲可能是镁,乙可能是铝C. 反应结束时,甲一定无剩余,乙可能有剩余
D. 甲的相对原子质量一定小于乙
二、填空及简答题(共5小题,计19分)
8. 中国的许多用具独具一格,既表现了中华民族不同于其他民族的风俗,又为世界文化的进步和发展作出
了贡献,其中典型的有被誉为“文房四宝”的笔、墨、纸、砚。
(1)制作毛笔“笔毫”的原料之一是白羊毛,生活中可用________法将其与合成纤维区分开。
(2)古代文人用墨作的字画可以保存至今而不褪色的原因是________。
(3)砚台是“文房四宝”之首,以石砚居多。制作石砚的过程发生了___(填“物理”或“化学”)变化。
9. 化学是研究物质的组成、结构、性质及变化规律的科学。
(1)下列符号能表示2个原子的是______(填序号)。
①2N ②2CO ③Mg2+④
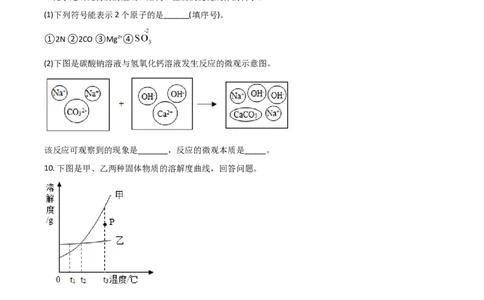
(2)下图是碳酸钠溶液与氢氧化钙溶液发生反应的微观示意图。
该反应可观察到的现象是_______,反应的微观本质是_____。
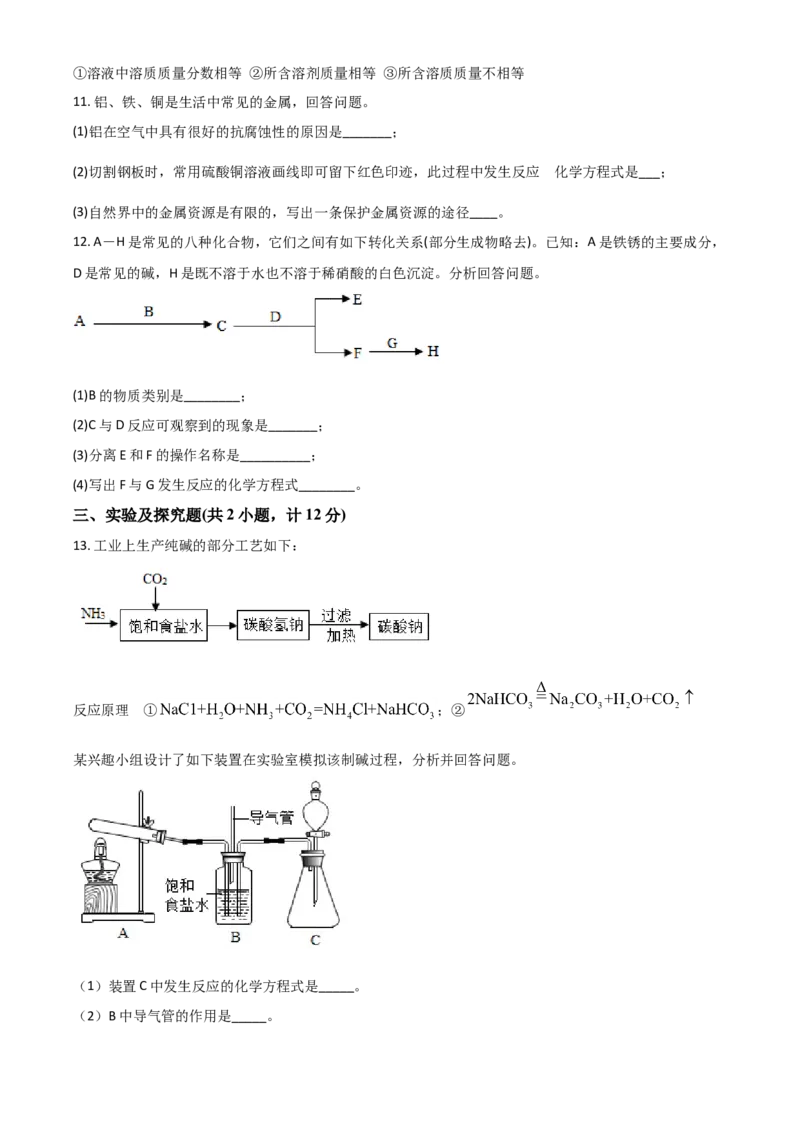
10. 下图是甲、乙两种固体物质的溶解度曲线,回答问题。
(1)t 时,甲、乙物质的溶解度大小关系是_______。
1
(2)t 时,要使一定质量的乙固体快速溶解在一定质量的水中,可采用的方法是_____(填一种)。
2
的
(3)P点表示t 时甲物质溶液 某种状态,若使其由该状态变成甲物质曲线上某点的状态,可采用的方法是
3
______(填一种)。
(4)t 时,将等质量的甲、乙的饱和溶液降温至t ,关于所得溶液的说法不正确的是_____(填序号)。
3 2①溶液中溶质质量分数相等 ②所含溶剂质量相等 ③所含溶质质量不相等
11. 铝、铁、铜是生活中常见的金属,回答问题。
(1)铝在空气中具有很好的抗腐蚀性的原因是_______;
的
(2)切割钢板时,常用硫酸铜溶液画线即可留下红色印迹,此过程中发生反应 化学方程式是___;
(3)自然界中的金属资源是有限的,写出一条保护金属资源的途径____。
12. A-H是常见的八种化合物,它们之间有如下转化关系(部分生成物略去)。已知:A是铁锈的主要成分,
D是常见的碱,H是既不溶于水也不溶于稀硝酸的白色沉淀。分析回答问题。
(1)B的物质类别是________;
(2)C与D反应可观察到的现象是_______;
(3)分离E和F的操作名称是__________;
(4)写出F与G发生反应的化学方程式________。
三、实验及探究题(共2小题,计12分)
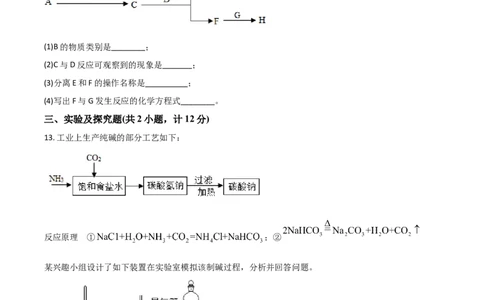
13. 工业上生产纯碱的部分工艺如下:
反应原理 ① ;②
是
某兴趣小组设计了如下装置在实验室模拟该制碱过程,分析并回答问题。
(1)装置C中发生反应的化学方程式是_____。
(2)B中导气管的作用是_____。(3)反应原理②的实验可在_____(填字母)装置中进行。
(4)反应过程中的副产品NH Cl是农业上常用的_____(填肥料种类)。
4
14. 化学课上,老师组织同学们观察铁丝、木炭、石蜡等物质分别在空气和氧气中反应的实验后,同学们
分析总结出了燃烧的特征和定义,同时得出影响反应速率的因素之一是______。为了激发学生的学习兴趣、
拓展知识视野,老师又演示了如下实验:将打磨光亮的镁条在空气中点燃后迅速伸入充满二氧化碳的集气
瓶中,观察到镁条继续燃烧,发出耀眼白光并伴有轻微爆炸声,集气瓶内壁上出现黑色颗粒,同时生成白
色固体。同学们对该实验中生成的白色固体的成分进行了探究。
【猜想假设】猜想一:氧化镁 猜想二:碳酸镁 猜想三:氢氧化镁 猜想四:氧化镁和碳酸镁
同学们讨论后,一致认为猜想三不成立,理由是_____。
【实验验证】请你和同学们一起设计并完成实验。
实验操作 实验现象 实验结论
。
______。 _______ 猜想一成立
【反思交流】
(1)请你结合已有知识和实验探究过程,写出镁在二氧化碳中燃烧的化学方程式______。
(2)综合上述实验,你对燃烧或二氧化碳性质的新认识是________(写一条)。
四、计算与分析题(5分)
15. 为测定一瓶未知浓度的盐酸的溶质质量分数,化学兴趣小组向含有酚酞的100g 4% 的氢氧化钠溶液中滴
加该盐酸,恰好完全反应时溶液总质量为150g。(酚酞质量不计)
(1)恰好完全反应时的现象是_______。
(2)计算盐酸的溶质质量分数。