文档内容
重难录 点击 蓄势
重难 而发
1.(2022·全国·高考真题)(2022·湖南·邵阳市第二中学模拟预测)将二氧化碳转化为高附加值碳基
燃料有利于实现碳中和。
已知:① ;
② ;
③ 。
(1)相关化学键的键能数据如表所示。
化学键 H—H H—O C—H
436 802 463 x
键能
则 __________ , __________。
(2)某温度下,将 和 充入容积可变的密闭容器中发生反应(设仅发生反应①和
反应②),保持体系压强为 ,反应起始时气体总体积为V L,平衡体系中 、 的物质的
量分数分别为40%、20%,则此时CO(g)的平衡分压为__________, 的浓度为__________
。
(3)将 和 充入容积可变的密闭容器中发生上述三个反应,保持体系压强为 ,
平衡体系中各气体组分的物质的量分数随温度的变化情况如图所示。
①曲线a代表平衡体系中__________(填化学式)的物质的量分数随温度的变化情况,该物质的量分数随着温度升高而减小的原因为__________。
② 时,反应②的压强平衡常数 __________(用含y、z、 的代数式表示)。
2.(2023年全国预测模拟)苯甲醛是生产氨苄青霉素、某些苯胺染料等产品的重要中间体。制备苯
甲醛的常用方法有气相催化氧化法和电催化氧化法。
I.气相催化氧化法(以Ce/ZSM-5为催化剂)主要反应:
(g)+O(g) (g)+HO(g)ΔH
2 2
(1)已知:
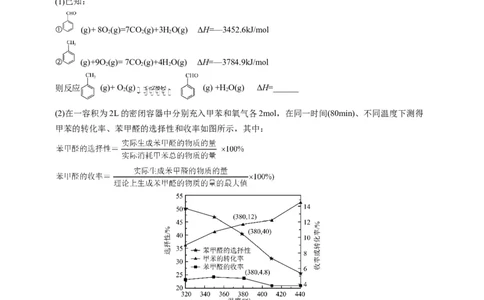
① (g)+ 8O (g)=7CO (g)+3HO(g) ΔH=—3452.6kJ/mol
2 2 2
② (g)+9O(g)= 7CO (g)+4HO(g) ΔH=—3784.9kJ/mol
2 2 2
则反应 (g)+ O (g) (g) +H O(g) ΔH=______
2 2
(2)在一容积为2L的密闭容器中分别充入甲苯和氧气各2mol,在同一时间(80min)、不同温度下测得
甲苯的转化率、苯甲醛的选择性和收率如图所示,其中:
温度控制在380℃,前80min内生成苯甲醛的平均反应速率为_______;甲苯的转化率随温度升高而
增大的原因是_______。
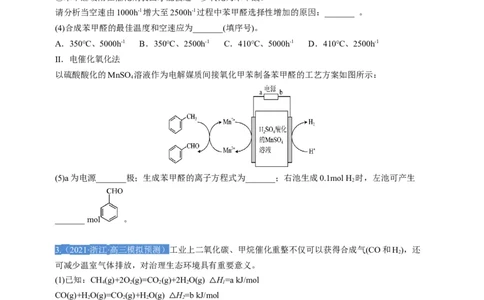
(3)其他条件相同、不同空速下测得苯甲醛的选择性和收率如图所示。已知:①空速指鼓入空气的速度,单位为h-1;
②苯甲醛吸附在催化剂表面才能被进一步氧化为苯甲酸。
请分析当空速由1000h-1增大至2500h-1过程中苯甲醛选择性增加的原因:_______ 。
(4)合成苯甲醛的最佳温度和空速应为_______(填序号)。
A.350℃、5000h-1 B.350℃、2500h-1 C.410℃、5000h-1 D.410℃、2500h-1
II.电催化氧化法
以硫酸酸化的MnSO 溶液作为电解媒质间接氧化甲苯制备苯甲醛的工艺方案如图所示:
4
(5)a为电源_______极;生成苯甲醛的离子方程式为_______;右池生成0.1mol H 时,左池可产生
2
_______ mol 。
3.(2021·浙江·高三模拟预测)工业上二氧化碳、甲烷催化重整不仅可以获得合成气(CO和H),还
2
可减少温室气体排放,对治理生态环境具有重要意义。
(1)已知:CH(g)+2O(g)=CO (g)+2HO(g) H=a kJ/mol
4 2 2 2 1
CO(g)+HO(g)=CO(g)+HO(g) H=b kJ/mol
2 2 2 2 △
2CO(g)+O(g)=2CO (g) H=c kJ/mol
2 2 3 △
催化重整反应CO(g)+CH (g)=2CO(g)+2H(g)的 H=_______。
2 △4 2 4
(2)以二氧化钛表面覆盖Cu Al O 为催化剂,还可以将CO 和CH 直接转化成乙酸。在不同温度下催
2 2 4 △ 2 4
化剂的催化效率与乙酸的生成速率如图所示。250-300℃时,温度升高而乙酸的生成速率降低的原因
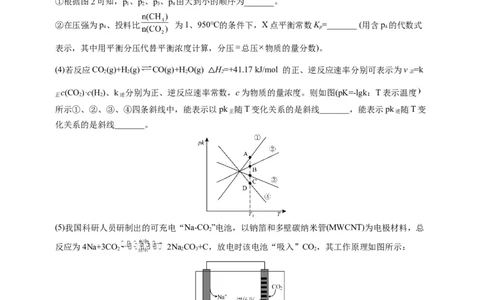
可能是_______。(3)催化重整 CO(g)+CH (g)=2CO(g)+2H(g)的反应,测得CH 的平衡转化率与温度及压强的关系如右
2 4 2 4
上图所示:
①根据图2可知,p、p、p、p 由大到小的顺序为_______。
1 2 3 4
②在压强为p、投料比 为1、950℃的条件下,X点平衡常数K =_______ (用含p 的代数式
4 p 4
表示,其中用平衡分压代替平衡浓度计算,分压 总压 物质的量分数)。
(4)若反应CO(g)+H(g) CO(g)+HO(g) H=+41.17 kJ/mol 的正、逆反应速率分别可表示为v =k
2 2 2 2 正
△
c(CO)·c(H )、k 分别为正、逆反应速率常数,c为物质的量浓度。则如图(pK=-lgk:T表示温度
正 2 2 逆
所示①、②、③、④四条斜线中,能表示以pk 随T变化关系的是斜线_______,能表示pk 随T变
正 逆
化关系的是斜线_______。
(5)我国科研人员研制出的可充电“Na-CO ”电池,以钠箔和多壁碳纳米管(MWCNT)为电极材料,总
2
反应为4Na+3CO 2NaCO+C,放电时该电池“吸入”CO,其工作原理如图所示:
2 2 3 2
放电时,正极的电极反应式为_______。
4.(2022·广东实验中学模拟预测)甲烷和氯气都是重要的化工原料。
I.CH 在光照条件下与C1 反应,可得到各种氯代甲烷。
4 2(1)CH 氯代的机理为自由基(带有单电子的原子或原子团,如C1·、·CH)反应,包括以下几步:
4 3
I.链引发 II.链传递 III.链终止
写 出
Cl∙+CH→∙CH +HCl 2Cl∙→Cl
由 4 3 2
Cl 2 2Cl∙ ∙CH 3 +Cl 2 →CH 3 Cl+Cl∙ Cl∙+∙CH 3 →CH 3 Cl CH
C …… …… l
3
生 成
CHCl 过程中链传递的方程式:_______,_______。
2 2
(2)丙烷氯代反应中链传递的一步反应能量变化如下。
推知−CH 中C−H键能比-CH-中C−H键能_______(填“大”或“小”)。
3 2
II.甲烷重整制合成气,主要反应如下:
i.CH(g)+HO(g)=CO(g)+3H(g) ΔH
4 2 2 1
ii.CH(g)+CO(g)=2CO(g)+2H(g) ΔH
4 2 2 2
各反应平衡常数与温度的关系如图。
(3)①假设ΔH、ΔS不随温度变化,平衡常数与温度间存在的关系为:lnK −lnK = ( − ),R为
1 2
正常数。则ΔH_______0(填“>”或“<”);ΔH_______ΔH(填“>”或“<”)。
1 1 2
②通过调整投料比可调控平衡时合成气 的值。1000K,平衡时 =2,则 =_______,
应控制投料比 =_______。
III.氯碱工业是化工产业的重要基础,其装置示意图如图。(4)X为_______,Y为_______。(写化学式)
(5)淡盐水中含少量的HClO,阴极区生成NaOH的物质的量小于氢气的两倍,下列关于造成NaOH的
物质的量小于氢气的两倍的原因中合理的是_______(填序号)。
a.Cl-在电极上放电,产生HClO
b.有H+穿过阳离子交换膜
c.阳离子交换膜破损导致OH-向阳极区迁移
d.O 在阴极放电
2
5.(2022·河北·邯郸一中模拟预测)含氯化合物的反应在化学工业中具有重要的地位。回答下列问题:
(1)次氯酸钠氧化法可以制备NaFeO。
2 4
已知:2H(g) +O (g)=2HO(l) ΔH=a kJ·mol-1
2 2 2
NaCl(aq)+H O(l)=NaClO(aq)+ H(g) ΔH =b kJ·mol-1
2 2
4NaFeO (aq) + 10H O(l)=4Fe(OH) (s) +3O (g)十8NaOH(aq) ΔH=c kJ·mol-1
2 4 2 3 2
反应2Fe(OH) (s)十3NaClO(aq) + 4NaOH(aq)=2Na FeO (aq) + 3NaCl(aq) +5H O(l)的
3 2 4 2
H=_______kJ·mol-1。
(2)光气(COCl )是重要的含氯化合物。常用于医药、农药制造,工业上利用一氧化碳和氯气反应制备,
△ 2
反应方程式为CO(g)+Cl (g) COCl (g)。在1 L恒温恒容密闭容器 中充入2.5molCO和
2 2
1.5molCl ,在催化剂作用下发生反应,测得CO及COCl 的物质的量随时间变化如图1所示:
2 2
①第一次平衡时,CO的平衡转化率为_______;此温度下,该反应的平衡常数K =_______(保留两位
C
有效数字)。
②在第20 s时,改变的条件是_______。(3)工业上常用氯苯(C H-Cl)和硫化氢(H S)反应来制备一种用途广泛的有机合成中间体苯硫酚(C H-
6 5 2 6 5
SH) ,但会有副产物苯(C H)生成。
6 6
I.C H-Cl(g)+H S(g) C H-SH(g)+HCl(g) ΔH= -16.8 kJ·mol-1;
6 5 2 6 5 1
II.C H- Cl(g)+ H S(g)=C H(g)+HCl(g)+ S(g) H= - 45.8 kJ·mol-1。
6 5 2 6 6 8 2
△
①将一定量的C H-Cl和HS的混合气体充入恒容的密闭容器中,控制反应温度为T(假设只发生反应
6 5 2
I),下列可以作为反应I达到平衡的判据是_______(填字母)。
A.气体的压强不变 B.平衡常数不变
C.v (H S)= v (HCl) D.容器内气体密度不变
正 2 逆
②现将一定量的C H-Cl和HS置于一固定容积的容器中模拟工业生产过程,在不同温度下均反应20
6 5 2
min测定生成物的浓度,得到图2和图3。
(R为HS与C H-Cl的起始物质的量之比),图2显示温度较低时C H-SH浓度的增加程度大于
2 6 5 6 5
C H,从活化能角度分析其主要原因是_______;结合图2和图3,该模拟工业生产制备C H - SH的
6 6 6 5
适宜条件为_______。
6.(2022·重庆·西南大学附中模拟预测)乙醇是一种重要的工业原料,被广泛应用于能源、化工、食
品等领域,以下两种方法可实现乙醇的制备。
I.公众号山城学术圈采用催化乙烯水合制乙醇,该反应过程中能量变化如下图所示:
(1)反应物分子有效碰撞几率最大的步骤对应的基元反应为_______。
(2)制备的无水乙醇在25℃,101kPa下,完全燃烧时放出热量QkJ,其燃烧生成的 用过量饱和石
灰水吸收可得100g 沉淀,则乙醇燃烧热的热化学方程式为_______。
II.以合成气催化合成乙醇是近年来研究的热点,其中乙酸甲酯 催化加氢是制取乙醇的
关键步骤之一,包括以下主要反应:①
②
(3)反应 的ΔH= _______ 。
(4)若在体积为2L的密闭容器中,控制 流速为 (已换算为标准状况),
的转化率为80.0%,则 的反应速率为_______mol∙L-1∙min-1(保留三位有效数
字), 流速过大时乙酸甲酯的转化率下降,原因是_______。
(5)向恒温恒压的两个密闭容器甲(25℃、 )、乙(25℃、 )放入物质的量均为amol的
和 ,若只发生反应②,其正反应速率 ,p为物质分压,若容器甲
与乙中平衡时正反应速率之比 ,则甲、乙容器的体积之比为_______。
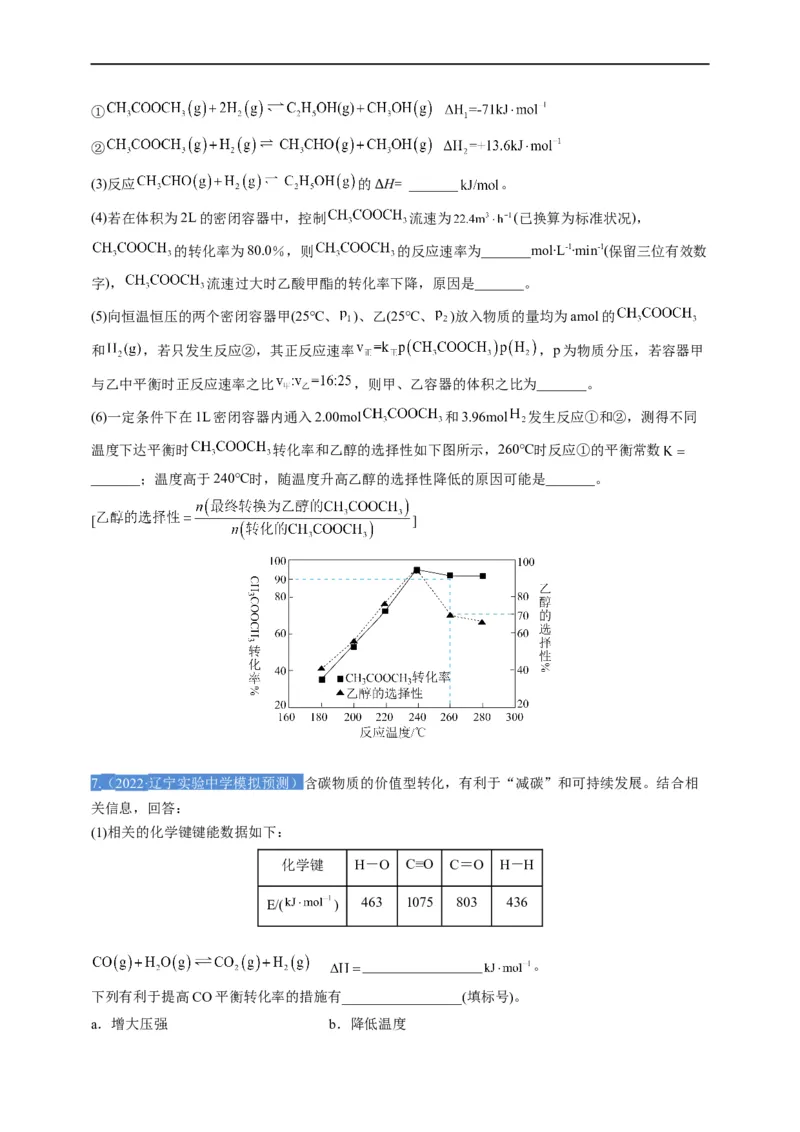
(6)一定条件下在1L密闭容器内通入2.00mol 和3.96mol 发生反应①和②,测得不同
温度下达平衡时 转化率和乙醇的选择性如下图所示,260℃时反应①的平衡常数
_______;温度高于240℃时,随温度升高乙醇的选择性降低的原因可能是_______。
[ ]
7.(2022·辽宁实验中学模拟预测)含碳物质的价值型转化,有利于“减碳”和可持续发展。结合相
关信息,回答:
(1)相关的化学键键能数据如下:
化学键 H-O C≡O C=O H-H
E/( ) 463 1075 803 436
_________________ 。
下列有利于提高CO平衡转化率的措施有_________________(填标号)。
a.增大压强 b.降低温度c.提高原料气中 的比例 d.使用高效催化剂
(2)已知将 、 催化重整为可用的化学品,对改善环境意义重大,某科研团队在密闭容器中进
行“合成气催化重整”,反应的化学方程式为
①下列能说明该反应达到化学平衡状态的是_________________。
a.混合气体的平均相对分子质量不再变化 B.
C.甲烷与氢气浓度比值不再变化 D.容器内混合气体的密度不再变化
②当投料比 时, 的平衡转化率( )与温度(T),初始压强(p)的关系如图所示。
可知:压强 _________________2MPa(填“>”“<”或“=”);当温度为 、压强为2MPa时,
a点时的v(逆)_________________v(正)(填“>”“<”或“=”)
起始时向1L恒容容器中加入2mol 和2mol ,在温度为 、初始压强为2MPa时反应,用
压强表示该反应平衡常数的值的 _____________(分压=总压×物质的量百分数)。
(3)图为一种可以循环利用人体呼出的 并提供 的装置,总反应方程式为 。写
出阴极的电极反应:_______________________
8.(2022·全国·统考高考真题)油气开采、石油化工、煤化工等行业废气普遍含有的硫化氢,需要回
收处理并加以利用。回答下列问题:
(1)已知下列反应的热化学方程式:
①
②③
计算 热分解反应④ 的 ________ 。
(2)较普遍采用的 处理方法是克劳斯工艺。即利用反应①和②生成单质硫。另一种方法是:利用
反应④高温热分解 。相比克劳斯工艺,高温热分解方法的优点是________,缺点是________。
(3)在 、 反应条件下,将 的混合气进行 热分解反应。平衡时混合
气中 与 的分压相等, 平衡转化率为________,平衡常数 ________ 。
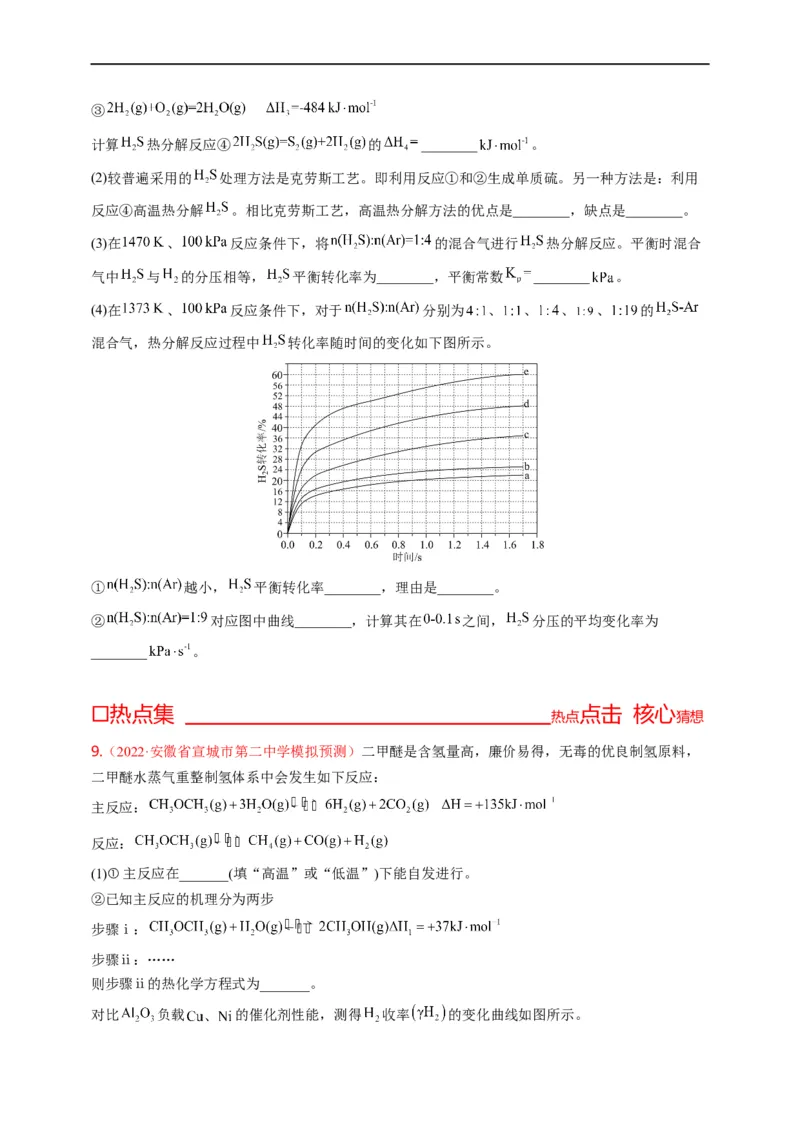
(4)在 、 反应条件下,对于 分别为 、 、 、 、 的
混合气,热分解反应过程中 转化率随时间的变化如下图所示。
① 越小, 平衡转化率________,理由是________。
② 对应图中曲线________,计算其在 之间, 分压的平均变化率为
________ 。
热点集 点击 核心
热点 猜想
9.(2022·安徽省宣城市第二中学模拟预测)二甲醚是含氢量高,廉价易得,无毒的优良制氢原料,
二甲醚水蒸气重整制氢体系中会发生如下反应:
主反应:
反应:
(1)①主反应在_______(填“高温”或“低温”)下能自发进行。
②已知主反应的机理分为两步
步骤ⅰ:
步骤ⅱ:……
则步骤ⅱ的热化学方程式为_______。
对比 负载 的催化剂性能,测得 收率 的变化曲线如图所示。已知:
二甲醚转化率
氢选择性
氢收率=二甲醚转化率×氢选择性
(2)三种催化剂中,催化活性最好的催化剂是_______。加入 后,催化剂的稳定性_______(填“上
升”或下降”)
(3)向恒压为p(非恒容)的体系中充入物质的量之比为 的 发生二甲醚水蒸气
重整制氢反应,测得在催化剂 催化下反应达到平衡时,二甲醚转化率为 ,且产物中
。
①能判断该反应达到平衡状态的标志为_______(填字母)。
A.混合气体中各物质分压保持不变
B.混合气体的密度保持不变
C.混合气体平均摩尔质量保持不变
D.消耗 时,有 生成
②反应达到平衡时, 的转化率为_______,二甲醚水蒸气重整制氢主反应的 _______(列出含
p的计算式即可)。
10.(2022·山东·模拟预测)氨气是重要的基础化工品。回答下列问题:
I. 在尿素合成塔中发生的反应可表示为: 2NH (g)+CO (g) NH COONH(l) [CO(NH)]
3 2 2 4 2 2
(s)+HO(g);已知第一步反应为快速反应,△H=-119.2kJ·mol-1,第二步反应为慢速反应,
2 1
H=+15.5kJ·mol-1,
2
(1)下列图像能表示尿素合成塔中发生反应的能量变化历程的是_______(填标号)。
△
A. B. C. D.II.工业上使用氨气生产尿素,在一个体积恒为1L的恒温密闭容器中充入2mol CO 和4mol NH 的混
2 3
合气体,经历反应1、2合成CO(NH),经历如下两个过程:
2 2
反应1;2NH (g)+CO (g) NH COONH(s) ΔH= - 159.50kJ·mol-1
3 2 2 4 1
反应2:NH COONH(s) CO(NH)(s) + HO(g) ΔH= + 72.50kJ·mol-1
2 4 ⇌ 2 2 2 2
(2)能说明反应1达到平衡状态的是(暂不考虑反应2) __ (填标号)。
⇌
①混合气体的压强不变
②混合气体的密度不变
③相同时间内断裂3molN-H键,同时形成1molCO
2
④混合气体的平均相对分子质量不变
⑤NH 的体积分数不变
3
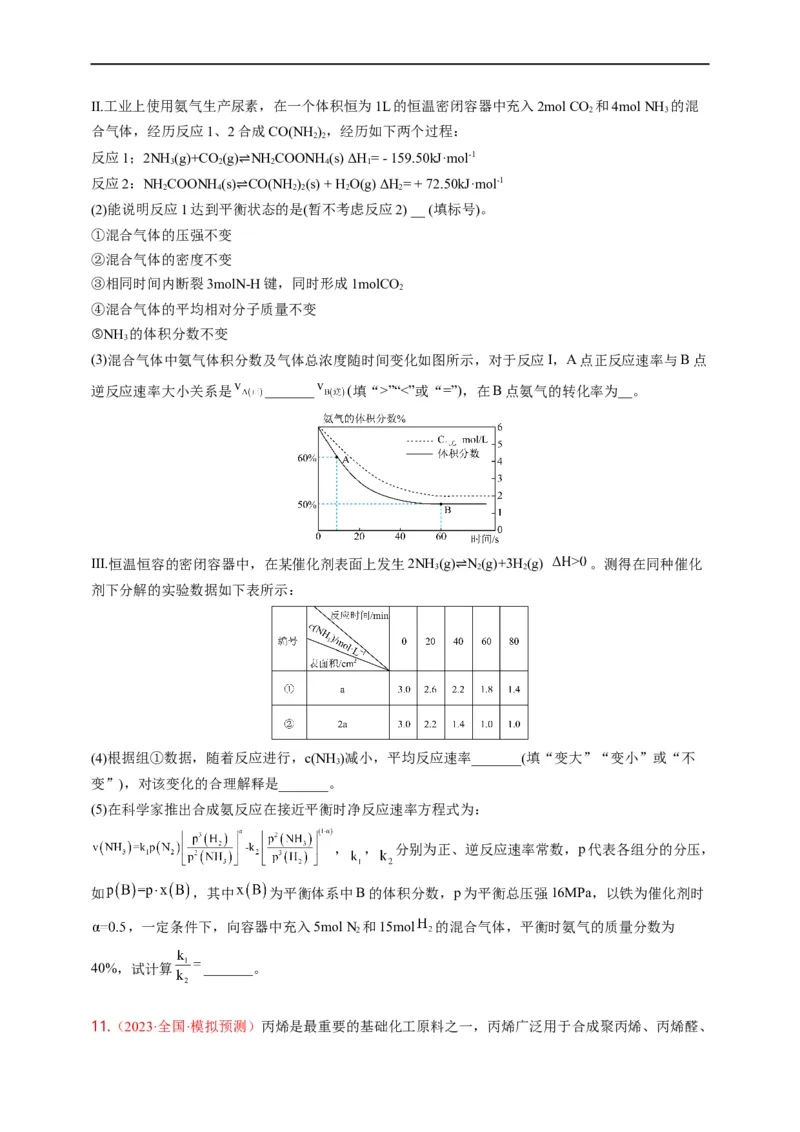
(3)混合气体中氨气体积分数及气体总浓度随时间变化如图所示,对于反应I,A点正反应速率与B点
逆反应速率大小关系是 _______ (填“>”“<”或“=”),在B点氨气的转化率为__。
III.恒温恒容的密闭容器中,在某催化剂表面上发生2NH (g) N(g)+3H(g) 。测得在同种催化
3 2 2
剂下分解的实验数据如下表所示:
⇌
(4)根据组①数据,随着反应进行,c(NH )减小,平均反应速率_______(填“变大”“变小”或“不
3
变”),对该变化的合理解释是_______。
(5)在科学家推出合成氨反应在接近平衡时净反应速率方程式为:
, , 分别为正、逆反应速率常数,p代表各组分的分压,
如 ,其中 为平衡体系中B的体积分数,p为平衡总压强16MPa,以铁为催化剂时
,一定条件下,向容器中充入5mol N 和15mol 的混合气体,平衡时氨气的质量分数为
2
40%,试计算 _______。
11.(2023·全国·模拟预测)丙烯是最重要的基础化工原料之一,丙烯广泛用于合成聚丙烯、丙烯醛、丙烯酸等工业领域.回答下列问题:
(1)丙烷无氧脱氢法制备丙烯反应如下: 已知标准生成
焓指在某温度下由稳定单质生成 化合物的焓变,记作 .在 下,气态丙烷的标准生成焓
,气态丙烯的标准生成焓 ,单质的标准生成焓为零。 生
成物的标准生成焓总和-反应物的标准生成焓总和,则上述反应的 _______
(2) 时,将 充入某恒容刚性密闭容器中,在催化作用下发生无氧脱氢反应。
用压强传感器测出容器内体系压强随时间的变化关系如表所示:
时间 24
0 60 120 180 300 360
0
压强 18
100 136 163 178 180 180
0
①已知: .前 ,用 的分压变化表示上述脱氢反应的平均反应速率为_______kPa/
min。
② 时,反应的平衡常数 _______ ( 为用各气体分压代替气体的浓度表示的平衡常数,
分压=总压 物质的量分数)
③已知: 。在 时,向体积可变的恒压密闭容
器中通入一定量的 ,有助于提高丙烯产率。原因是_______
(3)丙烷在有氧气参与的条件下也可以发生脱氢反应:
。下列说法正确的是_______A.相对于丙
烷直接催化脱氢法,有氧气催化脱氢,反应更容易进行
B.相同条件下,氢气、丙烯、丙烷三种气体中,还原性最强是氢气
C.恒温恒容下,当混合气体的密度不再随时间改变时,说明反应达到其限度
D.通入更多的氧气,有利于提高丙烷转化率,提高丙烯的产率
(4)科学家研究开发了利用太阳能在酸性介质中将工业排放的 电催化获得丙烯的技术,有利于实
现“碳中和”,原理如图所示
阴极的电极反应式为_______12.(2023·浙江·一模)利用CO 合成甲醇、二甲醚技术是有效利用CO 资源,实现“碳中和”目标
2 2
的重要途径。
(1)开发CO 直接催化加氢合成二甲醚技术是很好的一个研究方向。
2
主反应:2CO(g)+6H(g)⇌CH OCH (g)+3HO(g) △H=-122.54kJ•mol-1
2 2 3 3 2 1
副反应:CO(g)+H(g)⇌CO(g)+H O(g) △H
2 2 2 2
①已知25℃和101kPa下,H(g)、CO(g)的燃烧热△H分别为-285.8kJ•mol-1、-283.0kJ•mol-1,
2
HO(l)=HO(g) △H=+44kJ•mol-1,则△H=_______kJ/mol。
2 2 2
②其他条件相同时,反应温度对CO 平衡转化率影响如下图所示。CO 平衡转化率随温度的升高先减
2 2
小后增大的原因可能是_______。
③在催化剂作用下,向恒温恒压(250℃、3.0MPa)的密闭容器中充入反应气,n(CO):(CO):
2
n(H )=1:5:20。反应平衡时测得CO 的转化率为20%,二甲醚的选择性为80%(已知二甲醚的选择
2 2
性= ×100%),则副反应CO(g)+H(g)⇌CO(g)+H O(g)的K=_______(用平
2 2 2 p
衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(2)利用CO 合成甲醇也是有效利用CO 资源的重要途径。将原料气(CO):n(H )=1:3充入某一恒容
2 2 2 2
密闭容器中,只发生CO(g)+3H(g)⇌CH OH(g)+H O(g) △H<0,在不同催化剂作用下,反应tmin时
2 2 3 2 3
CO 的转化率随温度的变化如图所示。
2
①下列说法正确的是_______。
A.使用催化剂I时,d点已达到平衡
B.TK的平衡常数大于TK的平衡常数
3 4
C.若a点时,v(H ) =3v(CH OH) ,则此条件下反应已达到最大限度
2 正 3 逆
D.c点转化率比a点低的原因一定是催化剂活性降低
②若图中a点时反应已达平衡,现原料气按(CO):n(H )=1:2.8充入同一恒容密闭容器中,在催化
2 2
剂I的作用下发生反应。请在图中用实线画出了TK~TK之间CO 的平衡转化率变化曲线_______。
3 5 2
(3)水煤气变换反应的机理被广泛研究,其中有一种为羧基机理,某催化剂催化
CO*+HO*⇌CO *+H (g) (*表示吸附态、E 表示活化能)步骤如下:
2 2 2 aⅠ.H O*→OH*+H* E =141.7kJ/mol
2 a1
Ⅱ.CO*+OH*→COOH* E =39.5kJ/mol
a2
Ⅲ.COOH*→CO *+H* E =132.1kJ/mol
2 a3
Ⅳ.2H*→H (g) E =97.4kJ/mol
2 a4
反应CO*+HO*⇌CO *+H (g)的决速步骤是_______(填序号)。
2 2 2
13.(2023·四川成都·模拟预测)处理、回收利用CO是环境科学研究的热点课题。回答下列问题:
(1)CO用于处理大气污染物NO的反应为CO(g)+NO(g) CO(g)+N(g)。在Zn+作用下该反应的
2 2 2 2
具体过程如图1所示,反应过程中能量变化情况如图2所示。
总反应:CO(g)+NO(g) CO(g)+N(g) ΔH=_______kJ·mol-1,该总反应的决速步是反应_______(填
2 2 2
“①”或“②”),该判断的理由是_______。
(2)已知:CO(g)+NO(g) CO(g)+N(g)的速率方程为v=k·c(N O),k为速率常数,只与温度有关。
2 2 2 2
为提高反应速率,可采取的措施是_______(填字母序号)。
A.恒容时,再充入CO B.恒压时,再充入NO C.恒压时,再充入N D.
2 2
升温
(3)在总压为100kPa的恒容密闭容器中,充入一定量的CO(g)和NO(g)发生上述反应,在不同条件下
2
达到平衡时,在TK时NO的转化率与 、在 =1时NO的转化率与 的变化曲线如图
1 2 2
3所示:
①表示NO的转化率随 的变化曲线为_______曲线(填“I”或“Ⅱ”);
2
②T _______T(填“>”或“<”);
1 2(4)已知:该反应的标准平衡常数 ,其中pθ为标准压强(100kPa),p(CO)、
2
p(N )、p(N O)和p(CO)为各组分的平衡分压,则T 时,该反应的标准平衡常数Kθ=_______(计算结果
2 2 4
保留两位有效数字,P =P ×物质的量分数)。
分 总
14.(2023·湖南长沙·模拟预测)二氧化碳有效转化是“碳中和”的重要研究方向,在催化剂条件下
可以生成重要的化工原料乙烯,反应为 。根据此
项研究,回答下列问题:
(1)在恒压密闭容器中,起始充入2mol 和6mol 发生反应,该反应在不同的温度下达到
平衡时,各组分的体积分数随温度的变化如图所示。
①图中表示 的体积分数随温度变化的曲线是______(填字母)。C点时,反应达到平衡的标志为
______(填字母)。
a. b.容器中气体的平均摩尔质量不再变化
c.混合气体的密度不再变化 d. 不再变化
②A、B、C三点对应的化学平衡常数为 、 、 ,则从大到小的排列顺序为______。
③B点反应达到平衡后, 的平衡转化率为______(计算结果保留一位小数),若平衡时总压为
P,则平衡常数 ______(列出计算式,以分压表示,气体分压=总压×气体的物质的量分数)。
(2)其他条件相同,分别在X、Y两种催化剂作用下,将2mol 和6mol 充入体积为1L的
密闭容器内,测得反应相同时间时 的转化率与温度的关系如图。使用催化剂X,当温度高于320℃时, 的转化率逐渐下降,其原因是______。根据图像,
______(填“能”或“不能”)计算280℃时该反应的平衡常数,其理由是____________。
15.(2022·重庆·模拟预测)含氨污染物的有效去除和含碳资源的充分利用是重要研究课题。回答下
列问题:
(1)利用工业尾气 与 反应制备新型硝化剂 ,过程中涉及以下反应:
I.
II.
III.
平衡常数K与温度T的函数关系为 , , ,其中x、y、z
为常数,则反应I的活化能 (正)______ (逆)(填“>”或“<”), 的数值范围是______。(填标
号)
A. B. ~0 C.0~2 D.>2
(2) 与 重整是 利用的研究热点之一。该重整反应体系有以下反应:
I.
II.
III. (只在高温下自发进行)
①在一定压强和催化剂的条件下,将等物质的量的 和 通入重整反应器中,平衡时, 、
的物质的量分数及转化率随温度变化的关系如图所示。平衡时 的物质的量分数随温度变化
的曲线是______(填标号)。温度高于1300K后,曲线d超过曲线c的可能原因为__________________。
②在p MPa时,将 和 按物质的量之比为1∶1充入密闭容器中,分别在无催化剂和 催化
下反应相同时间,所得 的转化率与温度的关系如图所示。a点 转化率相等的原因是
___________。
③设 为相对压力平衡常数,用相对分压代替浓度即可得相对压力平衡常数的表达式[气体的相对分
压等于其分压(单位为kPa)除以标准压强 ]。某温度下反应Ⅲ的 ,向恒容密闭容
器中按 充入原料气,初始总压为150kPa,发生反应I、II、Ⅲ,体系达到平衡时
的分压为b kPa,则 的平衡转化率为______。(用含b的代数式表示)
16.(2022·浙江温州·模拟预测)C、CO、 是常见还原剂。不同的反应,选择合理的还原剂以达到
不同的工艺意图。工业上常见几种还原反应如下:
反应I:
反应II:
反应III:
反应IV:
反应V:
回答下列问题。
(1)从 的角度,说明反应I自发进行的可能性:_______。
(2)①其他条件不变,分别测定CO还原FeO、 还原FeO反应体系中,平衡时 、CO体积分数与
温度的关系如图所示。关于该类还原反应,有关说法不正确的是_______。
A.温度越高,FeO被CO还原的程度越大
B.温度越低, 还原生成铁所需的 的浓度越大
C.若 还原FeO活化能相对较小,则 混合气体系中的还原FeO速率由 决定
D. 宜在低温下进行
②结合反应I及图示信息,说明随温度升高,在平衡体系中, 与CO还原FeO的能力发生变化的
原因:_______。
③计算576℃反应III的平衡常数K=_______。
(3)根据反应IV,图中分别画出 、 的能量变化,并进行必要的标注。
(4)已知基元反应 的速率方程可表示为: (k为速率常数,下同)。碰
撞理论研究发现,大多数化学反应并不是经过简单的碰撞就能完成,往往需经过多个反应步骤才反
应过程能实现。用 还原 合成HI的反应 实际上经过两步基元反应完成的:
已知快反应近似平衡态。若在温度为T℃下, , 。写出T℃下
反应的速率方程:v=_______(用含 、 、 、a、b的代数式表示)