文档内容
2024 年中考第三次模拟考试(吉林卷)
化 学
(考试时间:45分钟 试卷满分:50分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32 Cl-35.5 Ag-108
一、单项选择题(每小题1分,共10分)
1.习近平总书记指出:“中华优秀传统文化是中华文明的智慧结晶和精华所在,是中华民族的根和
魂。”古诗词是中华传统文化的精髓,以下诗句中划线部分包含化学变化的是( )
A.竹外桃花三两枝,春江水暖鸭先知 B.爆竹声中一岁除,春风送暖入屠苏
C.忽如一夜春风来,千树万树梨花开 D.日照香炉生紫烟,遥看瀑布挂前川
【答案】B
【解析】A. 有新物质生成的变化是化学变化,无新物质生成的变化是物理变化。春江水暖鸭先知,无新
物质生成,属于物理变化,此选项不符合题意;
B. 爆竹声中一岁除,有新物质生成,属于化学变化,此选项符合题意;
C.千树万树梨花开,无新物质生成,属于物理变化,此选项不符合题意;
D. 日照香炉生紫烟,无新物质生成,属于物理变化,此选项不符合题意。
故选B。
2.下列化学用语的含义正确的是( )
A.H — 1个氢元素 B.H — 1个氢分子
2
C.H+ — 1个氢原子 D. — 1个氢离子
【答案】B
【解析】A、元素是宏观的,讲种类,不讲个数,故错误;
B、由分子构成的物质,化学式可以表示该物质的一个分子,故正确;
C、H+表示一个氢离子,故错误;
D、 表示氢元素的化合价为+1,故错误。
故选B。
3.下列物质属于纯净物的是( )
A. 生理盐水 B. 冰水混合物 C. 75%医用酒精 D. 洁净的空气
【答案】B【解析】A、生理盐水是由氯化钠和水组成的混合物,不符合题意;
B、冰水混合物只是物质状态不同,只有水一种物质,属于纯净物,符合题意;
C、医用酒精含有酒精、水,属于混合物,不符合题意;
D、洁净的空气含有氮气、氧气等多种物质,属于混合物,不符合题意。
故选B。
4.规范的实验操作是实验成功和安全的重要保证。下列实验操作正确的是
A. 气密性检验 B. 验满
C. 稀释浓硫酸 D. 测溶液
【答案】C
【解析】A、该装置未构成封闭体系,即左边的长颈漏斗与大气相通;无论该装置气密性是否良好,导管
口都不会有气泡产生,不能判断气密性是否良好,故图中所示操作错误;
B、检验二氧化碳是否收集满时,应将燃着的木条放在集气瓶口,不能伸入瓶中,故图中所示操作错误;
C、打开试剂瓶瓶塞,瓶塞要倒放,标签朝向手心;稀释浓硫酸时,要把浓硫酸慢慢地沿器壁注入水中,
同时用玻璃棒不断搅拌,以使热量及时的扩散;一定不能把水注入浓硫酸中,以防止酸液飞溅,故图中所
示操作正确;
D、用 试纸测定溶液的 时,正确的操作方法为在白瓷板或玻璃片上放一小片 试纸,用玻璃棒蘸
取待测液滴到 试纸上变色后,把试纸显示的颜色与标准比色卡比较,读出 ,不能将pH试纸伸入待
测液中,以免污染待测液,故图中所示操作错误。
故选C。
5.下列做法中不利于推动绿色发展,保护环境的是( )
A. 扩大燃煤发电规模,保障电力供应
B. 绿色出行,助力“碳中和”
C. 使用可降解塑料袋,减少“白色污染”
D. 污水处理达标排放,降低水体污染
【答案】A
【解析】A、扩大燃煤发电规模,会产生更多的有害气体污染空气,不利于推动绿色发展,保护环境,符
合题意;
B、绿色出行,可以减少二氧化碳的排放,有助于实现“碳中和”,有利于推动绿色发展,保护环境,不
符合题意;
C、使用可降解塑料袋,可以减少“白色污染” ,有利于推动绿色发展,保护环境,不符合题意;D、污水处理达标排放,可以降低水体污染,有利于推动绿色发展,保护环境,不符合题意;
故选A。
6.下列对有关实验的分析,正确的是( )
A.某固体加入到稀盐酸中有气泡产生,此固体一定为活泼金属
B.测定空气中氧气含量,装置气密性不好会导致测出的氧气体积分数偏大
C.配制6%的氯化钠溶液,量水时俯视读数,会导致溶液溶质质量分数偏小
D.用红磷在密闭容器中燃烧验证质量守恒定律,红磷量不足对实验结果无影响
【答案】D
【解析】A、稀盐酸和活泼金属反应生成氢气,和碳酸钠反应生成二氧化碳气体,则和盐酸反应生成气体
的,不一定为活泼金属,该选项分析不正确;
B、测定空气中氧气含量时,若装置气密性不好,会由于压强差而进入空气,则会导致测得的氧气体积分
数偏小,该选项分析不正确;
C、量水时俯视读数,会使量取的水的体积偏小,则会导致溶液溶质质量分数偏大,该选项分析不正确;
D、验证质量守恒定律时,只需证明反应前后质量相等即可,则红磷量不足也不会影响实验结果,该选项
分析正确。
故选D。
7.化学与生产生活密切相关,下列说法错误的是
A.天然气是一种可再生能源
B.炒菜时油锅着火,用锅盖盖灭
C.NaOH可作炉具清洁剂
D.铁制品表面刷漆可防止生锈
【答案】A
【解析】A、天然气是一种化石能源,在短期内得不到补充,属于不可再生能源,故选项说法错误;
B、炒菜时油锅着火,用锅盖盖灭,这是采用了隔绝氧气的原理来灭火,故选项说法正确;
C、氢氧化钠是一种碱,能与油污反应,因此NaOH可作炉具清洁剂,故选项说法正确;
D、铁在与氧气和水共存时会发生锈蚀,因此铁制品表面刷漆(隔绝铁与氧气和水的接触)可防止生锈,故选
项说法正确。
故选A。
8.将未打磨的铝片放入试管中,加入过量稀盐酸,反应过程中产生氢气的质量与时间的关系如图所示,
下列说法正确的是
A.0~a段时没有反应发生B.b点时发生反应的基本反应类型为置换反应
C.a~c段时试管中溶液质量减少
D.d点时向试管中滴加酚酞溶液,酚酞溶液变红
【答案】B
【解析】A、由分析可知,0~a段时氧化铝与稀盐酸反应生成氯化铝和水,故选项说法不正确;
B、由分析可知,a~c段时铝与稀盐酸反应生成氯化铝和氢气,该反应符合“一种单质与一种化合物反应,
生成另一种单质和另一种化合物”的特点,属于置换反应,故选项说法正确;
C、a~c段时铝与稀盐酸反应生成氯化铝和氢气,根据反应的化学方程式2Al+6HCl=2AlCl +3H ↑,每54
3 2
份质量的铝完全反应,生成6份质量的氢气,则反应过程中试管中溶液质量增加,故选项说法不正确;
D、d点时盐酸过量,溶液呈酸性,滴加酚酞溶液,酚酞溶液不变红,故选项说法不正确。
故选B。
9.证据推理是一种重要的化学思维方法。下列推理得出的结论正确的是
A.点燃氢气或者一氧化碳之前需要检验纯度,则点燃可燃性气体之前一定要验纯
B.活泼金属能与盐酸反应产生气体,因此能与盐酸反应产生气体的物质一定是活泼金属
C.溶液具有均一性和稳定性,因此具有均一性和稳定性的液体一定是溶液
D.中和反应生成盐和水,则生成盐和水的反应一定是中和反应
【答案】A
【解析】A、可燃性气体与空气混合点燃可能发生爆炸,点燃氢气或者一氧化碳前需要检验纯度,则点燃
可燃性气体之前一定要检验纯度,故A正确;
B、活泼金属能与稀盐酸反应生成氢气,但是能与稀盐酸反应生成气体的物质不一定是活泼金属,如碳酸
钙能与稀盐酸反应生成气体CO,故B错误;
2
C、溶液具有均一性、稳定性,但是具有均一性、稳定性的物质不一定是溶液,如液体水具有均一性、稳
定性,但是水属于纯净物,不属于溶液,故C错误;
D、中和反应生成盐和水,但是生成盐和水的反应不一定是中和反应,例如二氧化碳和氢氧化钠反应生成
碳酸钠和水,故D错误;
故选:A。
10.实验是进行科学研究的重要手段,实验方案的设计是实验成功的基本保证,下列实验方案设计不合理
的是( )
选项 实验目的 试验方法
A 区分羊毛和棉花 灼烧并闻气味
B 鉴别NH Cl和KCl 加熟石灰研磨,闻气味
4
C 除去CO中混有的CO 将混合气体通过灼热的氧化铜粉末
2D 比较Fe、Cu和Ag的金属活动性 将Fe和Ag分别加入CuSO 溶液中
4
【答案】C
【解析】A、羊毛的主要成分是蛋白质,灼烧有烧焦羽毛的气味,棉花的主要成分是纤维素,灼烧有纸燃
烧的气味,故灼烧并闻气味可以区分羊毛和棉花,不符合题意;
B、氯化铵属于铵态氮肥,能与熟石灰反应生成氨气,氨气有刺激性气味,氯化钾与熟石灰不反应,可以
用加熟石灰研磨、闻气味的方法来鉴别氯化铵和氯化钾,不符合题意;
C、一氧化碳能与氧化铜在加热的条件下反应生成铜和二氧化碳,二氧化碳与氧化铜不反应,不但没有除
去杂质,反而除去了原物质,方案设计不合理,符合题意;
D、将Fe和Ag分别加入CuSO 溶液中,铁能与硫酸铜反应生成硫酸亚铁和铜,有红色固体析出,说明在
4
金属活动性顺序里,铁位于铜之前,银不与硫酸铜反应,无明显现象,说明在金属活动性顺序里,银位于
铜之后,可以比较Fe、Cu和Ag的金属活动性,不符合题意。
故选C。
二、填空题(每空1分,共10分)
11.(3分)在宏观、微观和符号之间建立联系是化学学科的重要思维方式。下图是部分粒子的结构示意
图。
(1)A、B属于不同种元素,两者最本质的区别是 不同。
(2)A、C化学性质相似的原因是 相同。
(3)若图D带两个单位的正电荷,则X= 。
【答案】(1)质子数/核电荷数 (2)最外层电子数 (3)20
12.(3分)农业生产与化学息息相关,化学在农业生产中发挥着重要作用。
(1)纯棉衣服由于吸水性和透气性好,穿着舒适,深受人们喜爱。棉花属于 (填“金属”“天然”
或“合成”)纤维。
(2)粮食安全是“国之大者”,稻谷和小麦是我国重要的粮食作物,其中富含的营养素是 。合理施
肥是小麦增产的最有利措施,施用磷酸二氢铵(NH HPO )属于 (填序号)。
4 2 4
A.氮肥 B.钾肥
C.磷肥 D.复合肥
【答案】(1)天然
(2)糖类 D
【解析】(1)棉花是自然界中本来就有的,属于天然纤维;
(2)稻谷和小麦中富含的营养素是糖类;磷酸二氢铵(NH HPO )中含有农作物需求量大的氮元素和磷
4 2 4
元素,属于复合肥,故选D。
13.(4分)我国古代时期,金属的冶炼和使用就在当时出于世界领先水平。
(1)明代《天工开物》中记录了金属锡的冶炼方法。冶炼金属锡的原料为锡砂,锡砂中的SnO 和木炭高
2温下反应得到锡和二氧化碳,炼锡时混入少许铅形成合金,产物更易熔化流出,原因是 。
(2)如图为为古代炼锌工艺原理示意图。炉甘石成分是ZnCO ,高温易分解生成ZnO,再将ZnO还原得
3
到锌。
①泥罐外煤饼的主要作用是燃烧提供热量,泥罐内煤粉的主要作用是 。
②锌类似铝,可以形成致密的氧化膜具有耐腐蚀性。炼锌时必须冷却后才能取锌,目的是 。
(3)湿法冶金利用置换反应。向Cu(NO )、AgNO 混合液中加入Fe粉,充分反应后过滤。若滤渣中有两
3 2 3
种金属,则滤液中一定不含的金属阳离子是 。
【答案】(1)合金的熔点低于组成其纯金属的熔点
(2)①做还原剂 ②防止Zn被氧化
(3)Ag+
【解析】(1)合金的熔点低于其组成中纯金属的熔点,炼锡时混入少许铅形成合金,产物更易熔化流出,
原因是形成合金熔点降低,故填:合金的熔点低于组成其纯金属的熔点;
(2)①煤粉的主要成分是碳,在高温的条件下,碳酸锌分解为氧化锌和二氧化碳,在罐中,碳与氧化锌
在高温的条件下反应生成锌和二氧化碳,碳能夺取氧化锌中的氧将其还原为锌,所以泥罐内煤粉的主要作
用是做还原剂,故填:做还原剂;
②必须冷却后才能取锌,是为了防止生成的锌在较高温度下又被氧化成氧化锌,故填:防止Zn被氧化;
(3)根据金属活动性顺序:铁>氢>铜>银,向Cu(NO )、AgNO 混合液中加入Fe粉,铁会先与硝酸
3 2 3
银反应生成硝酸亚铁和银,待硝酸银反应完全,铁有剩余,铁会与硝酸铜反应生成硝酸亚铁和铜,充分反
应后过滤。若滤渣中有两种金属,则为银和铜,可确定硝酸银中的银一定被全部置换出来,无法判断硝酸
铜是否有剩余,则滤液中一定不含的金属阳离子是银离子,故填:Ag+。
三、简答题(每空1分,化学方程式2分,共12分)
14.(3分)向充满二氧化碳的锥形瓶中先注入氢氧化钠溶液,振病,未观察到明显现象,打开弹簧夹并
注入 (填一种试剂),产生气泡,证明氢氧化钠与二氧化碳已经反应,其反应的化学方程式为
。
【答案】稀盐酸或稀硫酸
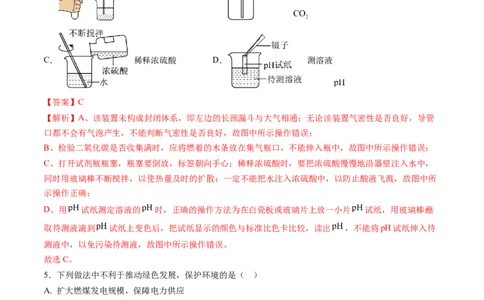
15.(3分)根据如图所示实验情境,回答下列问题。(1)实验一中,能说明温度达到着火点才会发生燃烧的现象是 。
(2)实验二,A、B两烧杯中分别装有足量的红磷和木炭,两物质完全燃烧后待装置冷却,打开a、b两个
活塞,A中现象与B中现象 (填“相同”或“不相同”);原因是 。
【答案】(1)铜片上白磷燃烧红磷不燃烧
(2)不相同 红磷燃烧产物为固体,木炭燃烧产物为气体
【解析】(1)实验一中铜片上的白磷与红磷均属于可燃物,均与氧气接触,但是铜片上的白磷燃烧,红
磷不燃烧,这说明燃烧需要温度达到着火点,故填:铜片上的白磷燃烧红磷不燃烧;
(2)装置中红磷和木炭都足量,待红磷和木炭燃烧完毕冷却至室温后,打开a、b两个活塞,看到的现象
是A瓶烧杯里的水倒吸到集气瓶内,集气瓶中的水约占集气瓶容积五分之一,B瓶烧杯里的水没有倒吸到
集气瓶内,产生该现象的原因是红磷燃烧的产物是固体,内外产生压强差,冷却到室温后,松开止水夹,
烧杯里的水倒吸到集气瓶内,集气瓶中的水约占集气瓶容积五分之一(氧气在空气中的含量),木炭燃烧
的产物是气体,内外没产生压强差,因此冷却到室温后,松开止水夹,烧杯里的水不会倒吸到集气瓶内,
故填:不相同、红磷燃烧产物为固体,木炭燃烧产物为气体。
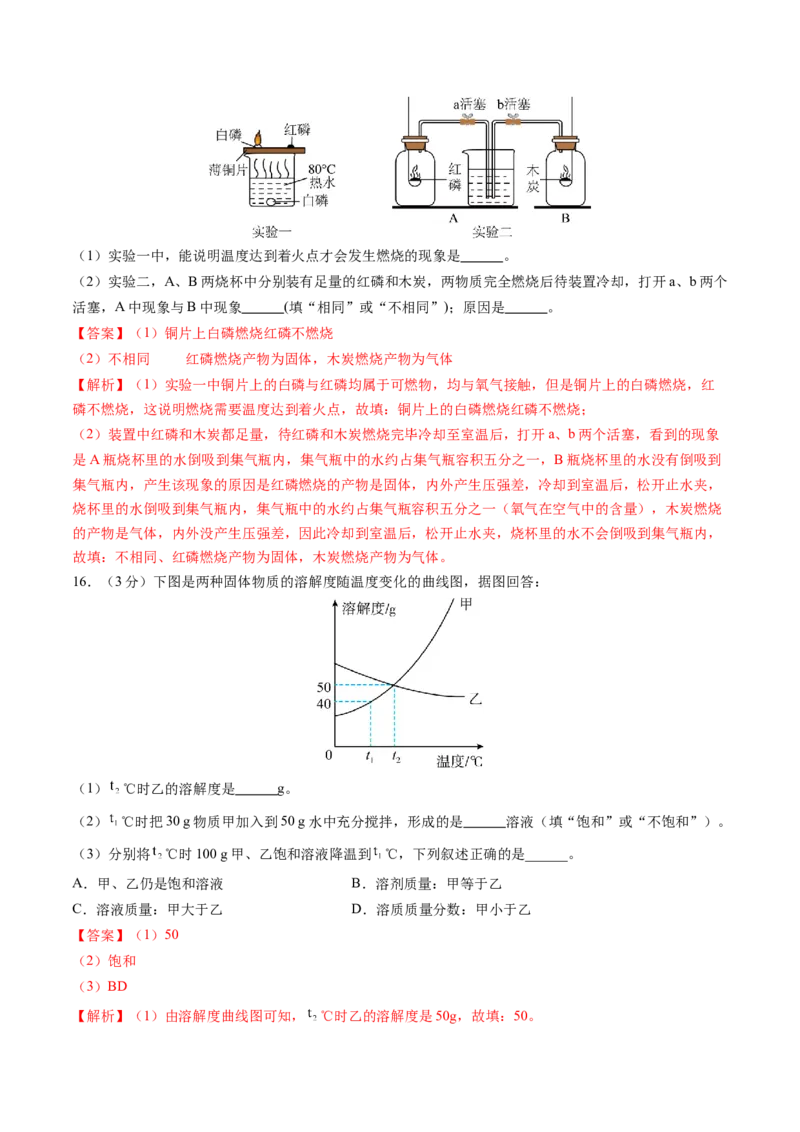
16.(3分)下图是两种固体物质的溶解度随温度变化的曲线图,据图回答:
(1) ℃时乙的溶解度是 g。
(2) ℃时把30 g物质甲加入到50 g水中充分搅拌,形成的是 溶液(填“饱和”或“不饱和”)。
(3)分别将 ℃时100 g甲、乙饱和溶液降温到 ℃,下列叙述正确的是______。
A.甲、乙仍是饱和溶液 B.溶剂质量:甲等于乙
C.溶液质量:甲大于乙 D.溶质质量分数:甲小于乙
【答案】(1)50
(2)饱和
(3)BD
【解析】(1)由溶解度曲线图可知, ℃时乙的溶解度是50g,故填:50。(2)由溶解度曲线图可知, ℃时物质甲的溶解度为40g, ℃时50 g水中最多能溶解20g甲物质,所以
℃时把30 g物质甲加入到50 g水中充分搅拌,形成的是饱和溶液。
(3)A.由溶解度曲线图可知,物质甲的溶解度随温度的降低而减小,物质乙的溶解度随温度的降低而增
大,分别将 ℃时100 g甲、乙饱和溶液降温到 ℃,甲仍是饱和溶液,乙变为不饱和溶液,故A错误;
B.降温过程中,甲、乙溶液中溶剂的质量不变,与 ℃时饱和溶液中溶剂的质量相等,由溶解度曲线图可
知, ℃时,甲、乙的溶解度相等,等质量的饱和溶液中所含的溶剂质量相等,分别将 ℃时100 g甲、
乙饱和溶液降温到 ℃,溶剂质量:甲等于乙,故B正确;
C.甲溶液中有晶体析出,溶液质量减小,乙溶液中无晶体析出,溶液质量不变,所以分别将 ℃时100 g
甲、乙饱和溶液降温到 ℃,溶液质量:甲小于乙,故C错误;
D.由溶解度曲线图可知, ℃时,甲、乙的溶解度相等,根据饱和溶液溶质质量分数=
,可知 ℃时甲、乙饱和溶液溶质的质量分数相等,分别将 ℃时100g甲、乙饱和
溶液降温到 ℃,甲溶液中有晶体析出,溶质质量分数减小,乙溶液中无晶体析出,溶质质量分数不变,
所以 ℃时溶质质量分数:甲小于乙,故D正确。
故选:BD。
17.(3分)在“宏观—微观—符号”之间建立联系,是化学学科特有的思维方式,如图为盐酸和氢氧化
钠溶液反应的微观示意图。
(1)从微观的角度分析,甲处应填入的离子符号为 。
(2)向滴有酚酞的稀氢氧化钠溶液中,逐滴加入稀盐酸至过量,溶液 (填现象)。
(3)向盛有饱和氢氧化钠溶液的试管中,边振荡边滴加36.5%的浓盐酸,观察到试管内产生大量白色沉淀
且溶液沸腾,推测试管内产生的白色沉淀是NaCl,产生的原因是 ;。
【答案】(1)OH-
(2)由红色变为无色
(3)相同温度下氯化钠的溶解度比氢氧化钠小,更容易达到饱和状态而析出
四、实验与探究题(每空1分,化学方程式2分,共12分)
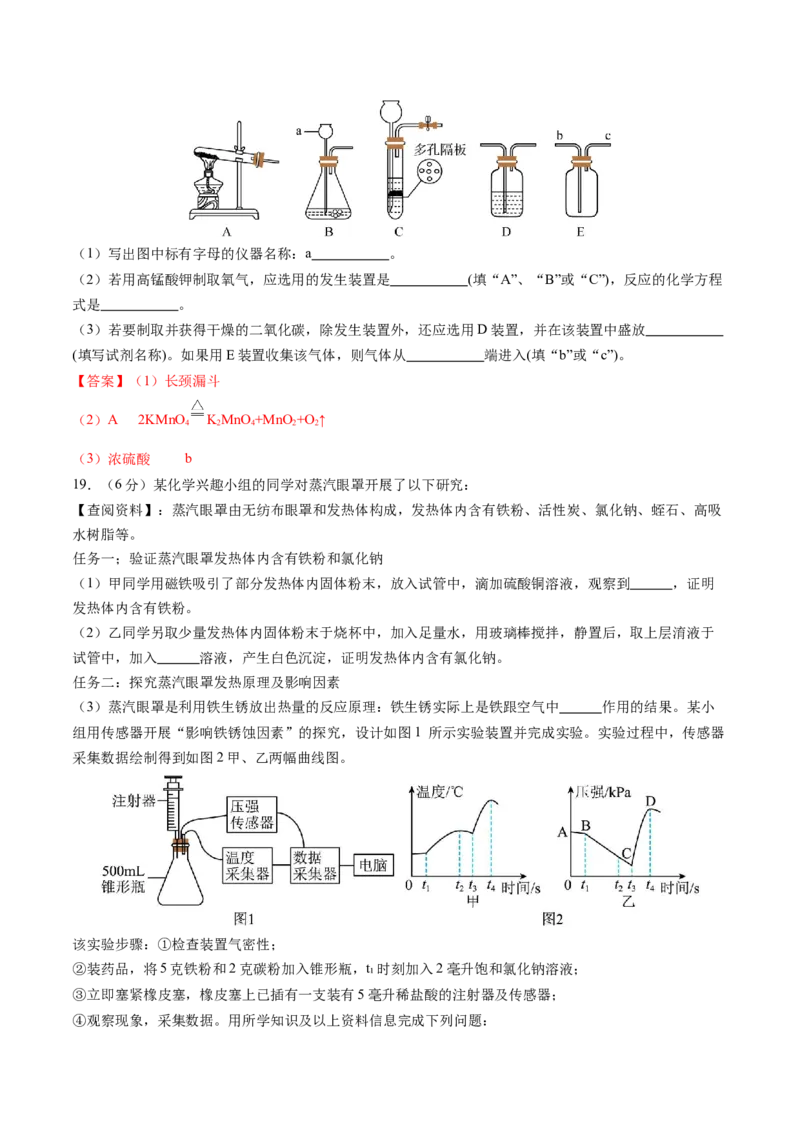
18.(6分)请结合下列实验常用装置,回答有关问题。(1)写出图中标有字母的仪器名称:a 。
(2)若用高锰酸钾制取氧气,应选用的发生装置是 (填“A”、“B”或“C”),反应的化学方程
式是 。
(3)若要制取并获得干燥的二氧化碳,除发生装置外,还应选用D装置,并在该装置中盛放
(填写试剂名称)。如果用E装置收集该气体,则气体从 端进入(填“b”或“c”)。
【答案】(1)长颈漏斗
(2)A 2KMnO KMnO +MnO+O ↑
4 2 4 2 2
(3)浓硫酸 b
19.(6分)某化学兴趣小组的同学对蒸汽眼罩开展了以下研究:
【查阅资料】:蒸汽眼罩由无纺布眼罩和发热体构成,发热体内含有铁粉、活性炭、氯化钠、蛭石、高吸
水树脂等。
任务一;验证蒸汽眼罩发热体内含有铁粉和氯化钠
(1)甲同学用磁铁吸引了部分发热体内固体粉末,放入试管中,滴加硫酸铜溶液,观察到 ,证明
发热体内含有铁粉。
(2)乙同学另取少量发热体内固体粉末于烧杯中,加入足量水,用玻璃棒搅拌,静置后,取上层淯液于
试管中,加入 溶液,产生白色沉淀,证明发热体内含有氯化钠。
任务二:探究蒸汽眼罩发热原理及影响因素
(3)蒸汽眼罩是利用铁生锈放出热量的反应原理:铁生锈实际上是铁跟空气中 作用的结果。某小
组用传感器开展“影响铁锈蚀因素”的探究,设计如图1 所示实验装置并完成实验。实验过程中,传感器
采集数据绘制得到如图2甲、乙两幅曲线图。
该实验步骤:①检查装置气密性;
②装药品,将5克铁粉和2克碳粉加入锥形瓶,t₁时刻加入2毫升饱和氯化钠溶液;
③立即塞紧橡皮塞,橡皮塞上已插有一支装有5毫升稀盐酸的注射器及传感器;
④观察现象,采集数据。用所学知识及以上资料信息完成下列问题:(4)实验进行一段时间后,注射器中的稀盐酸会自动注入瓶内,请从物理、化学两个角度分析原因是
,分析t₃时刻后压强突然变大的原因是 。
(5)图2乙曲线中,AB段与 段对比说明氯化钠可以加快铁的锈蚀。
【答案】(1)红色固体析出
(2)硝酸银/AgNO
3
(3)O、HO或氧气、水
2 2
(4)铁生锈消耗瓶内氧气,使瓶内压强减小 稀盐酸能与铁反应生成氢气,且该反应为放热反应
(5)BC
【解析】(1)根据结论发热体内含有铁粉,滴加硫酸铜溶液,铁和硫酸铜溶液反应生成硫酸亚铁和铜,
可观察到有红色固体析出;
(2)根据结论发热体内含有氯化钠,氯化钠与硝酸银反应生成氯化银白色沉淀,取少量发热体内固体粉
末于烧杯中,加入足量水,用玻璃棒搅拌,静置后,取上层淯液于试管中,加入硝酸银溶液,产生白色沉
淀,证明发热体内含有氯化钠;
(3)铁生锈实际上是铁跟空气中氧气和水作用的结果;
(4)铁生锈是铁与水、氧气共同作用的结果,则铁生锈消耗氧气,使瓶内压强变小,当瓶内气压减小一
定程度,大气压将注射器活塞下压,故注射器中的盐酸会自动注入瓶内;稀盐酸注入锥形瓶内,能与铁反
应生成氢气,且该反应为放热反应,则t 时刻后瓶中的压强增大;
3
(5)铁生锈是铁与水、氧气共同作用的结果,则铁锈蚀会消耗氧气,使装置中的气压降低,t 时刻向装置
1
中加入2毫升高浓度氯化钠溶液,根据图乙可知加入氯化钠溶液后压强下降速率较快,则说明反应速率加
快,图2乙曲线中,对比AB与BC断能说明氯化钠溶液能加快铁的锈蚀速率。
五、计算题(共6分)
20.硝酸银溶液可与指印遗留物中的氯化物起反应生成氯化银,氯化银在阳光作用下颜色逐渐变成黑色,
从而使指纹得以显现。同学们取指纹检验所用硝酸银溶液100g,向其中加入足量氯化钠溶液,充分反应后,
经过滤、洗涤、干燥,称得生成沉淀的质量为1.435g。计算该硝酸银溶液中溶质的质量分数。
【答案】解:设该硝酸银溶液中溶质的质量为x
解得x=1.7g
则该硝酸银溶液中溶质的质量分数为:
答:该硝酸银溶液中溶质的质量分数为1.7%。