文档内容
2024 年中考第一次模拟考试(吉林卷)
化 学
(本卷共20小题,满分50分,考试用时50分钟)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答非选择题时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 Mg-24 Cl-35.5 K-39
一、选择题(本大题共10小题,每小题1分,共10分。每小题给出的四个选项中,只有一个选项最符合
题目的要求)
1.2023年9月23日,第19届亚运会开幕式在杭州奥体中心体育场举行,其中涉及化学变化的是( )
A.运用三维动画,展示数字烟花
B.亚运会开幕式主火炬用绿色零碳甲醇点燃
C.使用“水玉琮”敲击出激昂鼓声,以水为礼,击鼓迎宾
D.在文艺表演环节,水墨人诗画,国风男子挥毫作画绘就山水画卷一风雅钱塘尽展眼前
2.近年昆明地铁发展迅速,修建地铁所用的钢材属于( )
A.天然材料 B.金属材料 C.合成材料 D.复合材料
3.某同学用PH试纸测定了生活中一些物质的pH如下。能使酚酞溶液变红的物质是( )
物质 食醋 橘子汁 食盐水 炉具清洁剂
pH 2 4 7 12
A.食醋 B.橘子汁 C.食盐水 D.炉具清洁剂
4.配制一定溶质质量分数的氯化钠溶液,下列实验操作错误的是( )
A.取用NaCl B.称量NaCl
C.量取水 D.溶解
5.下列物质的用途错误的是( )
A.干冰用于人工降雨 B.氧气用作航空燃料
C.KNO 用作复合肥料 D.小苏打用于治疗胃酸过多
36.学会用化学思维去认识和理解世界,下列说法正确的是( )
A.宏观与微观:20mL酒精和20mL水混合后体积小于40mL,是因为分子之间存在间隔
B.变化与守恒:镁条燃烧后质量增加,可得出该反应不遵循质量守恒定律
C.模型与推理:质子和中子可以构成原子核,所以原子核都是由质子和中子构成的
D.探究与鉴别:双氧水和水都是无色液体,可以通过品尝鉴别区分。
7.“绿色、智能、节俭、文明”是杭州第19届亚运会的办会理念。亚运会主火炬选择“零碳甲醇”作为
绿色燃料,下面关于甲醇( )的说法正确的是( )
A.甲醇中含有6个原子
B.甲醇的相对原子质量是30g
C.甲醇中氢元素的质量分数最小
D.甲醇中C、H、O的元素质量比是1∶4∶1
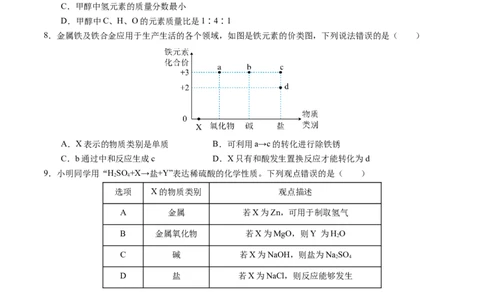
8.金属铁及铁合金应用于生产生活的各个领域,如图是铁元素的价类图,下列说法错误的是( )
A.X表示的物质类别是单质 B.可利用a→c的转化进行除铁锈
C.b通过中和反应生成c D.X只有和酸发生置换反应才能转化为d
9.小明同学用“HSO +X→盐+Y”表达稀硫酸的化学性质。下列观点错误的是( )
2 4
选项 X的物质类别 观点描述
A 金属 若X为Zn,可用于制取氢气
B 金属氧化物 若X为MgO,则Y 为HO
2
C 碱 若X为NaOH,则盐为NaSO
2 4
D 盐 若X为NaCl,则反应能够发生
10.下列实验操作能达到对应实验目的的是( )
选项 实验目的 实验操作
A 除去铁粉中混有的少量铜粉 加足量的稀盐酸,过滤
B 除去二氧化碳中混有的少量一氧化碳 将混合气体点燃
C 检验氧气是否收集满 将带火星的木条伸入集气瓶内
D 鉴别硝酸铵和氢氧化钠固体 取样,加水溶解,测溶液温度
二、填空题(每空1分,共10分)11.(3分)钙是维持人体正常功能所必需的元素,右图是补钙药品“金钙尔奇”的说明书,请你阅读并
回答问题。
(1)药品原料中,能为人体补充钙元素的物质是 ;
(2)按照规定用量服用,该补钙剂每天能为人体补充钙元素 mg;
(3)缺少钙元素,容易患_______。
A.青少年:佝偻病 B.贫血
C.老年人:骨质疏松 D.甲状腺肿大
12.(3分)电池的研发和使用动了我国能源结构的优化。
(1)锂元素在元素周期表中的相关信息如图甲所示,锂的相对原子质量是 。
(2)钠原子结构示意图如图丙所示,x= 。
(3)在化学反应中,锂原子和钠原子都易 (填“得到”或“失去”)电子。
13.(4分)生活中处处有化学,请根据所学化学知识回答下列问题。
(1)生活中常采用 的方法,将硬水转化为软水。
(2)用洗洁精可以洗去油污,是因为洗洁精具有 作用。
(3)生活中常接触到“高钙牛奶”,其中的“钙”应理解为 (填“元素”或“单质”)。
(4)酸性土壤不利于某些农作物的生长,农业上常用 改良酸性土壤。
三、简答题(每空1分,化学方程式2分,共12分)
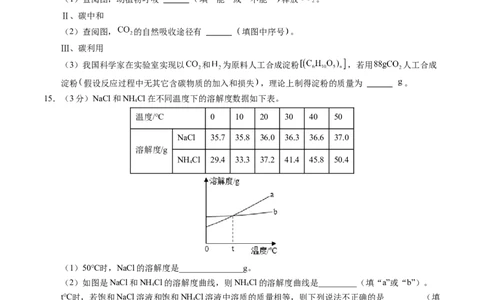
14.(3分)我国承诺: 年“碳达峰”, 年“碳中和”,体现大国担当。丁仲礼院士认为“碳中
和”是让人为排放的 ,被人为努力和自然过程所吸收。Ⅰ、碳排放
(1)查阅图,动植物呼吸 填“能”或“不能” 释放 。
Ⅱ、碳中和
(2)查阅图, 的自然吸收途径有 填图中序号 。
Ⅲ、碳利用
(3)我国科学家在实验室实现以 和 为原料人工合成淀粉 ,若用 人工合成
淀粉 假设反应过程中无其它含碳物质的加入和损失 ,理论上制得淀粉的质量为 。
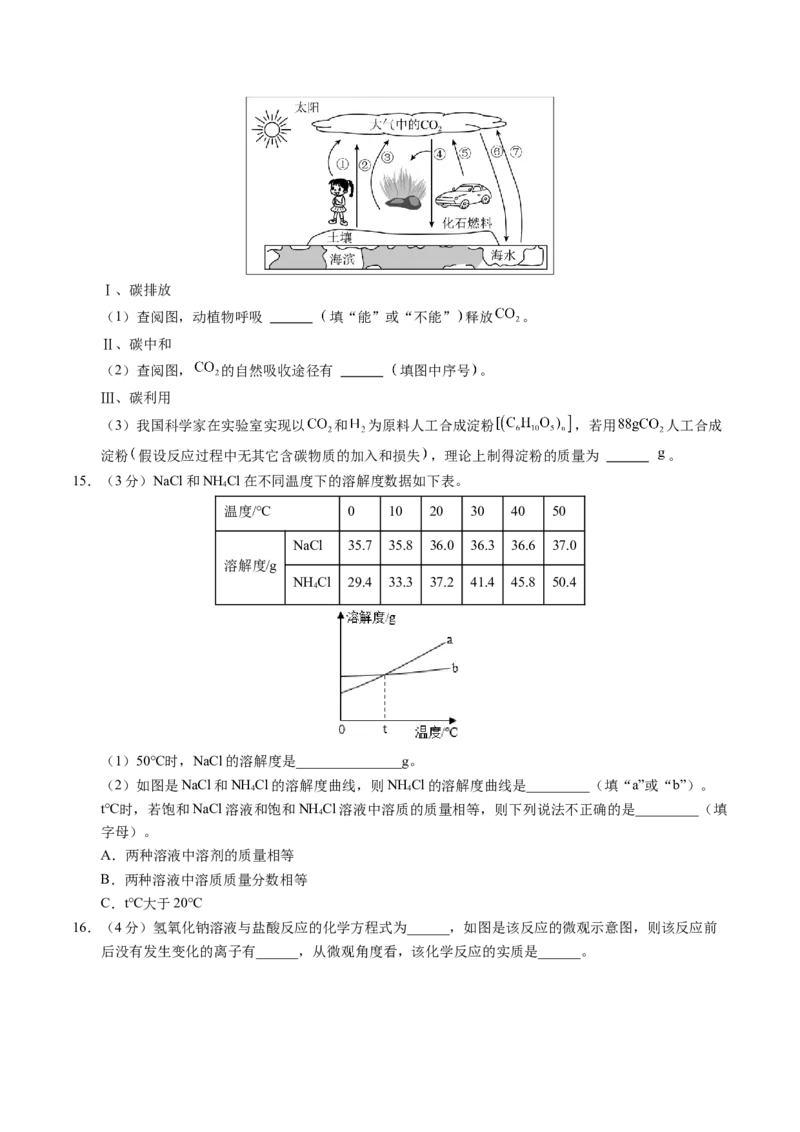
15.(3分)NaCl和NH Cl在不同温度下的溶解度数据如下表。
4
温度/℃ 0 10 20 30 40 50
NaCl 35.7 35.8 36.0 36.3 36.6 37.0
溶解度/g
NH Cl 29.4 33.3 37.2 41.4 45.8 50.4
4
(1)50℃时,NaCl的溶解度是_______________g。
(2)如图是NaCl和NH Cl的溶解度曲线,则NH Cl的溶解度曲线是_________(填“a”或“b”)。
4 4
t℃时,若饱和NaCl溶液和饱和NH Cl溶液中溶质的质量相等,则下列说法不正确的是_________(填
4
字母)。
A.两种溶液中溶剂的质量相等
B.两种溶液中溶质质量分数相等
C.t℃大于20℃
16.(4分)氢氧化钠溶液与盐酸反应的化学方程式为______,如图是该反应的微观示意图,则该反应前
后没有发生变化的离子有______,从微观角度看,该化学反应的实质是______。17.(2分)氯化钙常用作干燥剂,以石灰石(主要成分CaCO ,含少量MgCO 及不溶于水和盐酸的杂
3 3
质)制备氯化钙的主要过程如下:
(1)溶液A与石灰水反应的其中一个化学方程式为 ,该反应
的基本反应类型为 。
(2)实验室蒸发操作中玻璃棒的作用是 。
四、实验与探究题(每空1分,化学方程式2分,共12分)
18.(6分)如图是实验室中常用的装置,请结合装置回答下列问题。
(1)玻璃仪器a的名称是 ;
(2)在实验用 制取较纯净的氧气,选择的装置最佳组合是 填图示中的序号 ,该反
应的化学方程式为 ;
(3)实验室常用大理石和稀盐酸反应制取 ,该实验选用的发生装置是 填图示中的序号
,为了检验用此方法制得的 中是否混有 气体。可在发生和收集装置之间连接F装置,F内盛
装的试剂是 溶液 填写试剂名称 。
19.(6分)将一段去除氧化镁的镁条放入一定量的盐酸中,有气泡产生,充分反应后静置,发现试管中
有白色沉淀产生。为探究白色沉淀的成分,某中学九年级化学兴趣小组同学在老师的指导下进行如下
实验:
试管(盛有等体积等浓度的盐
① ② ③ ④
酸)
镁条质量(g) 1 1.5 2 2.5
实验现象 快速反应,试管发热,镁条全部消失
白色沉淀量(恢复至20℃) 无 少量 较多 很多【得出结论】(1)镁条与盐酸反应产生白色沉淀的量与 有关。
【提出问题】白色沉淀是什么物质?
【猜想与假设】
甲:白色沉淀可能是碳酸镁
乙:白色沉淀可能是生成的氯化镁增多析出的晶体
丙:白色沉淀可能是剩余的镁
丁:白色沉淀可能是氢氧化镁
(2)其他同学认为甲的猜想是错误的,原因是 。
【实验验证】
序号 操作步骤 实验现象 结论
取第一份白色不溶物于试管中,加入
1 (3) 乙同学猜想不成立
蒸馏水,振荡
取第二份白色不溶物于试管中,加入
2 没有气泡冒出 (4)
稀盐酸
(5)取第三份白色不溶物于试管 ①白色沉淀不溶解 ①丁同学猜想不成立
3
中, ②又出现白色沉淀 ②白色不溶物一定含氯元素
(6)在老师的帮助下,同学们得出白色沉淀物是Mg(OH)Cl 发应的化学方程式为
2 2 2
,若要镁恰好和稀盐酸完全反应生成白色沉淀物,
m(Mg):m(HCl)= 。(化为最简整数比)
五、计算题(6分)
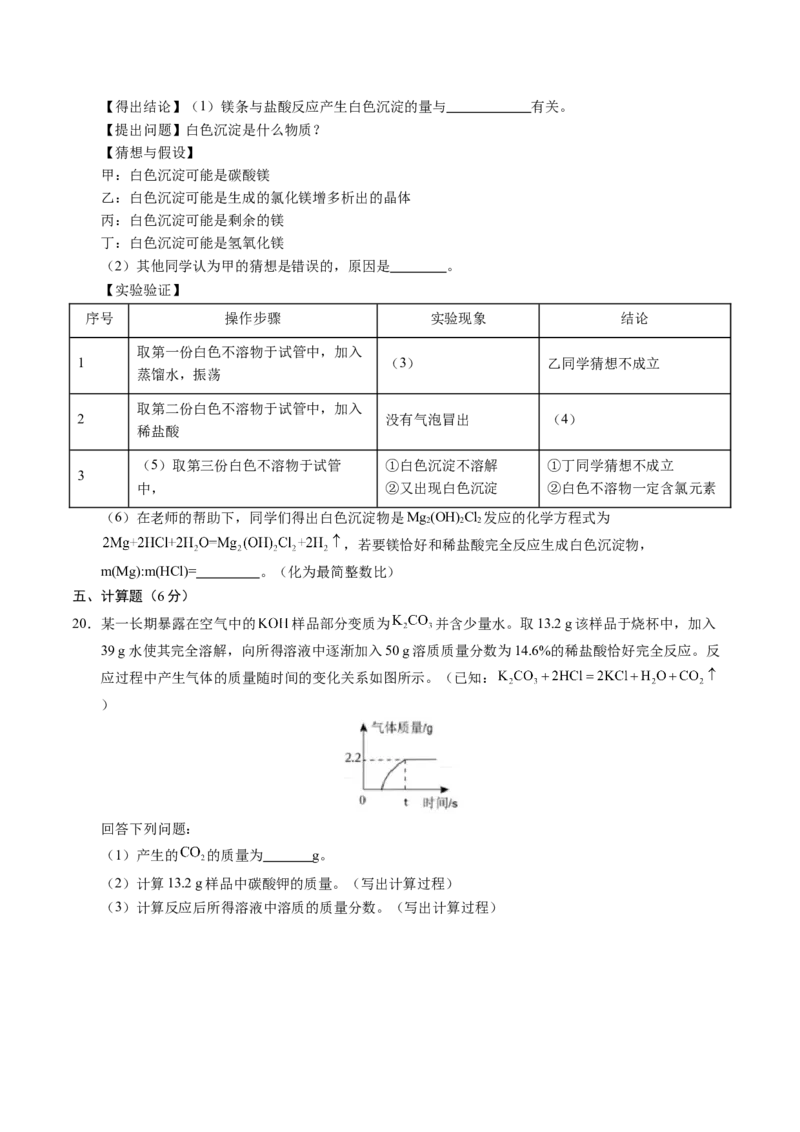
20.某一长期暴露在空气中的 样品部分变质为 并含少量水。取13.2 g该样品于烧杯中,加入
39 g水使其完全溶解,向所得溶液中逐渐加入50 g溶质质量分数为14.6%的稀盐酸恰好完全反应。反
应过程中产生气体的质量随时间的变化关系如图所示。(已知:
)
回答下列问题:
(1)产生的 的质量为 g。
(2)计算13.2 g样品中碳酸钾的质量。(写出计算过程)
(3)计算反应后所得溶液中溶质的质量分数。(写出计算过程)