文档内容
2024 年中考第一次模拟考试(广东卷)
化 学
(考试时间:60分钟 试卷满分:100分)
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答第Ⅰ卷时,选出每小题答案后,用2B铅笔把答题卡上对应题目的答案标号涂黑。如需改动,用橡
皮擦干净后,再选涂其他答案标号。写在本试卷上无效。
3.回答第Ⅱ卷时,将答案写在答题卡上。写在本试卷上无效。
4.考试结束后,将本试卷和答题卡一并交回。
可能用到的相对原子质量:H-1 C-12 N-14 O-16 Fe-56 Cl-35.5
第Ⅰ卷(选择题 共 45 分)
一、选择题:本大题共 15 小题,每小题 3 分,共 45 分。在每小题给出的四个选项中,只有一项是符
合题目要求的。
1.《天工开物》是我国古代科技发展的智慧结晶,下列记载的造物过程涉及化学变化的是
A.楠木制舟 B.轧蔗取浆 C.沙里淘金 D.烧石成灰
2.目前我国已发展成为名副其实的“材料大国”,新材料产业规模已达到全球第一。下列物品中,属于
用合成材料制成的是
A.铝合金门把手 B.木制桌椅 C.塑料快餐盒 D.纯羊毛衫
3.在测定锌、铟等元素的相对原子质量方面做出卓越贡献的中国科学家是
A.屠呦呦 B.张青莲 C.葛洪 D.侯德榜
4.下列实验操作正确的是
A.测量溶液的pH B.检查气密性
C.稀释浓硫酸 D.称量氢氧化钠
5.化学与人类生产、生活息息相关,下列叙述正确的是
A.棉花、涤纶、羊毛均为天然纤维
B.毛发、蛋清、皮肤的主要成分都是蛋白质
C.铁、锌、铅都为人体必需的微量元素D.化肥、农药对农业的高产丰收具有重要的作用,因此可以大量使用
6.下列化学符号的书写正确的是
A.两个氮原子:N B.氧化铝:AlO
2 2
C.两个钠离子:Na2+ D.两个水分子:2HO
2
7.空气是人类宝贵的自然资源。下列说法正确的是
A.硫在氧气中燃烧产生淡蓝色的火焰,放出热量,生成有刺激性气味的气体
B.稀有气体在任何条件下都不与其他物质发生化学反应
C.利用红磷可以测量出空气中氧气含量,体积约占空气总体积的五分之一
D.造成空气污染的主要气体有CO、CO、SO 、NO
2 2 2
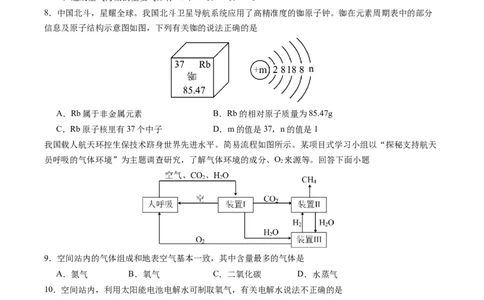
8.中国北斗,星耀全球。我国北斗卫星导航系统应用了高精准度的铷原子钟。铷在元素周期表中的部分
信息及原子结构示意图如图,下列有关铷的说法正确的是
A.Rb属于非金属元素 B.Rb的相对原子质量为85.47g
C.Rb原子核里有37个中子 D.m的值是37,n的值是1
我国载人航天环控生保技术跻身世界先进水平。简易流程如图所示。某项目式学习小组以“探秘支持航天
员呼吸的气体环境”为主题调查研究,了解气体环境的成分、O 来源等。回答下面小题
2
9.空间站内的气体组成和地表空气基本一致,其中含量最多的气体是
A.氮气 B.氧气 C.二氧化碳 D.水蒸气
10.空间站内,利用太阳能电池电解水可制取氧气,有关电解水说法不正确的是
A.太阳能直接转化为化学能 B.正极产生了氧气
C.产生的氢气循环使用 D.电解过程在装置(Ⅲ)进行
11.空间站里的氧气源自于电解水,所得氢气与二氧化碳反应生成水和甲烷(CH),该反应的微观示意
4
图如图所示。依据图示,下列叙述错误的是
A.化学反应前后分子种类不变 B.原子可以构成分子
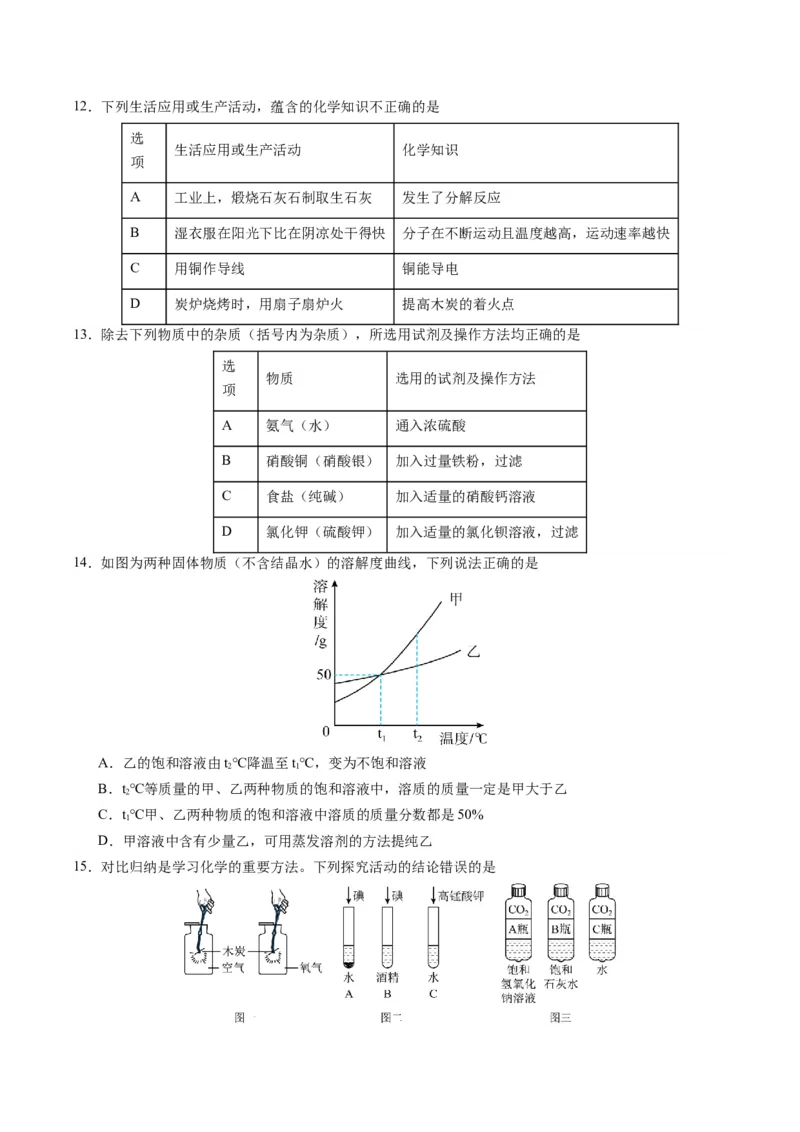
C.化学反应中分子可以再分 D.化学反应前后原子种类不变12.下列生活应用或生产活动,蕴含的化学知识不正确的是
选
生活应用或生产活动 化学知识
项
A 工业上,煅烧石灰石制取生石灰 发生了分解反应
B 湿衣服在阳光下比在阴凉处干得快 分子在不断运动且温度越高,运动速率越快
C 用铜作导线 铜能导电
D 炭炉烧烤时,用扇子扇炉火 提高木炭的着火点
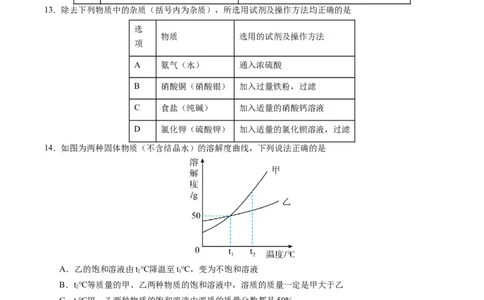
13.除去下列物质中的杂质(括号内为杂质),所选用试剂及操作方法均正确的是
选
物质 选用的试剂及操作方法
项
A 氨气(水) 通入浓硫酸
B 硝酸铜(硝酸银) 加入过量铁粉,过滤
C 食盐(纯碱) 加入适量的硝酸钙溶液
D 氯化钾(硫酸钾) 加入适量的氯化钡溶液,过滤
14.如图为两种固体物质(不含结晶水)的溶解度曲线,下列说法正确的是
A.乙的饱和溶液由t℃降温至t℃,变为不饱和溶液
2 1
B.t℃等质量的甲、乙两种物质的饱和溶液中,溶质的质量一定是甲大于乙
2
C.t℃甲、乙两种物质的饱和溶液中溶质的质量分数都是50%
1
D.甲溶液中含有少量乙,可用蒸发溶剂的方法提纯乙
15.对比归纳是学习化学的重要方法。下列探究活动的结论错误的是A.图一木炭在氧气中燃烧比在空气中更剧烈,氧气的浓度是影响燃烧剧烈程度的因素
B.图二A试管中固体几乎不溶,B试管中固体可溶,溶剂的种类是影响物质溶解性的因素;又补充了
C试管所示实验,溶质种类也是影响物质溶解性的因素
C.图三分别振荡二个软质塑料瓶,观察到塑料瓶变瘪的程度由大到小的顺序为 C>B>A
D.图三对比A瓶与C瓶的实验现象,可证明二氧化碳能与氢氧化钠溶液发生反应
第 II 卷(非选择题 共 55 分)
二、非选择题:本大题共 6 小题,第 16 小题 5 分,第 17 小题 10分,第 18~21 小题各 10 分, 共
55 分。
16.化学与生产和生活密切相关。请回答下列问题。
(1)人类每时每刻都离不开空气,因为空气中的氧气能 。
(2)俗语道“酒香不怕巷子深”,原因是 (用粒子的观点解
释)。
(3)某公司研发了一种以甲醇为原料的新型手机电池,其容量为锂电池的10倍,可连续使用1个月
才充一次电,其电池反应原理为2CHOH+3X+4NaOH=2Na CO+6H O。其中X的化学式为 。
3 2 3 2
(4)燃烧与人类生产、生活有着密切的关系。下列成语的原意与燃烧相关的是______(填字母)。
A.卧薪尝胆 B.釜底抽薪 C.火上浇油 D.煽风点火
(5)氢气是一种理想的能源,它的优点是 (合理即可)。
17. 阅读下面科普短文。
我国科学家屠呦呦因成功提取青蒿素而获得2015年诺贝尔生理学或医学奖。青蒿素是治疗疟疾的有效
成分,它的使用在全世界“拯救了几百万人的生命”。
很多中药古方都提到了青蒿入药抗疟疾。屠呦呦团队研究中医古籍,其中“青蒿一握,以水二升渍,
绞取汁,尽服之”,激发了她的灵感,是不是青蒿中抗疟的有效成分用水浸取后,蒸发水分时,高温
下被破坏了呢?于是采用沸点更低的乙醚在较低温度下进行提取,成功获得了青蒿素。完成样品纯化
后。通过元素分析等技术手段,测定相对分于质量为282,确定了青蒿素的化学式为C H O。
15 22 5
科学家在青蒿素的研究中进一步发现,一定条件下硼氢化钠能将青蒿素还原生成双氢青蒿素(化学式
为C H O),双氧青蒿素比青蒿素的水溶性好。治疗疟疾的效果更好。
15 24 5
回答下列问题。
(1)屠呦呦用乙醚提取青蒿素获得成功的关键在于改变的实验条件是 。
(2)青蒿素中氧元素的质量分数 (填“大于”或“等于”成“小于”)双氢青蒿素中氧元素
的质量分数。青蒿素分子中碳、氢原子的个数比 。双氢青蒿素的相对分子质量为 。
(3)从中国古代青蒿入药,到双氢青蒿素药物被世界卫生组织列为对抗疟疾的首选药物,经历了漫
长的历程。下列三项针对青蒿素的研究按时间先后排序(填序号) 。
①确定结构 ②分离提纯 ③人工合成
(4)“一定条件下硼氢化钠能将青蒿素还原生成双氢青蒿素”,这一变化说明
。
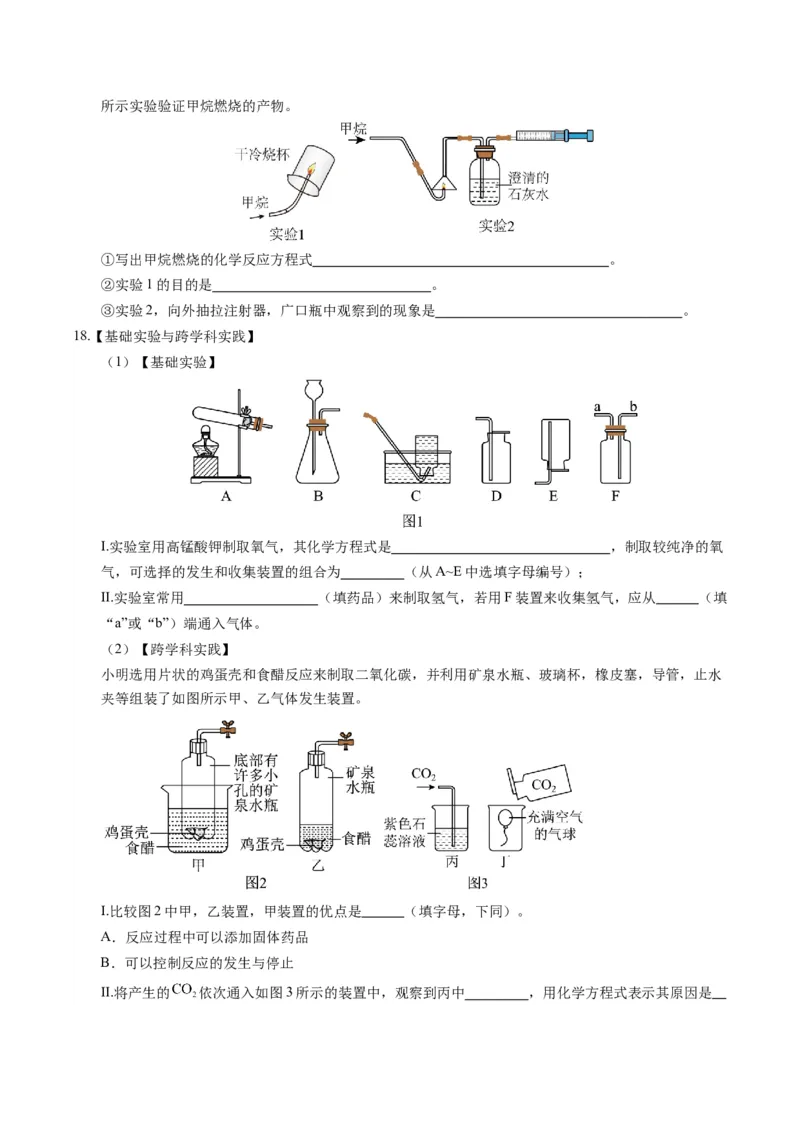
(5)确定物质的元素组成,也可以采用燃烧法。甲烷(化学式CH)燃烧生成水和二氧化碳,用下图
4所示实验验证甲烷燃烧的产物。
①写出甲烷燃烧的化学反应方程式 。
②实验1的目的是 。
③实验2,向外抽拉注射器,广口瓶中观察到的现象是 。
18.【基础实验与跨学科实践】
(1)【基础实验】
Ⅰ.实验室用高锰酸钾制取氧气,其化学方程式是 ,制取较纯净的氧
气,可选择的发生和收集装置的组合为 (从A~E中选填字母编号);
Ⅱ.实验室常用 (填药品)来制取氢气,若用F装置来收集氢气,应从 (填
“a”或“b”)端通入气体。
(2)【跨学科实践】
小明选用片状的鸡蛋壳和食醋反应来制取二氧化碳,并利用矿泉水瓶、玻璃杯,橡皮塞,导管,止水
夹等组装了如图所示甲、乙气体发生装置。
Ⅰ.比较图2中甲,乙装置,甲装置的优点是 (填字母,下同)。
A.反应过程中可以添加固体药品
B.可以控制反应的发生与停止
Ⅱ.将产生的 依次通入如图3所示的装置中,观察到丙中 ,用化学方程式表示其原因是;丁中 ,说明 密度比空气大。
19.为深度学习酸、碱、盐有关知识,某化学兴趣小组开展了下列探究活动。
(1)探究中和反应。
实验开始后将注射器内的液体缓慢地全部注入烧瓶内,用pH传感器测得烧瓶内溶液的pH变化如图
所示。
①烧瓶内发生反应的微观实质是 ;
②图中 点所示溶液中所含溶质是 (填化学式);
③下列试剂不能验证反应到达 点的是 (填字母序号)。
A.锌粒 B.硝酸银溶液 C.无色酚酞试液 D.氧化铁
(2)探究碱的性质。
氢氧化钠溶液露置于空气中容易变质,反应的化学方程式为 ;
【查阅资料】
I.氯化钙溶液呈中性。
Ⅱ.氯化钙溶液能与碳酸钠溶液反应:
为探究久置氢氧化钠溶液的变质程度,进行了如下实验:
【实验报告】
实验步骤 实验现象 实验结论
①取少量该溶液于试管中,向溶液中滴加过量的氯化钙 说明原溶液中一定有
有 生成
溶液,充分反应 ,
②取步骤①试管中的少量上层清液,滴加无色酚酞试液 溶液变红色 说明原溶液中一定有
【实验结论】氢氧化钠溶液 (填“部分”或“全部”)变质。
【反思与评价】在上述实验步骤①中,某同学提出可用氢氧化钙溶液代替氯化钙溶液,你认为该方案
是否可行: (填“是”或“否”);用化学方程式解释其原因
。
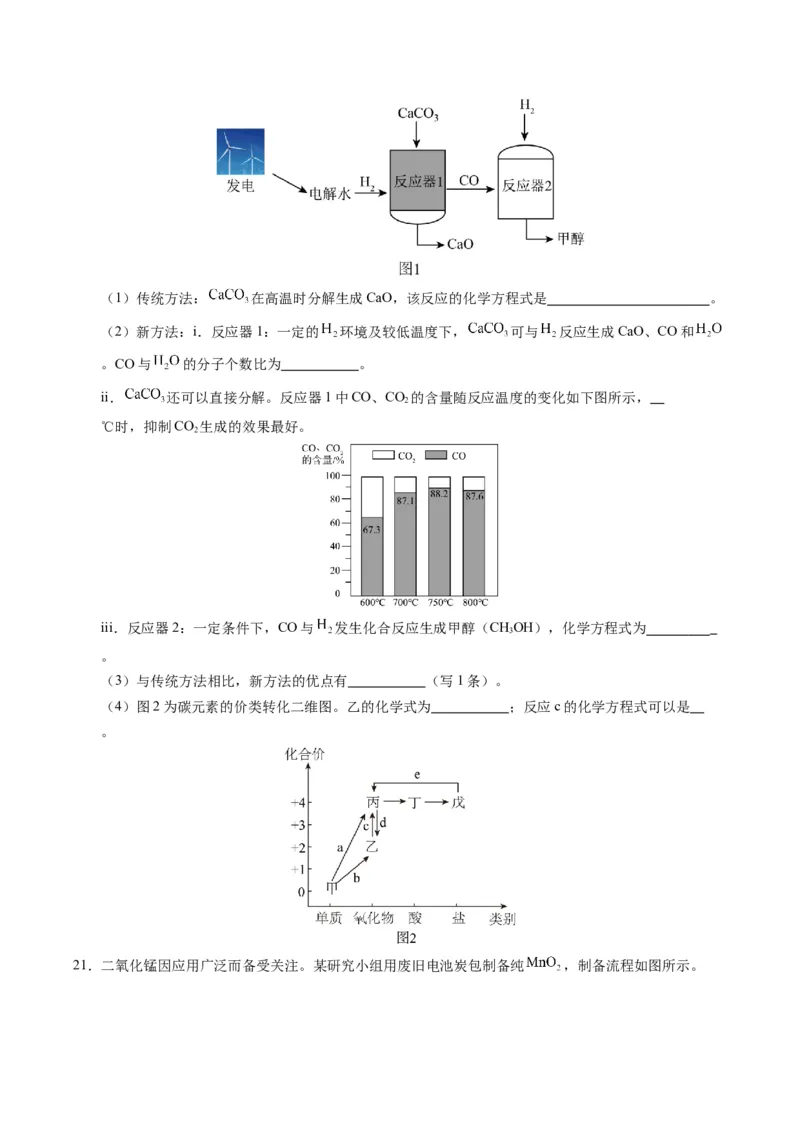
20.电解水制氢联合碳酸钙分解制备氧化钙,能减少碳排放,助力碳中和。该新方法的示意图如下图1所
示。(1)传统方法: 在高温时分解生成CaO,该反应的化学方程式是 。
(2)新方法:i.反应器1:一定的 环境及较低温度下, 可与 反应生成CaO、CO和
。CO与 的分子个数比为 。
ii. 还可以直接分解。反应器1中CO、CO 的含量随反应温度的变化如下图所示,
2
℃时,抑制CO 生成的效果最好。
2
iii.反应器2:一定条件下,CO与 发生化合反应生成甲醇(CHOH),化学方程式为
3
。
(3)与传统方法相比,新方法的优点有 (写1条)。
(4)图2为碳元素的价类转化二维图。乙的化学式为 ;反应c的化学方程式可以是
。
21.二氧化锰因应用广泛而备受关注。某研究小组用废旧电池炭包制备纯 ,制备流程如图所示。已知:焙烧 制取 的化学方程式为 。
请回答下列问题:
(1)加入 溶液后发生反应的基本反应类型为 ;过滤Ⅱ后洗涤滤渣,证
明滤渣已洗净的方法是 。
(2)试根据化学方程式求46.0g 通过焙烧最多制得的 的质量是多少?(请写出计算过
程)。
(3)焙烧 的过程中,固体产物的质量和成分随温度的变化如下图所示,则焙烧 制取
应该控制反应温度不高于 ℃;若把焙烧46.0g 温度控制在
900℃,充分反应后的固体产物质量为 g。