文档内容
第六讲 常见的酸
模块一 酸碱指示剂
知识精讲
知识点一 酸碱指示剂
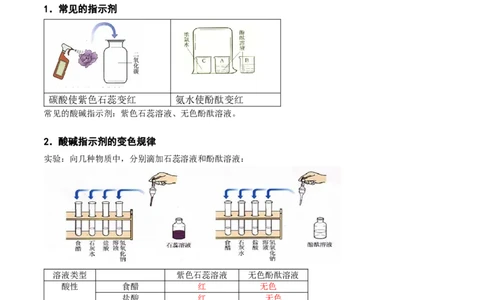
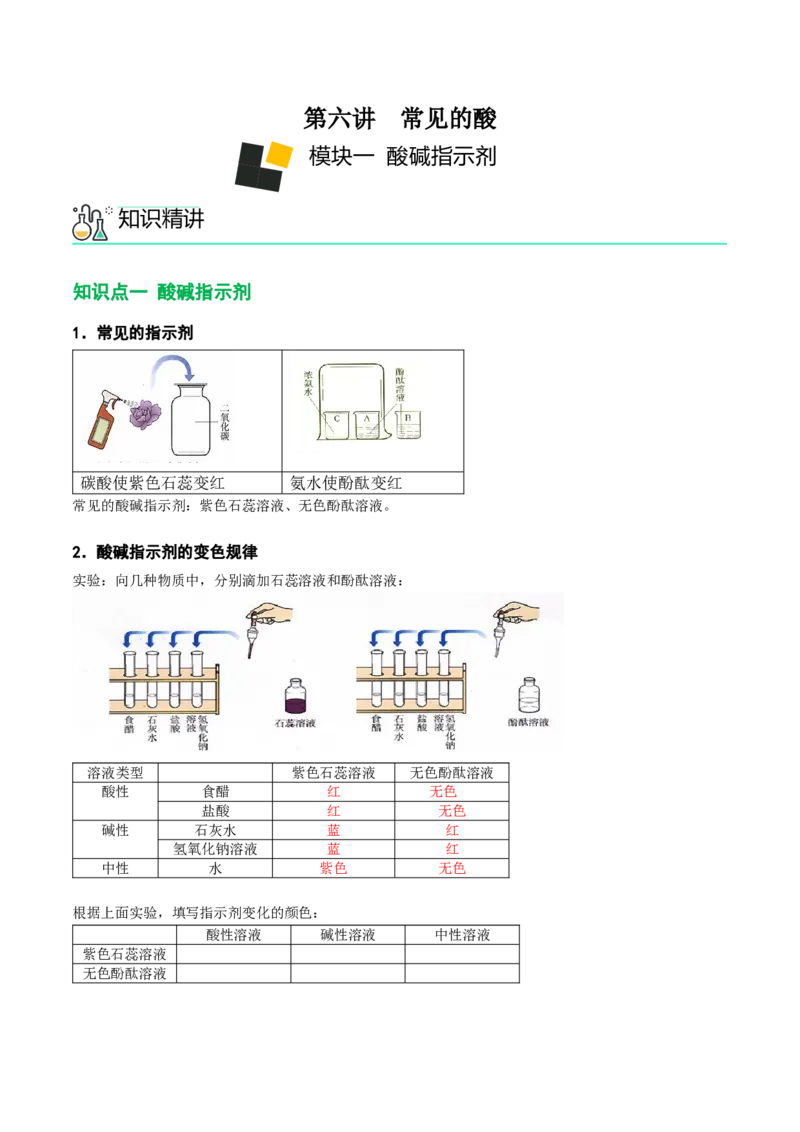
1.常见的指示剂
碳酸使紫色石蕊变红 氨水使酚酞变红
常见的酸碱指示剂:紫色石蕊溶液、无色酚酞溶液。
2.酸碱指示剂的变色规律
实验:向几种物质中,分别滴加石蕊溶液和酚酞溶液:
溶液类型 紫色石蕊溶液 无色酚酞溶液
酸性 食醋 红 无色
盐酸 红 无色
碱性 石灰水 蓝 红
氢氧化钠溶液 蓝 红
中性 水 紫色 无色
根据上面实验,填写指示剂变化的颜色:
酸性溶液 碱性溶液 中性溶液
紫色石蕊溶液
无色酚酞溶液归纳总结
1.记忆口诀:紫色石蕊‘遇碱变蓝、遇酸变红’。无色酚酞‘遇碱变红、遇酸不变’。
2.指示剂变色是化学变化。比如酚酞在碱性溶液中生成新物质,这种物质显红色。
思考与交流
(1)紫色石蕊能使盐酸变红色,对吗?此过程中,盐酸有变化吗?紫色石蕊变化了吗?
(2)向某溶液滴加无色酚酞溶液,溶液不变色,则该溶液一定是酸性吗?
3.生活中自制指示剂
某些植物的花汁可作为酸碱指示剂。向紫甘蓝中滴加蒸馏水、稀酸溶液、稀碱溶液,颜色如下表。
在不同溶液中的颜色变化
花汁
中性溶液 酸性溶液 碱性溶液
紫甘蓝 紫色 红色 黄色
(1)向食醋中滴加紫甘蓝汁液后,溶液颜色变 。(填‘紫色’、‘红色’或‘黄色’)
(2)向柠檬汁中滴加紫甘蓝汁液后变红色,由此可知柠檬汁显 。(填‘酸性’、‘碱
性’或‘中性’)
经典例题
紫色石蕊和无色酚酞溶液
【例1】日常生活中的下列物质能使紫色石蕊溶液变蓝的是 ( )
A.蒸馏水 B.稀盐酸 C.石灰水 D.食醋
【例2】向某液体中滴入无色酚酞试液后不变色,向该溶液中滴入紫色石蕊试液,则( )
A.一定显红色 B.可能为紫色也可能为红色
C. 可能显蓝色 D.一定显无色
【例3】“雪碧“是一种无色的碳酸饮料,将少量“雪碧“滴入紫色石蕊试液中,然后再加热,溶液的颜
色变化情况是( )
A.先变红后变紫 B.变红后颜色不再改变
C.先变无色后变红 D.先变蓝后变紫
自制指示剂
【例1】一种卷心菜的菜汁呈紫色,遇醋酸变成红色,遇碱性洗涤剂变成黄绿色,下列也能使卷心菜菜汁
呈黄绿色的物质是( )A.肥皂水 B.柠檬汁 C.食盐水 D.雪碧
模块二 常见的酸
知识点一 酸的含义
酸:解离时产生的阳离子全部是H+的化合物。酸都含有H+。
盐酸:HCl在水溶液中以H+和Cl-形式存在,发生解离:HCl=H++Cl-
资料卡片——解离常见强酸在溶液中发生解离:通式:酸= H+ + 酸根。
(1)氢碘酸:HI=H++I-
(2)硫酸:HSO =2H++SO2-
2 4 4
模仿上述,写出解离的离子:
(3)氢溴酸:HBr=
(4)硝酸:HNO=
3
(5)硫酸氢钠:NaHSO =Na++H++SO2-,它也能解离出H+,它属于酸吗?
4 4
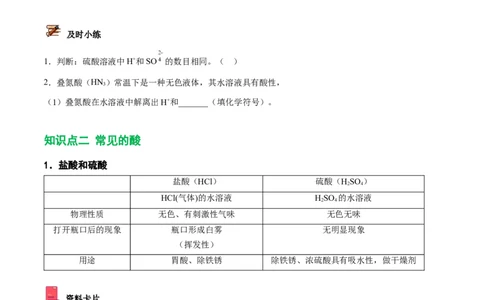
及时小练
1.判断:硫酸溶液中H+和SO 的数目相同。( )
2.叠氮酸(HN )常温下是一种无色液体,其水溶液具有酸性,
3
(1)叠氮酸在水溶液中解离出H+和_______(填化学符号)。
知识点二 常见的酸
1.盐酸和硫酸
盐酸(HCl) 硫酸(HSO )
2 4
HCl(气体)的水溶液 HSO 的水溶液
2 4
物理性质 无色、有刺激性气味 无色无味
打开瓶口后的现象 瓶口形成白雾 无明显现象
(挥发性)
用途 胃酸、除铁锈 除铁锈、浓硫酸具有吸水性,做干燥剂
资料卡片
(1)为什么打开盐酸后,瓶口形成白雾?
盐酸易挥发,挥发出的氯化氢气体与空气中的水蒸气接触,形成盐酸小液滴。
(2)镁的燃烧时,会产生大量白烟,这又是什么原因?
镁与氧气反应生成MgO的固体小颗粒,分散在空气中形成固体小颗粒。
白雾——液体小液滴。白烟——固体小颗粒。2.浓盐酸和浓硫酸敞口后的变化
密度 物理特性 溶质质量 溶剂质量 溶液质量 溶质质量分
数
浓盐酸(37%) 1.19g/cm3 挥发性
浓硫酸(98%) 1.84g/cm3 吸水性
【练1】如图所示,已平衡的天平两端放着两个分别盛有浓盐酸和浓硫酸的敞口烧杯,过一段时间后,天
平会( )
A.左端下沉 B.右端下沉 C.仍平衡 D.无法判断
经典例题
盐酸和硫酸
【例1】下列关于盐酸的描述,错误的是( B )
A.盐酸中的溶质是HCl B.盐酸能使紫色石蕊溶液变蓝
C.人体胃液中含有盐酸,可帮助消化 D.打开装有浓盐酸的试剂瓶瓶盖,瓶口处有白雾出现
浓酸敞口放置变化
【例1】下列说法正确的是 ( )
A.盐酸能使紫色石蕊溶液变蓝
B.浓硫酸露置于空气中,溶质的质量分数变小
C.长期露置于空气中的浓硫酸,其成分不会发生变化
D.打开盛浓硫酸的试剂瓶,瓶口会产生白雾
【例2】下列物质存放在烧杯中一段时间后,质量变小的是( )
A.澄清石灰水 B.浓硫酸 C.浓盐酸 D.生石灰
3.浓硫酸
(1)腐蚀性(脱水性)
①浓硫酸具有强烈的腐蚀性。它能将纸张、木材、皮肤里的氢、氧元素按2:1的比例脱去,生成黑色的炭。图1 用浓硫酸在纸上写字 图2 浓硫酸倒在蔗糖里,蔗糖变黑且膨胀,形成‘黑面包’
②如果不慎浓硫酸沾在皮肤上,该怎么办呢?
应立即用大量水冲洗,然后涂上3%~5%的NaHCO 溶液。
3
(2)浓硫酸的稀释
(1)浓硫酸:密度:1.84g/cm3,浓硫酸溶于水放出大量的热。
(2)操作方法:应将浓硫酸沿烧杯内壁,缓慢注入水里,并用玻璃棒不断搅拌。(记忆口诀:‘杯壁下
流’)
思考与交流
(1)若向浓硫酸中倒水,会产生什么后果?(已知信息:浓硫酸:密度:1.84g/cm3,浓硫酸溶于水
放出大量的热。)
经典例题
浓硫酸的腐蚀性
【例1】下列试剂瓶应有 标志的是( )A.氯化钠 B.蒸馏水 C.浓硫酸 D.葡萄糖
浓硫酸的稀释
【例1】下列实验操作和处理不正确的是( )
A.用装浓硫酸的洗气瓶干燥、制备氢气
B.用蘸浓硫酸的玻璃棒在纸上写字,观察其脱水性
C.往浓硫酸里慢慢的小心的滴蒸馏水,配置稀硫酸
D.实验时不慎沾浓硫酸在皮肤上,立即用干布抹去,再用大量水冲洗
【例2】下列实验操作正确的是( )
A.稀释浓硫酸 B.检查装置的气密性
C.滴加少量的液体 D.过滤泥沙水
模块三 酸的化学性质
知识精讲
知识点三 酸的化学性质
1.与活泼金属反应
回顾金属活动性顺序表:
(1)排在H前的金属能与酸反应,置换出氢气。即酸的化学性质之一是能与活泼金属反应。
回忆所学的知识,完成下表。
与稀盐酸反应的化学方程式 与稀硫酸反应的化学方程式镁 Mg+2HCl===MgCl 2 +H 2 ↑ Mg+H 2 SO 4 ===MgSO 4 +H 2 ↑
铁 Fe+2HCl===FeCl 2 +H 2 ↑ Fe+H 2 SO 4 ===FeSO 4 +H 2 ↑
资料卡片——金属的蚀刻
用酸在金属表面雕刻美图。
2.与金属氧化物反应
(1)稀盐酸的用途之一是除铁锈(FeO)。
2 3
现象 化学方程式
Fe O+6HCl===2FeCl +3H O
铁锈+盐酸 2 3 3 2
铁锈逐渐消失,溶液由无色变为黄色
铁锈+稀硫酸
(2)与氧化铜(CuO)反应
现象 化学方程式
氧化铜+盐酸 CuO + 2HCl = CuCl 2 + H 2 O
黑色粉末溶解,溶液由无色变为蓝色
氧化铜+稀硫酸
思考与交流(1)现有一片久置的铝箔,金属铝表面有氧化铝,若加入稀盐酸,会有什么现象?用化学方程式表示
出来。
【练1】将生锈的铁钉放入稀盐酸中片刻,观察到的现象是 ,发生反应的
化学方程式为 ;反应一段时间后,又观察到的现象是
,溶液变为浅绿色,发生反应的化学方程式为 。
经典例题
酸与金属反应
【例1】在铁件表面镀铬(Cr)前,要除去铁件表面的铁锈,可用的试剂是( )
A.水 B.稀盐酸 C.氢氧化钠溶液 D.石灰水
酸与金属氧化物反应
【例 1】醋酸(CHCOOH 是食醋的成分之一,其水溶液中存在 H+和 CHCOO-。下列说法正确的是
3 3
( )
A.醋酸属于氧化物 B.醋酸不能用于除铁锈
C.醋酸能与镁反应产生氢气 D.醋酸中碳元素的质量分数最大
【例2】取2g氧化铜固体于烧杯中,向其中加入一定量的稀硫酸,恰好完全反应,得到的溶液质量为
51g。请计算:该稀硫酸中溶质的质量分数。
酸的通性
【例1】柠檬酸(C HO)是一种较强的有机酸,在水溶液中可以解离出H+,从而呈酸性,主要用于制香料或作饮
6 8 7
料的酸化剂。下列物质不能与柠檬酸反应的是 ( )
A.Mg B.Fe O C.CO D.FeO
2 3 2
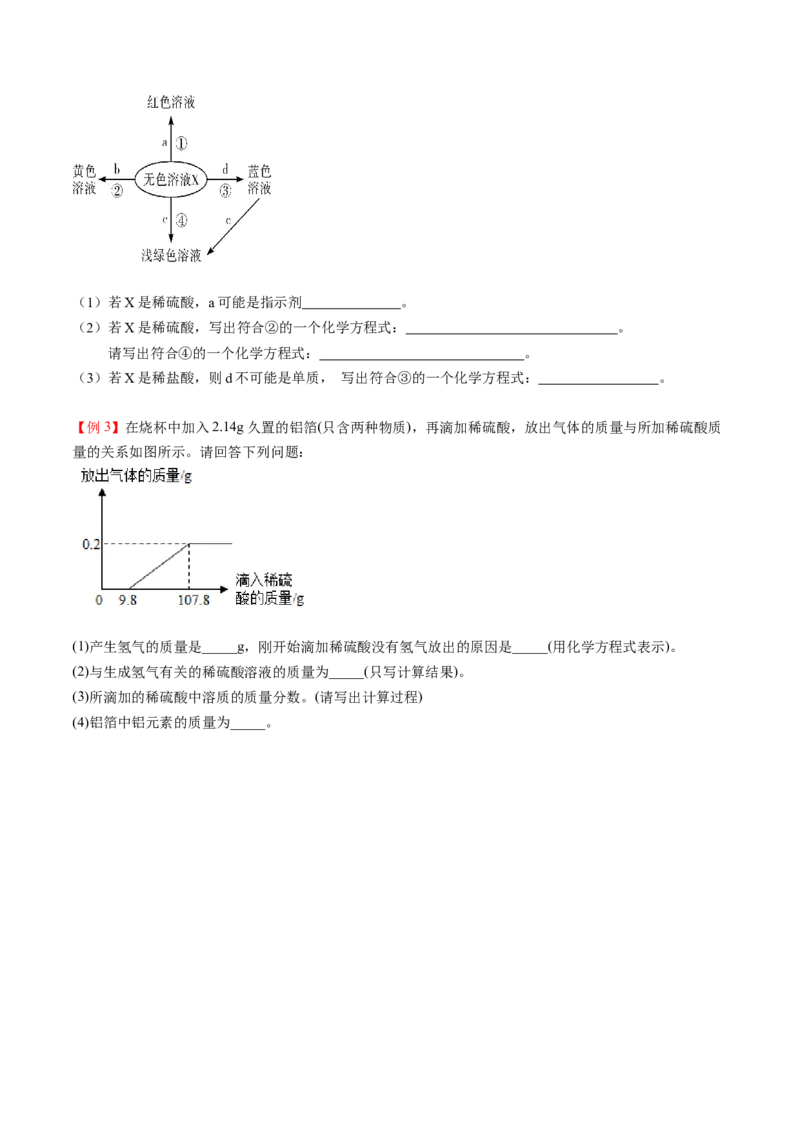
【例2】如图表示化学反应中溶液的颜色变化,请回答下列问题。(1)若X是稀硫酸,a可能是指示剂 。
(2)若X是稀硫酸,写出符合②的一个化学方程式: 。
请写出符合④的一个化学方程式: 。
(3)若X是稀盐酸,则d不可能是单质, 写出符合③的一个化学方程式: 。
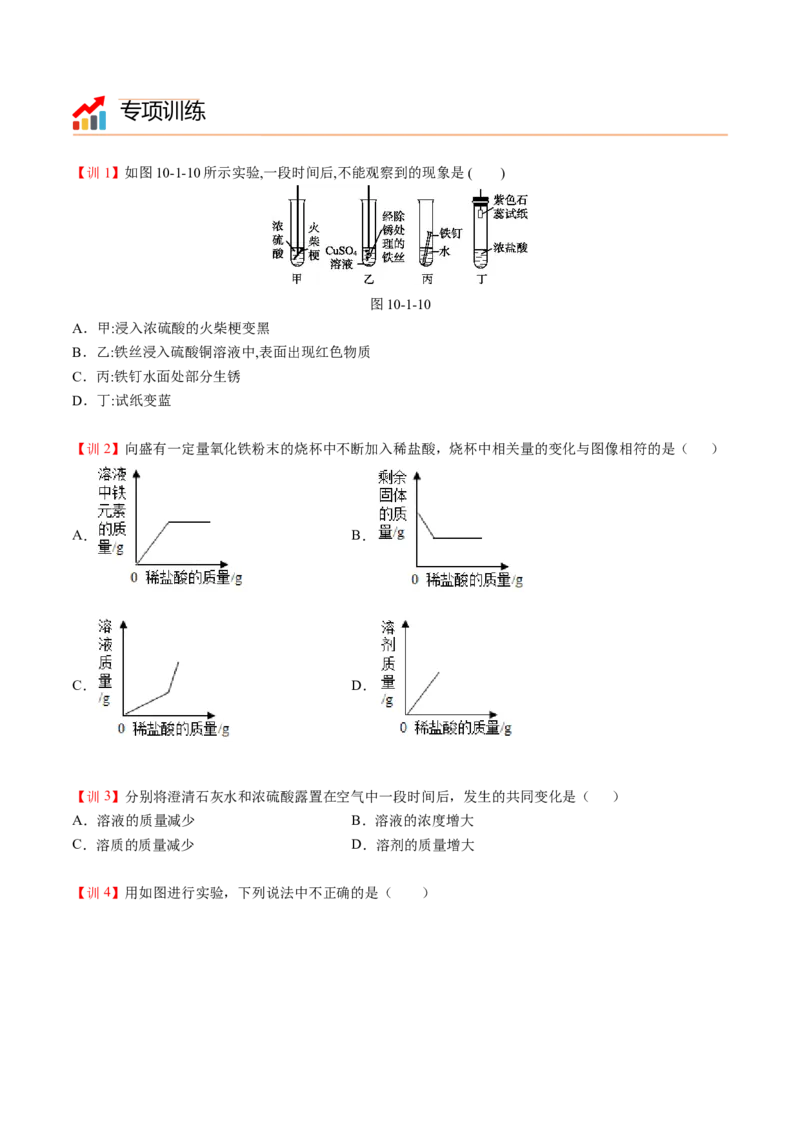
【例3】在烧杯中加入2.14g久置的铝箔(只含两种物质),再滴加稀硫酸,放出气体的质量与所加稀硫酸质
量的关系如图所示。请回答下列问题:
(1)产生氢气的质量是_____g,刚开始滴加稀硫酸没有氢气放出的原因是_____(用化学方程式表示)。
(2)与生成氢气有关的稀硫酸溶液的质量为_____(只写计算结果)。
(3)所滴加的稀硫酸中溶质的质量分数。(请写出计算过程)
(4)铝箔中铝元素的质量为_____。专项训练
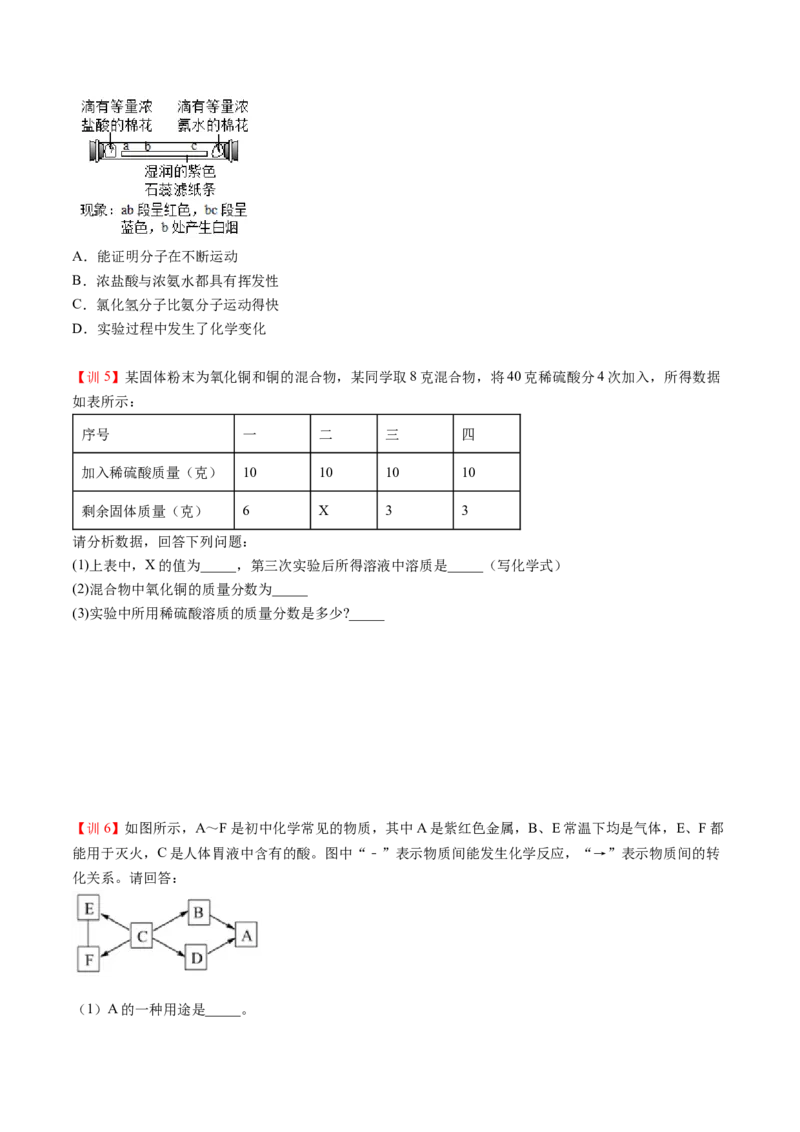
【训1】如图10-1-10所示实验,一段时间后,不能观察到的现象是( )
图10-1-10
A.甲:浸入浓硫酸的火柴梗变黑
B.乙:铁丝浸入硫酸铜溶液中,表面出现红色物质
C.丙:铁钉水面处部分生锈
D.丁:试纸变蓝
【训2】向盛有一定量氧化铁粉末的烧杯中不断加入稀盐酸,烧杯中相关量的变化与图像相符的是( )
A. B.
C. D.
【训3】分别将澄清石灰水和浓硫酸露置在空气中一段时间后,发生的共同变化是( )
A.溶液的质量减少 B.溶液的浓度增大
C.溶质的质量减少 D.溶剂的质量增大
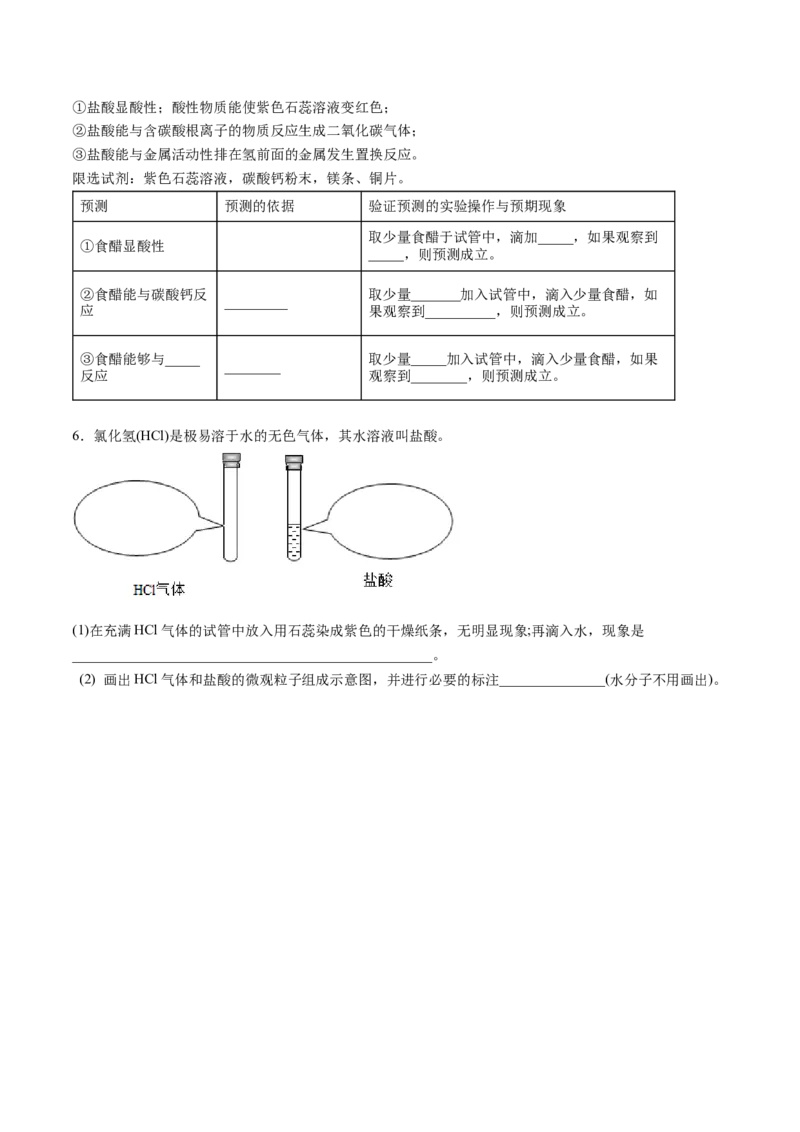
【训4】用如图进行实验,下列说法中不正确的是( )A.能证明分子在不断运动
B.浓盐酸与浓氨水都具有挥发性
C.氯化氢分子比氨分子运动得快
D.实验过程中发生了化学变化
【训5】某固体粉末为氧化铜和铜的混合物,某同学取8克混合物,将40克稀硫酸分4次加入,所得数据
如表所示:
序号 一 二 三 四
加入稀硫酸质量(克) 10 10 10 10
剩余固体质量(克) 6 X 3 3
请分析数据,回答下列问题:
(1)上表中,X的值为_____,第三次实验后所得溶液中溶质是_____(写化学式)
(2)混合物中氧化铜的质量分数为_____
(3)实验中所用稀硫酸溶质的质量分数是多少?_____
【训6】如图所示,A~F是初中化学常见的物质,其中A是紫红色金属,B、E常温下均是气体,E、F都
能用于灭火,C是人体胃液中含有的酸。图中“﹣”表示物质间能发生化学反应,“→”表示物质间的转
化关系。请回答:
(1)A的一种用途是_____。(2)B、E的化学式分别为_____、_____。
(3)E﹣F的化学方程式为_____。
(4)B→A的化学方程式为_____。
提分作业
1.化学学习小组做实验时,记录了下列实验现象,其中正确的是( )
A.碳在氧气中燃烧发出白光,生成二氧化碳
B.向稀氨水中滴加几滴酚酞试液,溶液变成红色
C.细铁丝在空气中剧烈燃烧,火星四射,有黑色固体生成
D.红磷在空气中燃烧,发出红色的火焰,产生大量白色烟雾
2.关于硫酸的说法错误的是( )
A.稀硫酸与锌反应可制得氢气 B.稀硫酸可用于除铁锈
C.可将水注入浓硫酸中进行稀释 D.浓硫酸可用来干燥氢气
3.下图是物质间发生化学反应的颜色变化,其中X是( )
A.稀硫酸 B.氯化钠溶液
C.硫酸钠溶液 D.澄清石灰水
4.小明设计了右图装置探究“微粒是不断运动的”,一段时间后,可观察到紫红色石蕊变红色,
则A 物质是( )
A.浓氨水 B.浓硫酸 C.生石灰 D.浓盐酸
5.食醋的某些性质与盐酸相似,某化学兴趣小组为探究食醋的化学性质,进行了以下实验:
查阅资料可知:①盐酸显酸性;酸性物质能使紫色石蕊溶液变红色;
②盐酸能与含碳酸根离子的物质反应生成二氧化碳气体;
③盐酸能与金属活动性排在氢前面的金属发生置换反应。
限选试剂:紫色石蕊溶液,碳酸钙粉末,镁条、铜片。
预测 预测的依据 验证预测的实验操作与预期现象
取少量食醋于试管中,滴加_____,如果观察到
①食醋显酸性
_____,则预测成立。
②食醋能与碳酸钙反 取少量_______加入试管中,滴入少量食醋,如
_________
应 果观察到__________,则预测成立。
③食醋能够与_____ 取少量_____加入试管中,滴入少量食醋,如果
________
反应 观察到________,则预测成立。
6.氯化氢(HCl)是极易溶于水的无色气体,其水溶液叫盐酸。
(1)在充满HCl气体的试管中放入用石蕊染成紫色的干燥纸条,无明显现象;再滴入水,现象是
___________________________________________________。
(2) 画出HCl气体和盐酸的微观粒子组成示意图,并进行必要的标注_______________(水分子不用画出)。