文档内容
4、下列反应属于氧化还原反应的是( )
2024-2025学年度第一学期福九联盟(高中)期中联考
高中一年化学科试卷 A、CuSO BaCl CuCl BaSO
4 2 2 4
B、NaHH ONaOHH
2 2
考试日期:11月15日 完卷时间:75分钟 满 分:100分 C、CaOCO CaCO
2 3
D、Mg N 6H O3Mg(OH) 2NH
3 2 2 2 3
可能用到的相对原子质量:H-1 He-4 C-12 N-14 O-16 Ne-20 Na-23 S-32
Cl-35.5 Ba-137 Ca-40 Fe-56
5、某蓝色液中含下列离子中的若干种:Cu2+、Na+、Ba2+、Cl-、NO-、SO2-,各种离子的
3 4
I 卷
数目相等。取适量该溶液加入硝酸银溶液,有白色沉淀生成,滴加硝酸后仍存有沉淀。
一、选择题(共16小题,每小题 3分,共48 分。每小题有且仅有一个正确答案)
根据上述实验,以下推测不正确的是(已知:硫酸银会溶于硝酸)
CCl
1、中国科学技术大学的钱逸泰教授等人以 4和金属钠为原料,在700℃时制造出纳米 A.溶液中可能有Na+ B.溶液中可能有Ba2+
级金刚石粉末(直径约5nm)。该成果发表在世界权威的科学杂志上,被科学届评价为
C.溶液中可能有NO- D.溶液中可能有SO2-
3 4
“稻草变黄金”。下列说法错误的是( )
6、用N表示阿伏加德罗常数的值,下列叙述正确的是( )
A、化学是一门具有创造性的科学 A
A、含有N个氦原子的氦气体积约为22.4 L
B、“稻草变黄金”的过程中元素种类没有变化 A
C、纳米级金刚石粉末(直径约5nm)属于胶体 B、25 ℃,1.01×105 Pa,32 g SO 中含有的原子数为1.5N
2 A
D、将该金刚石粉末分散到水中能产生丁达尔效应 C、在常温常压下,11.2 L Cl 含有的分子数为0.5N
2 A
2、我国力争在2060年前实现“碳中和”,体现了中国对解决气候问题的大国担当。在
D、1molMgCl 固体溶于1L水中,所得溶液Cl浓度为2molL1
实际生产中,可利用反应CO+NaOH=NaHCO 来捕捉废气中的CO,下列有关化学用语或 2
2 3 2
7、下列关于物质分类的正确组合是( )
说法正确的是( )
碱 酸 盐 碱性氧化物 酸性氧化物
A、中子数为8的碳原子:C B、Na+的结构示意图:
8
A Ba(OH) NaHSO NaHCO AlO CO
2 4 3 2 3 2
C、NaHCO 的摩尔质量是84g D、16O、17O、18O互为氧元素的同位素 B NaOH HCl NaCl NaO CO
3 2
3、检验某溶液中是否含有下列常见离子的方法、现象及结论正确的是( )
C Cu(OH)CO HS CaF MgO SO
2 2 3 2 2 2
A、加入NaOH溶液并加热,有能使湿润的红色石蕊试纸变蓝的气体产生,说明一定含NH
4
D KOH HNO CaCO CaO SO
3 3 3
B、先加入硝酸无现象,再滴加BaCl 溶液产生白色沉淀,说明一定含SO2ˉ A、 A B、 B
2 4
C、 C D、 D
C、先加入盐酸无现象,再滴加AgNO 溶液产生白色沉淀,说明一定含Clˉ
3
D、用洁净的玻璃棒蘸取少许溶液在酒精灯上灼烧,观察火焰呈黄色,则一定有Na+
高一化学试卷 -1-(共8页) 高一化学试卷 -2-(共8页)
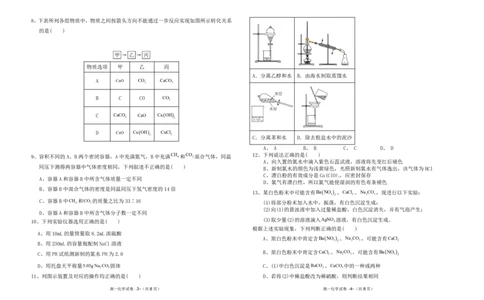
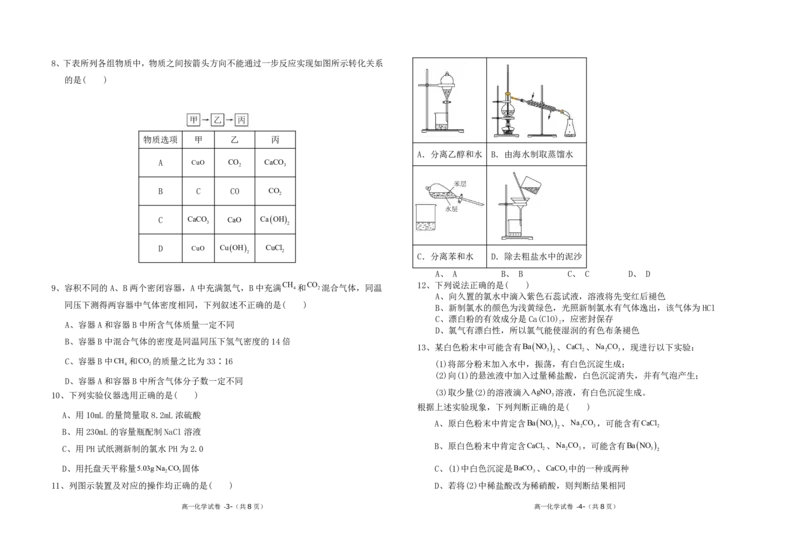
{#{QQABTYQUggiAABIAAQhCQQHyCkKQkhEAAYgOQEAIoAAByQFABAA=}#}8、下表所列各组物质中,物质之间按箭头方向不能通过一步反应实现如图所示转化关系
的是( )
物质选项 甲 乙 丙
A.分离乙醇和水 B.由海水制取蒸馏水
A CuO CO CaCO
2 3
B C CO CO
2
C CaCO CaO CaOH
3 2
D CuO CuOH CuCl
2 2 C.分离苯和水 D.除去粗盐水中的泥沙
A、 A B、 B C、 C D、 D
9、容积不同的A、B两个密闭容器,A中充满氮气,B中充满CH 和CO 混合气体,同温 12、下列说法正确的是( )
4 2
A、向久置的氯水中滴入紫色石蕊试液,溶液将先变红后褪色
同压下测得两容器中气体密度相同,下列叙述不正确的是( )
B、新制氯水的颜色为浅黄绿色,光照新制氯水有气体逸出,该气体为HCl
C、漂白粉的有效成分是Ca(ClO),应密封保存
A、容器A和容器B中所含气体质量一定不同 2
D、氯气有漂白性,所以氯气能使湿润的有色布条褪色
B、容器B中混合气体的密度是同温同压下氢气密度的14倍
13、某白色粉末中可能含有BaNO 、CaCl 、Na CO ,现进行以下实验:
3 2 2 2 3
C、容器B中CH 和CO 的质量之比为33∶16
(1)将部分粉末加入水中,振荡,有白色沉淀生成;
4 2
(2)向(1)的悬浊液中加入过量稀盐酸,白色沉淀消失,并有气泡产生;
D、容器A和容器B中所含气体分子数一定不同
10、下列实验仪器选用正确的是( )
(3)取少量(2)的溶液滴入AgNO 溶液,有白色沉淀生成。
3
根据上述实验现象,下列判断正确的是( )
A、用10mL的量筒量取8.2mL浓硫酸
A、原白色粉末中肯定含BaNO 、Na CO ,可能含有CaCl
3 2 2 3 2
B、用230mL的容量瓶配制NaCl溶液
C、用PH试纸测新制的氯水PH为 2.0 B、原白色粉末中肯定含CaCl 、Na CO ,可能含有BaNO
2 2 3 3 2
D、用托盘天平称量5.03gNa CO 固体 C、(1)中白色沉淀是BaCO 、CaCO 中的一种或两种
2 3 3 3
11、列图示装置及对应的操作均正确的是( ) D、若将(2)中稀盐酸改为稀硝酸,则判断结果相同
高一化学试卷 -3-(共8页) 高一化学试卷 -4-(共8页)
{#{QQABTYQUggiAABIAAQhCQQHyCkKQkhEAAYgOQEAIoAAByQFABAA=}#}14、焰色试验过程中铂丝的清洗和灼烧与钾焰色的观察两项操作如图所示。下列叙述中 ③准确量取50.00mL溶液,加入足量的NaOH溶液至沉淀完全,过滤、洗涤、干燥、
正确的是( ) 灼烧至恒重,得到FeO 固体3.20g。
2 3
该聚合硫酸铁组成中x∶y∶z的值为( )
A、 2∶4∶1 B、 1∶1∶2 C、 1∶1∶1 D、 2∶3∶1
Ⅱ卷
二、填空题(共4 题,共52 分)
17、回答下列问题(用N 表示阿伏加德罗常数的值)
A
(1)标准状况下,和2molNH 含有相同氢原子数的CH 的体积为 。
3 4
A、用灼热的铂丝蘸取某固体样品进行焰色实验,火焰颜色为黄色,证明该固体样品
(2)从1LAl SO 溶液中取出100mL,向其中加入 200mL0.9molL1的BaCl 溶液恰好使SO2
中含有钠元素而不含钾元素 2 4 3 2 4
B、可以用光洁无锈的铁丝代替铂丝进行焰色试验
完全沉淀,则原溶液中 Al3的物质的量浓度为 。
C、可用稀硫酸代替盐酸清洗铂丝 (3)某盐混合溶液中含有离子: Na、Mg2、 Cl、SO 2,测得 Na、Mg2和 Cl的物质的
4
D、可用焰色试验鉴别NaCO 与 KHCO 溶液,是利用了NaCO 与KHCO 化学性质的不同
2 3 3 2 3 3
15、氯化钠(NaCl)是生活中常用的化学品,也是重要的化工生产原料。粗盐中一般含有
量浓度依次为: 0.2molL1、 0.25molL1、0.3mol.L-1,则c SO
4
2 。
(4)人造空气(氧气和氦气的混合气)可用于减轻某些疾病或供深水潜水员使用。在标准状
CaCl 、MgCl 、CaSO 和MgSO 杂质。粗盐制得精盐的过程如下:
2 2 4 4
况下,22.4L“人造空气”的质量是9.6g,其中氧气和氦气的分子数之比是 。
(5)室温下,某容积固定的密闭容器由可移动的活塞隔成A、B两室,向A室充入H、O
2 2
混合气体,向B室充入1mol空气,此时活塞的位置如图所示。
下列说法错误的是( )
实验测得A室混合气体的质量为34g,若将A室H、O 的混合气体点燃恢复原温度后,
A、试剂I是足量BaNO 溶液 2 2
3 2 (非气体体积忽略不计)最终活塞停留的位置在___________刻度处。
B、操作a所需的玻璃仪器有烧杯、漏斗、玻璃棒
(6)11gTO中含有的质子数和中子数分别为___________、___________。
2
C、试剂II为碳酸钠,其作用为除去溶液中的Ca2和Ba2 18、根据物质的组成、结构、性质等进行分类,可预测物质的性质及变化
现有①石墨;②铁;③酒精;④氨气;⑤硫化氢;⑥碳酸氢钠固体;
D、用pH试纸检验溶液B,可发现溶液 B显碱性
⑦氢氧化钠溶液;⑧纯醋酸;⑨氯气。
16、聚合硫酸铁[Fe(OH)(SO)](铁元素化合价为+3)是一种高效的混凝剂,常用于净水,
x y 4 z
(1)上述条件下能导电的是___________;属于非电解质的是___________;
它的组成可以通过以下实验测定:
属于电解质的是___________。
①称取一定质量的聚合硫酸铁配成500.00mL的溶液。
(2)等质量④和⑤中分子的数目之比为___________;
②准确量取50.00mL溶液,加入盐酸酸化的BaCl 溶液至沉淀完全,过滤、洗涤、干
2
(3)写出⑥在水中的电离方程式_______;写出少量⑨通入足量⑦中的化学方程式_____。
燥至恒重,得到白色固体4.66g。
高一化学试卷 -5-(共8页) 高一化学试卷 -6-(共8页)
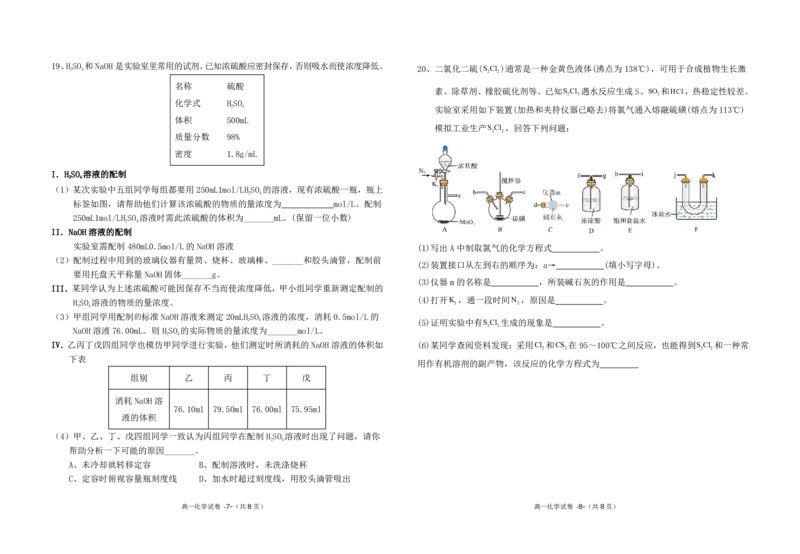
{#{QQABTYQUggiAABIAAQhCQQHyCkKQkhEAAYgOQEAIoAAByQFABAA=}#}19、HSO 和NaOH是实验室里常用的试剂。已知浓硫酸应密封保存,否则吸水而使浓度降低。
2 4 20、二氯化二硫(S Cl )通常是一种金黄色液体(沸点为138℃),可用于合成植物生长激
2 2
名称 硫酸
素、除草剂、橡胶硫化剂等。已知S Cl 遇水反应生成S、SO 和HCl,热稳定性较差。
2 2 2
化学式 HSO
2 4 实验室采用如下装置(加热和夹持仪器已略去)将氯气通入熔融硫磺(熔点为113℃)
体积 500mL
模拟工业生产S Cl ,回答下列问题:
2 2
质量分数 98%
密度 1.8g/mL
I.H SO 溶液的配制
2 4
(1)某次实验中五组同学每组都要用250mL1mol/LHSO 的溶液,现有浓硫酸一瓶,瓶上
2 4
标签如图,请帮助他们计算该浓硫酸的物质的量浓度为 mol/L。配制
250mL1mol/LHSO 溶液时需此浓硫酸的体积为_______mL。(保留一位小数)
2 4
II.NaOH溶液的配制
实验室需配制480mL0.5mol/L 的NaOH溶液 (1)写出A中制取氯气的化学方程式 。
(2)配制过程中用到的玻璃仪器有量筒、烧杯、玻璃棒、_______和胶头滴管,配制前
(2)装置接口从左到右的顺序为:a→ (填小写字母)。
要用托盘天平称量NaOH固体_______g。
(3)仪器m的名称是 ,所装碱石灰的作用是 。
III.某同学认为上述浓硫酸可能因保存不当而使浓度降低,甲小组同学重新测定配制的
HSO 溶液的物质的量浓度。
(4)打开K ,通一段时间N ,原因是 。
2 4 1 2
(3)甲组同学用配制的标准NaOH溶液来测定20mLHSO 溶液的浓度,消耗0.5mol/L的
2 4 (5)证明实验中有S Cl 生成的现象是 。
2 2
NaOH溶液76.00mL。则HSO 的实际物质的量浓度为_______mol/L。
2 4
IV.乙丙丁戊四组同学也模仿甲同学进行实验,他们测定时所消耗的NaOH溶液的体积如 (6)某同学查阅资料发现:采用Cl 和CS 在95~100℃之间反应,也能得到S Cl 和一种常
2 2 2 2
下表
用作有机溶剂的副产物,该反应的化学方程式为
组别 乙 丙 丁 戊
消耗NaOH溶
76.10ml 79.50ml 76.00ml 75.95ml
液的体积
(4)甲、乙、丁、戊四组同学一致认为丙组同学在配制HSO 溶液时出现了问题,请你
2 4
帮助分析一下可能的原因_______。
A、未冷却就转移定容 B、配制溶液时,未洗涤烧杯
C、定容时俯视容量瓶刻度线 D、加水时超过刻度线,用胶头滴管吸出
高一化学试卷 -7-(共8页) 高一化学试卷 -8-(共8页)
{#{QQABTYQUggiAABIAAQhCQQHyCkKQkhEAAYgOQEAIoAAByQFABAA=}#}