文档内容
湖北省部分高中协作体 2024--2025 学年下学期五月联考
高一化学试题
本试卷共 8 页,19 题,全卷满分 100 分,考试用时 75 分钟。
★祝考试顺利★
注意事项:
1、答题前,请将自己的姓名、准考证号、考场号、座位号填写在试卷和答
题卡上,并将准考证号条形码粘贴在答题卡上的制定位置。
2、选择题的作答:每小题选出答案后,用 2B 铅笔把答题卡上对应题目的答
案标号涂黑,写在试卷、草稿纸和答题卡上的非答题区域均无效。
3、非选择题作答:用黑色签字笔直接答在答题卡对应的答题区域内,写在
试卷、草稿纸和答题卡上的非答题区域均无效。
4、考试结束后,请将答题卡上交。
一、选择题:本题共 15 小题,每题 3 分,共 45 分,每小题仅有一项是符
合题意。
1.戏曲是中华文化的瑰宝,其人物的装扮具有鲜明的特色且与化学知识有关。
某人物的装扮如图所示,下列有关说法错误的是( )
A.头上所带的银簪由金属材料制成
B.丝绸云袖的主要成分为蛋白质
C.衣服挂件上的珍珠属于硅酸盐
D.脚上穿的木质鞋履的主要成分是纤维素
2.对某无色溶液分别进行下列操作,所得现象和结论均正确的是( )
共 8 页,第 1页A.加入氨水,产生白色沉淀,证明原溶液中存在 Al3+
B.加入 AgNO 溶液,产生白色沉淀,证明原溶液中存在 Cl-
3
C.加入盐酸酸化的 BaCl 溶液,生成白色沉淀,证明原溶液中存在 SO2-4
2
D.加入浓 NaOH 溶液并加热,产生使湿润的红色石蕊试纸变蓝的气体,证
明原溶液中存在 NH+4
3.含 XO-3 的溶液与亚硫酸钠(Na SO )溶液恰好反应完全,已知 Na SO 被
2 3 2 3
氧化为 Na SO ,并且参加反应的 XO-3 与 SO2-3 的个数比为 1∶2。则还原产
2 4
物中元素 X 的生成物可能是( )
A.XO- B.XO-2
C.XO-4 D.X-
4.下列说法不正确的是( )
A.1 mol H O 中含 2 mol H 和 1 mol O
2
B.“摩尔”是物质的量的单位
C.1 mol 任何物质都约含 6.02×1023 个原子
D.1 mol 水所含的水分子数和 1 mol Al 所含的 Al 原子数都约为 6.02×1023
5.硫代硫酸钠(Na S O )常用于碘量法中测定碘的标准溶液。现需要配制 500
2 2 3
mL 0.10 mol·L-1 Na S O 溶液,下列情况会导致所配制的溶液浓度偏高的是
2 2 3
( )
A.用托盘天平称取 7.9 g Na S O ·5H O
2 2 3 2
B.定容时,仰视容量瓶刻度线
C.没有用蒸馏水洗涤转移后的烧杯和玻璃棒
D.用 Na S O 溶液润洗过的容量瓶配制溶液
2 2 3
6.28 g 铁粉溶于稀盐酸中,然后加入足量的 Na O 固体,充分反应后过滤,
2 2
将滤渣加强热,最终得到的固体质量为( )
A.36 g B.40 g
共 8 页,第 2页C.80 g D.160 g
7.下列关于钠的实验现象的叙述不正确的是( )
选项 实验操作 实验现象
切开一小块钠,观察切面颜色的变
A 钠切面颜色变暗,最后呈淡黄色
化
钠熔化成闪亮的小球,在液面上四
B 把一小块钠投入 CuSO 溶液中 处游动,发出“嘶嘶”的响声,产
4
生蓝色沉淀
钠熔化成闪亮的小球,在液面上四
把一小块钠投入滴有紫色石蕊溶液
C 处游动,发出“嘶嘶”的响声,反
的冷水中
应后溶液变蓝
把一小块钠迅速投入热坩埚中,继 钠熔成小球,然后剧烈燃烧,发
出 D
续加热坩埚片刻 黄色火焰,生成淡黄色固体
8.中科院化学所研制的晶体材料——纳米四氧化三铁,在核磁共振造影及医
药上有广泛用途,其生产过程的部分流程如下所示。
FeCl ·6H O――→环丙胺①FeOOH――→CO②纳米四氧化三铁
3 2
下列有关叙述不合理的是( )
A.纳米四氧化三铁具有磁性,可作为药物载体用于治疗疾病
B.纳米四氧化三铁可分散在水中,它与 FeCl 溶液中分散质直径大小相等
3
C.在反应①中环丙胺的作用可能是促进氯化铁水解
D.反应②的化学方程式为 6FeOOH+CO===2Fe O +3H O+CO
3 4 2 2
9.化学在生产和日常生活中有着重要的应用。下列说法不正确的是( )
A.铝比铁活泼,但铝制品比铁制品在空气中耐腐蚀
B.铝热反应不仅用于焊接钢轨,而且还常用于冶炼熔点较高的金属
C.电解 AlCl 饱和溶液可制得金属铝
3
共 8 页,第 3页D.Al O 、MgO 的熔点很高,可用于制作耐高温材料
2 3
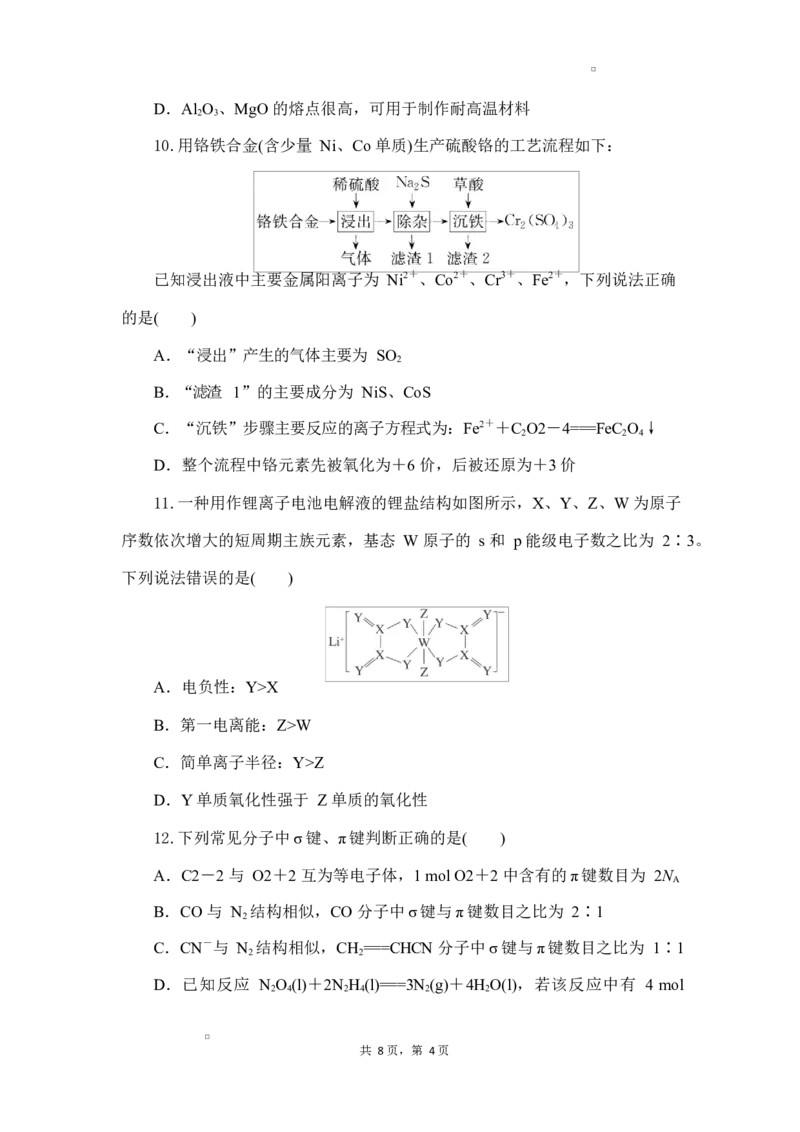
10.用铬铁合金(含少量 Ni、Co 单质)生产硫酸铬的工艺流程如下:
已知浸出液中主要金属阳离子为 Ni2+、Co2+、Cr3+、Fe2+,下列说法正确
的是( )
A.“浸出”产生的气体主要为 SO
2
B.“滤渣 1”的主要成分为 NiS、CoS
C.“沉铁”步骤主要反应的离子方程式为:Fe2++C O2-4===FeC O ↓
2 2 4
D.整个流程中铬元素先被氧化为+6 价,后被还原为+3 价
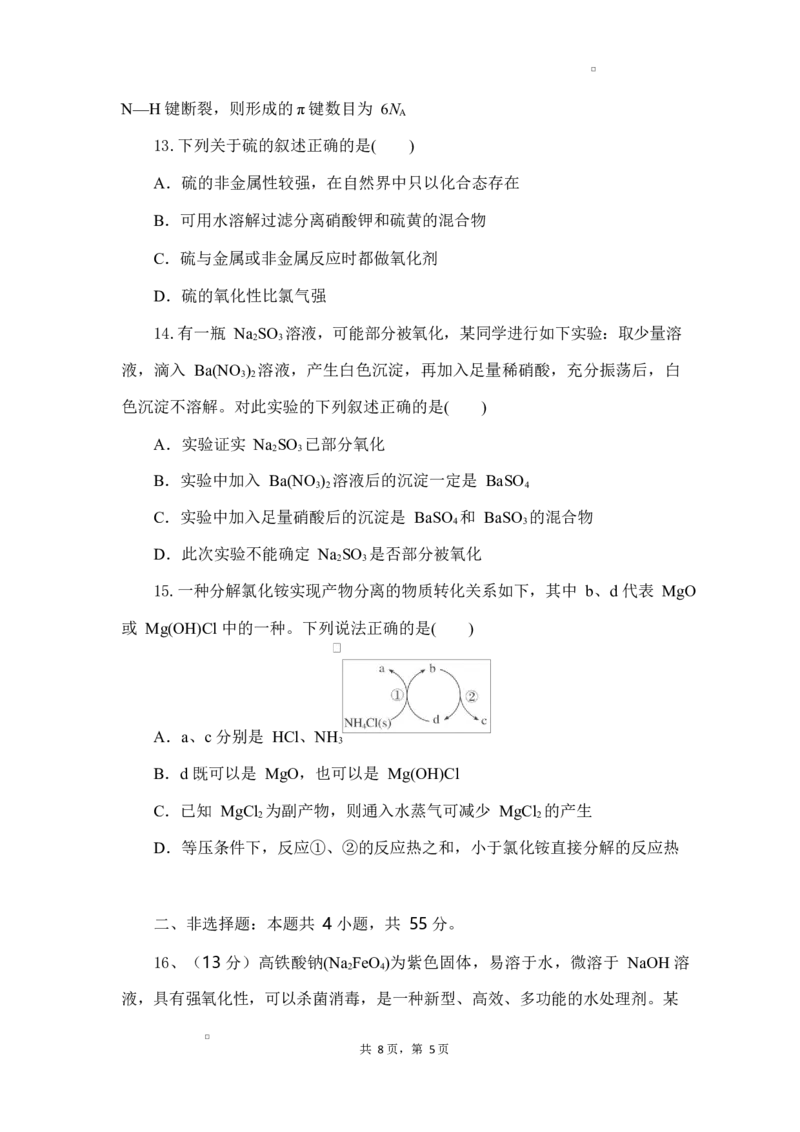
11.一种用作锂离子电池电解液的锂盐结构如图所示,X、Y、Z、W 为原子
序数依次增大的短周期主族元素,基态 W 原子的 s 和 p 能级电子数之比为 2∶3。
下列说法错误的是( )
A.电负性:Y>X
B.第一电离能:Z>W
C.简单离子半径:Y>Z
D.Y 单质氧化性强于 Z 单质的氧化性
12.下列常见分子中σ键、π键判断正确的是( )
A.C2-2 与 O2+2 互为等电子体,1 mol O2+2 中含有的π键数目为 2N
A
B.CO 与 N 结构相似,CO 分子中σ键与π键数目之比为 2∶1
2
C.CN-与 N 结构相似,CH ===CHCN 分子中σ键与π键数目之比为 1∶1
2 2
D.已知反应 N O (l)+2N H (l)===3N (g)+4H O(l),若该反应中有 4 mol
2 4 2 4 2 2
共 8 页,第 4页N—H 键断裂,则形成的π键数目为 6N
A
13.下列关于硫的叙述正确的是( )
A.硫的非金属性较强,在自然界中只以化合态存在
B.可用水溶解过滤分离硝酸钾和硫黄的混合物
C.硫与金属或非金属反应时都做氧化剂
D.硫的氧化性比氯气强
14.有一瓶 Na SO 溶液,可能部分被氧化,某同学进行如下实验:取少量溶
2 3
液,滴入 Ba(NO ) 溶液,产生白色沉淀,再加入足量稀硝酸,充分振荡后,白
3 2
色沉淀不溶解。对此实验的下列叙述正确的是( )
A.实验证实 Na SO 已部分氧化
2 3
B.实验中加入 Ba(NO ) 溶液后的沉淀一定是 BaSO
3 2 4
C.实验中加入足量硝酸后的沉淀是 BaSO 和 BaSO 的混合物
4 3
D.此次实验不能确定 Na SO 是否部分被氧化
2 3
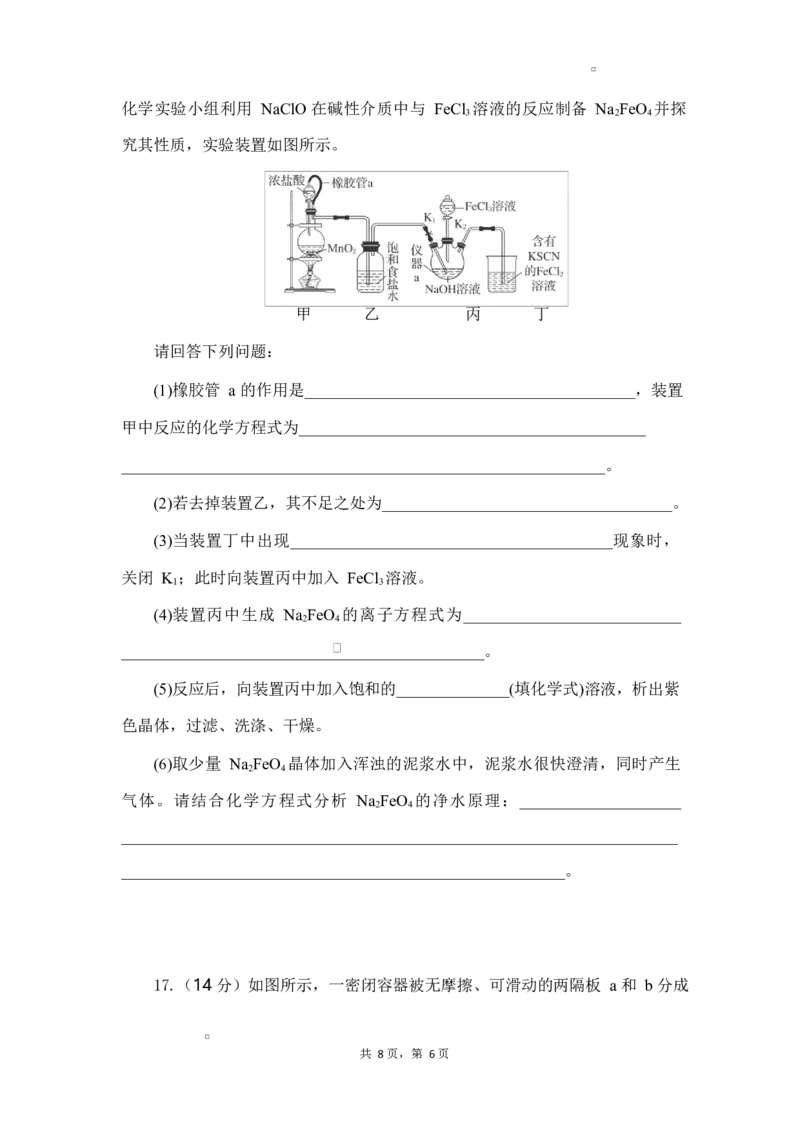
15.一种分解氯化铵实现产物分离的物质转化关系如下,其中 b、d 代表 MgO
或 Mg(OH)Cl 中的一种。下列说法正确的是( )
A.a、c 分别是 HCl、NH
3
B.d 既可以是 MgO,也可以是 Mg(OH)Cl
C.已知 MgCl 为副产物,则通入水蒸气可减少 MgCl 的产生
2 2
D.等压条件下,反应①、②的反应热之和,小于氯化铵直接分解的反应热
二、非选择题:本题共 4 小题,共 55 分。
16、(13 分)高铁酸钠(Na FeO )为紫色固体,易溶于水,微溶于 NaOH 溶
2 4
液,具有强氧化性,可以杀菌消毒,是一种新型、高效、多功能的水处理剂。某
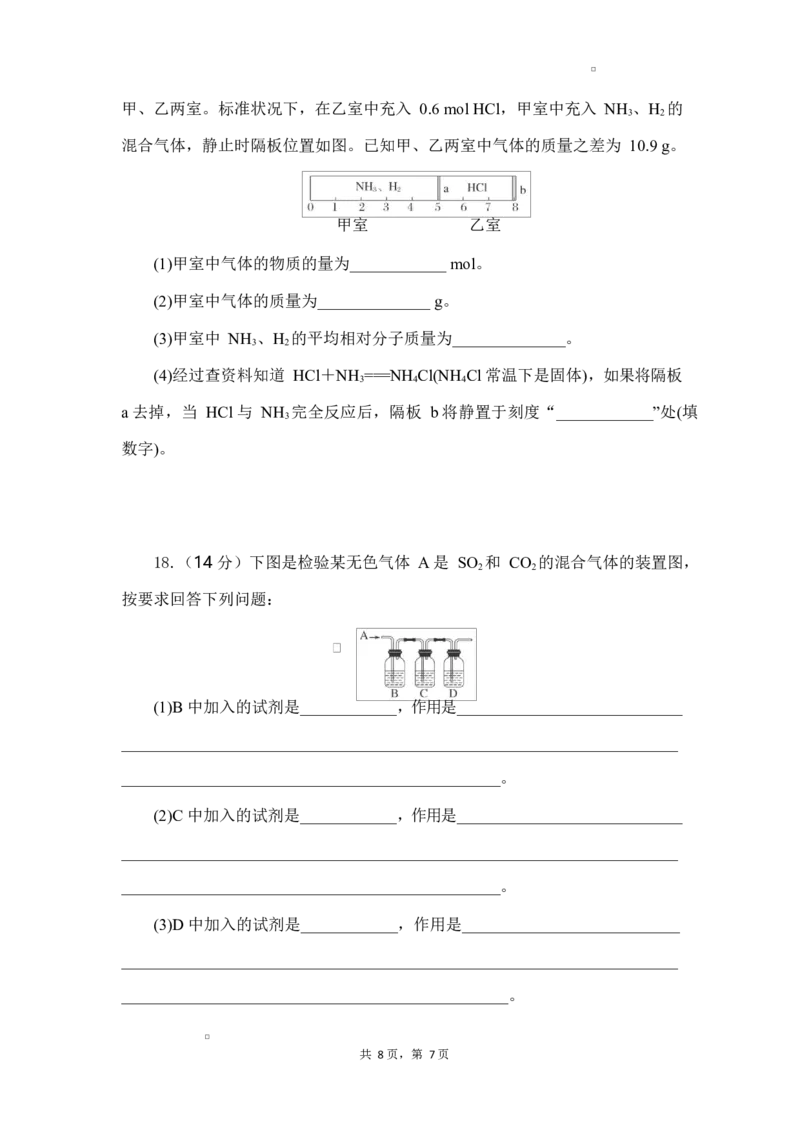
共 8 页,第 5页化学实验小组利用 NaClO 在碱性介质中与 FeCl 溶液的反应制备 Na FeO 并探
3 2 4
究其性质,实验装置如图所示。
甲 乙 丙 丁
请回答下列问题:
(1)橡胶管 a 的作用是_________________________________________,装置
甲中反应的化学方程式为___________________________________________
____________________________________________________________。
(2)若去掉装置乙,其不足之处为____________________________________。
(3)当装置丁中出现________________________________________现象时,
关闭 K ;此时向装置丙中加入 FeCl 溶液。
1 3
(4)装置丙中生成 Na FeO 的离子方程式为___________________________
2 4
_____________________________________________。
(5)反应后,向装置丙中加入饱和的______________(填化学式)溶液,析出紫
色晶体,过滤、洗涤、干燥。
(6)取少量 Na FeO 晶体加入浑浊的泥浆水中,泥浆水很快澄清,同时产生
2 4
气体。请结合化学方程式分析 Na FeO 的净水原理:____________________
2 4
_____________________________________________________________________
_______________________________________________________。
17.(14 分)如图所示,一密闭容器被无摩擦、可滑动的两隔板 a 和 b 分成
共 8 页,第 6页甲、乙两室。标准状况下,在乙室中充入 0.6 mol HCl,甲室中充入 NH 、H 的
3 2
混合气体,静止时隔板位置如图。已知甲、乙两室中气体的质量之差为 10.9 g。
甲室 乙室
(1)甲室中气体的物质的量为____________ mol。
(2)甲室中气体的质量为______________ g。
(3)甲室中 NH 、H 的平均相对分子质量为______________。
3 2
(4)经过查资料知道 HCl+NH ===NH Cl(NH Cl 常温下是固体),如果将隔板
3 4 4
a 去掉,当 HCl 与 NH 完全反应后,隔板 b 将静置于刻度“____________”处(填
3
数字)。
18.(14 分)下图是检验某无色气体 A 是 SO 和 CO 的混合气体的装置图,
2 2
按要求回答下列问题:
(1)B 中加入的试剂是____________,作用是____________________________
_____________________________________________________________________
_______________________________________________。
(2)C 中加入的试剂是____________,作用是____________________________
_____________________________________________________________________
_______________________________________________。
(3)D 中加入的试剂是____________,作用是___________________________
_____________________________________________________________________
________________________________________________。
共 8 页,第 7页(4)实验时,C 中应观察到的现象是________________________________
_____________________________________________________________________
___________________________________________。
19.(14 分)如图为化学教学中所用的喷泉实验装置。某同学用烧瓶中盛不
同成分的气体进行喷泉实验,请帮助分析实验后烧瓶中所得溶液的浓度(假设是
在标准状况下完成实验,且溶质不扩散)。
(1)若用 HCl 气体,则 c(HCl)=____________________________。
(2)若用 NO 气体,则 c(HNO )=___________________________。
2 3
(3)若用 n(NO )∶n(O )=2∶1 的混合气体,则 c(HNO )=__________。
2 2 3
共 8 页,第 8页