文档内容
厦门英才学校中学部 2025—2026 学年度
第一学期 9 月份考试
高一化学试卷
考试时间:60分钟 满分100分
注意:
1.本学科试卷分试题卷和答题卷两部分。全部答案必须按要求填在答题卷的相应答
题栏内,否则不能得分。
2.可能用到的相对原子质量:H-1 C-12 N-14 O-16 Na-23 S-32
一、选择题(本题共15小题,每小题4分,共60分。在每小题给出的四个选项中,只有
一项是符合题目要求的)
一、单选题
1. 化学与人体健康及环境保护息息相关。下列叙述不正确的是
A.珍爱生命,拒绝毒品 B.生活垃圾,分类处理
C.节能减排,绿色化学 D.工业废水,随意排放
2.化学在原子、分子水平上研究的内容不包括
A.物质的组成 B.物质的导电性 C.物质的结构 D.物质的转化
3.下列关于物质用途的说法中,不正确的是
A.二氧化氯可用于自来水消毒 B.过氧化钠可作供氧剂
C.氢氧化钠可作食品干燥剂 D.苏打可用于食用碱或工业用碱
4.下列叙述正确的是
A. 1molNH 的质量为17g
3
B. CH 的摩尔质量为16g
4
C. 个SO 分子质量约为64g
2
D.标准状况下, 0.5mol任何物质的体积均约为11.2L
5.下列说法正确的是( )
A.将一小块钠放入水中,钠将沉在水底B.将一小块钠放在稀盐酸中,钠先与水反应生成NaOH和H ,生成的NaOH再与HCl
2
反应生成NaCl和HO
2
C.将一小块钠放在CuSO 溶液中发生如下反应:2Na+CuSO ===Na SO +Cu
4 4 2 4
D.钠可用于冶炼金属
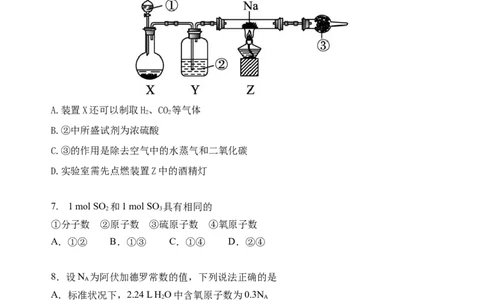
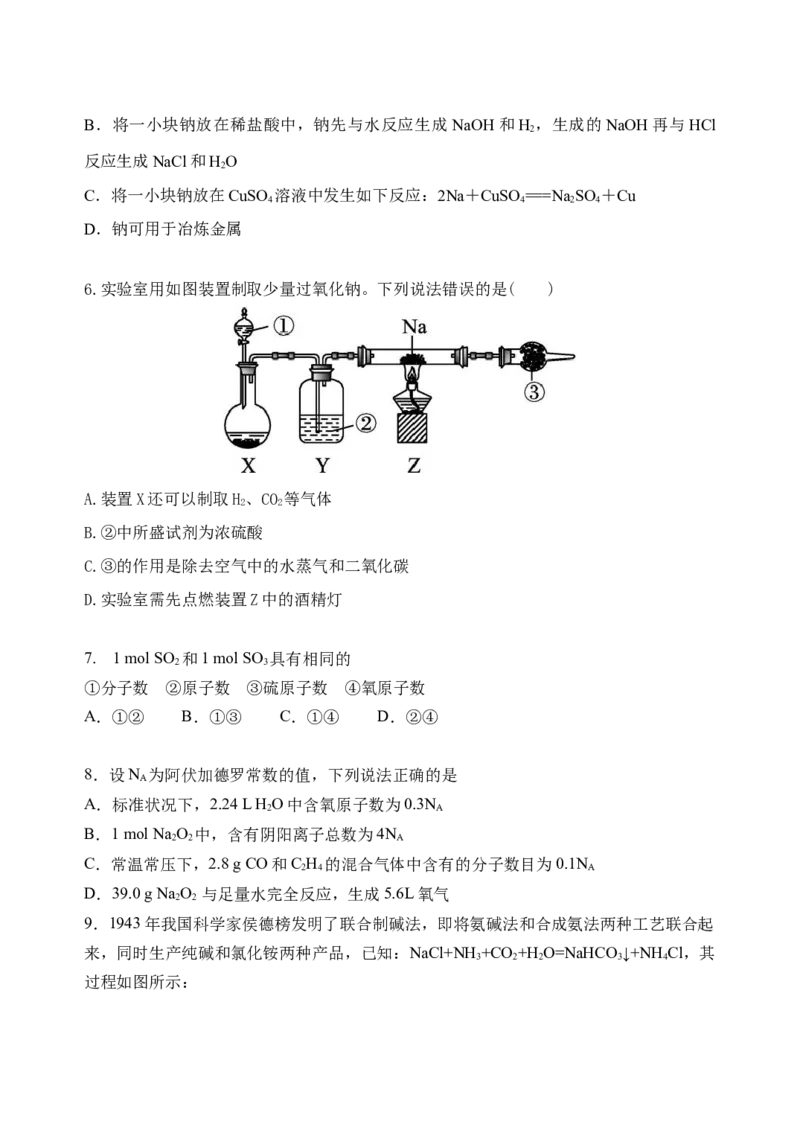
6.实验室用如图装置制取少量过氧化钠。下列说法错误的是( )
A.装置X还可以制取H、CO 等气体
2 2
B.②中所盛试剂为浓硫酸
C.③的作用是除去空气中的水蒸气和二氧化碳
D.实验室需先点燃装置Z中的酒精灯
7. 1 mol SO 和1 mol SO 具有相同的
2 3
①分子数 ②原子数 ③硫原子数 ④氧原子数
A.①② B.①③ C.①④ D.②④
8.设N 为阿伏加德罗常数的值,下列说法正确的是
A
A.标准状况下,2.24 L H O中含氧原子数为0.3N
2 A
B.1 mol Na O 中,含有阴阳离子总数为4N
2 2 A
C.常温常压下,2.8 g CO和C H 的混合气体中含有的分子数目为0.1N
2 4 A
D.39.0 g Na O 与足量水完全反应,生成5.6L氧气
2 2
9.1943年我国科学家侯德榜发明了联合制碱法,即将氨碱法和合成氨法两种工艺联合起
来,同时生产纯碱和氯化铵两种产品,已知:NaCl+NH +CO +H O=NaHCO ↓+NHCl,其
3 2 2 3 4
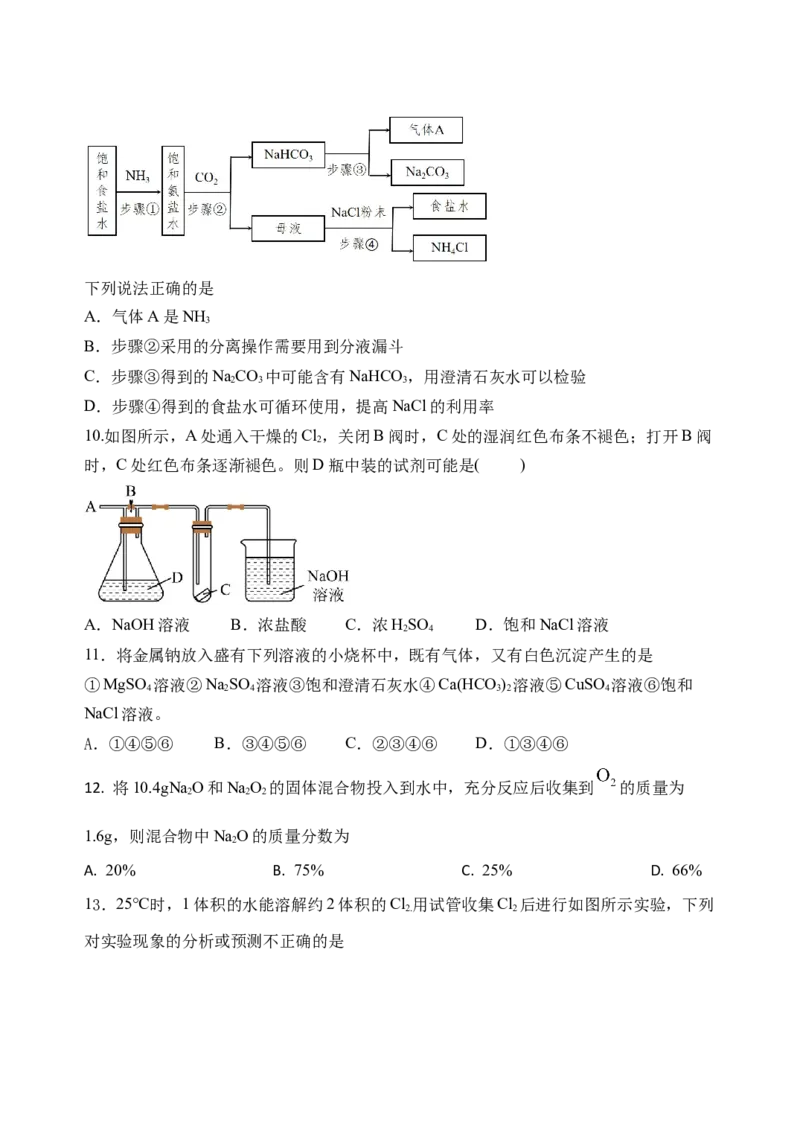
过程如图所示:下列说法正确的是
A.气体A是NH
3
B.步骤②采用的分离操作需要用到分液漏斗
C.步骤③得到的NaCO 中可能含有NaHCO ,用澄清石灰水可以检验
2 3 3
D.步骤④得到的食盐水可循环使用,提高NaCl的利用率
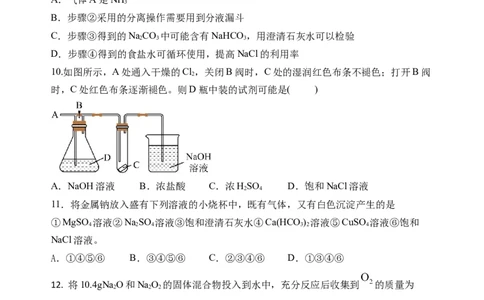
10.如图所示,A处通入干燥的Cl,关闭B阀时,C处的湿润红色布条不褪色;打开B阀
2
时,C处红色布条逐渐褪色。则D瓶中装的试剂可能是( )
A.NaOH溶液 B.浓盐酸 C.浓HSO D.饱和NaCl溶液
2 4
11.将金属钠放入盛有下列溶液的小烧杯中,既有气体,又有白色沉淀产生的是
①MgSO 溶液②NaSO 溶液③饱和澄清石灰水④Ca(HCO ) 溶液⑤CuSO 溶液⑥饱和
4 2 4 3 2 4
NaCl溶液。
A.①④⑤⑥ B.③④⑤⑥ C.②③④⑥ D.①③④⑥
12. 将10.4gNaO和NaO 的固体混合物投入到水中,充分反应后收集到 的质量为
2 2 2
1.6g,则混合物中NaO的质量分数为
2
A. 20% B. 75% C. 25% D. 66%
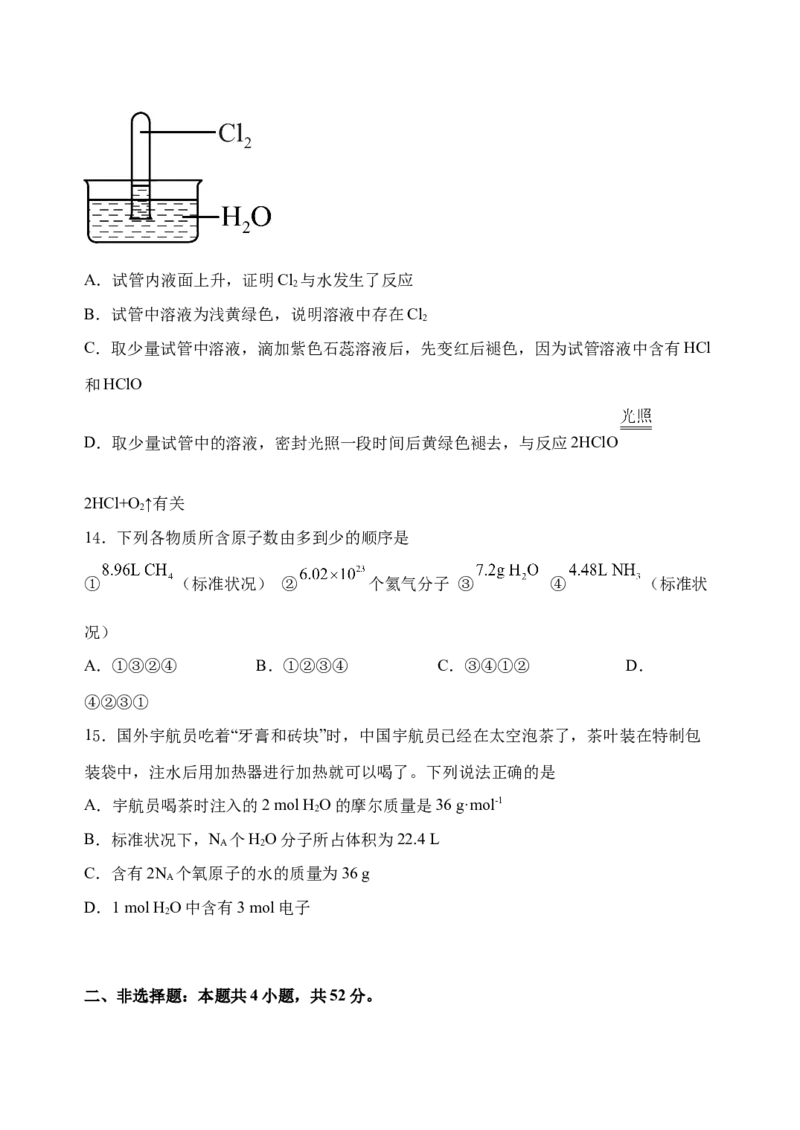
13.25℃时,1体积的水能溶解约2体积的Cl 用试管收集Cl 后进行如图所示实验,下列
2. 2
对实验现象的分析或预测不正确的是A.试管内液面上升,证明Cl 与水发生了反应
2
B.试管中溶液为浅黄绿色,说明溶液中存在Cl
2
C.取少量试管中溶液,滴加紫色石蕊溶液后,先变红后褪色,因为试管溶液中含有HCl
和HClO
D.取少量试管中的溶液,密封光照一段时间后黄绿色褪去,与反应2HClO
2HCl+O ↑有关
2
14.下列各物质所含原子数由多到少的顺序是
① (标准状况) ② 个氦气分子 ③ ④ (标准状
况)
A.①③②④ B.①②③④ C.③④①② D.
④②③①
15.国外宇航员吃着“牙膏和砖块”时,中国宇航员已经在太空泡茶了,茶叶装在特制包
装袋中,注水后用加热器进行加热就可以喝了。下列说法正确的是
A.宇航员喝茶时注入的2 mol H O的摩尔质量是36 g·mol-1
2
B.标准状况下,N 个HO分子所占体积为22.4 L
A 2
C.含有2N 个氧原子的水的质量为36 g
A
D.1 mol H O中含有3 mol电子
2
二、非选择题:本题共4小题,共52分。16.(10分)按要求书写化学方程式。
(1)加热时钠与氧气反应:
(2)钠与水的反应:
(3)铁丝在氯气中燃烧:
(4)次氯酸见光分解:
(5)漂白粉漂白原理:
17.(12分)物质的量是联系宏观和微观的桥梁,为我们提供了一个定量认识物质组成
的新视角。按要求回答下列问题:
(1) 的质量是 g,在标准状况下的体积为 L。
(2) 中含有的电子数是 个。
(3) g的氢气中所含H原子的数目与 相同。
(4) 中含有 ,则 的摩尔质量为 。
(5)电解1.8 g 所得的 在标准状况下的体积为 。
18.(9分)为探究氯水中含有的部分粒子及某些粒子的性质,某化学兴趣小组做了如下
实验:
(1)在氯水的试管中加有色布条,发现有色布条褪色,说明氯水中含有__________ (填化
学式);
(2)写出氯气与水反应的化学方程式 。
(3)下列有关氯气的叙述中,不正确的是_______。
A.氯气是一种黄绿色、有刺激性气味的气体
B.氯气、液氯和氯水是同一种物质
C.氯气能溶于水
D.氯气是一种有毒气体
(4)将氯气通入 溶液中可以制得具有杀菌消毒作用的84消毒液,该反应的化学方程
式为 。将氯气通入紫色石蕊溶液中,可以观察到的现象是
。
19.(9分)钠及其化合物是中学化学比较重要的化学知识,根据所学回答下面问题:
Ⅰ.用套管实验装置可以更好地比较 和 的热稳定性,其中小试管内有沾有无水硫酸铜粉末的棉花球,实验装置如图。
请探究下列问题
(1)实验时,小试管内棉花球上的无水硫酸铜由白色变为蓝色,说明 受热分解生
成了 ,烧杯 中澄清石灰水变浑浊,书写该过程 受热分解化学方程式
。
(2)实验时,烧杯 中澄清石灰水不变浑浊,而烧杯 中澄清石灰水变浑浊,由此可得热
稳定性大小关系: (填“ ”或“ ”) 。
(3)关于金属钠,下列说法正确的是_____。
A.钠的熔点低,硬度小 B.钠着火可以用二氧化碳扑灭
C.钠在空气中燃烧生成氧化钠 D.反应后剩余的钠应使用废液缸回收
(4)过氧化钠可以吸收人体呼出的二氧化碳,写出该反应的化学方程式:
。