文档内容
高一化学
可能用到的相对原子质量:H 1 C 12 N 14 O 16 Ca 40
一、选择题:本题共15小题,每小题3分,共45分。在每小题给出的四个选项中,只有一项是符合题
目要求的。
1. 中国传统文化蕴含着丰富的化学知识。下列物质属于有机化合物的是
A. 《千里江山图》中的绿色颜料—铜绿
为
B. 《淮南万毕术》中“ 曾青得铁则化 铜 ”—“ 曾青 ”
C. 《送元二使安西》中“劝君更尽一杯酒,西出阳关无故人 ”—“酒 ”
.
D 《石灰吟》中“千锤万凿出深山,烈火焚烧若等闲 ”—石灰石
的
2. 化学是在原子、分子水平上研究物质 组成、结构、性质及其应用的基础自然科学,下列说法错误的是
A. 在资源、材料、健康、环境等领域,化学都发挥着极其重要的作用
B. 学习化学需坚持实验和理论并重,有利于我们提升对物质及其变化的认识水平
C. 依据物质类别和元素价态,可以解释和预测物质的性质
D. 意大利科学家阿伏加德罗发现了元素周期律,使化学的研究变得有规律可循
3. 运用分类法可以做到举一反三,触类旁通,提高效率。下列分类正确的是
选
单质 碱 混合物
项
A 生铁 纯碱
B 邢窑白瓷 熟石灰
C 大理石
D 金刚石 冰水混合物
A. A B. B C. C D. D
4. 常温下,甲、乙、丙、丁四位同学对四组无色透明溶液进行离子检验,四位同学各鉴定一组,得出如下结论,其中
一定错误的是
实验人
实验结论
员
甲同学 溶液中含有乙同学 溶液中含有
丙同学 溶液中含有
丁同学 溶液中含有
A. 甲同学 B. 乙同学 C. 丙同学 D. 丁同学
5. 下列说法中正确的是
①电解质本身一定能导电
②能导电的物质一定是电解质
③酸一定含有氢元素
④碱性氧化物常温下一定可以和水反应生成相应的碱
A. ①②③ B. ②③④ C. ② D. ③
6. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 的溶液中:
B. 遇石蕊变蓝的溶液中:
C. 无色透明的溶液中:
D. 含大量 的溶液中:
7. 由等质量的石灰石制备碳酸钙的两种实验方案如下(部分反应物或反应条件略)。下列说法正确的是
方案甲:
方案乙:
A. 四大基本反应类型在上述①~⑤五个反应中均有涉及
B. X一定是
C. 方案乙与方案甲相比,优点为步骤少,纯度高,耗能低
D. 若每一步均完全转化,则理论上方案乙一定比方案甲的二氧化碳排放少
8. 下列离子方程式不正确的是
A. 碳酸氢钠溶液与少量氢氧化钙溶液反应:B. 向硫酸氢钠溶液滴加少量碳酸氢钡溶液:
C. 用盐酸除去铁锈:
D. 向碳酸钠稀溶液中通入CO :
2
9. 已知有如下反应:①KCr O+14HCl(浓)=2KCl+2CrCl +3Cl↑+7H O②Cr+2HCl(稀)=CrCl +H ↑;
2 2 7 3 2 2 2 2
③2KMnO +16HCl(稀)=2KCl+2MnCl +5Cl↑+8H O,下列说法错误的是
4 2 2 2
A. 氧化性:KMnO >KCr O>Cl
4 2 2 7 2
B. 反应③中氧化剂与还原剂的物质的量之比为1:5
C. 向Cr (SO ) 溶液中滴入酸性KMnO 溶液,可发生反应:10Cr3++6 +11H O=5 +6Mn2++22H+
2 4 3 4 2
D. 向金属Cr中滴入浓硝酸无明显变化,说明两者不能发生反应
10. 某无色溶液中只可能含有 中的一种或几种,对其进行如下实验操作:
①取少量溶液,加入足量 溶液,产生白色沉淀;
②向①所得混合物中加足量盐酸,沉淀部分溶解,并有无色气体生成;
③将②)所得混合物过滤,向滤液中加入 溶液,有白色沉淀生成。
下列对该溶液的说法正确的是
A. 一定含有 B. 可能含有
C. 一定含有 D. 一定不含
11. 某化学试剂厂不慎发生了氯气泄漏事故,下列关于安全处理措施不正确的是
A. 紧急组织群众沿逆风方向疏散
B. 处在该厂附近家中的群众,应用肥皂水浸湿毛巾捂住口鼻,向低洼处撤离
C. 处在该厂实验室的工作人员,撤离时可以用NaHCO 溶液浸湿毛巾捂住口鼻
3
D. 消防官兵赶到现场后,把泄漏的氯气钢瓶投入一盛有石灰水的水池中
12. 下列各组数据中,前者刚好是后者两倍的是
A. 2mol水的摩尔质量和1mol水的摩尔质量
的
B. 溶液中 个数与 HCl溶液中的 个数
C. 标准状况下,22.4L一氧化碳中氧原子数和16g二氧化硫中氧原子数D. 200mL 氯化钙溶液中 和100mL 氯化钾溶液中
13. 在标准状况下,将V L A气体(摩尔质量为M g·mol-1)溶于0.1L水中,所得溶液的密度为dg·cm-3,则溶液的物质
的量浓度为
A. mol·L-1 B. mol·L-1
C. mol·L-1 D. mol·L-1
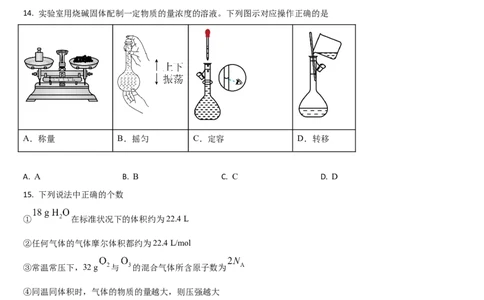
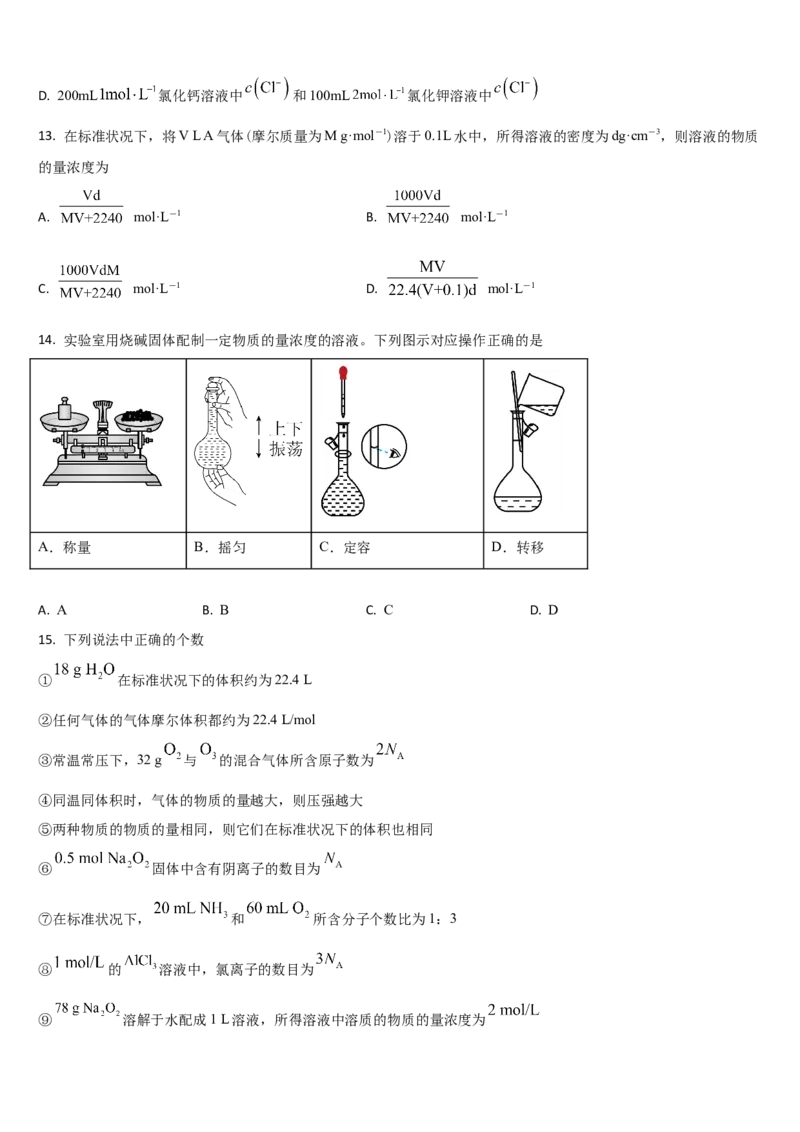
14. 实验室用烧碱固体配制一定物质的量浓度的溶液。下列图示对应操作正确的是
A.称量 B.摇匀 C.定容 D.转移
A. A B. B C. C D. D
15. 下列说法中正确的个数
① 在标准状况下的体积约为22.4 L
②任何气体的气体摩尔体积都约为22.4 L/mol
③常温常压下,32 g 与 的混合气体所含原子数为
④同温同体积时,气体的物质的量越大,则压强越大
⑤两种物质的物质的量相同,则它们在标准状况下的体积也相同
⑥ 固体中含有阴离子的数目为
⑦在标准状况下, 和 所含分子个数比为1:3
⑧ 的 溶液中,氯离子的数目为
⑨ 溶解于水配成1 L溶液,所得溶液中溶质的物质的量浓度为A. 4 B. 5 C. 6 D. 7
二、非选择题
16. 化学计量在生产和科研中应用广泛。回答下列问题:
(1)某气态氧化物的化学式为RO,标准状况下1.28 g该氧化物的体积为448 mL,则RO 的摩尔质量为___________。
2 2
(2)若a g某气体A,含有的分子数为N,c g A 气体在标准状况下的体积约为b L,则阿伏加德罗常数可表示为
2 2
___________(用含字母的代数式表示)。
(3)标准状况下将a L X气体(摩尔质量为M g·mol-1 )全部溶于0.1 L水(水的密度为1 g·cm-3)中(假设气体与水不反应),
所得溶液的密度为d g·cm-3,则此溶液的物质的量浓度为___________。
(4)将10 mL 1.00 mol·L-1 Na CO 溶液与10 mL 1.00 mol·L-1 CaCl 溶液相混合,则混合溶液中Na+的物质的量浓度为
2 3 2
___________(忽略混合前后溶液体积的变化)。
的
(5)某混合溶液中含有离子:Na+、Mg2+、Cl-、 测得Na+、Mg2+和 物质的量浓度依次为:0.2 mol·L-1、
0.25 mol·L-1、0.2 mol·L-1,则该混合溶液中c(Cl-)=___________。
(6)标准状况下,15.2 g由CO 与O 组成的混合气体的总体积为8.96 L,该混合气体中O 的体积分数为___________。
2 2 2
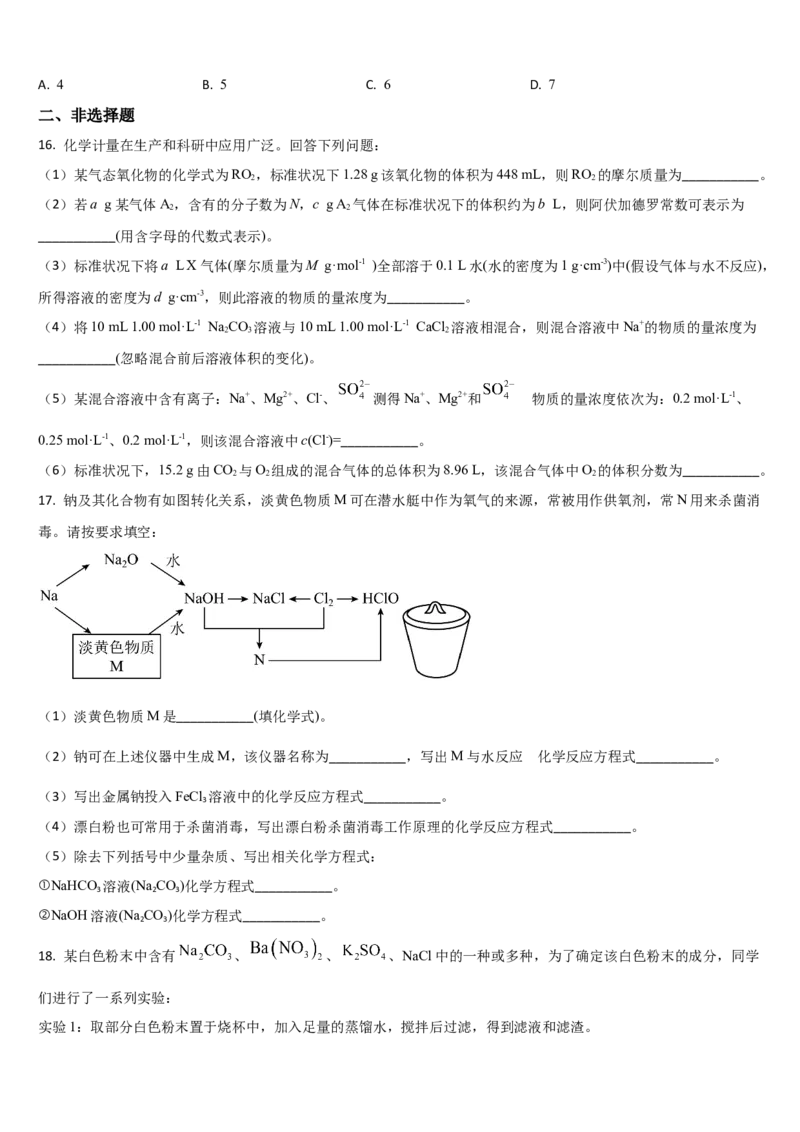
17. 钠及其化合物有如图转化关系,淡黄色物质M可在潜水艇中作为氧气的来源,常被用作供氧剂,常N用来杀菌消
毒。请按要求填空:
(1)淡黄色物质M是___________(填化学式)。
的
(2)钠可在上述仪器中生成M,该仪器名称为___________,写出M与水反应 化学反应方程式___________。
(3)写出金属钠投入FeCl 溶液中的化学反应方程式___________。
3
(4)漂白粉也可常用于杀菌消毒,写出漂白粉杀菌消毒工作原理的化学反应方程式___________。
(5)除去下列括号中少量杂质、写出相关化学方程式:
①NaHCO 溶液(Na CO )化学方程式___________。
3 2 3
②NaOH溶液(Na CO )化学方程式___________。
2 3
18. 某白色粉末中含有 、 、 、NaCl中的一种或多种,为了确定该白色粉末的成分,同学
们进行了一系列实验:
实验1:取部分白色粉末置于烧杯中,加入足量的蒸馏水,搅拌后过滤,得到滤液和滤渣。实验2:向实验1所得滤渣中加入过量的稀盐酸,滤渣部分溶解,并产生了一种无色无味的气体。
实验3:向实验1所得滤液中加入过量的稀硝酸,充分反应后再加入硝酸银溶液,无明显实验现象。
已知: 能溶于稀硝酸。
请回答下列问题:
(1)写出 在水中的电离方程式:___________。
(2)过滤时需要使用的玻璃仪器有玻璃棒、___________。
(3)实验1中滤渣的主要成分是___________(写化学式),写出滤渣中成分与稀盐酸反应的离子方程式:___________。
(4)该白色粉末中肯定含有___________(写化学式,下同),肯定不含___________。
(5)某同学取实验1中少量滤液于试管中,并滴加硝酸银溶液,观察到试管中生成白色沉淀,他认为该白色粉末中
一定含有NaCl。你认为他的结论是否合理并说明理由:___________。
19.将少量饱和 FeCl 溶液分别滴加到下列物质中,得到三种分散系,完成相关问题:
3
甲:饱和 FeCl 溶液滴加到 NaOH 溶液中;
3
乙:饱和 FeCl 溶液滴加到冷水中;
3
丙:饱和 FeCl 溶液滴加到沸水中。
3
(1)将丙继续加热煮沸得到红褐色透明液体,反应的化学方程式为_____。
(2)用最简单的方法判断丙中是否成功制备胶体,请写出相关的操作、现象和结论_____。
(3)向经过检验后的丙中逐滴加入稀盐酸,会出现一系列变化:
①先出现和甲中相同的现象,原因为_____。
②随后发生变化得到和乙相同的溶液,此反应的离子反应方程式为_____。
(4)向丙中加入电极通电后,Fe(OH) 胶体粒子移向_____极;(填“阴极”或“阳极”)
3
(5)可用如图所示的装置除去 Fe(OH) 胶体中的杂质离子来提纯 Fe(OH) 胶体,实验过程中需不断更换烧杯中的蒸
3 3
馏水。更换蒸馏水若干次后,取少量烧杯中的液体,向其中加入 AgNO 溶液,若_____(填实验现象),则说明该
3
Fe(OH) 胶体中的杂质离子已经完全除去。
3CDCBD BCBDA BCBDA
16
(1)64g/mol
(2)
(3)
(4)
(5)
(6)50%
17
(1)Na O
2 2
(2) ①. 坩埚 ②.
(3)
(4)
(5) ①. ②.
18
(1)
(2)烧杯、漏斗 (3) ①. 、 ②.
(4) ①. 、 、 ②.
(5)不合理,若滤液中含有 或 ,滴加硝酸银溶液会生成白色沉淀 或 ,无法确定白色沉
淀中含有19
FeCl +3H O Fe(OH) ( 胶体)+3HCl 用一束光通过制得的液体,若有光亮的“通路”则已经制备成功
3 2 3
由于Fe(OH) 胶体遇到电解质会发生聚沉,因而形成红褐色沉淀 Fe(OH) +3H+ =Fe3++3H O 阴 不出现
3 3 2
白色沉淀