文档内容
2021 学年第一学期初三综合测试练习卷(2022.01)
化 学 部 分
1.试卷满分50分。
2.按要求在答题纸上规定的位置作答,在试卷、草稿纸上答题一律无效。
可能用到的相对原子质量:H-1 C-12 O-16 Cu-64
五、选择题(本大题共17题,共20分)请将正确选项的代号用2B铅笔填涂在答题纸的相应
位置上,更改答案时,用橡皮擦去,重新填涂。
21-34每题只有1个正确选项,每题1分,共14分。
1. 空气中含量最多的气体是
A. 氮气 B. 氧气 C. 二氧化碳 D. 氩气
【答案】A
【解析】
【详解】空气中含量最多的气体是氮气,大约占空气体积的78%。故选A。
2. 2021年6—8月,奉贤博物馆展出了一批三星堆出土的珍贵文物,有青铜器、玉石器、金器、象牙等。
古人制作这些物品的过程中涉及到化学变化的是
A. 冶炼金属 B. 雕刻玉石 C. 锤打黄金 D. 打磨象牙
【答案】A
【解析】
【分析】化学变化是有新物质生成的变化。
【详解】A、冶炼金属是将金属矿物质转变为金属单质的过程,该过程有新物质生成,属于化学变化,符
合题意;
B、雕刻玉石只是改变了玉石的形状和大小,没有新物质生成,属于物理变化,不符合题意;
C、捶打黄金只是改变了黄金的形状,没有新物质生成,属于物理变化,不符合题意;
D、打磨象牙改变的是象牙的的形状和大小,没有新物质生成,属于物理变化,不符合题意。
故选A。
【点睛】物理变化与化学变化的本质区别是是否有新物质生成。
3. 属于纯净物的是
A. 空气 B. 海水 C. 甲烷 D. 石油
【答案】C
【解析】
【分析】
学科网(北京)股份有限公司【详解】A、空气中含有氮气、氧气等多种成分,属于混合物。
B、海水中含有水和氯化钠等多种物质,属于混合物。
C、甲烷由一种物质组成,属于纯净物。
D、石油中含有汽油、煤油、柴油等多种成分,属于混合物。
故选:C。
4. 引起酸雨的主要物质是
A. 一氧化碳 B. 二氧化碳 C. 二氧化硫 D. 氮气
【答案】C
【解析】
【详解】引起酸雨的物质是非金属氧化物与水反应生成酸,空气中造成酸雨的主要气体有二氧化硫和二氧
化氮,二氧化碳与水生成碳酸,酸性较弱,不能形成酸雨,故选:C。
5. 厨房中常用的调味品放入足量水中,不能形成溶液的是
A. 白醋 B. 食盐 C. 蔗糖 D. 麻油
【答案】D
【解析】
【分析】
【详解】物质溶于水形成均一、稳定的混合物属于溶液,白醋、食盐、蔗糖都能溶于水,都能形成溶液,
而食用油不能溶于水,不能形成溶液,故选:D。
6. 自来水生产中通入氯气的主要作用是( )
A. 除去异味 B. 消毒杀菌 C. 吸附颗粒 D. 沉降杂质
【答案】B
【解析】
【详解】氯气与水反应生成次氯酸和盐酸,次氯酸具有氧化性,能起到消毒杀菌的作用。
故选B。
7. 下列物质中碱性最强的是
A. 柠檬汁 pH=3 B. 食盐水 pH=7 C. 牙膏 pH=8 D. 肥皂水 pH=10
【答案】D
【解析】
【
详解】pH>7时,pH值越大碱性越强,越小碱性越弱;pH<7时,pH值越小酸性越强,越大酸性越弱;
故选D。
8. 互为同素异形体的一组物质是
A. 氢气与液氢 B. 氧气与臭氧 C. 水与双氧水 D. 生石灰与熟石灰
学科网(北京)股份有限公司【答案】B
【解析】
【分析】同种元素形成的不同单质之间互称同素异形体。
【详解】A、氢气和液氢是氢气的不同存在状态,属于同一种物质,A不符合题意;
B、氧气和臭氧是氧元素形成的不同单质,属于同素异形体,B符合题意;
C、水分子式是HO,双氧水的分子式是HO,二者都是化合物,C不符合题意。
2 2 2
D、生石灰的化学式是CaO,熟石灰的化学式是Ca(OH) ,二者都是化合物,D不符合题意。故选B。
2
【点睛】满足同素异形体的前提条件首先是单质,之所以同种元素形成了不同的单质是因为构成单质的原
子之间排列方式不同。
9. 加湿器可增加室内空气湿度,这是因为
A. 分子间有间隔 B. 分子体积很小
C. 分子发生分解 D. 分子不断运动
【答案】D
【解析】
【详解】根据分子的性质可知,加湿器可增加室内空气湿度,是由于分子在不断的运动。故选D。
10. 含有游离态氧元素的是
A. 氯酸钾 B. 过氧化氢 C. 二氧化锰 D. 液氧
【答案】D
【解析】
【分析】元素以游离态存在即是以单质形式存在。
【详解】A、氯酸钾是由钾、氯、氧3种元素组成的纯净物,属于化合物,氧元素以化合态形式存在,选
项A错误;
B、过氧化氢是由氢、氧2种元素组成的纯净物,属于化合物,氧元素以化合态形式存在,选项B错误;
C、二氧化锰是由不同种元素组成的纯净物,属于化合物,氧元素以化合态形式存在,选项C错误;
D、液氧是由一种元素组成的纯净物,属于单质,氧元素以游离态形式存在,选项D正确。
故选:D。
11. 表示2个氢分子的是
A. H B. 2H C. 2H D. 2HO
2 2 2 2
【答案】C
【解析】
【分析】
学科网(北京)股份有限公司【详解】A、H 可以表示氢气这种物质,也可以表示1个氢分子,A不符合题意;
2
B、2H只表示2个氢原子,B不符合题意;
C、分子式前面的数字表示分子的个数,2H 表示2个氢分子,C符合题意;
2
D、2HO 表示2个过氧化氢分子,D不符合题意。
2 2
故选C。
12. 物质的用途主要由其化学性质决定的是
A. 活性炭吸附异味 B. 干冰作制冷剂
C. 稀有气体作保护气 D. 金刚石切割玻璃
【答案】C
【解析】
【详解】A、活性炭结构疏松多孔,具有吸附性,属于物理性质,故A错误;
B、干冰做制冷剂是利用其升华吸热的特点,属于物理性质,故B错误;
C、稀有气体化学性质很稳定,故用做保护气,是利用其化学性质,故C正确;
D、金刚石切割玻璃是利用其硬度大的特点,属于其物理性质,故D错误;
故选C。
13. 下列化学方程式中书写正确的是
A. B.
C. D.
【答案】C
【解析】
【详解】化学方程式书写时,要符合实际反应情况、要正确使用符号标识、要遵循质量守恒定律。
A、反应前有气体,反应后生成的气体不用标气体符号,故A错误;
B、反应前后氧原子个数不守恒,故B错误;
C、碳酸钙高温分解生成氧化钙和二氧化碳,符合反应事实,符号标识使用正确,遵循质量守恒,故C正
确;
D、过氧化氢分解产生水和二氧化碳,没有氢气产生,且一般情况下需要二氧化锰作催化剂,故D错误;
故选C。
14. 有关摩尔质量叙述正确的是
A. 单位是摩尔
B. 等于物质的量乘以质量
学科网(北京)股份有限公司C. 数值上等于物质的式量
D. 表示单位体积物质的质量
【答案】C
【解析】
【详解】试题分析:单位物质的量的物质所具有的质量,称为摩尔质量,当物质的质量以克为单位时,摩
尔质量在数值上等于该物质的相对分子质量或相对原子质量,摩尔质量的单位是克/摩尔,故选C
考点:摩尔质量
35-37每题有1—2个正确选项,每题2分,共6分。有2个正确选项的,选对1个得1分,多
选或错选得0分。
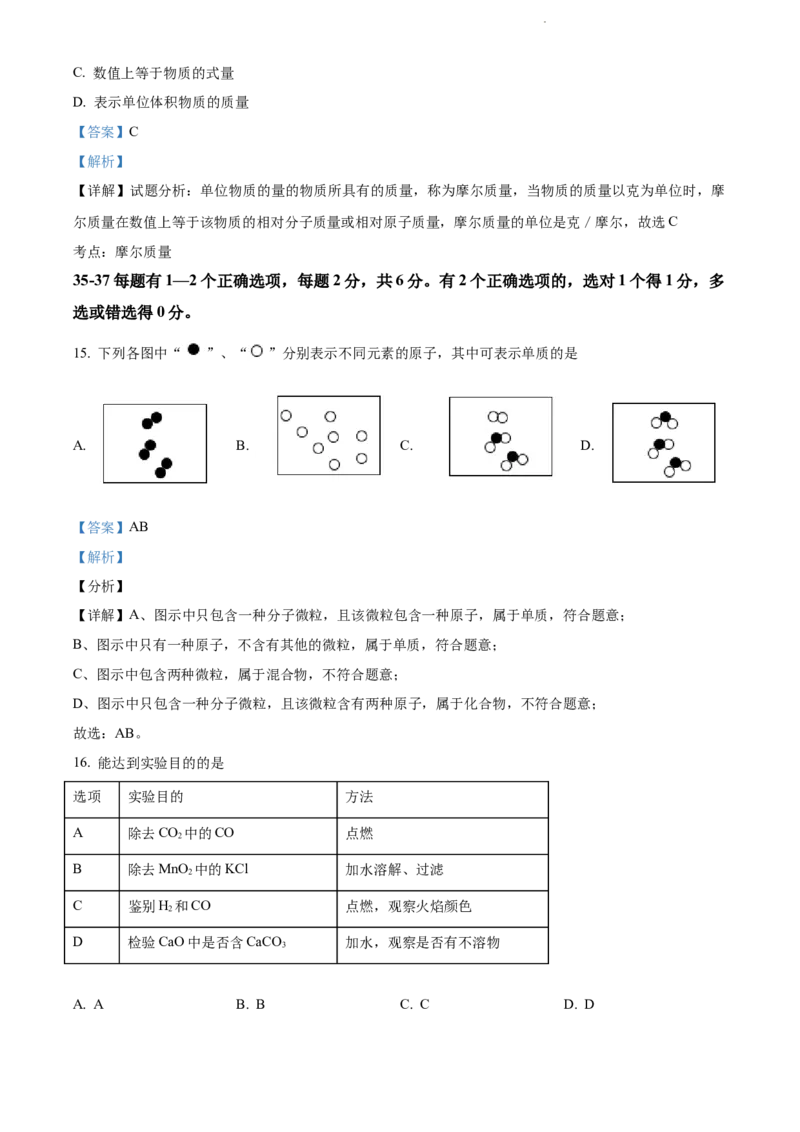
15. 下列各图中“ ”、“ ”分别表示不同元素的原子,其中可表示单质的是
A. B. C. D.
【答案】AB
【解析】
【分析】
【详解】A、图示中只包含一种分子微粒,且该微粒包含一种原子,属于单质,符合题意;
B、图示中只有一种原子,不含有其他的微粒,属于单质,符合题意;
C、图示中包含两种微粒,属于混合物,不符合题意;
D、图示中只包含一种分子微粒,且该微粒含有两种原子,属于化合物,不符合题意;
故选:AB。
16. 能达到实验目的的是
选项 实验目的 方法
A 除去CO 中的CO 点燃
2
B 除去MnO 中的KCl 加水溶解、过滤
2
C 鉴别H 和CO 点燃,观察火焰颜色
2
D 检验CaO中是否含CaCO 加水,观察是否有不溶物
3
A. A B. B C. C D. D
学科网(北京)股份有限公司【答案】B
【解析】
【分析】
【详解】A、二氧化碳不具有助燃性,除去CO 中的CO,不能点燃,错误。
2
B、氯化钾溶于水,二氧化锰不溶于水,除去MnO 中的KCl加水溶解、过滤,正确。
2
C、氢气燃烧淡蓝色火焰,一氧化碳燃烧蓝色火焰,火焰颜色相近,无法区分,错误。
D、氧化钙和水生成氢氧化钙微溶于水,即使有不溶物,也不能确定是碳酸钙,可能是氢氧化钙,错误。
故选:B。
17. 关于化合反应说法正确的是
A. 氧化反应一定是化合反应
B. 有单质参加的反应一定是化合反应
C. 化合反应中生成物中元素的存在形态一定是化合态
D. 化合反应中生成物的物质的量可能等于反应物的物质的量之和
【答案】CD
【解析】
【分析】
【详解】A、氧化反应不一定是化合反应,如蜡烛燃烧,错误。
B、有单质参加的反应不一定是化合反应,如铁和硫酸反应属于置换反应,错误。
C、化合反应中生成物中元紫的存在形态一定是化合态,正确。
D、化合反应中生成物的物质的量可能等于反应物的物质的量之和,如氢气和氯气生成氯化氢,正确。
故选:CD。
六、简答题(本大题共4题,共30分)
18. 2020年9月,中国向世界宜布了2030年前实现“碳达峰”、2060年前实现“碳中和”的目标。
(1)实现“碳中和”,能源转型首当其冲,氢能是绿色能源,光伏发电可为电解水制氢气提供电能,电
解水的化学方程式为______。光伏发电用到的高纯硅可用SiO 制取,SiO 中Si元素的化合价为______。
2 2
(2)CO 的捕获与封存也是实现膜中和的重要途径,有科学家提出设想:将排放到空气中的二氧化碳液化
2
后压入到冰冷的深海中进行封存,二氧化碳在深海中溶解度比在通常状况下水中的溶解度______(填
“大”、“小”或“不变”),原因是______。
(3)CO 若合理利用,也是一种重要原料。CO 与H 在催化条件下能反应生成甲醇(CHO),反应的化
2 2 2 4
学方程式为 ,X的化学式为______,CHO由______种不同元素组成,
4
学科网(北京)股份有限公司1molCH O中约含______个碳原子。
4
【答案】(1) ①. ②. +4##+4价
的
(2) ①. 大 ②. 温度越低,压强越大,气体 溶解度增大
(3) ①. HO ②. 3##三 ③. 6.02×1023
2
【解析】
【分析】
【小问1详解】
电解水生成氢气和氧气,该反应的化学方程式为: ,SiO 中氧元素的化合价为-2
2
价 , 根 据 化 学 式 中 正 负 化 合 价 的 代 数 和 为 零 , 则 Si 元 素 的 化 合 价 为 +4 价 , 故 填 :
;+4或+4价。
【小问2详解】
将排放到空气中的二氧化碳液化后压入到冰冷的深海中进行封存,二氧化碳在深海中溶解度比在通常状况
下水中的溶解度大,因为温度越低,压强越大,气体的溶解度增大,故填:大;温度越低,压强越大,气
体的溶解度增大。
【小问3详解】
根据质量守恒定律,化学反应前后原子的种类和数目不变,反应前碳、氧、氢原子的数目分别是:1、2、
6,反应后碳、氧、氢原子的数目也分别是:1、2、6,则一个X分子中含有2个氢原子、1个氧原子,所
以X的化学式为HO;CHO是由碳、氧、氢3种元素组成;1个CHO分子中含有1个碳原子,1molCH O
2 4 4 4
中约含6.02×1023个碳原子,故填:HO;3或三;6.02×1023。
2
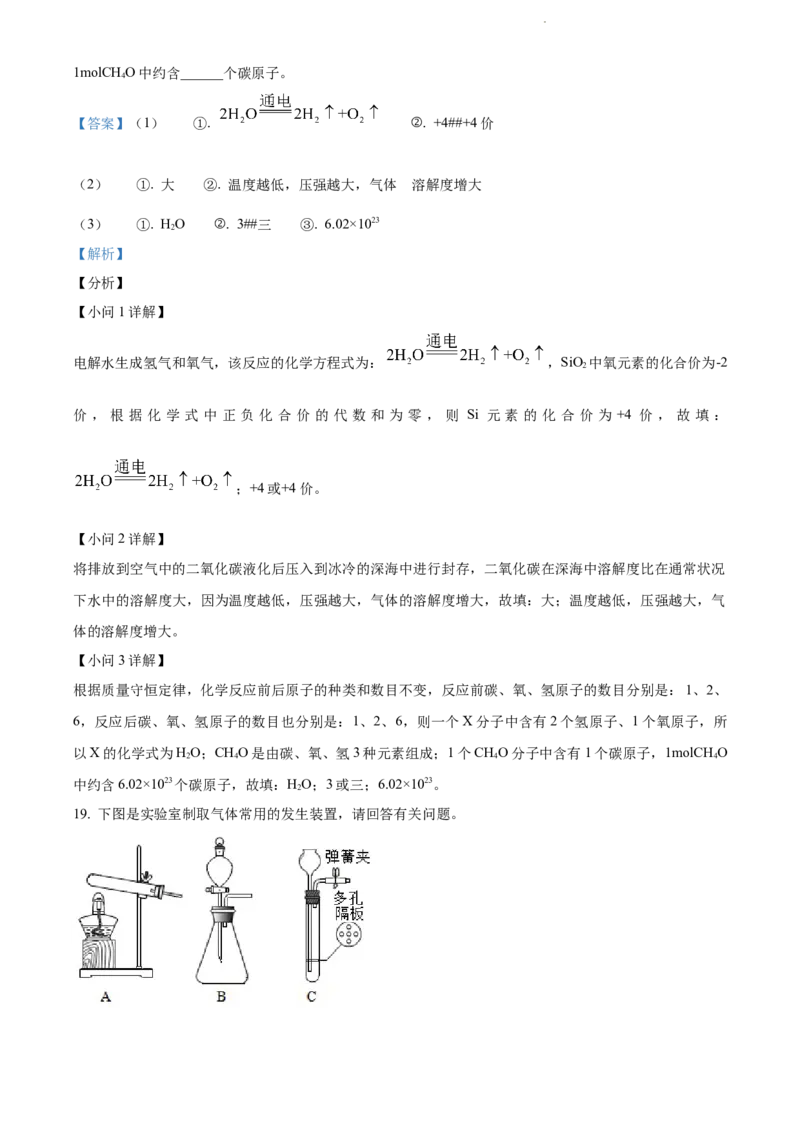
19. 下图是实验室制取气体常用的发生装置,请回答有关问题。
学科网(北京)股份有限公司(1)实验室制氧气 。
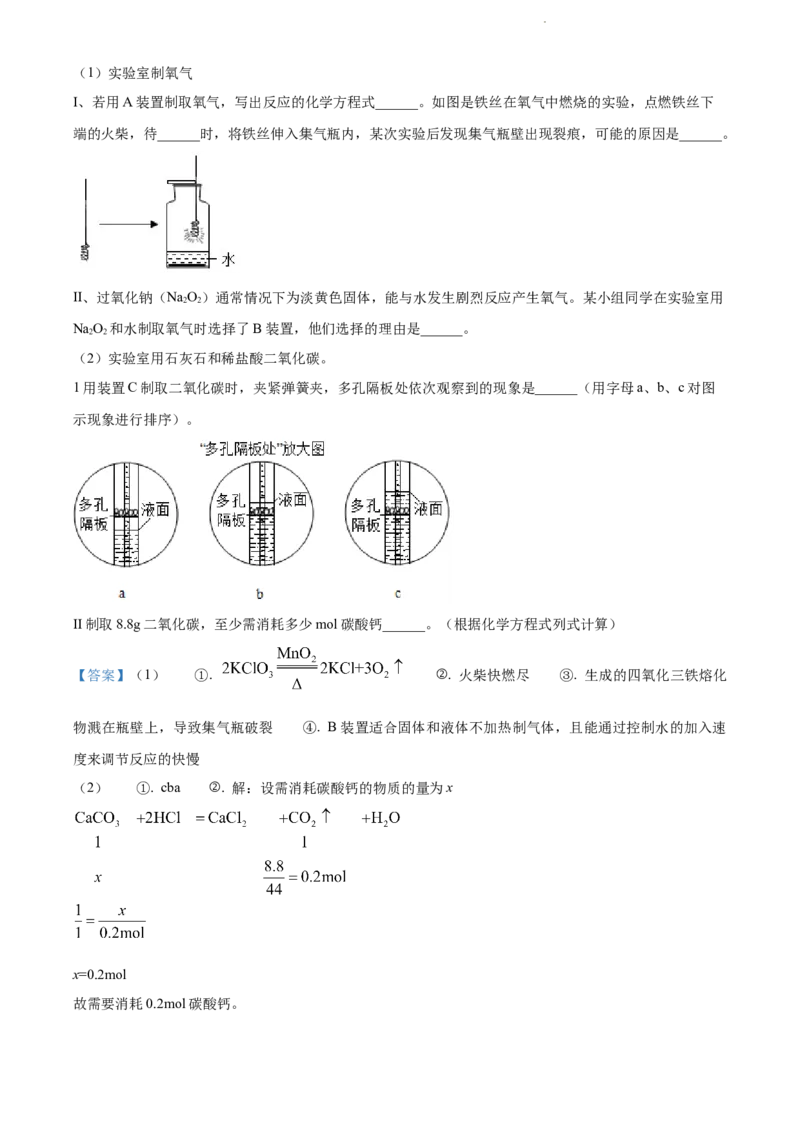
I、若用A装置制取氧气,写出反应的化学方程式______。如图是铁丝在氧气中燃烧的实验,点燃铁丝下
端的火柴,待______时,将铁丝伸入集气瓶内,某次实验后发现集气瓶壁出现裂痕,可能的原因是______。
II、过氧化钠(NaO)通常情况下为淡黄色固体,能与水发生剧烈反应产生氧气。某小组同学在实验室用
2 2
NaO 和水制取氧气时选择了B装置,他们选择的理由是______。
2 2
(2)实验室用石灰石和稀盐酸二氧化碳。
1用装置C制取二氧化碳时,夹紧弹簧夹,多孔隔板处依次观察到的现象是______(用字母a、b、c对图
示现象进行排序)。
II制取8.8g二氧化碳,至少需消耗多少mol碳酸钙______。(根据化学方程式列式计算)
【答案】(1) ①. ②. 火柴快燃尽 ③. 生成的四氧化三铁熔化
物溅在瓶壁上,导致集气瓶破裂 ④. B装置适合固体和液体不加热制气体,且能通过控制水的加入速
度来调节反应的快慢
(2) ①. cba ②. 解:设需消耗碳酸钙的物质的量为x
x=0.2mol
故需要消耗0.2mol碳酸钙。
学科网(北京)股份有限公司【解析】
【分析】本题考查了气体制备的反应原理和气体发生装置的选择,以及和制得的气体相关联的知识。气体
发生装置的选择,主要是根据反应物的状态和反应条件来确定。装置C制备气体时,是启普发生器原理。
【小问1详解】
I、A装置制备气体属于固体加热型,试管口没有棉花团,可以选择氯酸钾和二氧化锰混合物加热分解,化
学方程式为: 。
在做铁丝和氧气的反应试验时,点燃铁丝下端的火柴后,待火柴燃尽时,将铁丝伸入集气瓶中,此时铁丝
温度较高且可以避免火柴燃烧消耗较多氧气;
如果发现瓶壁出现裂痕,可能是熔化的四氧化三铁溅在瓶壁上造成的;
II、过氧化钠和水反应制备氧气时,属于固体和液体不加热制气体的类型,可以选择B装置,而且B装置
可以通过控制水加入的速度来调节反应的快慢。
【小问2详解】
I、用装置C制取二氧化碳的原理是启普发生器原理,制取二氧化碳时,如果夹紧弹簧夹,则气体不能放出,
使得试管内压强增大,试管内液体被压入到长颈漏斗中,故依次观察到的现象是cba。
II、计算过程见答案。
【点睛】启普发生器及其改进装置的优点都是可以控制反应的发生和停止,即“随开随用,随关随停”。
20. 下表是NaCl、CaCl 在不同温度下的溶解度。
2
温度/℃ 20 40 60 80
NaCl 36.0 36.6 37.0 38.4
溶解度(g/100gH O)
2
CaCl 27.6 39.8 41.4 43.2
2
请回答下列问题:
(1)20°C时溶解度较大的物质是______。
(2)使接近饱和的CaCl 溶液变为饱和,可采用的一种方法是______。
2
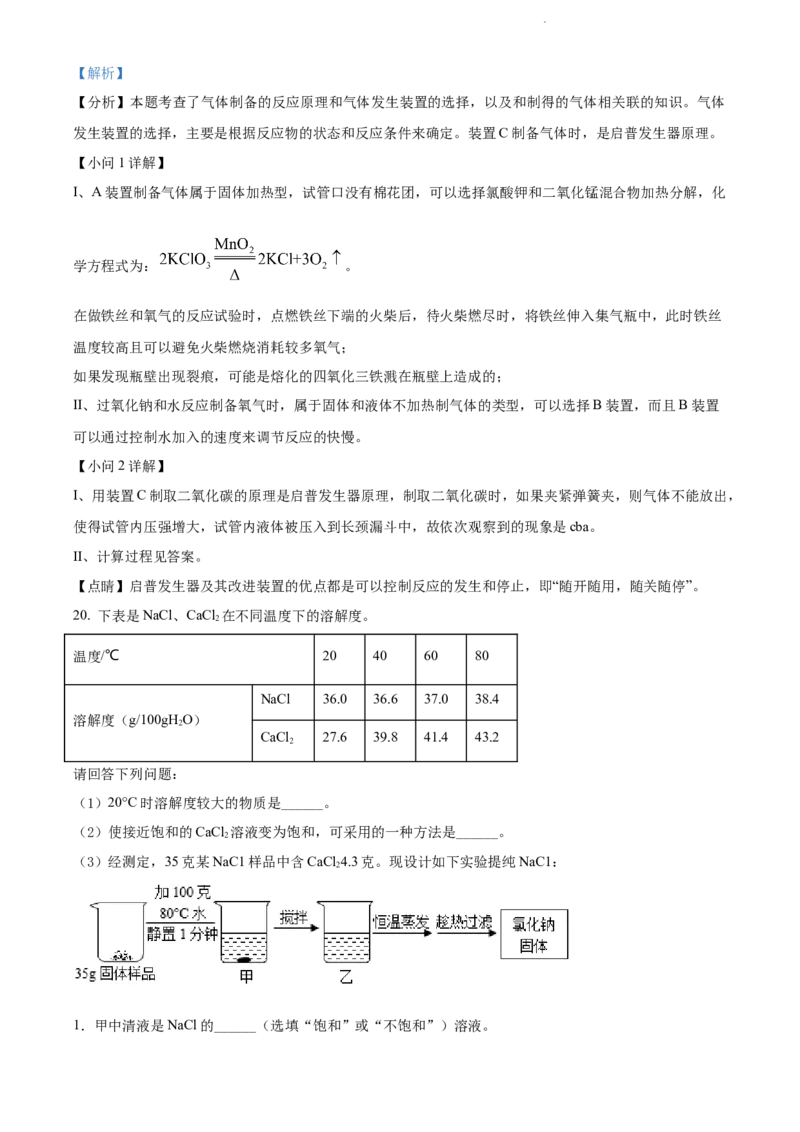
(3)经测定,35克某NaC1样品中含CaCl 4.3克。现设计如下实验提纯NaC1:
2
1.甲中清液是NaCl的______(选填“饱和”或“不饱和”)溶液。
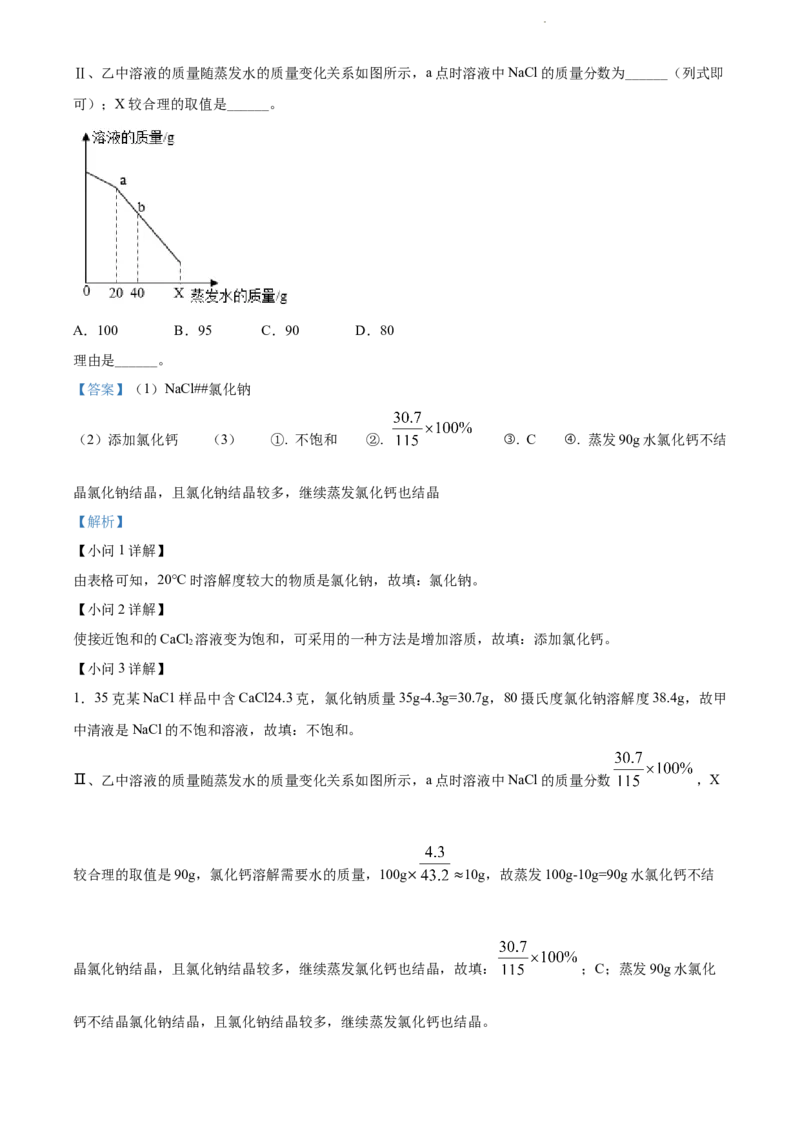
学科网(北京)股份有限公司Ⅱ、乙中溶液的质量随蒸发水的质量变化关系如图所示,a点时溶液中NaCl的质量分数为______(列式即
可);X较合理的取值是______。
A.100 B.95 C.90 D.80
理由是______。
【答案】(1)NaCl##氯化钠
(2)添加氯化钙 (3) ①. 不饱和 ②. ③. C ④. 蒸发90g水氯化钙不结
晶氯化钠结晶,且氯化钠结晶较多,继续蒸发氯化钙也结晶
【解析】
【小问1详解】
由表格可知,20°C时溶解度较大的物质是氯化钠,故填:氯化钠。
【小问2详解】
使接近饱和的CaCl 溶液变为饱和,可采用的一种方法是增加溶质,故填:添加氯化钙。
2
【小问3详解】
1.35克某NaC1样品中含CaCl24.3克,氯化钠质量35g-4.3g=30.7g,80摄氏度氯化钠溶解度38.4g,故甲
中清液是NaCl的不饱和溶液,故填:不饱和。
Ⅱ、乙中溶液的质量随蒸发水的质量变化关系如图所示,a点时溶液中NaCl的质量分数 ,X
较合理的取值是90g,氯化钙溶解需要水的质量,100g 10g,故蒸发100g-10g=90g水氯化钙不结
× ≈
晶氯化钠结晶,且氯化钠结晶较多,继续蒸发氯化钙也结晶,故填: ;C;蒸发90g水氯化
钙不结晶氯化钠结晶,且氯化钠结晶较多,继续蒸发氯化钙也结晶。
学科网(北京)股份有限公司21. 某研究性学习小组对炭粉与氧化铜反应产物中气体的成分进行研究。
【提出假设】该反应的气体产物除二氧化碳外还有其他气体。
【查阅资料】氮气不能跟碳粉和氧化铜发生反应,也不跟石灰水反应,可用来隔绝氧气。
【设计方案】将一定量氧化铜在隔绝氧气的条件下与过量炭粉充分反应。通过测定反应前后和关物质的质
量进行判断。
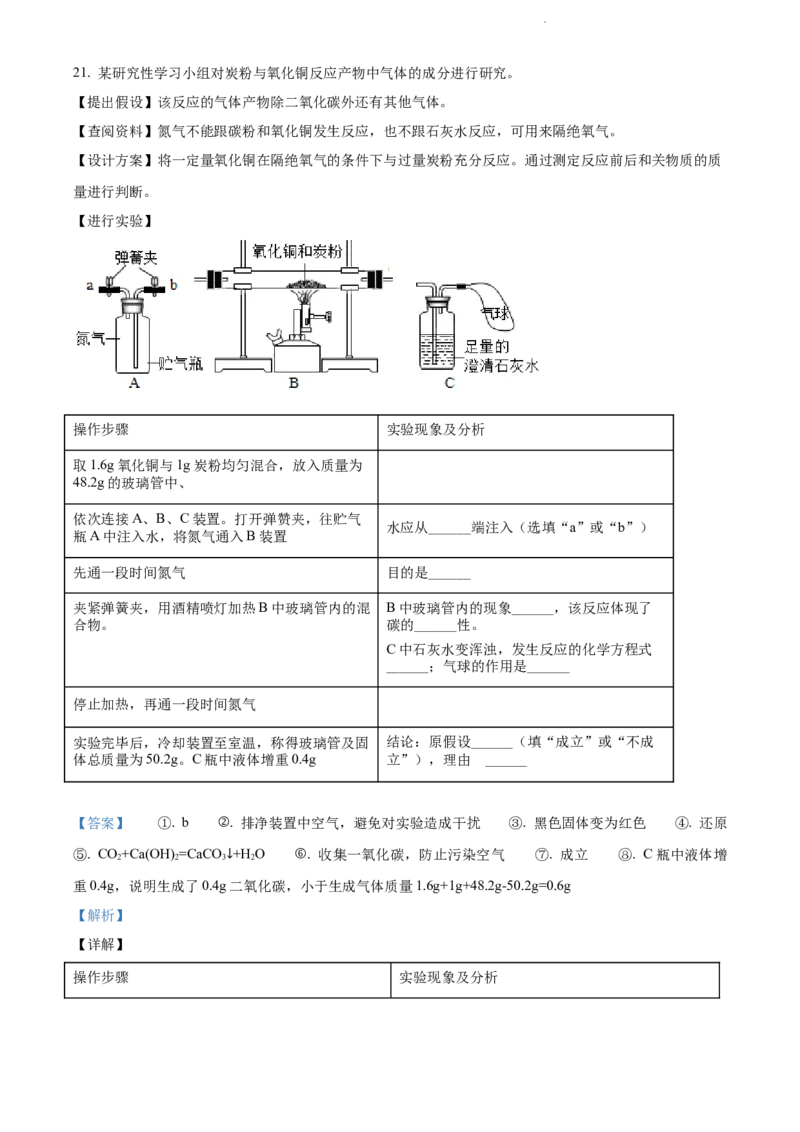
【进行实验】
操作步骤 实验现象及分析
取1.6g氧化铜与1g炭粉均匀混合,放入质量为
48.2g的玻璃管中、
依次连接A、B、C装置。打开弹赞夹,往贮气
水应从______端注入(选填“a”或“b”)
瓶A中注入水,将氮气通入B装置
先通一段时间氮气 目的是______
夹紧弹簧夹,用酒精喷灯加热B中玻璃管内的混 B中玻璃管内的现象______,该反应体现了
合物。 碳的______性。
C中石灰水变浑浊,发生反应的化学方程式
______;气球的作用是______
停止加热,再通一段时间氮气 。
实验完毕后,冷却装置至室温,称得玻璃管及固 结论:原假设______(填“成立”或“不成
体总质量为50.2g。C瓶中液体增重0.4g 立”),理由 是______
【答案】 ①. b ②. 排净装置中空气,避免对实验造成干扰 ③. 黑色固体变为红色 ④. 还原
⑤. CO+Ca(OH) =CaCO +H O ⑥. 收集一氧化碳,防止污染空气 ⑦. 成立 ⑧. C瓶中液体增
2 2 3 2
重0.4g,说明生成了0.4g↓二氧化碳,小于生成气体质量1.6g+1g+48.2g-50.2g=0.6g
【解析】
【详解】
操作步骤 实验现象及分析
学科网(北京)股份有限公司取1.6 g氧化铜与1 g炭粉均匀混合,放入质量为
48.2 g的B装置的玻璃管中。
打开弹簧夹,往贮气瓶A中注入水,将氮气通入
水的密度比氮气大,水应从b端注入,故填:b。
B装置中。
氮气不能跟碳粉和氧化铜发生反应,目的是排尽装
先通一段时间氮气。 置中的空气,故填:排净装置中的空气,避免对实
验造成干扰。
碳还原氧化铜生成铜和二氧化碳。玻璃管中的现象
是黑色固体逐渐变为红色,体现了碳的还原性,C
中二氧化碳和氢氧化钙生成碳酸钙和水,澄清石灰
夹紧弹簧夹,用酒精喷灯加热玻璃管内的混合 水变浑浊,化学方程式
物。 CO+Ca(OH) =CaCO +H O,气球作用是收集一氧
2 2 3 2
化碳,防止污染空气,故填:黑色固体变为红色;
还原;CO+Ca(OH) =↓CaCO +H O;收集一氧化
2 2 3 2
碳,防止污染空气。
↓
停止加热,再通入一段时间氮气。
C瓶中液体增重0.4g,说明生成了0.4g二氧化碳,
小于生成气体质量1.6g+1g+48.2g-50.2g=0.6g,说
实验完毕后,冷却装置至室温,称得B玻璃管及 明还有不能被澄清石灰水吸收的气体生成,故猜想
固体总质量为50.2 g,称得C瓶中液体增重0.4 g。 成立,故填:成立;C瓶中液体增重0.4g,说明生
成了0.4g二氧化碳,小于生成气体质量
1.6g+1g+48.2g-50.2g=0.6g。
学科网(北京)股份有限公司