文档内容
2021 学年第一学期初三综合测试练习卷(2022.01)
化 学 部 分
1.试卷满分50分。
2.按要求在答题纸上规定的位置作答,在试卷、草稿纸上答题一律无效。
可能用到的相对原子质量:H-1 C-12 O-16 Cu-64
五、选择题(本大题共17题,共20分)请将正确选项的代号用2B铅笔填涂在答题纸的相应
位置上,更改答案时,用橡皮擦去,重新填涂。
21-34每题只有1个正确选项,每题1分,共14分。
的
1. 空气中含量最多 气体是
A. 氮气 B. 氧气 C. 二氧化碳 D. 氩气
2. 2021年6—8月,奉贤博物馆展出了一批三星堆出土的珍贵文物,有青铜器、玉石器、金器、象牙等。
古人制作这些物品的过程中涉及到化学变化的是
A. 冶炼金属 B. 雕刻玉石 C. 锤打黄金 D. 打磨象牙
3. 属于纯净物的是
.
A 空气 B. 海水 C. 甲烷 D. 石油
4. 引起酸雨的主要物质是
A. 一氧化碳 B. 二氧化碳 C. 二氧化硫 D. 氮气
5. 厨房中常用的调味品放入足量水中,不能形成溶液的是
A. 白醋 B. 食盐 C. 蔗糖 D. 麻油
6. 自来水生产中通入氯气的主要作用是( )
A. 除去异味 B. 消毒杀菌 C. 吸附颗粒 D. 沉降杂质
7. 下列物质中碱性最强的是
A. 柠檬汁 pH=3 B. 食盐水 pH=7 C. 牙膏 pH=8 D. 肥皂水 pH=10
的
8. 互为同素异形体 一组物质是
A. 氢气与液氢 B. 氧气与臭氧 C. 水与双氧水 D. 生石灰与熟石灰
9. 加湿器可增加室内空气湿度,这是因为
A. 分子间有间隔 B. 分子体积很小
C. 分子发生分解 D. 分子不断运动
10. 含有游离态氧元素的是
学科网(北京)股份有限公司A. 氯酸钾 B. 过氧化氢 C. 二氧化锰 D. 液氧
11. 表示2个氢分子的是
A. H B. 2H C. 2H D. 2HO
2 2 2 2
12. 物质的用途主要由其化学性质决定的是
A. 活性炭吸附异味 B. 干冰作制冷剂
C. 稀有气体作保护气 D. 金刚石切割玻璃
13. 下列化学方程式中书写正确的是
A. B.
C. D.
14. 有关摩尔质量叙述正确的是
A. 单位是摩尔
B. 等于物质的量乘以质量
C. 数值上等于物质的式量
D. 表示单位体积物质的质量
35-37每题有1—2个正确选项,每题2分,共6分。有2个正确选项的,选对1个得1分,多
选或错选得0分。
15. 下列各图中“ ”、“ ”分别表示不同元素的原子,其中可表示单质的是
A. B. C. D.
16. 能达到实验目的的是
选项 实验目的 方法
A 除去CO 中的CO 点燃
2
B 除去MnO 中的KCl 加水溶解、过滤
2
C 鉴别H 和CO 点燃,观察火焰颜色
2
D 检验CaO中是否含CaCO 加水,观察是否有不溶物
3
学科网(北京)股份有限公司A. A B. B C. C D. D
17. 关于化合反应说法正确的是
A. 氧化反应一定是化合反应
的
B. 有单质参加 反应一定是化合反应
C. 化合反应中生成物中元素的存在形态一定是化合态
D. 化合反应中生成物的物质的量可能等于反应物的物质的量之和
六、简答题(本大题共4题,共30分)
18. 2020年9月,中国向世界宜布了2030年前实现“碳达峰”、2060年前实现“碳中和”的目标。
(1)实现“碳中和”,能源转型首当其冲,氢能是绿色能源,光伏发电可为电解水制氢气提供电能,电
解水的化学方程式为______。光伏发电用到的高纯硅可用SiO 制取,SiO 中Si元素的化合价为______。
2 2
(2)CO 的捕获与封存也是实现膜中和的重要途径,有科学家提出设想:将排放到空气中的二氧化碳液化
2
后压入到冰冷的深海中进行封存,二氧化碳在深海中溶解度比在通常状况下水中的溶解度______(填
“大”、“小”或“不变”),原因是______。
(3)CO 若合理利用,也是一种重要原料。CO 与H 在催化条件下能反应生成甲醇(CHO),反应的化
2 2 2 4
学方程式为 ,X的化学式为______,CHO由______种不同元素组成,
4
1molCH O中约含______个碳原子。
4
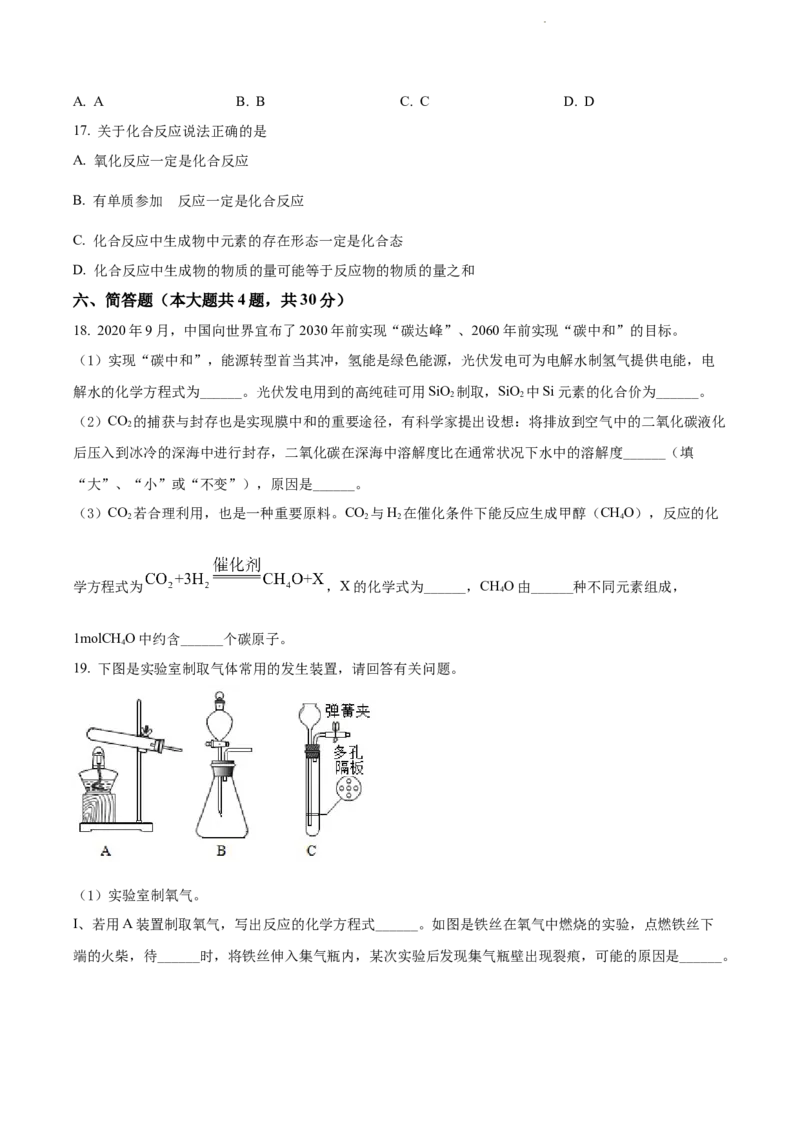
19. 下图是实验室制取气体常用的发生装置,请回答有关问题。
(1)实验室制氧气。
I、若用A装置制取氧气,写出反应的化学方程式______。如图是铁丝在氧气中燃烧的实验,点燃铁丝下
端的火柴,待______时,将铁丝伸入集气瓶内,某次实验后发现集气瓶壁出现裂痕,可能的原因是______。
学科网(北京)股份有限公司II、过氧化钠(NaO)通常情况下为淡黄色固体,能与水发生剧烈反应产生氧气。某小组同学在实验室用
2 2
NaO 和水制取氧气时选择了B装置,他们选择的理由是______。
2 2
(2)实验室用石灰石和稀盐酸二氧化碳。
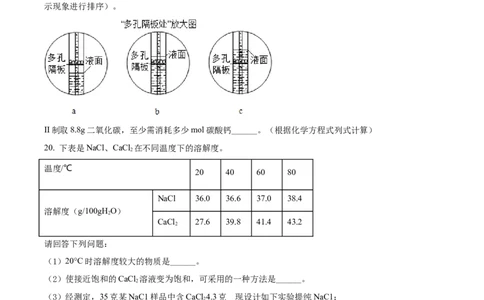
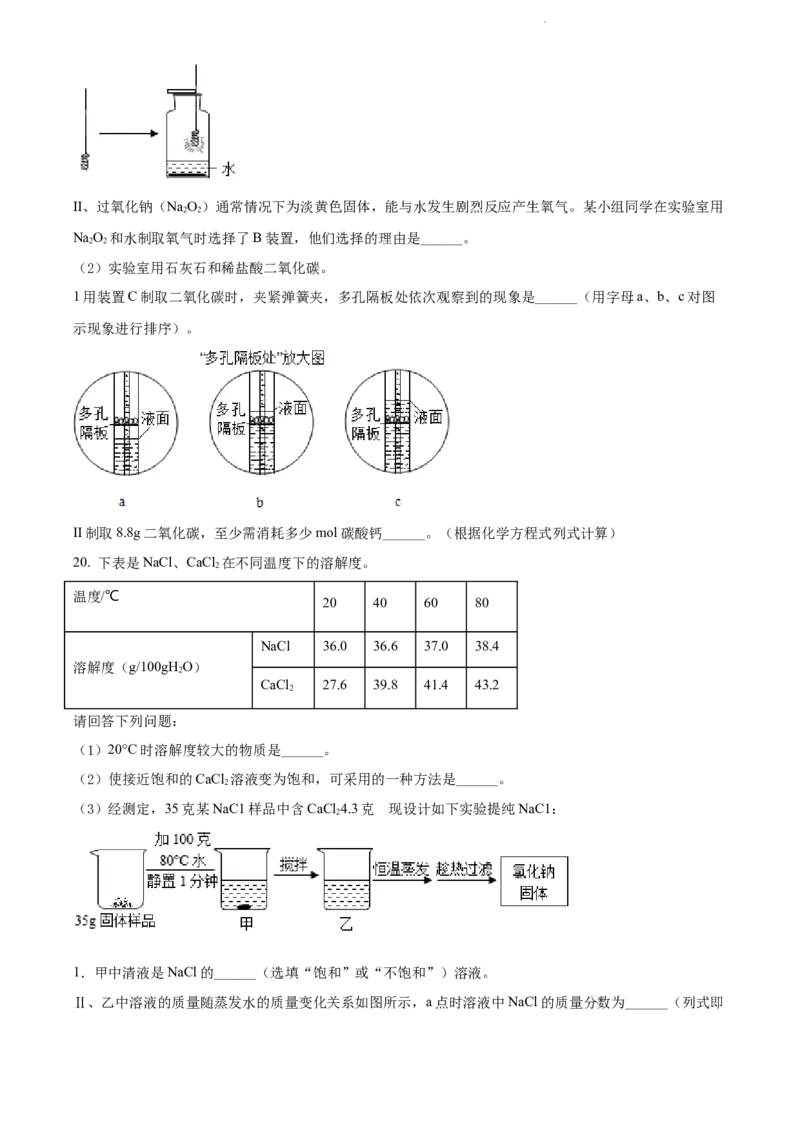
1用装置C制取二氧化碳时,夹紧弹簧夹,多孔隔板处依次观察到的现象是______(用字母a、b、c对图
示现象进行排序)。
II制取8.8g二氧化碳,至少需消耗多少mol碳酸钙______。(根据化学方程式列式计算)
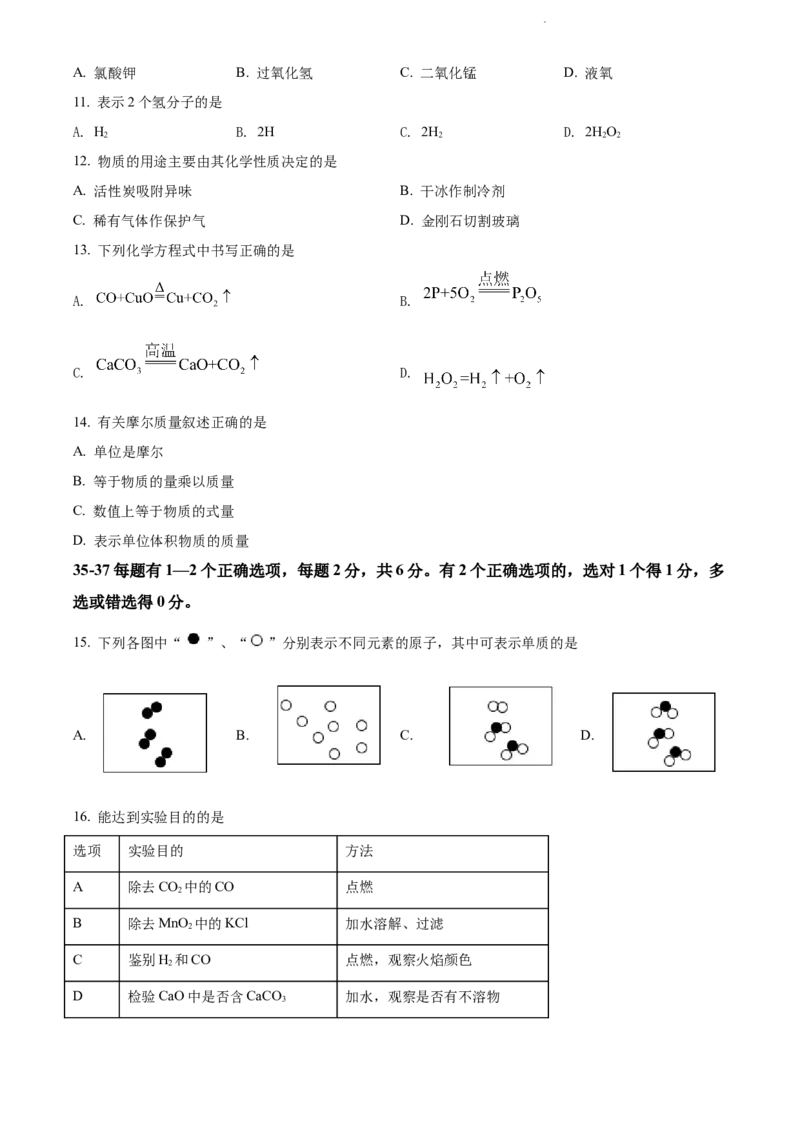
20. 下表是NaCl、CaCl 在不同温度下的溶解度。
2
温度/℃
20 40 60 80
NaCl 36.0 36.6 37.0 38.4
溶解度(g/100gH O)
2
CaCl 27.6 39.8 41.4 43.2
2
请回答下列问题:
(1)20°C时溶解度较大的物质是______。
(2)使接近饱和的CaCl 溶液变为饱和,可采用的一种方法是______。
2
(3)经测定,35克某NaC1样品中含CaCl 4.3克 。现设计如下实验提纯NaC1:
2
1.甲中清液是NaCl的______(选填“饱和”或“不饱和”)溶液。
Ⅱ、乙中溶液的质量随蒸发水的质量变化关系如图所示,a点时溶液中NaCl的质量分数为______(列式即
学科网(北京)股份有限公司可);X较合理的取值是______。
A.100 B.95 C.90 D.80
理由是______。
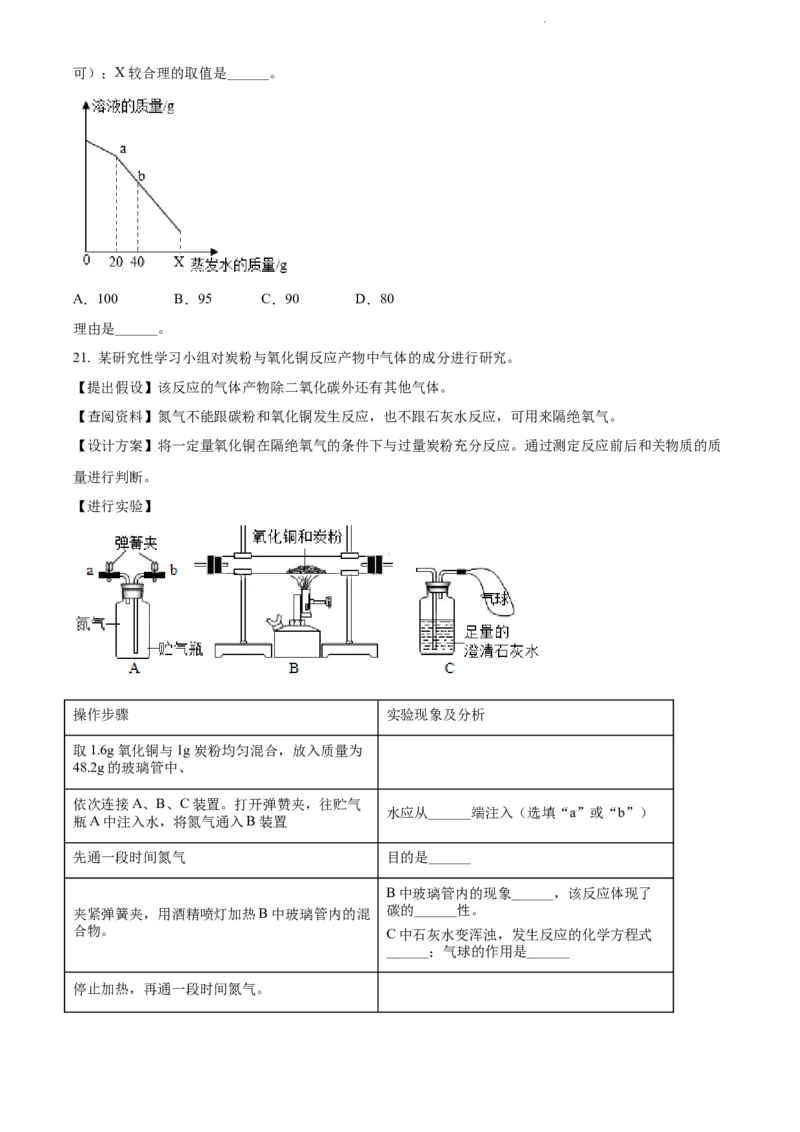
21. 某研究性学习小组对炭粉与氧化铜反应产物中气体的成分进行研究。
【提出假设】该反应的气体产物除二氧化碳外还有其他气体。
【查阅资料】氮气不能跟碳粉和氧化铜发生反应,也不跟石灰水反应,可用来隔绝氧气。
【设计方案】将一定量氧化铜在隔绝氧气的条件下与过量炭粉充分反应。通过测定反应前后和关物质的质
量进行判断。
【进行实验】
操作步骤 实验现象及分析
取1.6g氧化铜与1g炭粉均匀混合,放入质量为
48.2g的玻璃管中、
依次连接A、B、C装置。打开弹赞夹,往贮气
水应从______端注入(选填“a”或“b”)
瓶A中注入水,将氮气通入B装置
先通一段时间氮气 目的是______
B中玻璃管内的现象______,该反应体现了
夹紧弹簧夹,用酒精喷灯加热B中玻璃管内的混 碳的______性。
合物。 C中石灰水变浑浊,发生反应的化学方程式
______;气球的作用是______
停止加热,再通一段时间氮气。
学科网(北京)股份有限公司实验完毕后,冷却装置至室温,称得玻璃管及固 结论:原假设______(填“成立”或“不成
体总质量为50.2g。C瓶中液体增重0.4g 立”),理由是______
学科网(北京)股份有限公司