文档内容
上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
2023 年上海市松江区高考化学二模试卷
学校:___________姓名:___________班级:___________考号:___________
题号 一 二 三 总分
得分
注意事项:
1.答卷前,考生务必将自己的姓名、准考证号填写在答题卡上。
2.回答选择题时,选出每小题答案后,用铅笔把答题卡对应题目的答案标号涂黑;如需改动,
用橡皮擦干净后,再选涂其他答案标号。回答非选择题时,将答案写在答题卡上,写在试卷
上无效。
3.考试结束后,本试卷和答题卡一并交回。
第I卷(选择题)
一、单选题(本大题共20小题,共40.0分)
1. 2023年2月,我国海关在对进境邮件进行查验时,查获违法红珊瑚制品。珊瑚显红色,
源于在海底长期积淀某种元素的氧化物,该元素是( )
A. C B. Si C. Fe D. Na
2. “碳中和”是指CO 的排放总量和减少总量相当。下列措施能促进碳中和最直接有效
2
的是( )
A. 将重质油裂解为轻质油作为燃料 B. 大规模开采可燃冰作为新能源
C. 通过清洁煤技术减少煤燃烧污染 D. 研发催化剂将CO 还原为甲醇
2
3. 春季是流感、诺如病毒等疾病的高发期,需要对重点场所做好定期清洁消毒。下列物质
中,不是消毒剂的是( )
A. 漂粉精 B. 洁厕灵 C. 碘酒 D. 臭氧
4. 下列物质中,分子的空间结构为直线型的是( )
A. 乙烯 B. 甲烷 C. 氨 D. 二氧化碳
5. 科学家们创造出了最轻的镁同位素❑ 18Mg,❑ 18Mg与❑ 24Mg具有( )
A. 不同电子数 B. 不同物理性质 C. 不同核电荷数 D. 不同化学性质
6. 在FeSO 、CuSO 、Al (SO ) 的混合溶液中通入适量H S,产生的沉淀物是( )
4 4 2 4 3 2
A. Al(OH) B. Al S C. CuS D. FeS
3 2 3
7. 在合成氨和接触法制硫酸的工业生产中,下列说法错误的是( )
A. 均采用高压条件 B. 均选择较高温度 C. 均进行循环操作 D. 均使用合适催化剂
第 页 共 页
1 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
8. 一定条件下,存在“一种物质过量,另一种物质仍不能完全反应”情况的是( )
A. 一氧化氮与过量氧气 B. 氯化铝溶液与过量稀氨水
C. 铁片与过量浓硝酸 D. 澄清石灰水与过量二氧化碳
9. 海水提溴与海带提碘,共同点是( )
A. 浓缩方法 B. 采用热空气吹出 C. 四氯化碳萃取 D. 氧化剂可选择氯水
10. 下列物质间的转化关系中不能全部通过一步反应完成的是( )
A. Na→NaOH→Na CO →NaCl
2 3
B. Fe→FeCl →Fe(OH) →Fe O
3 3 2 3
C. Al→Al O →Al(OH) →AlCl
2 3 3 3
D. Mg→MgCl →Mg(OH) →MgSO
2 2 4
11. 下列各组在溶液中的反应,不管反应物的量多少,都能用同一离子方程式表示的是
( )
A. FeBr 与Cl B. Ba(OH) 与NaHSO
2 2 2 4
C. HCl与Na CO D. Ca(HCO ) 与Ca(OH)
2 3 3 2 2
12. 侯氏制碱法制造纯碱同时副产氯化铵。下列有关母液处理的说法错误的是( )
A. 升高温度,有利于N H Cl更多地析出
4
B. 加入食盐,增大Cl−的浓度,使N H Cl更多地析出
4
C. 通入氨气,增大N H+ 的浓度,使N H Cl更多地析出
4 4
D. 通入氨气,使NaHCO 转化为Na CO ,提高析出的N H Cl纯度
3 2 3 4
13. 如图装置用于实验室中制取干燥氨气的实验,其中能达到实验目的的是 ( )
A. 用装置甲制备氨气 B. 用装置乙除去氨气中的少量水
C. 用装置丙收集氨气 D. 用装置丁吸收多余的氨气
第 页 共 页
2 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
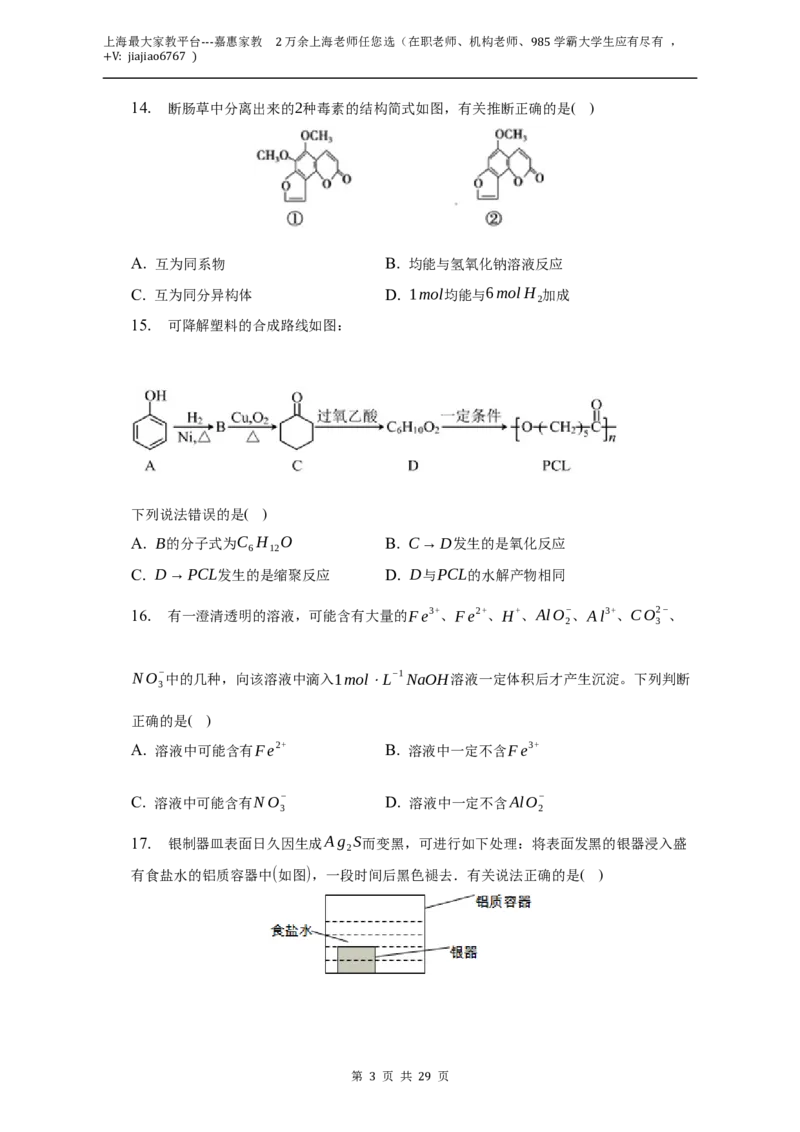
14. 断肠草中分离出来的2种毒素的结构简式如图,有关推断正确的是( )
A. 互为同系物 B. 均能与氢氧化钠溶液反应
C. 互为同分异构体 D. 1mol均能与6molH 加成
2
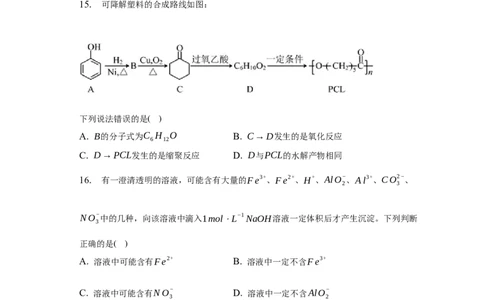
15. 可降解塑料的合成路线如图:
下列说法错误的是( )
A. B的分子式为C H O B. C→D发生的是氧化反应
6 12
C. D→PCL发生的是缩聚反应 D. D与PCL的水解产物相同
16. 有一澄清透明的溶液,可能含有大量的Fe3+、Fe2+、H+、AlO− 、Al3+、CO2− 、
2 3
NO− 中的几种,向该溶液中滴入1mol⋅L−1NaOH溶液一定体积后才产生沉淀。下列判断
3
正确的是( )
A. 溶液中可能含有Fe2+ B. 溶液中一定不含Fe3+
C. 溶液中可能含有NO− D. 溶液中一定不含AlO−
3 2
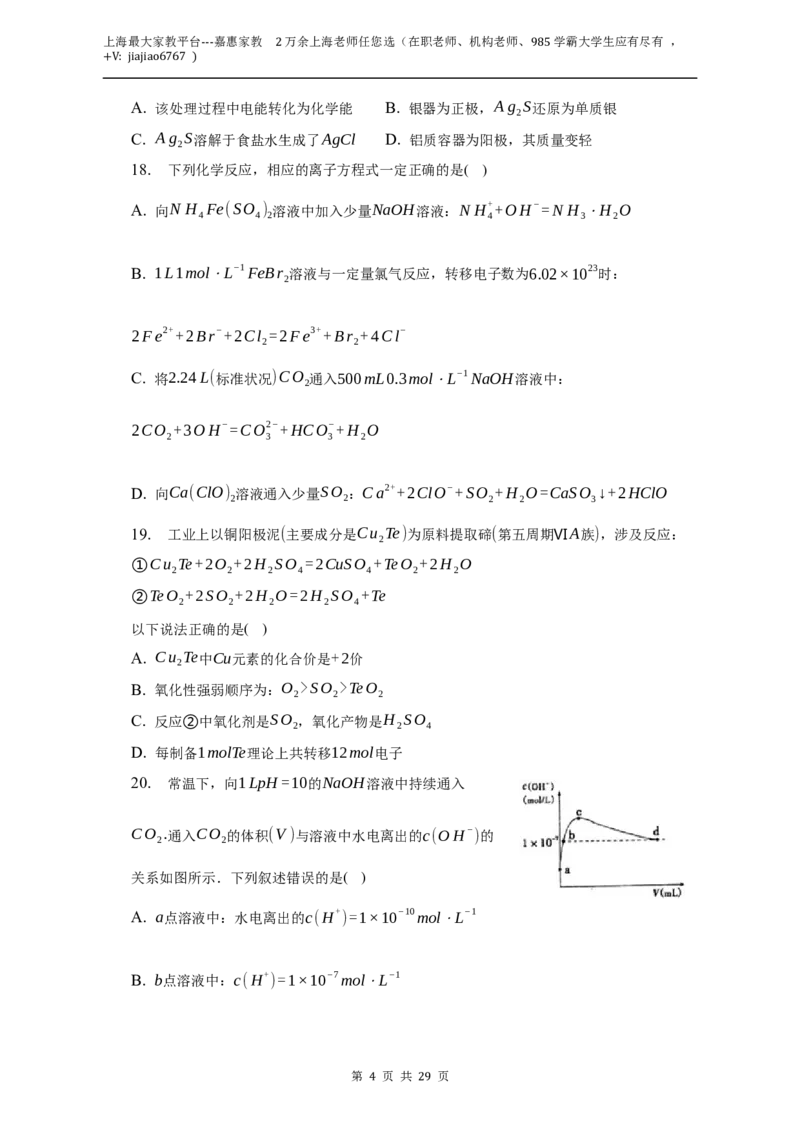
17. 银制器皿表面日久因生成Ag S而变黑,可进行如下处理:将表面发黑的银器浸入盛
2
有食盐水的铝质容器中(如图),一段时间后黑色褪去.有关说法正确的是( )
第 页 共 页
3 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
A. 该处理过程中电能转化为化学能 B. 银器为正极,Ag S还原为单质银
2
C. Ag S溶解于食盐水生成了AgCl D. 铝质容器为阳极,其质量变轻
2
18. 下列化学反应,相应的离子方程式一定正确的是( )
A. 向N H Fe(SO ) 溶液中加入少量NaOH溶液:N H++OH−=N H ⋅H O
4 4 2 4 3 2
B. 1L1mol⋅L−1FeBr 溶液与一定量氯气反应,转移电子数为6.02×1023时:
2
2Fe2++2Br−+2Cl =2Fe3++Br +4Cl−
2 2
C. 将2.24L(标准状况)CO 通入500mL0.3mol⋅L−1NaOH溶液中:
2
2CO +3OH−=CO2−+HCO−+H O
2 3 3 2
D. 向Ca(ClO) 溶液通入少量SO :Ca2++2ClO−+SO +H O=CaSO ↓+2HClO
2 2 2 2 3
19. 工业上以铜阳极泥(主要成分是Cu Te)为原料提取碲(第五周期ⅥA族),涉及反应:
2
①Cu Te+2O +2H SO =2CuSO +TeO +2H O
2 2 2 4 4 2 2
②TeO +2SO +2H O=2H SO +Te
2 2 2 2 4
以下说法正确的是( )
A. Cu Te中Cu元素的化合价是+2价
2
B. 氧化性强弱顺序为:O >SO >TeO
2 2 2
C. 反应②中氧化剂是SO ,氧化产物是H SO
2 2 4
D. 每制备1molTe理论上共转移12mol电子
20. 常温下,向1LpH=10的NaOH溶液中持续通入
CO .通入CO 的体积(V)与溶液中水电离出的c(OH− )的
2 2
关系如图所示.下列叙述错误的是( )
A. a点溶液中:水电离出的c(H+ )=1×10−10mol⋅L−1
B. b点溶液中:c(H+ )=1×10−7mol⋅L−1
第 页 共 页
4 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
C. c点溶液中:c(Na+ )>c(HCO− )>c(CO2− )
3 3
D. d点溶液中:c(Na+ )=2c(CO2− )+c(HCO− )
3 3
第II卷(非选择题)
二、实验题(本大题共1小题,共15.0分)
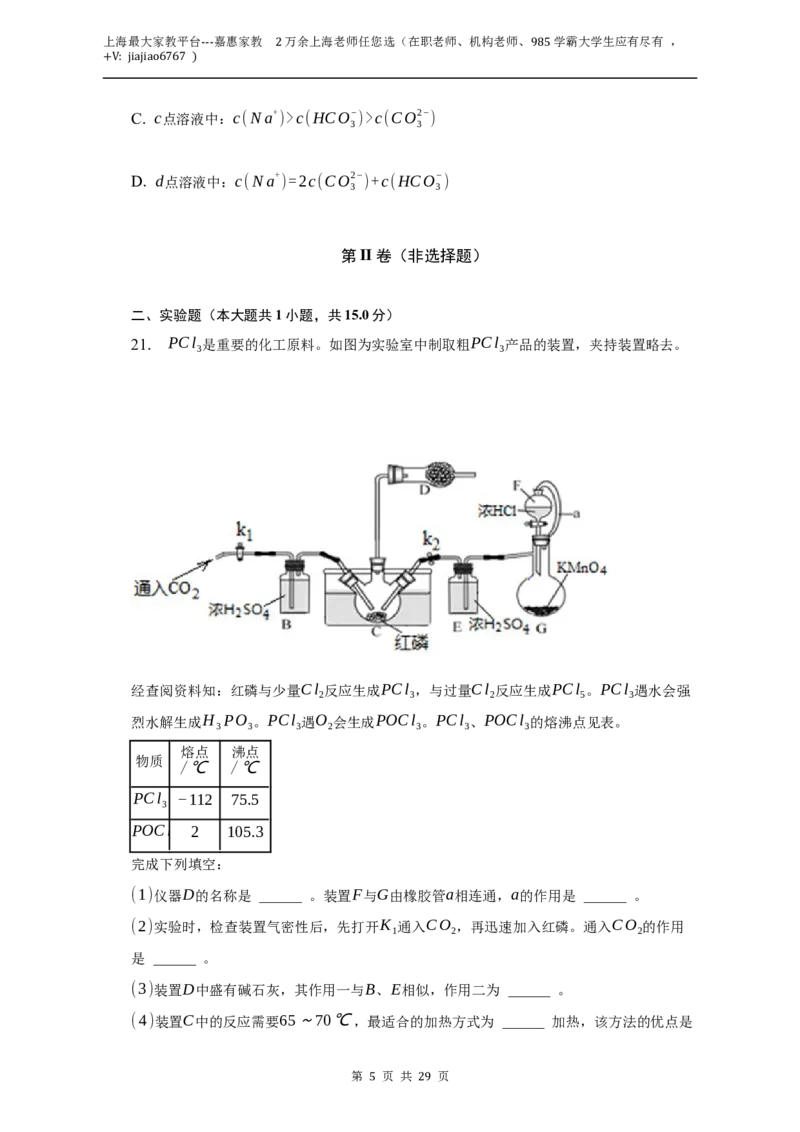
21. PCl 是重要的化工原料。如图为实验室中制取粗PCl 产品的装置,夹持装置略去。
3 3
经查阅资料知:红磷与少量Cl 反应生成PCl ,与过量Cl 反应生成PCl 。PCl 遇水会强
2 3 2 5 3
烈水解生成H PO 。PCl 遇O 会生成POCl 。PCl 、POCl 的熔沸点见表。
3 3 3 2 3 3 3
熔点 沸点
物质
/℃ /℃
PCl −112 75.5
3
POCl 2 105.3
3
完成下列填空:
(1)仪器D的名称是 ______ 。装置F与G由橡胶管a相连通,a的作用是 ______ 。
(2)实验时,检查装置气密性后,先打开K 通入CO ,再迅速加入红磷。通入CO 的作用
1 2 2
是 ______ 。
(3)装置D中盛有碱石灰,其作用一与B、E相似,作用二为 ______ 。
(4)装置C中的反应需要65~70℃,最适合的加热方式为 ______ 加热,该方法的优点是
第 页 共 页
5 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
______ 。制得的PCl 粗产品中常含有POCl 、PCl 等。加入红磷加热除去PCl 后,通过
3 3 5 5
______ (填实验操作名称),即可得到较纯净的PCl 。
3
(5)通过实验测定粗产品中PCl 的质量分数,实验步骤如下(不考虑杂质的反应):
3
第一步:迅速移取20.000gPCl 粗产品,加水完全水解;
3
第二步:配成500mL溶液,移取25.00mL溶液置于锥形瓶中;
第三步:加入0.500mol⋅L−1碘溶液20.00mL,碘过量,H PO 完全反应生成H PO ,
3 3 3 4
反应方程式为H PO +H O+I =H PO +2HI;
3 3 2 2 3 4
第四步:加入几滴淀粉溶液,用1.000mol⋅L−1Na S O 标准溶液滴定过量的碘,反应方
2 2 3
程式为I +2Na S O =Na S O +2NaI,滴至终点时消耗Na S O 标准溶液12.00mL。
2 2 2 3 2 4 6 2 2 3
第二步需要的定量仪器名称为 ______ 。根据上述数据,计算该产品中PCl 的质量分数为
3
______ 。
三、简答题(本大题共3小题,共45.0分)
22. H O (过氧化氢)应用领域非常广泛。
2 2
已知:2H O (l)⇌2H O(l)+O (g)+Q(Q>0)
2 2 2 2
H O (aq)⇌H+ (aq)+HO− (aq),K(25℃)=2.24×10−12
2 2 2
完成下列填空:
(1)氧原子最外层成对电子和未成对电子数目之比为 ______ 。
(2)H O 的电子式为 ______ 。对H O 分子结构,有以下两种推测:
2 2 2 2
要确定H O 分子结构,需要测定H O 分子中的 ______ 。(选填序号)
2 2 2 2
a.H−O键长
b.O−O键长
c.H−O−O键角
第 页 共 页
6 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
d.H−O、O−O键能
(3)H O 分解反应的平衡常数表达式K= ______ 。不同温度下H O 分解反应的平衡常数
2 2 2 2
K(25℃) ______ K(40℃)(选填“>”“<”或“=”)。标准状况下,某5mLH O 溶
2 2
液60s内产生氧气22.4mL(溶液体积变化忽略不计)。则0~60s,v(H O )= ______ 。
2 2
(4)25℃,pH(H O ) ______ pH(H O)(选填“>”“<”或“=”)。
2 2 2
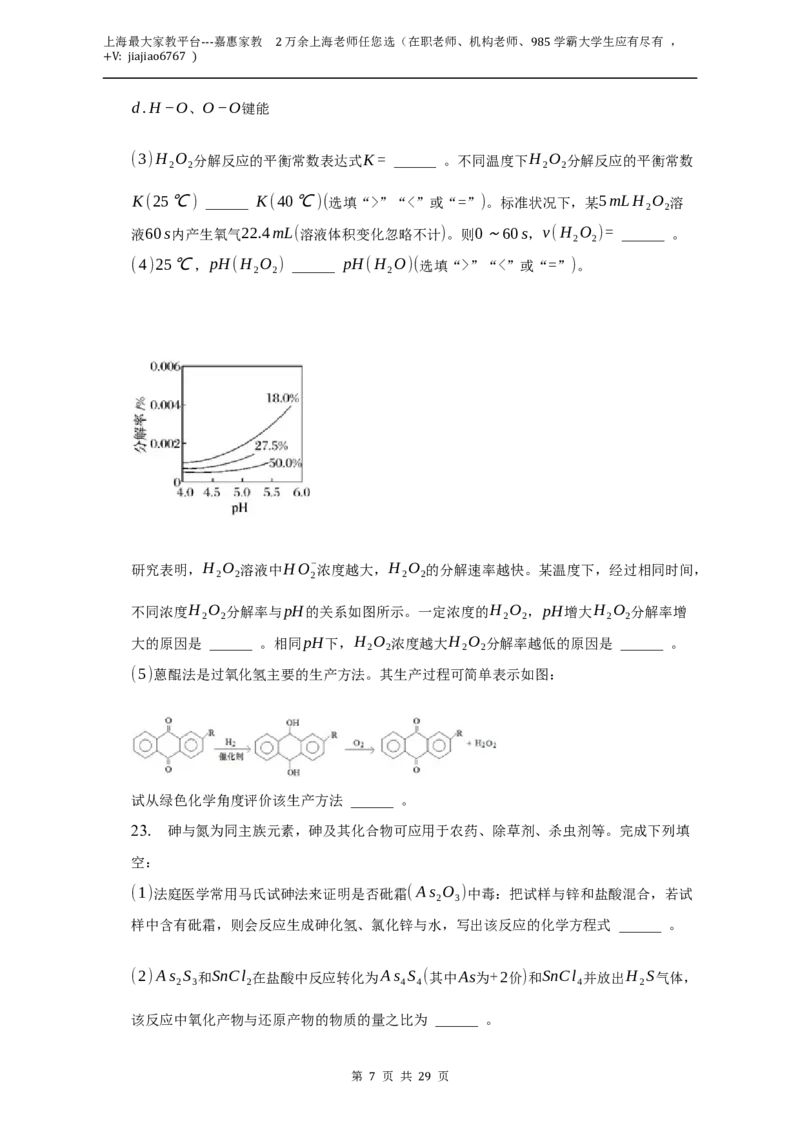
研究表明,H O 溶液中HO− 浓度越大,H O 的分解速率越快。某温度下,经过相同时间,
2 2 2 2 2
不同浓度H O 分解率与pH的关系如图所示。一定浓度的H O ,pH增大H O 分解率增
2 2 2 2 2 2
大的原因是 ______ 。相同pH下,H O 浓度越大H O 分解率越低的原因是 ______ 。
2 2 2 2
(5)蒽醌法是过氧化氢主要的生产方法。其生产过程可简单表示如图:
试从绿色化学角度评价该生产方法 ______ 。
23. 砷与氮为同主族元素,砷及其化合物可应用于农药、除草剂、杀虫剂等。完成下列填
空:
(1)法庭医学常用马氏试砷法来证明是否砒霜(As O )中毒:把试样与锌和盐酸混合,若试
2 3
样中含有砒霜,则会反应生成砷化氢、氯化锌与水,写出该反应的化学方程式 ______ 。
(2)As S 和SnCl 在盐酸中反应转化为As S (其中As为+2价)和SnCl 并放出H S气体,
2 3 2 4 4 4 2
该反应中氧化产物与还原产物的物质的量之比为 ______ 。
第 页 共 页
7 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
(3)一定条件下,雄黄(As S )与O 生成As O 与物质a。若该反应中1molAs S 参加反
4 4 2 2 3 4 4
应时,转移28mol电子。写出物质a的化学式 ______ 。
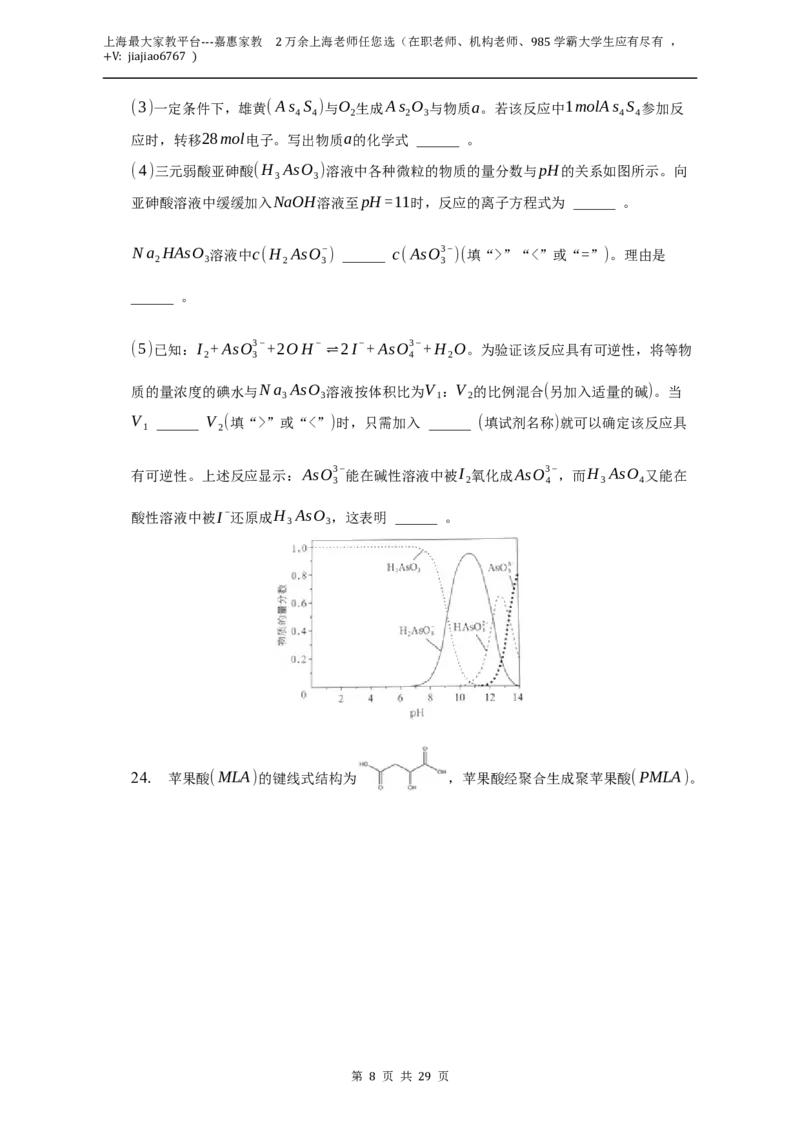
(4)三元弱酸亚砷酸(H AsO )溶液中各种微粒的物质的量分数与pH的关系如图所示。向
3 3
亚砷酸溶液中缓缓加入NaOH溶液至pH=11时,反应的离子方程式为 ______ 。
Na HAsO 溶液中c(H AsO− ) ______ c(AsO3− )(填“>”“<”或“=”)。理由是
2 3 2 3 3
______ 。
(5)已知:I +AsO3−+2OH− ⇌2I−+AsO3−+H O。为验证该反应具有可逆性,将等物
2 3 4 2
质的量浓度的碘水与Na AsO 溶液按体积比为V :V 的比例混合(另加入适量的碱)。当
3 3 1 2
V ______ V (填“>”或“<”)时,只需加入 ______ (填试剂名称)就可以确定该反应具
1 2
有可逆性。上述反应显示:AsO3− 能在碱性溶液中被I 氧化成AsO3− ,而H AsO 又能在
3 2 4 3 4
酸性溶液中被I−还原成H AsO ,这表明 ______ 。
3 3
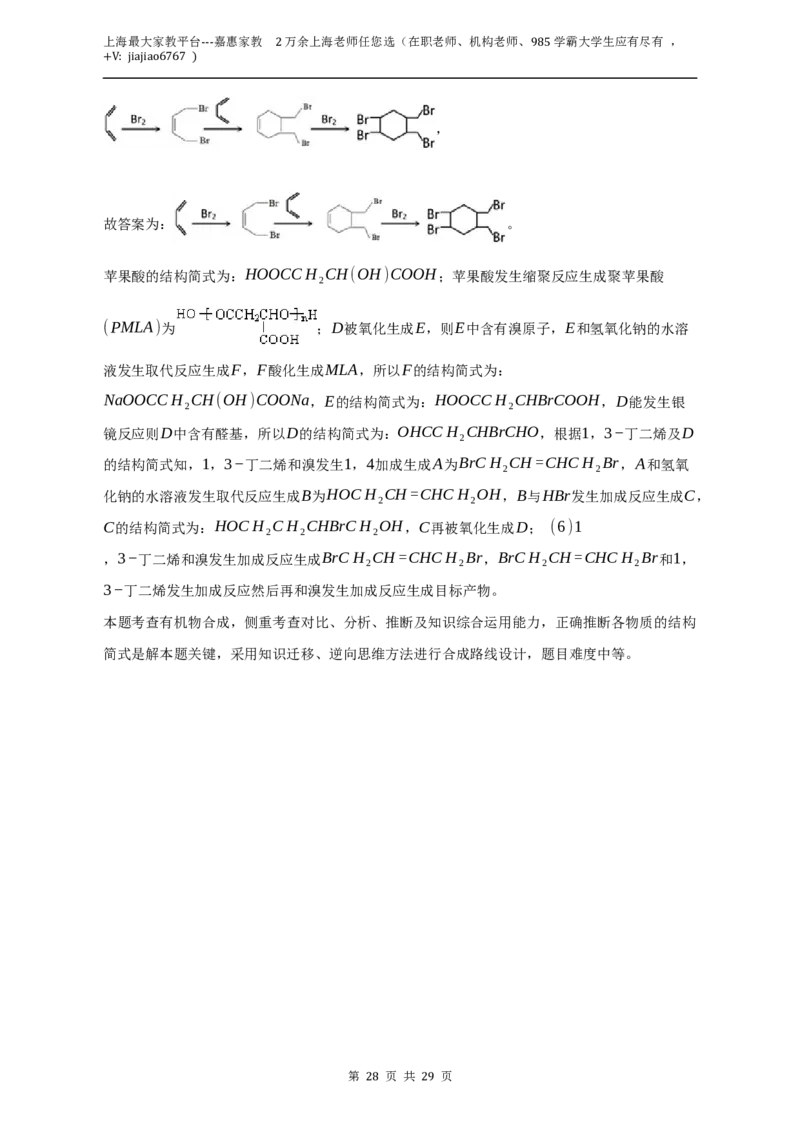
24. 苹果酸(MLA)的键线式结构为 ,苹果酸经聚合生成聚苹果酸(PMLA)。
第 页 共 页
8 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
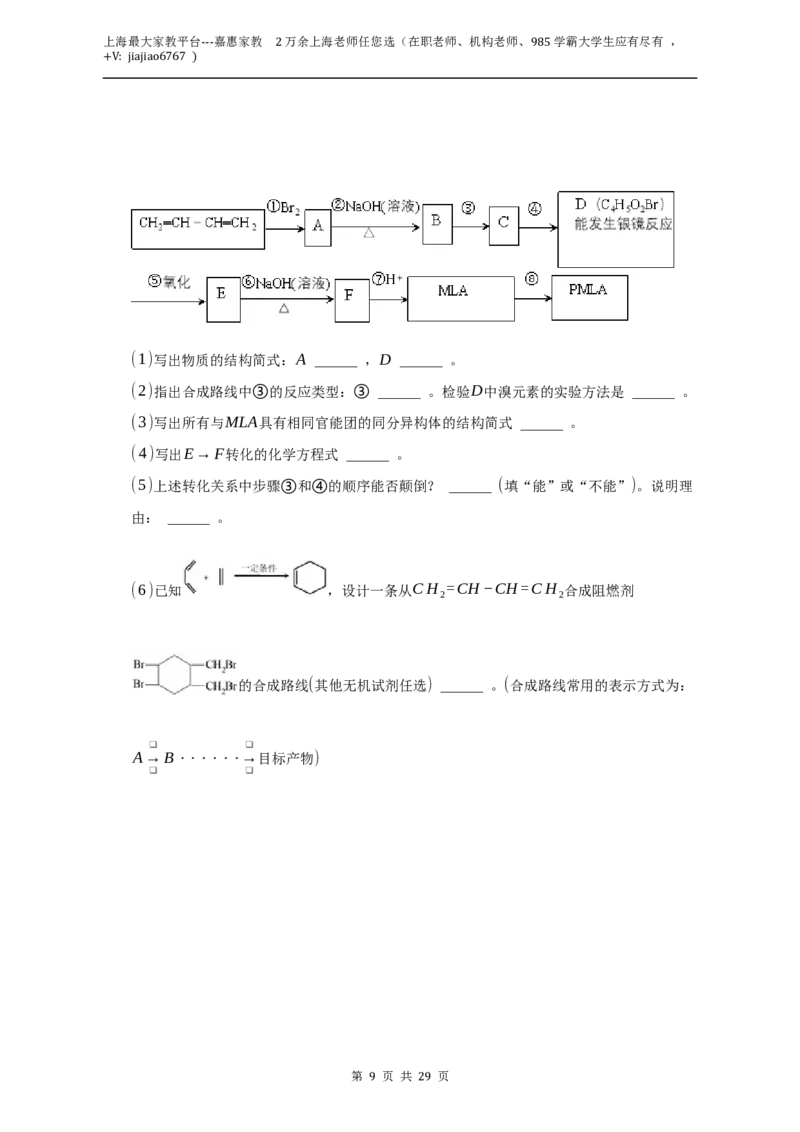
(1)写出物质的结构简式:A ______ ,D ______ 。
(2)指出合成路线中③的反应类型:③ ______ 。检验D中溴元素的实验方法是 ______ 。
(3)写出所有与MLA具有相同官能团的同分异构体的结构简式 ______ 。
(4)写出E→F转化的化学方程式 ______ 。
(5)上述转化关系中步骤③和④的顺序能否颠倒? ______ (填“能”或“不能”)。说明理
由: ______ 。
(6)已知 ,设计一条从CH =CH−CH=CH 合成阻燃剂
2 2
的合成路线(其他无机试剂任选) ______ 。(合成路线常用的表示方式为:
❑ ❑
A→B⋅⋅⋅⋅⋅⋅→目标产物)
❑ ❑
第 页 共 页
9 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
答案和解析
1.【答案】C
【解析】解:A.碳元素形成的氧化物:CO、CO 均为无色气体,无红色物质形成,故A错误;
2
B.海水中硅元素含量很低,硅元素形成的氧化物SiO 是无色晶体,无红色物质生成,故B错误;
2
C.铁元素形成氧化铁呈红色,珊瑚在生长过程中吸收氧化铁形成红色,故C正确;
D.钠形成的氧化物:Na O是白色固体、Na O是淡黄色固体,无红色物质形成,故D错误;
2 2
故选:C。
红珊瑚的化学成分主要是CaCO ,矿物成分以徽晶方解石集合体形式存在,红色是珊瑚在生长
3
过程中吸收海水中1%左右的氧化铁而形成的,所以红色是铁元素形成的氧化铁呈现的。
本题考查了红珊瑚的知识应用,较简单,熟练掌握铁及其化合物的性质和颜色,了解珊瑚的形成
过程是关键。
2.【答案】D
【解析】解:A.将重质油裂解为轻质油,轻质油燃烧时仍旧会产生二氧化碳,无法减少二氧化
碳的排放量,不能实现碳中和,故A错误;
B.可燃冰的主要成分为甲烷,甲烷在燃烧时也会产生二氧化碳,不能实现碳中和,故B错误;
C.通过清洁煤技术减少煤燃烧污染,不能减少二氧化碳的排放量,无法实现碳中和,故C错误;
D.研发催化剂将二氧化碳还原为甲醇,可以减少二氧化碳的排放量,从而实现碳中和,故D正确;
故选:D。
“碳中和”是指CO 的排放总量和减少总量相当.即减少二氧化碳的排放或将二氧化碳转化为
2
其它可利用的物质。
本题主要考查环境保护与绿色化学,侧重考查学生解决实际问题的能力,试题比较简单。
3.【答案】B
第 页 共 页
10 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
【解析】解:A.漂粉精的主要成分是次氯酸钙,具有强氧化性,能杀菌消毒,故A正确;
B.洁厕灵的主要成分的HCl,具有酸性,用于清除水垢,不是消毒剂,故B错误;
C.碘酒是碘的乙醇溶液,能使蛋白质变性,能杀菌消毒,故C正确;
D.臭氧具有强氧化性,可以杀菌消毒且不会产生气体污染性物质,故D正确;
故选:B。
A.漂粉精的主要成分是次氯酸钙,具有强氧化性;
B.洁厕灵的主要成分的HCl,具有酸性;
C.碘酒是碘的乙醇溶液,能使蛋白质变性;
D.臭氧具有强氧化性。
本题考查常见的消毒剂,明确每种消毒剂的消毒原理是解题的关键,注意对基础知识的积累,难
度不大。
4.【答案】D
【解析】解:A.乙烯的结构简式为CH =CH ,是平面型结构,故A错误;
2 2
B.甲烷的分子式为CH ,是正四面体结构,故B错误;
4
C.氨的分子式是N H ,是三角锥形结构,故C错误;
3
D.二氧化碳的分子式是CO ,是直线型分子,三原子在一条直线上,故D正确;
2
故选:D。
根据乙烯、甲烷、氨、二氧化碳的空间构型,进行分析判断。
本题主要考查常见物质的空间构型,属于基本知识的考查,难度不大。
5.【答案】B
【解析】解:A.❑ 18Mg与❑ 24Mg的质子数均为12,核外电子数也均为12,核外电子数相同,
故A错误;
B.❑ 18Mg与❑ 24Mg的中子数不同,分别为6和12,质量数不同,物理性质不同,故B正确;
C.❑ 18Mg与❑ 24Mg的质子数均为12,核电荷数也均为12,核电荷数相同,故C错误;
D.❑ 18Mg与❑ 24Mg的核外电子数相同,核外排布相同,化学性质相同,故D错误;
故选:B。
❑
18Mg与❑ 24Mg都是镁元素的同位素,其质子数相同,核外电子数相同,中子数和质量数不同,
据此分析作答。
第 页 共 页
11 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
本题主要考查原子的构成,质子数、中子数、质量数、核外电子数、核电荷数之间的关系,属于
基本知识的考查,难度不大,
6.【答案】C
【解析】解:FeSO 、CuSO 、Al (SO ) 的混合溶液中通入适量H S,硫酸亚铁、硫酸铝和
4 4 2 4 3 2
硫化氢不反应,硫酸铜和硫化氢反应生成硫化铜沉淀难溶于水和酸,发生反应的离子方程式为
H S+Cu2+=CuS↓+2H+ ,
2
故选:C。
在FeSO 、CuSO 、Al (SO ) 的混合溶液中通入适量H S,硫酸亚铁、硫酸铝和硫化氢不反
4 4 2 4 3 2
应,硫酸铜和硫化氢反应生成硫化铜沉淀难溶于水和酸,以此解答该题。
本题考查了硫的化合物的性质,为高频考点,掌握物质之间的反应是解题关键,注意硫化铜难溶
于水和酸,题目难度不大。
7.【答案】A
【解析】解:A.合成氨的反应条件是高温、高压、催化剂作用下,氮气和氢气反应生成氨气,
接触法制硫酸中的各步反应,不需要高压条件,故A错误;
B.分析可知,工业合成氨和工业制备硫酸的过程中都需要高温条件,故B正确;
C.工业合成氨的反应为可逆反应,平衡混合气体分离出氨气后可以循环使用,工业制备硫酸的过
程中,二氧化硫催化氧化反应为可逆反应,平衡气体分理处三氧化硫后可以循环使用,故C正确;
D.合成氨需要铁触媒做催化剂,二氧化硫的催化氧化需要五氧化二钒做催化剂,均使用合适催化
剂,故D正确;
故选:A。
合成氨反应的条件是高温高压催化剂作用下,氮气和氢气反应生成氨气,
,反应为可逆反应,接触法制硫酸是铁矿石在高温条件下和氧气反应生
催化剂
成氧化铁和二氧化硫,二氧化硫在常压下加热,催化氧化生成三氧化硫,2SO +O 2SO ,
2 2 3
反应为可逆反应,三氧化硫溶于水生成硫酸。
第 页 共 页
12 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
本题考查了工业合成氨、工业制硫酸的工艺流程,主要是原理的理解应用,题目难度不大。
8.【答案】C
【解析】解:A.当氧气过量时,NO能完全转化为NO ,不会有NO剩余,不符合题干要求,故
2
A错误;
B.氨水过量时,能将铝离子完全沉淀为氢氧化铝,不会有铝离子剩余,不符合题干要求,故B错
误;
C.常温下,铁在浓硝酸中会钝化,铁的反应程度很小,即浓硝酸过量,铁也不会完全反应,符合
题干要求,故C正确;
D.向澄清石灰水中通入二氧化碳直至过量,先生成碳酸钙沉淀,后沉淀溶解生成碳酸氢钙,即当
二氧化碳过量时,不会有氢氧化钙剩余,不符合题干要求,故D错误;
故选:C。
A.当氧气过量时,NO能完全转化为NO ;
2
B.氨水过量时,能将铝离子完全沉淀为氢氧化铝;
C.常温下,铁在浓硝酸中会钝化;
D.向澄清石灰水中通入二氧化碳直至过量,先生成碳酸钙沉淀,后沉淀溶解。
本题考查物质的性质,题目难度不大,注意化学反应中的一些特殊情况,注意反应的可逆性和物
质的浓度对反应进行程度的影响。
9.【答案】D
【解析】解:A.海水中溴离子的浓度太小,通过海水浓缩后,再加入氧化剂氧化,海带提碘,
不需要浓缩,是干海带在坩埚中灼烧、浸取得到含碘离子的溶液,故A错误;
B.溴单质易挥发,生成的溴单质采用热空气吹出,生成的碘单质是利用萃取剂萃取分液后,蒸馏
得到,不能用热空气吹出,故B错误;
C.溴离子被氧化为溴单质,通过吸收、再氧化富集得到溴单质,利用溴单质易挥发分离,不需要
四氯化碳萃取,碘离子被氧化生成碘单质,用四氯化碳萃取出I ,故C错误;
2
D.氯气氧化性大于碘单质、溴单质,氧化碘离子、溴离子的氧化剂可选择氯水,故D正确;
故选:D。
海水提溴的原理是:浓缩的海水中通入氯气氧化溴离子生成溴,Cl +2Br−=Br +2Cl− ,热空
2 2
第 页 共 页
13 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
气吹出溴,用试剂吸收,如用二氧化硫吸收,二氧化硫与溴发生氧化还原反应生成HBr和硫酸,
再通入氯气与HBr反应生成溴,富集溴元素,利用溴单质易挥发,蒸馏分离出液溴;海带提碘的
原理是:干海带灼烧后,浸取、过滤分离出浸取液含I−,加氧化剂氯气或过氧化氢溶液发生氧化
还原反应,Cl +2I−=I +2Cl− 或2I−+2H++H O =I +2H O,用四氯化碳萃取出I ,分液
2 2 2 2 2 2 2
分离出碘的四氯化碳溶液,分离得到碘单质。
本题考查海水资源的应用,为高频考点,把握物质的性质、发生的反应、混合物的分离提纯为解
答的关键,侧重分析与应用能力的考查,注意元素化合物知识的应用,题目难度不大。
10.【答案】C
【解析】解:A.Na和水反应生成NaOH,NaOH和二氧化碳反应生成碳酸钠,碳酸钠和稀盐
酸反应生成NaCl,所以物质之间能一步转化,故A不选;
B.Fe在氯气中燃烧生成氯化铁,氯化铁和NaOH反应生成氢氧化铁,氢氧化铁受热分解生成氧
化铁,所以物质之间能一步转化,故B不选;
C.氧化铝和水不反应,所以氧化铝不能一步转化为氢氧化铝,故C选;
D.Mg和盐酸反应生成氯化镁,氯化镁和NaOH反应生成氢氧化镁,氢氧化镁和稀硫酸反应生成
硫酸镁,所以物质之间能一步转化,故D不选;
故选:C。
A.Na和水反应生成NaOH,NaOH和二氧化碳反应生成碳酸钠,碳酸钠和稀盐酸反应生成
NaCl;
B.Fe在氯气中燃烧生成氯化铁,氯化铁和NaOH反应生成氢氧化铁,氢氧化铁受热分解生成氧
化铁;
C.氧化铝和水不反应;
D.Mg和盐酸反应生成氯化镁,氯化镁和NaOH反应生成氢氧化镁,氢氧化镁和稀硫酸反应生成
硫酸镁。
本题考查物质之间转化,侧重考查基础知识的掌握和灵活应用,明确元素化合物性质及物质之间
转化关系是解本题关键,熟练掌握常见元素化合物性质,题目难度不大。
11.【答案】D
第 页 共 页
14 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
【解析】解:A.亚铁离子的还原性大于溴离子,若氯气少量,亚铁离子优先被氧化,若氯气足
量,亚铁离子和溴离子都被氧化,所以氯气的用量不同,反应产物不同,相应的离子方程式不同,
故A错误;
B.Ba(OH) 与NaHSO 溶液反应,当NaHSO 足量时可以发生
2 4 4
2H++SO2−+Ba2++2OH−=BaSO ↓+2H O,当Ba(OH) 足量时可能发生
4 4 2 2
H++SO2−+Ba2++OH−=BaSO ↓+H O,与反应物的量有关,故B错误;
4 4 2
C.Na CO 溶液与稀盐酸反应,盐酸量少,反应生成碳酸氢钠,离子反应为
2 3
CO2−+H+=HCO−
,而盐酸量多时,反应生成二氧化碳和水,离子反应为
3 3
CO2−+2H+=H O+CO ↑,不能用同一个离子方程式来表示,故C错误;
3 2 2
D.Ca(HCO ) 与Ca(OH) 反应,无论两者的比例如何均能用同一个离子方程式
3 2 2
HCO−+OH−+Ca2+=H O+CaCO ↓来表示,故D正确。
3 2 3
故选:D。
在溶液中的反应,若反应产物与反应物的量无关时,只发生一个化学反应,反应物相同,生成物
也相同,则能用同一离子方程式表示,若反应产物与反应物的量有关时,不能用同一个离子方程
式表示,以此来解答。
本题考查离子方程式的书写,为高考常见题型,侧重于与量有关的离子的方程式的书写和判断,
注意把握物质的性质,为解答该题的关键,难度不大。
12.【答案】A
【解析】解:A.氯化铵溶解度随温度升高增大,不利于N H Cl更多地析出,故A错误;
4
B.加入食盐,增大Cl−的浓度,有利于N H Cl更多地析出,故B正确;
4
C.氨气溶于水后生成氨水,氨水电离成铵根,增大铵根的浓度有利于氯化铵的析出来,故C正确;
第 页 共 页
15 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
D.通入氨气使溶液碱性增强,使碳酸氢钠转化为溶解度较大的碳酸钠,可以提高氯化铵的纯度,
故D正确;
故选:A。
A.氯化铵溶解度随温度升高增大;
B.增大氯离子浓度有利于氯化铵晶体析出;
C.向母液中通氨气,溶液中的铵根离子浓度增大有利于氯化铵晶体析出;
D.向母液中通氨气,溶液中的铵根离子浓度增大有利于氯化铵晶体析出,可以是碳酸氢钠转化为
溶解度更大的碳酸钠,提高氯化铵的纯度。
本题以侯氏制碱工业为载体考查物质的制备,明确侯氏制碱法原理,明确物质分离提纯方法是解
本题关键,侧重考查学生分析判断能力,注意离子浓度和温度对物质溶解性的影响判断,题目难
度中等。
13.【答案】A
【解析】解:A.装置甲是“固+液”常温型装置,可以用装置甲制备氨气,故A正确;
B.浓硫酸与氨气反应,则不能利用浓硫酸干燥氨气,故B错误;
C.应用双孔塞,收集气体不能密闭,故C错误;
D.氨气极易溶于水,吸收氨气防止发生倒吸,漏斗不能完全浸没在水中,不能防倒吸,故D错误;
故选:A。
A.装置甲是“固+液”常温型装置;
B.浓硫酸与氨气反应;
C.应用双孔塞;
D.氨气极易溶于水,吸收氨气防止发生倒吸。
本题考查化学实验方案的评价,为高频考点,把握实验装置图的作用、物质的性质为解答的关键,
侧重干燥、物质制备、除杂等实验操作和原理的考查,注意实验的操作性、评价性分析,题目难
度不大。
14.【答案】B
第 页 共 页
16 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
【解析】解:A.前者含有两个甲氧基、后者含有一个甲氧基,二者结构不相似,所以不互为同
系物,故A错误;
B.二者都含有酯基,所以都能和NaOH溶液反应,故B正确;
C.前者含有2个甲氧基、后者含有1个甲氧基,所以二者分子式不同,不互为同分异构体,故C
错误;
D.苯环和氢气以1:3发生加成反应,碳碳双键和氢气以1:1发生加成反应,酯基中碳氧双键和
氢气不反应,二者都含有1个苯环、2个碳碳双键,所以1mol均能与5mol氢气反应,故D错误;
故选:B。
A.结构相似,在分子组成上相差一个或n个CH 原子团的有机物互为同系物;
2
B.酯基能和NaOH溶液反应;
C.分子式相同、结构不同的有机物互为同分异构体;
D.苯环和氢气以1:3发生加成反应,碳碳双键和氢气以1:1发生加成反应,酯基中碳氧双键和
氢气不反应。
本题考查有机物的结构和性质,侧重考查分析、判断及知识综合运用能力,明确官能团及其性质
的关系、基本概念内涵是解本题关键,题目难度不大。
15.【答案】C
【解析】解:A.B中C、H、O原子个数依次是6、12、1,分子式为C H O,故A正确;
6 12
B.D被C多一个氧原子,则C发生氧化反应生成D,故B正确;
C.D发生开环反应生成PCL,该反应不是缩聚反应,故C错误;
D.D为 ,D、PCL中酯基都可在NaOH溶液中水解,得到的产物都是
HOCH CH CH CH CH COONa,所以得到的水解产物相同,故D正确;
2 2 2 2 2
故选:C。
A和氢气发生加成反应生成B,B发生氧化反应生成C,根据C的结构简式知,B为 ,C发
第 页 共 页
17 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
生氧化反应生成D,根据PCL的结构简式及D的分子式知,D为 ,D发生开环反应生成
PCL;
A.B中C、H、O原子个数依次是6、12、1;
B.C发生氧化反应生成D;
C.D发生开环反应生成PCL;
D.D为 ,D、PCL中酯基都可在NaOH溶液中水解,得到的产物都是
HOCH CH CH CH CH COONa。
2 2 2 2 2
本题考查有机物合成,侧重考查对比、分析、判断及知识综合运用能力,正确推断各物质的结构
简式是解本题关键,注意:D生成PCL的反应不是缩聚反应。
16.【答案】D
【解析】解:A.由上述分析可知,溶液中一定不含有Fe2+,故A错误;
B.由上述分析可知,溶液中至少含有Fe3+或Al3+中至少一种,可能含有Fe3+,故B错误;
C.由上述分析可知,溶液中一定含有NO−
,故C错误;
3
D.由上述分析可知,溶液中一定不含AlO−
,故D正确;
2
故选:D。
向该溶液中逐滴滴入NaOH溶液一定体积后才产生沉淀,即开始没有沉淀,说明溶液呈酸性,
溶液中一定含有大量的H+,AlO− 、CO2− 与H+不能共存,则溶液中不含有AlO− 、CO2−
,而
2 3 2 3
后才有沉淀生成,能够生成沉淀的是Fe3+、Fe2+或Al3+,即含有Fe3+、Fe2+或Al3+中的一种
或几种,根据溶液不显电性可知,溶液中一定含有NO− ,但Fe2+、H+、NO−
不能共存,则溶
3 3
液中一定不含有Fe2+,综上原溶液中一定含有H+、NO− 、Fe3+或Al3+中至少一种,一定不含
3
第 页 共 页
18 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
有Fe2+、AlO− 、CO2− ,可能含有Fe3+或Al3+的一种,据此分析解答。
2 3
本题考查常见离子的检验方法,掌握物质的性质、离子的检验方法和溶液不显电性原则是解题关
键,侧重考查学生的分析能力及逻辑推理能力,题目难度中等。
17.【答案】B
【解析】解:A、将表面发黑的银器浸入盛有食盐水的铝质容器中,形成原电池反应,能量变化
是化学能转化为电能,故A错误;
B、依据原电池原理分析,铝和硫化银在食盐水中形成原电池反应,铝做负极,银器做正极,硫
化银被还原为银,故B正确;
C、原电池反应中硫化银被还原为银单质,不是Ag S溶解于食盐水生成了AgCl,故C错误;
2
D、铝在原电池中做负极质量减轻,电极名称错误,故D错误;
故选B.
A、将表面发黑的银器浸入盛有食盐水的铝质容器中,形成原电池反应,能量变化是化学能转化
为电能;
B、依据原电池原理分析,铝和硫化银在食盐水中形成原电池反应,铝做负极,银器做正极,硫
化银被还原为银;
C、原电池反应中硫化银被还原为银单质;
D、铝在原电池中做负极质量减轻;
本题考查了原电池原理分析应用,电极反应,电极判断是解题关键,题目难度中等.
18.【答案】C
【解析】解:A.向N H Fe(SO ) 溶液中加入少量NaOH溶液,离子方程式为:
4 4 2
Fe3++3OH−=3Fe(OH) ↓,故A错误;
3
B.1L1mol⋅L−1FeBr 溶液与一定量氯气反应,转移电子数为6.02×1023,离子方程式为:
2
2Fe2++Cl =2Fe3++2Cl−
,故B错误;
2
C.将2.24L(标准状况)CO 通入500mL0.3mol⋅L−1NaOH溶液中,离子方程式为:
2
第 页 共 页
19 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
2CO +3OH−=CO2−+HCO−+H O,故C正确;
2 3 3 2
D.向Ca(ClO) 溶液中通入少量SO 发生氧化还原反应,其反应的离子方程式为:
2 2
Ca2++3ClO−+SO +H O=CaSO ↓+2HClO+Cl− ,故D错误;
2 2 4
故选:C。
A.氢氧化钠少量先与铁离子反应;
B.1L1mol⋅L−1FeBr 溶液与一定量氯气反应,转移电子数为6.02×1023时,只氧化亚铁离子;
2
C.二氧化碳与氢氧化钠物质的量之比为2:3反应生成碳酸钠、碳酸氢钠和水;
D.二氧化硫被氧化生成硫酸根离子。
本题考查离子反应,侧重考查学生离子方程式正误判断的掌握情况,试题难度中等。
19.【答案】D
【解析】解:A.碲位于第五周期ⅥA族,因此Cu Te中Te元素为−2价,Cu元素的化合价为+1
2
价,故A错误;
B.反应①中Te元素化合价升高被氧化,O元素化合价降低被还原,氧化剂为O ,氧化产物为
2
TeO ,氧化性O >TeO ,反应②中Te元素的化合价降低,S元素的化合价升高,则SO 为还原
2 2 2 2
剂,TeO 为氧化剂,氧化剂的氧化性大于还原剂,则有氧化性:TeO >SO ,则氧化性
2 2 2
O >TeO >SO ,故B错误;
2 2 2
C.反应②中Te元素的化合价降低,S元素的化合价升高,则氧化剂是TeO ,氧化产物是H SO ,
2 2 4
故C错误;
D.每制备1molTe反应②转移4mol电子,反应①转移8mol电子,因此每制备1molTe理论上共
转移12mol电子,故D正确;
故选:D。
A.碲位于第五周期ⅥA族,因此Cu Te中Te元素为−2价,Cu元素的化合价为+1价;
2
B.氧化剂的氧化性大于氧化产物;
C.反应②中Te元素的化合价降低,S元素的化合价升高,则氧化剂是TeO ,氧化产物是H SO ;
2 2 4
第 页 共 页
20 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
D.每制备1molTe反应②转移4mol电子,反应①转移8mol电子。
本题主要考查氧化还原反应的基本规律,为高频考点,题目难度不大。
20.【答案】C
【解析】解:A.a点溶液中的溶质是NaOH,水电离出的c(H+ )=10−pH=1×10−10mol⋅L−1,
故A正确;
B.常温下,c(OH− )=1×10−7mol/L,溶液呈中性,则c(OH− )=c(H+ ),所以
c(H+ )=1×10−7mol⋅L−1,故B正确;
C.c点溶液中,当水电离出的OH−离子浓度最大时,说明此时的溶液是碳酸钠溶液,碳酸根离子
水解生成碳酸氢根离子但程度较小,所以离子浓度大小顺序是c(Na+ )>c(CO2− )>c(HCO−
),
3 3
故C错误;
D.d点溶液中,溶液呈中性,则c(OH− )=c(H+ ),溶液中存在电荷守恒,根据电荷守恒得
c(Na+ )=2c(CO2− )+c(HCO−
),故D正确;
3 3
故选C.
本题考查离子浓度大小比较,为高频考点,明确溶液中的溶质及其性质是解本题关键,结合电荷
守恒进行解答,注意计算碱性溶液中水电离出氢离子和氢氧根离子的方法.
21.【答案】球形干燥管 使F与G压强相同,便于浓盐酸顺利滴出 赶尽装置中空气,防止PCl
3
被氧化 吸收未反应的氯气,防止污染空气 水浴 受热均匀,便于控制加热温度 蒸馏 滴定管
和500mL容量瓶 55%
【解析】解:(1)仪器D的名称是球形干燥管,装置F与G由橡胶管a相连通,a的作用是使F与
G压强相同,便于浓盐酸顺利滴出,
故答案为:球形干燥管;使F与G压强相同,便于浓盐酸顺利滴出;
第 页 共 页
21 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
(2)实验时,检查装置气密性后,先打开K 通入CO ,再迅速加入红磷,通入CO 的作用是赶
1 2 2
尽装置中空气,防止PCl 被氧化,
3
故答案为:赶尽装置中空气,防止PCl 被氧化;
3
(3)装置D中盛有碱石灰,其作用一为干燥,吸水,作用二为吸收未反应的氯气,防止污染空气,
故答案为:吸收未反应的氯气,防止污染空气;
(4)装置C中的反应需要65~70℃,最适合的加热方式为水浴加热,该方法的优点是受热均匀,
便于控制加热温度,制得的PCl 粗产品中常含有POCl 、PCl 等,加入红磷加热除去PCl 后,
3 3 5 5
通过蒸馏,即可得到较纯净的PCl ,
3
故答案为:水浴;受热均匀,便于控制加热温度;蒸馏;
(5)第二步配成500mL溶液,需要的定量移取20.000gPCl 粗产品,其仪器名称为滴定管和
3
500mL容量瓶,反应的关系式为I ~2Na S O ,PCl ~H PO ~I ,该产品中PCl 的质
2 2 2 3 3 3 3 2 3
量分数
1
(0.5×20×10−3−1×12×10−3× )×20×137.5
三氯化磷的质量 2 ,
= ×100%= ×100%=55%
样品的质量 20
故答案为:滴定管和500mL容量瓶;55%。
(1)仪器D的名称是球形干燥管,橡胶管a使F与G压强相同,便于浓盐酸顺利滴出;
(2)实验时,检查装置气密性后,先打开K 通入CO ,赶尽装置中空气,防止PCl 被氧化;
1 2 3
(3)碱石灰可以吸收未反应的氯气;
(4)装置C中的反应需要65~70℃,所得混合物互溶,且沸点相差较大不同,通过蒸馏分离;
(5)第二步配成500mL溶液,需要的定量移取20.000gPCl 粗产品,其仪器名称为滴定管和
3
500mL容量瓶,反应的关系式为I ~2Na S O ,PCl ~H PO ~I ,该产品中PCl 的质
2 2 2 3 3 3 3 2 3
三氯化磷的质量
量分数= ×100%。
样品的质量
本题考查制备实验方案的设计,侧重考查学生仪器、装置和产品纯度计算的掌握情况,试题难度
中等。
第 页 共 页
22 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
22.【答案】2:1 c c(O ) > 0.0067mol⋅L−1 ⋅s−1 < pH升高,HO− 的浓度
2 2
增加,H O 分解速率加快 H O 浓度越高,电离程度越低,分解率越小 该法生产原子利用率
2 2 2 2
是100%,符合“绿色化学工艺”
【解析】解:(1)O元素核外电子数为8,根据能量最低原理,核外最外层电子排布式为2s22p4,
成单电子为2,成对电子为4,氧原子最外层成对电子和未成对电子数目之比为4:2=2:1,
故答案为:2:1;
(2)过氧化氢为共价化合物,分子中氧原子之间形成一对共用电子对,电子式为: ,
要确定H O 分子结构,需要测定H O 分子中的键角判断分子结构,故选c,
2 2 2 2
故答案为: ;c;
(3)2H O (l)⇌2H O(l)+O (g)+Q(Q>0),H O 分解反应的平衡常数表达式K=c(O ),
2 2 2 2 2 2 2
反应为放热反应,升高温度,平衡逆向进行,不同温度下H O 分解反应的平衡常数
2 2
K(25℃)>K(40℃),标准状况下,某5mLH O 溶液60s内产生氧气22.4mL(溶液体积变
2 2
22.4L
化忽略不计),n(O )= =0.1mol,反应的n(H O )=0.2mol,则0~60s,
2 22.4L/mol 2 2
0.2mol
5L ,
v(H O )= ≈0.0067mol⋅L−1 ⋅s−1
2 2 60s
故答案为:c(O );>;0.0067mol⋅L−1 ⋅s−1;
2
(4)H O (aq)⇌H+ (aq)+HO− (aq)K(25℃)=2.24×10−12 ,过氧化氢为二元弱酸,H O
2 2 2 2
为中性,则25℃,pH(H O )0),平衡常数
2 2 2 2
生成物平衡浓度幂次方乘积
K= ,纯液体和固体不写入表达式,反应为放热反应,升温平衡
反应物平衡浓度幂次方乘积
正向进行,一定浓度的H O ,pH增大H O 分解率增加;
2 2 2 2
(4)H O (aq)⇌H+ (aq)+HO− (aq)K(25℃)=2.24×10−12 ,过氧化氢为二元弱酸,显弱
2 2 2
酸性,一定浓度的H O ,pH增大HO− 的浓度增加,H O 分解率增大,相同pH下,H O 浓
2 2 2 2 2 2 2
度越大,H O 的电离程度越小,分解率越低;
2 2
(5)绿色化学是指原子利用率100%,无污染、从源头上杜绝污染。
本题考查了原子结构、反应速率计算、平衡影响因素的理解应用、弱电解质电离平衡等知识点,
第 页 共 页
24 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
注意知识的熟练掌握,题目难度不大。
23.【答案】6Zn+As O +12HCl=6ZnCl +2AsH ↑+3H O 2:1 SO
2 3 2 3 2 2
H AsO +OH−=H AsO−+H O > Na HAsO 溶液呈碱性,HAsO2− 水解程度大于其电
3 3 2 3 2 2 3 3
离程度 < 淀粉溶液 溶液的酸碱性影响物质的氧化还原性
【解析】解:(1)法庭医学常用马氏试砷法来证明是否砒霜(As O )中毒:把试样与锌和盐酸混
2 3
合,若试样中含有砒霜,则会反应生成砷化氢、氯化锌与水,该反应的化学方程式为
6Zn+As O +12HCl=6ZnCl +2AsH ↑+3H O,
2 3 2 3 2
故答案为:6Zn+As O +12HCl=6ZnCl +2AsH ↑+3H O;
2 3 2 3 2
(2)As S 和SnCl 在盐酸中反应转化为As S (其中As为+2价)和SnCl 并放出H S气体,该
2 3 2 4 4 4 2
反应中氧化产物是SnCl ,Sn元素由+2价升高到+4价,升高2价,还原产物是As S ,As元素
4 4 4
由+3价降低到+2价,得到1个As S ,化合价共降低1×4=4价,根据化合价升降守恒可得,氧
4 4
化产物与还原产物的物质的量之比为2:1,
故答案为:2:1;
(3)一定条件下,雄黄(As S )与O 生成As O 与物质a,若该反应中1molAs S 参加反应时,
4 4 2 2 3 4 4
转移28mol电子,即消耗7molO ,根据原子守恒和化合价升降守恒,可得反应的方程式为:
2
❑
As S +7O =2As O +4SO ,则物质a的化学式为SO ,
4 4 2 2 3 2 2
故答案为:SO ;
2
(4)由图可知,向亚砷酸溶液中缓缓加入NaOH溶液至pH=11时,反应的离子方程式为
H AsO +OH−=H AsO−+H O,Na HAsO 溶液中c(H AsO− )>c(AsO3− ),理由是
3 3 2 3 2 2 3 2 3 3
Na HAsO 溶液呈碱性,HAsO2− 水解程度大于其电离程度,
2 3 3
故答案为:H AsO +OH−=H AsO−+H O;>;Na HAsO 溶液呈碱性,HAsO2− 水解程
3 3 2 3 2 2 3 3
度大于其电离程度;
第 页 共 页
25 29上海最大家教平台 嘉惠家教 万余上海老师任您选(在职老师、机构老师、 学霸大学生应有尽有 ,
--- 2 985
+V: jiajiao6767 )
(5)已知:I +AsO3−+2OH− ⇌2I−+AsO3−+H O,为验证该反应具有可逆性,将等物质的
2 3 4 2
量浓度的碘水与Na AsO 溶液按体积比为V :V 的比例混合(另加入适量的碱),当V