文档内容
虹口区 2022 学年第二学期初三质量调研
(2023.05)
(满分50分,考试时间40分钟)
相对原子质量:H-1 C-12 O-16 Na-23
一、选择题(1~14每题只有1个正确选项,每题1分,共14分)
1.空气中含量最多的是( )
A.氧气 B.氮气 C.二氧化碳 D.水蒸气
【答案】B
【解答】解:空气的成分按体积计算,大约是:氮气78%、氧气21%、稀有气体0.94%、二氧化碳0.03%
、其它气体和杂质0.03%,故空气中含量最多的是氮气。
故选:B。
2.物质在氧气中燃烧发出蓝紫色火焰的是( )
A.氢气 B.木炭 C.硫 D.磷
【答案】C
【解答】解:A、氢气在氧气中燃烧,产生淡蓝色火焰,故选项错误。
B、木炭在氧气中燃烧,发出白光,故选项错误。
C、硫在氧气中燃烧,产生明亮的蓝紫色火焰,故选项正确。
D、磷在氧气中燃烧,产生大量的白烟,故选项错误。
故选:C。
3.与金刚石互为同素异形体的物质是( )
A.活性炭 B.碳﹣60 C.一氧化碳 D.碳酸钙
【答案】B
【解答】解:A、活性炭的主要成分是碳,属于混合物,与金刚石不属于同素异形体,故选项错误。
B、碳﹣60是碳元素形成的单质,与金刚石属于同素异形体,故选项正确。
C、一氧化碳为化合物,与金刚石不属于同素异形体,故选项错误。
D、碳酸钙为化合物,与金刚石不属于同素异形体,故选项错误。
故选:B。
4.放入水中能形成溶液的是( )
A.氧化铜 B.大理石 C.氢氧化铁 D.硝酸银
【答案】D
【解答】解:A、氧化铜不溶于水,与水混合形成不均一、不稳定的悬浊液,故A错;
B、大理石不溶于水,与水混合形成不均一、不稳定的悬浊液,故B错;
C、氢氧化铁不溶于水,与水混合形成不均一、不稳定的悬浊液,故C错;
D、硝酸银易溶于水,形成均一、稳定的混合物,属于溶液,故D正确。
第 2 页 共 5 页
学学科科网网((北北京京))股股份份有有限限公公司司故选:D。
5.属于纯净物的是( )
A.奶茶 B.蒸馏水 C.米醋 D.汽水
【答案】B
【解答】解:A、奶茶中含有茶碱、蛋白质等多种物质,属于混合物,故A错;
B、蒸馏水是由一种物质组成,属于纯净物,故B正确;
C、米醋中含有乙酸、水等多种物质,属于混合物,故C错;
D、汽水中含有碳酸、水等物质,属于混合物,故D错。
故选:B。
6.属于有机物的是( )
A.木炭 B.二氧化碳 C.碳酸 D.葡萄糖
【答案】D
【解答】解:A、木炭含有碳元素,但木炭不是化合物,不属于有机物,故A错误;
B、二氧化碳的组成和性质与无机物相似,二氧化碳属于无机物,故B错误;
C、碳酸的组成和性质与无机物相似,碳酸属于无机物,故C错误;
D、葡萄糖是含有碳元素的化合物,且不含碳酸根,属于有机物,故D正确;
故选:D。
7.能引起酸雨的物质是( )
A.二氧化硫 B.氮气 C.二氧化碳 D.氢气
【答案】A
【解答】解:二氧化硫、氮氧化物是导致酸雨的主要物质,酸雨的形成与氮气、二氧化碳、氢气无关。
故选:A。
8.NH Cl中,N元素的化合价是( )
4
A.﹣3 B.+3 C.+5 D.﹣5
【答案】A
【解答】解:在化合物中,氢元素显+1价,氯元素显﹣1价,设氮元素的化合价是x,根据在化合物中
正负化合价代数和为零,可得:x+(+1)×4+(﹣1)=0,则x=﹣3。
故选:A。
9.属于钾肥的是( )
A.K CO B.Ca(H PO ) C.NaNO D.CO(NH )
2 3 2 4 2 3 2 2
【答案】A
【解答】解:A、K CO 中只含有营养元素中钾元素,属于钾肥,故正确;
2 3
B、Ca(H PO ) 中只含有营养元素中的磷元素,属于磷肥,故错误;
2 4 2
C、NaNO 中只含有营养元素中的氮元素,属于氮肥,故错误;
3
D、CO(NH ) 中只含有营养元素中的氮元素,属于氮肥,故错误;
2 2
第 2 页 共 5 页
学学科科网网((北北京京))股股份份有有限限公公司司故选:A。
10.属于复分解反应的是( )
A.4P+5O 2P O
2 2 5
B.CO +4H CH +2H O
2 2 4 2
C.Ca(OH) +2HCl═CaCl +2H O
2 2 2
D.H +CuO Cu+H O
2 2
【答案】C
【解答】解:A.4P+5O 2P O ,反应物有两种,生成物有一种,符合多变一的特点,为化合反应
2 2 5
,故错误;
B.CO +4H CH +2H O,反应物有两种,生成物有两种,为氧化还原反应,不符合化学反应基
2 2 4 2
本类型,故错误;
C.Ca(OH)+2HCl═CaCl +2H O,两种化合物相互交换成分,生成两种新的化合物,属于复分解反应
2 2 2
,故正确;
D.H +CuO Cu+H O,单质与化合物起反应生成新的单质和新的化合物,属于置换反应,故错误;
2 2
故选:C。
11.自来水生产过程中,属于化学变化的是( )
A.沉降 B.过滤 C.吸附 D.杀菌消毒
【答案】D
【解答】解:A、沉降过程中没有新物质生成,属于物理变化,故错误。
B、过滤过程中没有新物质生成,属于物理变化,故错误。
C、吸附过程中没有新物质生成,属于物理变化,故错误。
D、杀菌消毒过程中有新物质生成,属于化学变化,故正确。
故选:D。
12.关于H O和H O 的比较,正确的是( )
2 2 2
A.一定条件下都可以反应生成O
2
B.两种物质中氢元素的质量分数相等
C.构成两种物质的微粒中都含有氢分子
D.等质量的两种物质含有的分子数相同
【答案】A
【解答】解:A.电解水H O生成氢气和氧气,H O 在二氧化锰催化作用下分解产生水和氧气,故正确;
2 2 2
B.水的相对分子质量为18,氢元素质量分数为 ×100%≈11%;过氧化氢的相对分子质量为34,氢元
第 2 页 共 5 页
学学科科网网((北北京京))股股份份有有限限公公司司素的质量分数为 ×100%≈5.9%,所以两种物质中氢元素的质量分数不相等,故错误;
C.H O是由水分子构成的,H O 是由过氧化氢分子构成的,构成两种物质的微粒中不含氢分子,故错误
2 2 2
;
D.水的相对分子质量为18,过氧化氢的相对分子质量为34,因此等质量的两种物质含有的分子数不相同
,故错误;
故选:A。
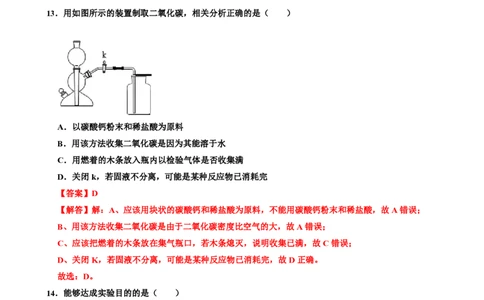
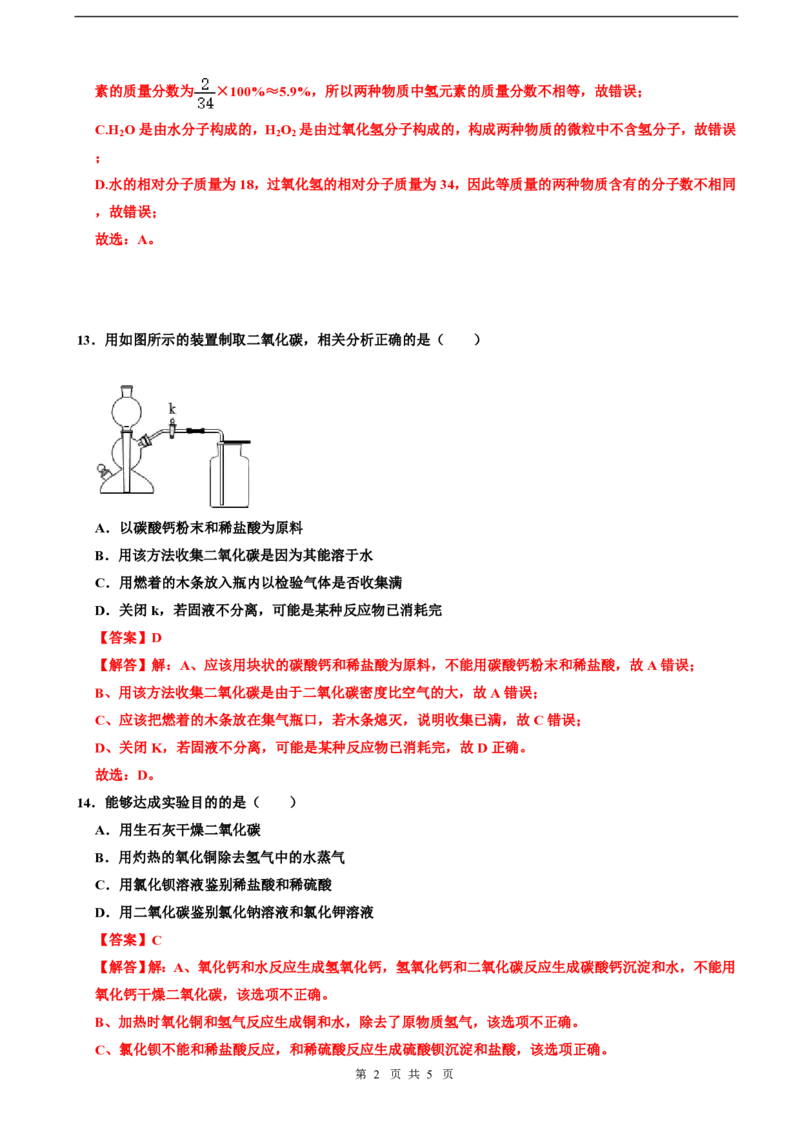
13.用如图所示的装置制取二氧化碳,相关分析正确的是( )
A.以碳酸钙粉末和稀盐酸为原料
B.用该方法收集二氧化碳是因为其能溶于水
C.用燃着的木条放入瓶内以检验气体是否收集满
D.关闭k,若固液不分离,可能是某种反应物已消耗完
【答案】D
【解答】解:A、应该用块状的碳酸钙和稀盐酸为原料,不能用碳酸钙粉末和稀盐酸,故A错误;
B、用该方法收集二氧化碳是由于二氧化碳密度比空气的大,故A错误;
C、应该把燃着的木条放在集气瓶口,若木条熄灭,说明收集已满,故C错误;
D、关闭K,若固液不分离,可能是某种反应物已消耗完,故D正确。
故选:D。
14.能够达成实验目的的是( )
A.用生石灰干燥二氧化碳
B.用灼热的氧化铜除去氢气中的水蒸气
C.用氯化钡溶液鉴别稀盐酸和稀硫酸
D.用二氧化碳鉴别氯化钠溶液和氯化钾溶液
【答案】C
【解答】解:A、氧化钙和水反应生成氢氧化钙,氢氧化钙和二氧化碳反应生成碳酸钙沉淀和水,不能用
氧化钙干燥二氧化碳,该选项不正确。
B、加热时氧化铜和氢气反应生成铜和水,除去了原物质氢气,该选项不正确。
C、氯化钡不能和稀盐酸反应,和稀硫酸反应生成硫酸钡沉淀和盐酸,该选项正确。
第 2 页 共 5 页
学学科科网网((北北京京))股股份份有有限限公公司司D、二氧化碳不能和氯化钠、氯化钾反应,不能鉴别两种物质,该选项不正确。
故选:C。
15~17每题均有1~2个正确选项(选对1个得1分,多选或错选得0分)
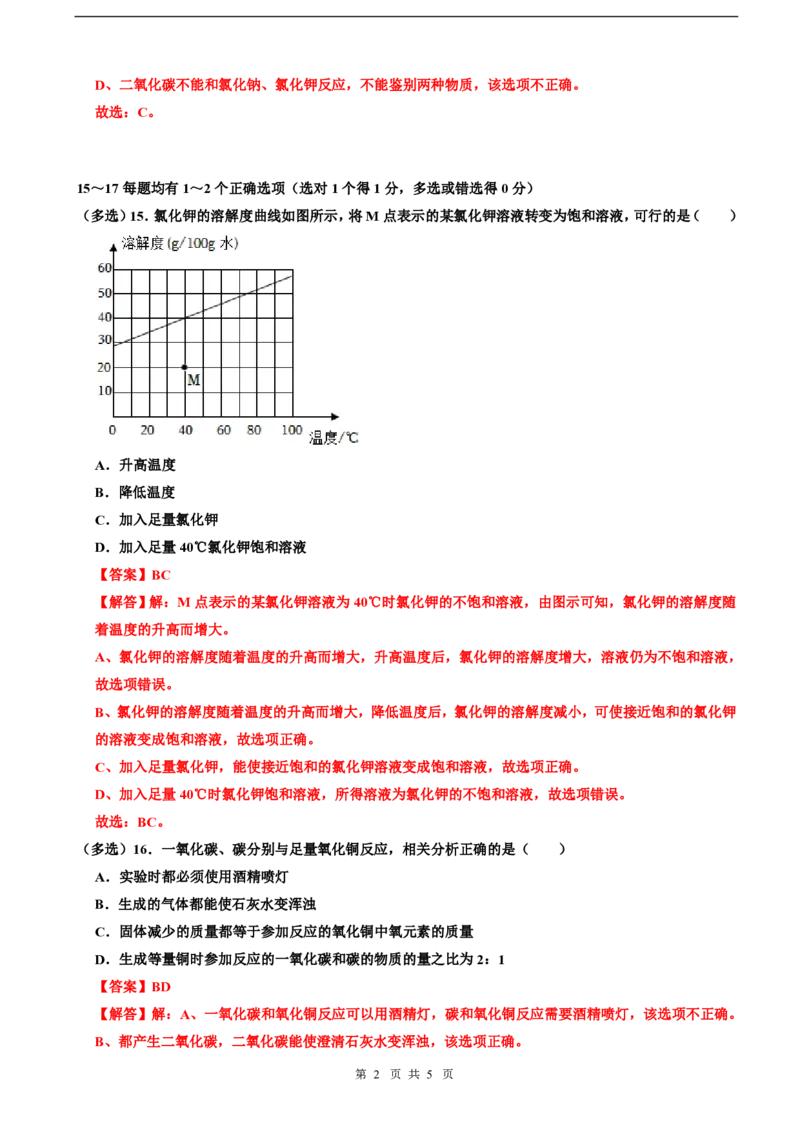
(多选)15.氯化钾的溶解度曲线如图所示,将M点表示的某氯化钾溶液转变为饱和溶液,可行的是( )
A.升高温度
B.降低温度
C.加入足量氯化钾
D.加入足量40℃氯化钾饱和溶液
【答案】BC
【解答】解:M点表示的某氯化钾溶液为40℃时氯化钾的不饱和溶液,由图示可知,氯化钾的溶解度随
着温度的升高而增大。
A、氯化钾的溶解度随着温度的升高而增大,升高温度后,氯化钾的溶解度增大,溶液仍为不饱和溶液,
故选项错误。
B、氯化钾的溶解度随着温度的升高而增大,降低温度后,氯化钾的溶解度减小,可使接近饱和的氯化钾
的溶液变成饱和溶液,故选项正确。
C、加入足量氯化钾,能使接近饱和的氯化钾溶液变成饱和溶液,故选项正确。
D、加入足量40℃时氯化钾饱和溶液,所得溶液为氯化钾的不饱和溶液,故选项错误。
故选:BC。
(多选)16.一氧化碳、碳分别与足量氧化铜反应,相关分析正确的是( )
A.实验时都必须使用酒精喷灯
B.生成的气体都能使石灰水变浑浊
C.固体减少的质量都等于参加反应的氧化铜中氧元素的质量
D.生成等量铜时参加反应的一氧化碳和碳的物质的量之比为2:1
【答案】BD
【解答】解:A、一氧化碳和氧化铜反应可以用酒精灯,碳和氧化铜反应需要酒精喷灯,该选项不正确。
B、都产生二氧化碳,二氧化碳能使澄清石灰水变浑浊,该选项正确。
第 2 页 共 5 页
学学科科网网((北北京京))股股份份有有限限公公司司C、一氧化碳和氧化铜反应时,固体减少的质量等于参加反应的氧化铜中氧元素的质量,碳和氧化铜反应
时,固体减少的质量等于参加反应的氧化铜中氧元素的质量和反应的碳的质量和,该选项不正确。
D、反应的化学方程式是CuO+CO Cu+CO 、2CuO+C 2Cu+CO ↑,生成等量铜时参加
2 2
反应的一氧化碳和碳的物质的量之比为2:1,该选项正确。
故选:BD。
(多选)17.氯酸钾受热分解的实验中,反应物、生成物的质量与时间的变化关系如图所示,相关分析正确
的是( )
A.t 时反应开始,t 时反应停止
1 2
B.最终生成氧气的质量为(a﹣d)g
C.反应后,剩余固体的质量是(b+d)g
D.反应前后固体中只有钾元素的质量不变
【答案】AC
【解答】解:氯酸钾受热分解的反应是氯酸钾在二氧化锰的催化作用和加热的条件下生成氯化钾和氧气,
A、由图可知,t 时质量开始开始变化,t 时质量变化停止,则t 时反应开始,t 时反应停止,故选项说
1 2 1 2
法正确。
B、由反应的化学方程式2KClO 2KCl+3O ↑可知,每245份质量的氯酸钾完全分解,生成149份
3 2
质量的氯化钾和96份质量的氧气,二氧化锰是催化剂,反应前后质量不变,则a是氯酸钾、二氧化锰混
合物的质量,b是生成氯化钾的质量,c是生成氧气的质量,d是二氧化锰的质量,所以最终生成氧气的
质量为cg,故选项说法错误。
C、由B的分析可知,b是生成氯化钾的质量,d是二氧化锰的质量,则反应后,剩余固体的质量是(b+d
)g,故选项说法正确。
D、由反应的化学方程式2KClO 2KCl+3O ↑可知,反应前后固体中钾元素、氯元素、锰元素的质
3 2
量都不变,故选项说法错误。
故选:AC。
三、简答题(共30分)请根据要求在答题纸相应的位置作答。
18.化学可以帮助我们分析并解决生活中的一些问题。
①75%的酒精溶液可用于杀菌消毒。
第 2 页 共 5 页
学学科科网网((北北京京))股股份份有有限限公公司司I 酒精的化学式是 C2H6O,由______种元素组成, 1mol C2H6O 中约含有_________个碳原子;
II 将少量酒精溶液样品,滴入盛有白色硫酸铜粉末的试管中,证明溶液中含有水的现象是_______________。
②早在 2006 年国家已发布相关规定, 要求用稀有气体代替氢气作为气球的填充物。
氦气的化学式是__________;氢气在空气中燃烧的化学方程式是_____________________;氦气可以替代
氢气的原因是__________________________________。
③食盐、蔗糖是厨房中常见的物质。
I 取少量食盐, 进行焰色反应, 火焰呈_______色;
II 室温时,将等质量的食盐和蔗糖分别加入 10mL 水中,充分混合,蔗糖全部溶解、部分食盐固体未溶解, 则
室温时两种物质中溶解度较大的是__________。
第 2 页 共 5 页
学学科科网网((北北京京))股股份份有有限限公公司司上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸
大学生应有尽有 ,+V: jiajiao6767 )
【答案】①Ⅰ、3,1.206×1024;
Ⅱ、白色硫酸铜粉末变成蓝色;
②He;2H +O 2H O;氦气的化学性质稳定;
2 2 2
③Ⅰ、黄;
Ⅱ、蔗糖。
【解答】解:①Ⅰ、酒精的化学式是C H O,由3种元素组成,1molC H O中约含有
2 6 2 6
的原子个数为:2×6.02×1023=1.206×1024个;
Ⅱ、将少量酒精溶液样品,滴入盛有白色硫酸铜粉末的试管中,证明溶液中含有水的现
象是:白色硫酸铜粉末变成蓝色;
②氦气的化学式是He;氢气和氧气在点燃的条件下生成水,化学方程式是:2H +O
2 2
2H O;氦气可以替代氢气的原因是:氦气的化学性质稳定;
2
③Ⅰ、取少量食盐,进行焰色反应,火焰呈黄色;
Ⅱ、室温时,将等质量的食盐和蔗糖分别加入10mL水中,充分混合,蔗糖全部溶解,
部分食盐固体未溶解,则室温时两种物质中溶解度较大的是蔗糖。
故答案为:①Ⅰ、3,1.206×1024;
Ⅱ、白色硫酸铜粉末变成蓝色;
②He;2H +O 2H O;氦气的化学性质稳定;
2 2 2
③Ⅰ、黄;
Ⅱ、蔗糖。
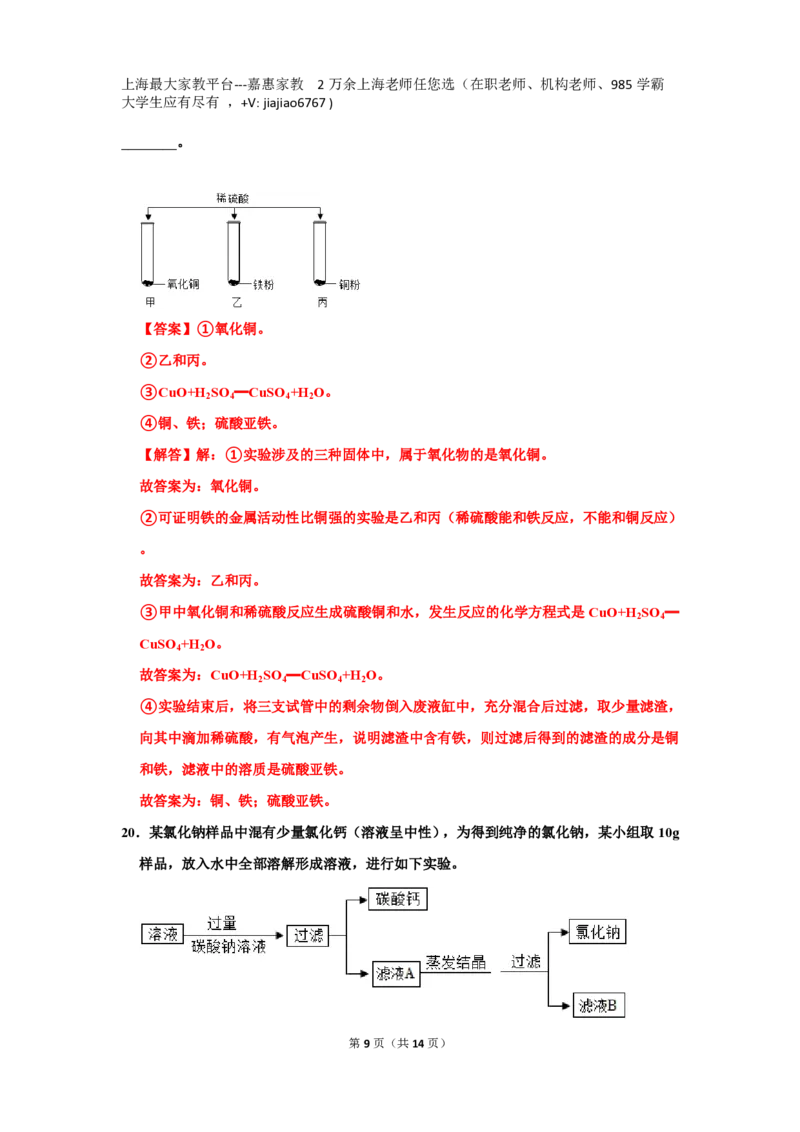
19 为研究稀硫酸的化学性质, 某小组如右图所示进行实验, 充分反应后, 只有试管甲中无固
体剩余。
①实验涉及的三种固体中,属于氧化物的是_________;
②可证明铁的金属活动性比铜强的实验是_______ (选填试管编号) 。
③甲中发生反应的化学方程式是____________________。
④实验结束后,将三支试管中的剩余物倒入废液缸中, 充分混
合后过滤,取少量滤渣,向其中滴加稀硫酸,有气泡产生。则
过滤后得到的滤渣的成分是 _________ ,滤液中的溶质是
第8页(共14页)上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸
大学生应有尽有 ,+V: jiajiao6767 )
________。
【答案】①氧化铜。
②乙和丙。
③CuO+H SO ═CuSO +H O。
2 4 4 2
④铜、铁;硫酸亚铁。
【解答】解:①实验涉及的三种固体中,属于氧化物的是氧化铜。
故答案为:氧化铜。
②可证明铁的金属活动性比铜强的实验是乙和丙(稀硫酸能和铁反应,不能和铜反应)
。
故答案为:乙和丙。
③甲中氧化铜和稀硫酸反应生成硫酸铜和水,发生反应的化学方程式是CuO+H SO ═
2 4
CuSO +H O。
4 2
故答案为:CuO+H SO ═CuSO +H O。
2 4 4 2
④实验结束后,将三支试管中的剩余物倒入废液缸中,充分混合后过滤,取少量滤渣,
向其中滴加稀硫酸,有气泡产生,说明滤渣中含有铁,则过滤后得到的滤渣的成分是铜
和铁,滤液中的溶质是硫酸亚铁。
故答案为:铜、铁;硫酸亚铁。
20.某氯化钠样品中混有少量氯化钙(溶液呈中性),为得到纯净的氯化钠,某小组取10g
样品,放入水中全部溶解形成溶液,进行如下实验。
第9页(共14页)上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸
大学生应有尽有 ,+V: jiajiao6767 )
①向碳酸钠溶液中滴加酚酞,溶液呈________色。
②上述过程中, 加入过量碳酸钠溶液的目的是_______________________。
③甲同学认为,上述过程中得到的氯化钠的质量等于10g 样品中氯化钠的质量,请分析说明该说
法的正误。
____________________________________________________________________________
④为得到尽可能多的氯化钠,对滤液 B 继续实验,后续操作是______________。
【答案】①红;
②除去氯化钙杂质;
③错误;上述流程中,发生了CaCl +Na CO =CaCO ↓+2NaCl反应,反应又产生了
2 2 3 3
氯化钠;
④向滤液B中加入过量的稀盐酸,直至不再产生气泡,对剩余液体蒸发结晶,过滤。
【解答】解:①碳酸钠溶液显碱性,向碳酸钠溶液中滴加酚酞,溶液呈红色;
②上述过程中,加入过量碳酸钠溶液的目的是除去氯化钙杂质;
③上述流程中,发生了CaCl +Na CO =CaCO ↓+2NaCl反应,反应又产生了氯化钠,
2 2 3 3
因此上述过程中得到的氯化钠的质量大于10g样品中氯化钠的质量,甲同学认为上述过
程中得到的氯化钠的质量等于10g样品中氯化钠的质量的说法是错误;
④为得到尽可能多的氯化钠,对滤液B继续实验,后续操作是向滤液B中加入过量的
稀盐酸,直至不再产生气泡,对剩余液体蒸发结晶,过滤可以得到氯化钠。
故答案为:
①红;
②除去氯化钙杂质;
③错误;上述流程中,发生了CaCl +Na CO =CaCO ↓+2NaCl反应,反应又产生了
2 2 3 3
氯化钠;
④向滤液B中加入过量的稀盐酸,直至不再产生气泡,对剩余液体蒸发结晶,过滤。
第10页(共14页)上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸
大学生应有尽有 ,+V: jiajiao6767 )
21.为探究氢氧化钠与盐酸反应的热量变化及溶液酸碱性的变化,某小组同学进行如下实
验。
【实验一】配制氢氧化钠溶液
氢氧化钠的部分溶解度如表所示。
温度(℃) 10 20 30 40 60
溶解度(g/100g 98 109 119 129 174
水)
①10℃时,氢氧化钠的溶解度是 g/100g水。
②20℃时,40g氢氧化钠与60g水混合,所得溶液是氢氧化钠的 (选填“饱和”或
“不饱和”)溶液;配制100g、4%的氢氧化钠溶液,需要水 g。
【实验二】探究氢氧化钠与盐酸的反应中,溶液酸碱性的变化。
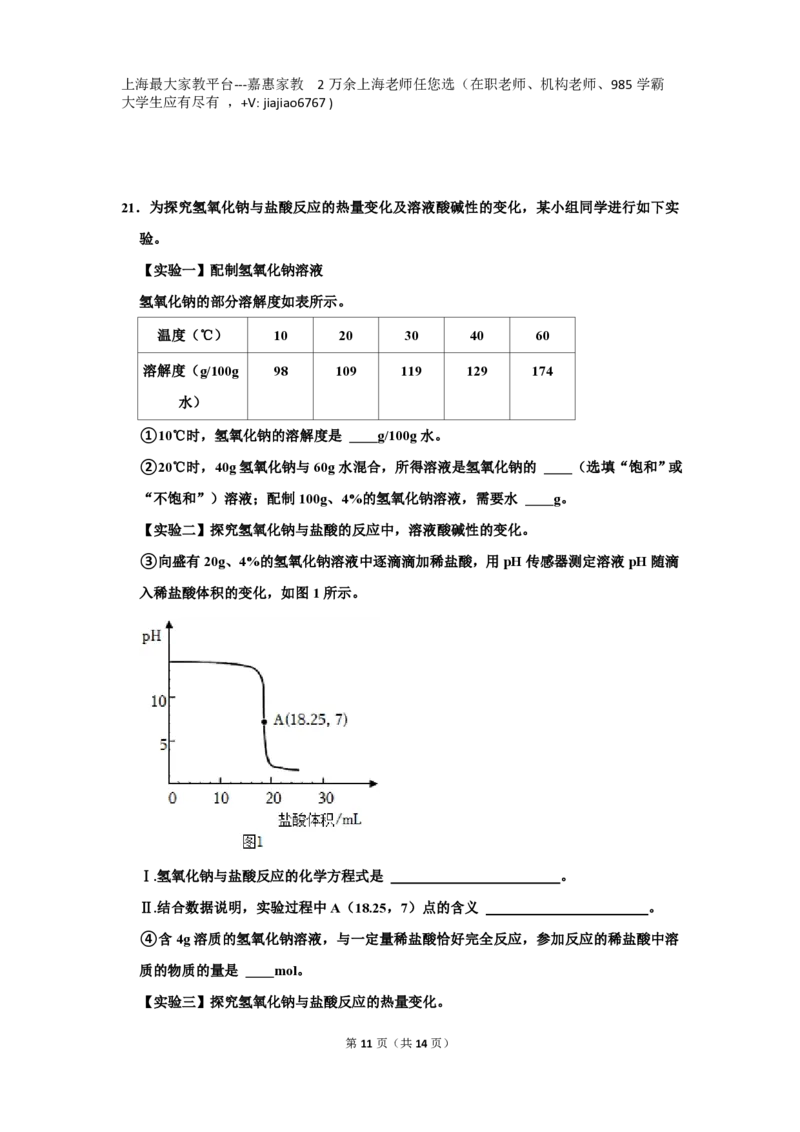
③向盛有20g、4%的氢氧化钠溶液中逐滴滴加稀盐酸,用pH传感器测定溶液pH随滴
入稀盐酸体积的变化,如图1所示。
Ⅰ.氢氧化钠与盐酸反应的化学方程式是 。
Ⅱ.结合数据说明,实验过程中A(18.25,7)点的含义 。
④含4g溶质的氢氧化钠溶液,与一定量稀盐酸恰好完全反应,参加反应的稀盐酸中溶
质的物质的量是 mol。
【实验三】探究氢氧化钠与盐酸反应的热量变化。
第11页(共14页)上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸
大学生应有尽有 ,+V: jiajiao6767 )
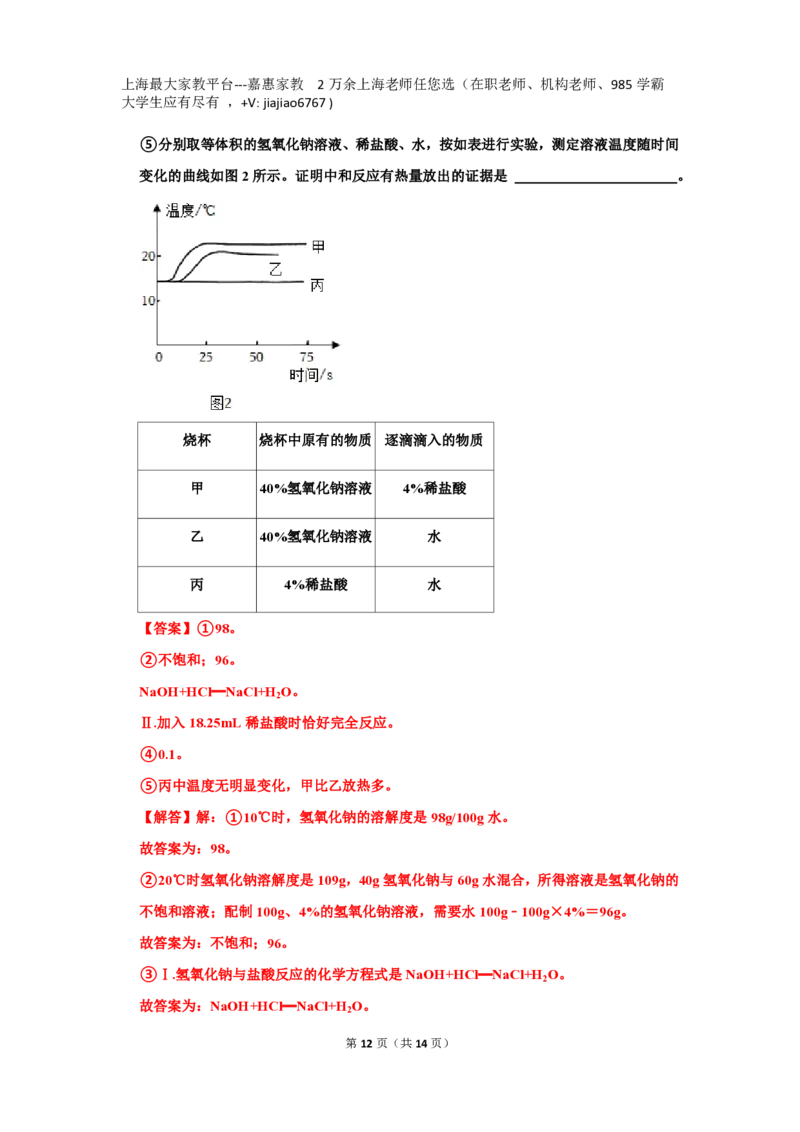
⑤分别取等体积的氢氧化钠溶液、稀盐酸、水,按如表进行实验,测定溶液温度随时间
变化的曲线如图2所示。证明中和反应有热量放出的证据是 。
烧杯 烧杯中原有的物质 逐滴滴入的物质
甲 40%氢氧化钠溶液 4%稀盐酸
乙 40%氢氧化钠溶液 水
丙 4%稀盐酸 水
【答案】①98。
②不饱和;96。
NaOH+HCl═NaCl+H O。
2
Ⅱ.加入18.25mL稀盐酸时恰好完全反应。
④0.1。
⑤丙中温度无明显变化,甲比乙放热多。
【解答】解:①10℃时,氢氧化钠的溶解度是98g/100g水。
故答案为:98。
②20℃时氢氧化钠溶解度是109g,40g氢氧化钠与60g水混合,所得溶液是氢氧化钠的
不饱和溶液;配制100g、4%的氢氧化钠溶液,需要水100g﹣100g×4%=96g。
故答案为:不饱和;96。
③Ⅰ.氢氧化钠与盐酸反应的化学方程式是NaOH+HCl═NaCl+H O。
2
故答案为:NaOH+HCl═NaCl+H O。
2
第12页(共14页)上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸
大学生应有尽有 ,+V: jiajiao6767 )
Ⅱ.实验过程中A(18.25,7)点的含义是加入18.25mL稀盐酸时恰好完全反应。
故答案为:加入18.25mL稀盐酸时恰好完全反应。
④含4g溶质的氢氧化钠溶液(氢氧化钠物质的量是0.1mol),与一定量稀盐酸恰好完
全反应,氢氧化钠和氯化氢物质的量之比是1:1,参加反应的稀盐酸中溶质的物质的量
是0.1mol。
故答案为:0.1。
⑤证明中和反应有热量放出的证据是丙中温度无明显变化,甲比乙放热多。
故答案为:丙中温度无明显变化,甲比乙放热多。
声明:试题解析著作权属所有,未经书面同意,不得复制发布日期:2023/5/16 14:35:06;
用户:天空之城;邮箱:2230668592@qq.com;学号:20667957
第13页(共14页)上海最大家教平台---嘉惠家教 2万余上海老师任您选(在职老师、机构老师、985学霸
大学生应有尽有 ,+V: jiajiao6767 )
第14页(共14页)