文档内容
2025 学年第一学期徐汇区学习能力诊断卷
初三化学试卷
注意:
1.考试时间90分钟,满分100分。
2.选择题未标注说明的,为单选,每题只能选一个选项;标注“不定项”的,每题应选一个
或多个选项;标注“多选”的,每题应选两个或两个以上的选项。
相对原子质量:H-1 C-12 N-14 O-16 S-32 Ca-40 Fe-56
一、化肥(8分)
氯化钾是一种常用的化肥。
1. 氯化钾属于
A. 氮肥 B. 磷肥 C. 钾肥 D. 复合肥
2. 氯化钾在土壤中会释放出钾离子( ),下列关于钾原子和钾离子的说法正确的是
A. 钾原子的质子数等于核外电子数 B. 钾离子属于负离子
C. 钾离子和钾原子的核外电子数相同 D. 钾离子和钾原子的质子数相同
3. 钼(读作mù)是植物必需的微量营养元素之一,为此科学家设计了钼肥。元素周期表提供的钼元素的
信息如下图所示。
42 Mo
钼
95.95
(1)钼的元素符号为________。
(2)钼的相对原子质量为________,钼原子中的质子数为________。
3.科学施用化肥才能提高施肥效果。
4. 土壤的酸碱度会影响施肥效果,土壤酸性过大,可使用________调节。
A. 氢氧化钠 B. 氢氧化钙 C. 氯化钠 D. 稀硫酸
5. 合理使用化肥要测算用量,若要提供氮元素28 g,需要 ________g。
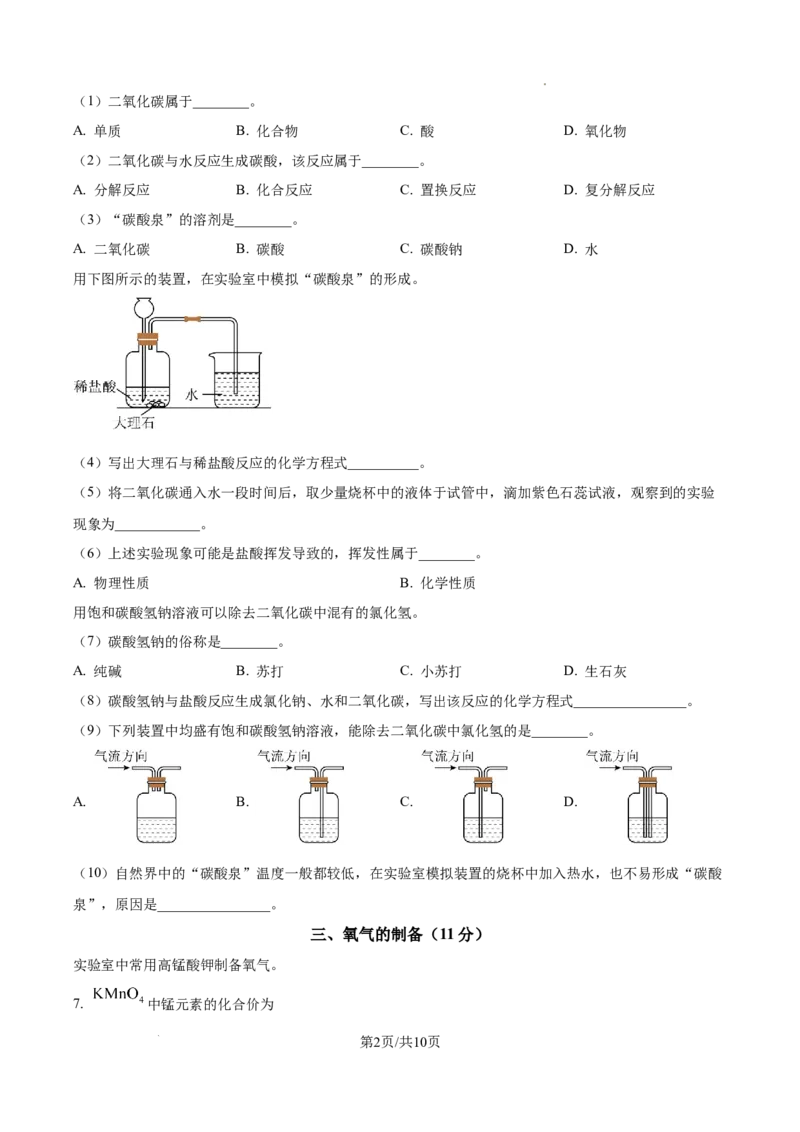
二、“碳酸泉”的形成(13分)
6. “碳酸泉”是由地壳中的二氧化碳溶于水形成的。
第1页/共10页
学科网(北京)股份有限公司(1)二氧化碳属于________。
A. 单质 B. 化合物 C. 酸 D. 氧化物
(2)二氧化碳与水反应生成碳酸,该反应属于________。
A. 分解反应 B. 化合反应 C. 置换反应 D. 复分解反应
(3)“碳酸泉”的溶剂是________。
A. 二氧化碳 B. 碳酸 C. 碳酸钠 D. 水
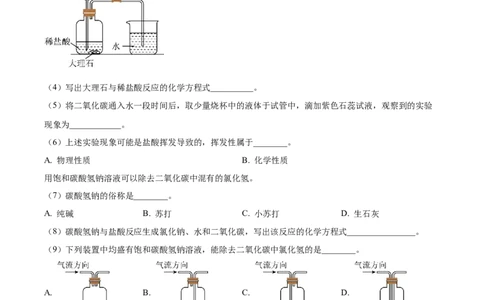
用下图所示的装置,在实验室中模拟“碳酸泉”的形成。
(4)写出大理石与稀盐酸反应的化学方程式__________。
(5)将二氧化碳通入水一段时间后,取少量烧杯中的液体于试管中,滴加紫色石蕊试液,观察到的实验
现象为____________。
(6)上述实验现象可能是盐酸挥发导致的,挥发性属于________。
A. 物理性质 B. 化学性质
用饱和碳酸氢钠溶液可以除去二氧化碳中混有的氯化氢。
(7)碳酸氢钠的俗称是________。
A. 纯碱 B. 苏打 C. 小苏打 D. 生石灰
(8)碳酸氢钠与盐酸反应生成氯化钠、水和二氧化碳,写出该反应的化学方程式________________。
(9)下列装置中均盛有饱和碳酸氢钠溶液,能除去二氧化碳中氯化氢的是________。
A. B. C. D.
(10)自然界中的“碳酸泉”温度一般都较低,在实验室模拟装置的烧杯中加入热水,也不易形成“碳酸
泉”,原因是________________。
三、氧气的制备(11分)
实验室中常用高锰酸钾制备氧气。
7. 中锰元素的化合价为
第2页/共10页
学科网(北京)股份有限公司.
A B. C. D.
8. 写出加热高锰酸钾制备氧气的化学方程式________________。
的
9. 请简述利用该装置检查装置气密性 方法 _____ 。
10. 用下图所示的装置制取氧气
(1)仪器a的名称是________。
(2)玻璃棉是由玻璃材质的细丝构成的。在该实验中,试管口放置一团玻璃棉而不是棉花,原因是
________。
A. 棉花是可燃物,而玻璃棉不是 B. 棉花能透气,而玻璃棉不能
C. 玻璃棉能截留固体小颗粒,而棉花不能 D. 玻璃棉能吸水,而棉花不能
(3)检验氧气集满的方法是________________。
11. 根据下表中物质的溶解性,设计从加热高锰酸钾后剩余的固体中回收二氧化锰的实验方案。
物质
溶解
可溶 易溶 难溶
性
________________
四、金属的蚀刻(9分)
化学社团的同学要用两片生锈的薄铁片,制作两幅金属蚀刻工艺品。
12. 铁锈的主要成分是氧化铁,氧化铁的化学式是
A. FeO B. C. D.
13. 清洗铁片上的铁锈,可使用的试剂是
第3页/共10页
学科网(北京)股份有限公司A. 氢氧化钠溶液 B. 稀盐酸 C. 氯化钠溶液 D. 澄清石灰水
14. 第一幅工艺品要在薄铁片上镂空出“化”字
步骤Ⅰ:在薄铁片上覆盖化学性质稳定的保护膜,仅“化”字笔画处正反面没有覆盖保护膜,如下图所示。
步骤Ⅱ:将上述处理的薄铁片浸泡在稀硫酸中,待“化”字笔画处的铁完全溶解后,取出薄铁片,清洗并
除去保护膜。
(1)步骤Ⅱ中也可以用稀盐酸代替稀硫酸,这两种溶液都具有酸性,其原因是都含有大量的________。
A. 氢离子 B. 氢氧根离子 C. 氯离子 D. 硫酸根离子
(2)若步骤Ⅱ中有2.8 g铁被溶解,根据化学方程式列式计算消耗硫酸的质量。
15. 第二幅工艺品要在薄铁片上呈现出“红底白字”的效果,如下图所示。
(1)第二片薄铁片覆上保护膜后,应浸泡在________中。
A. 硝酸银溶液 B. 氯化锌溶液 C. 硫酸亚铁溶液 D. 硫酸铜溶液
(2)写出上述反应的化学方程式________________。
的
(3)在下图中设计该铁片上 保护膜,将有保护膜的区域用铅笔涂黑。
五、过氧化氢的制备与应用(12分)
第4页/共10页
学科网(北京)股份有限公司电解水生成氢气和氧气,再用氢气和氧气制备过氧化氢。
16. 水电解前需要净化,吸附水中的色素,可以使用
A. 明矾 B. 活性炭 C. 氯化铁 D. 金刚石
17. 若要除去水中的氯化钠,需要进行的操作是
A. 过滤 B. 结晶 C. 蒸发 D. 蒸馏
18. 电解水生成氢气和氧气,在下图中画出与电源负极连接的电极上生成气体体积和反应时间的关系。
19. 氢气和氧气在钯基催化剂表面可反应生成过氧化氢,微观示意图①~④代表该反应的某段历程:
(1)下列关于钯基催化剂的说法正确的是 。(多选)
A. 钯基催化剂在反应前后质量不变
B. 钯基催化剂在反应前后化学性质不变
C. 在该反应中使用钯基催化剂能加快过氧化氢生成
D. 消耗等量的反应物,钯基催化剂能增加生成过氧化氢的量
(2)上述微观过程的正确排序为________,该方法制取过氧化氢的化学方程式为________________。
(3)用该方法制取过氧化氢时必须严禁明火,原因是________________。
过氧化氢溶液可用于废水处理。
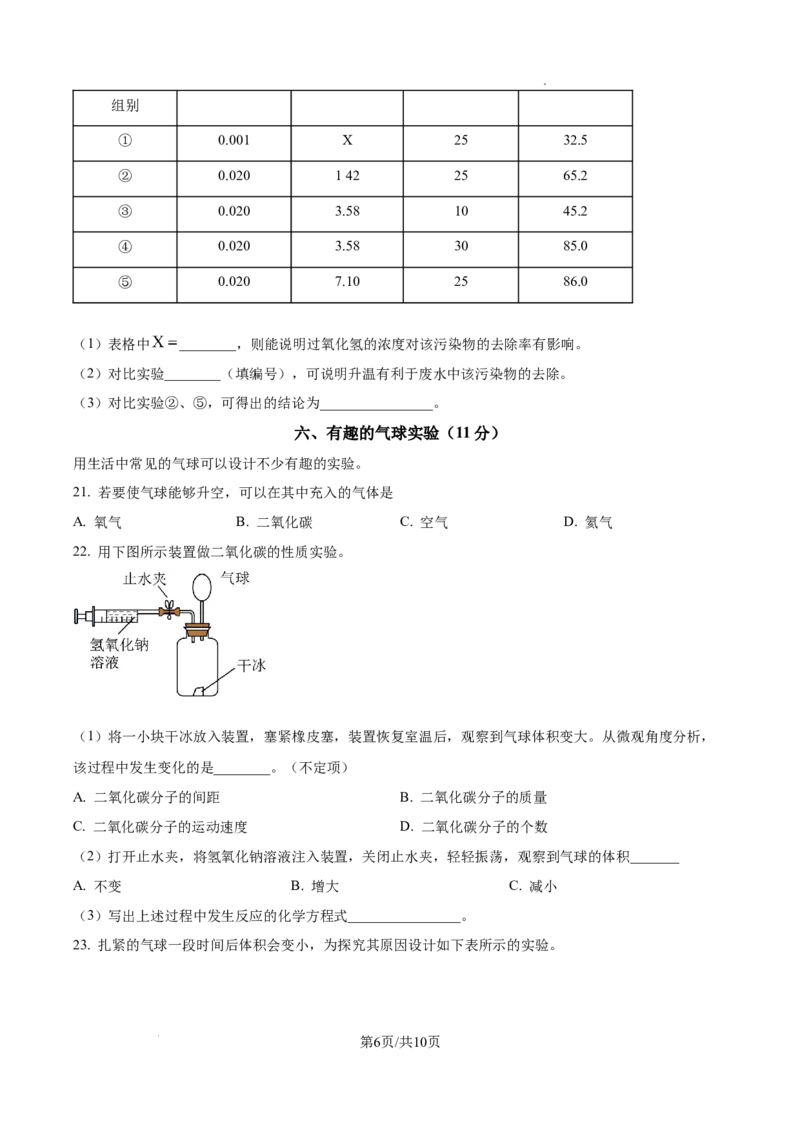
20. 探究过氧化氢去除某污染物的影响因素。取等量的废水,加入等体积一定质量分数的过氧化氢溶液和
硫酸铁,按下表进行分组实验,获得不同条件下某污染物的去除率数据,见下表。某污染物的去除率
过氧化氢的质 加入硫酸铁的 某污染物的去
实验 温度(℃)
量分数(%) 质量(g) 除率(%)
第5页/共10页
学科网(北京)股份有限公司组别
① 0.001 X 25 32.5
.
② 0.020 142 25 65.2
③ 0.020 3.58 10 45.2
④ 0.020 3.58 30 85.0
⑤ 0.020 7.10 25 86.0
(1)表格中 ________,则能说明过氧化氢的浓度对该污染物的去除率有影响。
(2)对比实验________(填编号),可说明升温有利于废水中该污染物的去除。
(3)对比实验②、⑤,可得出的结论为________________。
六、有趣的气球实验(11分)
用生活中常见的气球可以设计不少有趣的实验。
21. 若要使气球能够升空,可以在其中充入的气体是
A. 氧气 B. 二氧化碳 C. 空气 D. 氦气
22. 用下图所示装置做二氧化碳的性质实验。
(1)将一小块干冰放入装置,塞紧橡皮塞,装置恢复室温后,观察到气球体积变大。从微观角度分析,
该过程中发生变化的是________。(不定项)
A. 二氧化碳分子的间距 B. 二氧化碳分子的质量
C. 二氧化碳分子的运动速度 D. 二氧化碳分子的个数
(2)打开止水夹,将氢氧化钠溶液注入装置,关闭止水夹,轻轻振荡,观察到气球的体积_______
A. 不变 B. 增大 C. 减小
(3)写出上述过程中发生反应的化学方程式________________。
23. 扎紧的气球一段时间后体积会变小,为探究其原因设计如下表所示的实验。
第6页/共10页
学科网(北京)股份有限公司图示
步骤Ⅲ:向气
步骤Ⅱ:将空 球中充入二氧 步骤Ⅳ:将气球排
步骤Ⅰ:称量空瘪
步骤 瘪的气球放入 化碳,扎紧气 空,清洗并干燥后
的气球质量
澄清石灰水 球,再放入澄 再称量
清石灰水中
现象或 澄清石灰水变
2.0 g 无明显现象 2.0 g
数据 浑浊
【资料】实验中所用气球的材质是橡胶,橡胶由分子构成。
(1)上述实验中橡胶与澄清石灰水________化学反应 。
A. 发生 B. 没有发生
(2)上述实验中橡胶与二氧化碳________化学反应。
A. 发生 B. 没有发生
(3)写出步骤Ⅲ中发生反应的化学方程式________________。
(4)根据上述实验,从微观角度分析,扎紧的二氧化碳气球一段时间后体积会变小的原因是
________________。
七、甘露醇的提纯与应用(13分)
24. 甘露醇是一种白色针状晶体,从海带中提取的甘露醇中含有少量氯化钠,根据下表所示的溶解度数据,
提纯甘露醇。
温度(℃) 20 40 60 80
甘露醇的溶解度
18.5 35 64 115
(g)
氯化钠的溶解度
35.9 36.6 37.3 38.4
(g)
(1)甘露醇的化学式为 ,它由________种元素组成。
(2)在20~80℃范围内,溶解度随温度变化更明显的是________。
A. 氯化钠 B. 甘露醇
(3)40℃时,甘露醇的溶解度为________g。
有一份含有110 g甘露醇和15 g氯化钠的样品,按下图所示的流程进行提纯。
第7页/共10页
学科网(北京)股份有限公司(4)溶液a中的溶质是________。
(5)操作a的名称是________。
(6)20℃下,溶液b是氯化钠的________溶液(选填“饱和”或“不饱和”)。
(7)固体c是甘露醇,其表面有少量氯化钠溶液,可通过洗涤除去,洗涤时应使用________(选填“冷
水”或“热水”),理由是________________。
甘露醇注射液(20%的甘露醇水溶液)可治疗某些疾病
(8)配制250 g 20%的甘露醇水溶液需要甘露醇________g,水________mL。
(9)有一袋密封的甘露醇注射液存放在20℃的环境中,一段时间后,析出白色针状晶体。此时袋内甘露
醇溶液的溶质质量分数________20%(选填“大于”“小于”或“等于”)。请解释该条件下溶液析出晶
体原因________________。
八、铜暖手炉的使用与防锈(13分)
25. 我国古代工匠用铜制作各种暖手炉,其中一款的结构如下图所示。
(1)点燃木炭,观察到的现象是________。
A. 发出耀眼白光 B. 发出红色的光 C. 生成无色液滴 D. 生成白色的烟
(2)打开炉盖和铜网,将燃烧的木炭放入炉身内,盖上铜网。若木炭在炉中完全燃烧,化学方程式为
________________。若木炭不完全燃烧,则会生成________(填物质的名称)。
(3)若炉身底部没有小孔,使用时炉身会变形,原因是________________。
(4)盖上炉盖一段时间后,燃烧的木炭会熄灭,原因是________________。
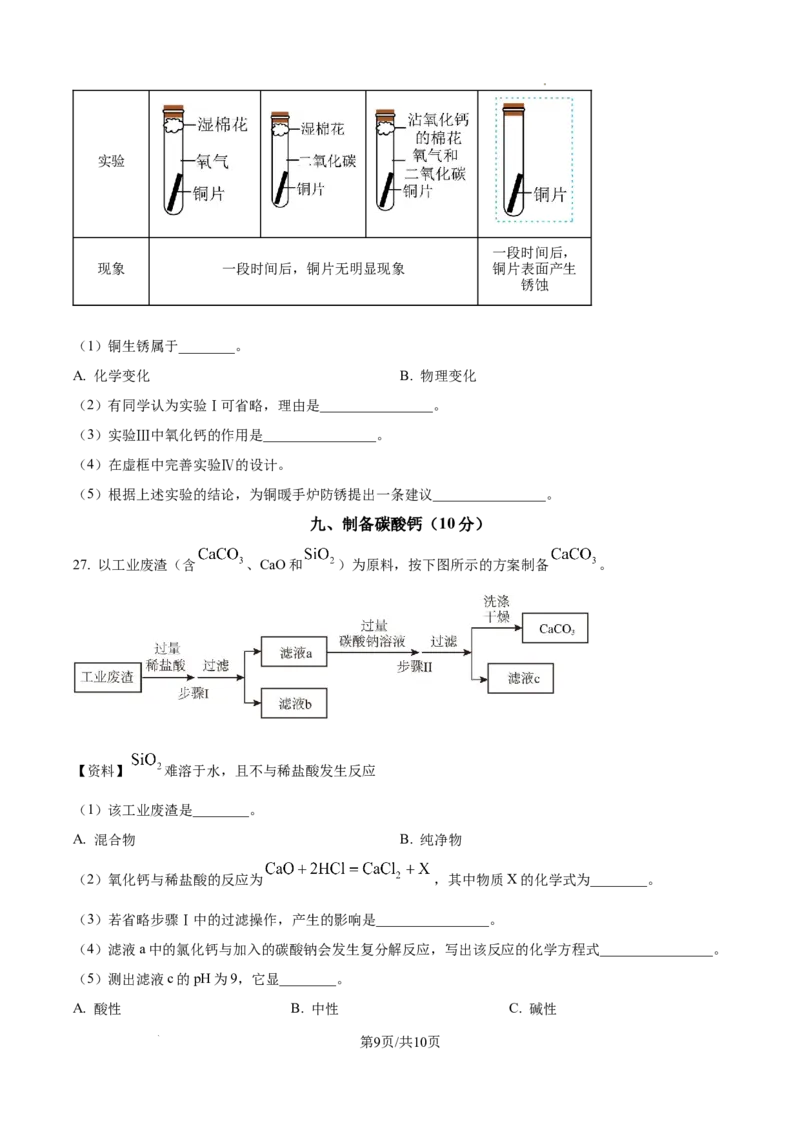
26. 铜器保存不当会生锈,铜锈的主要成分为碱式碳酸铜【化学式: 】,为探究其生成的
条件,设计如下四组实验。
编号 Ⅰ Ⅱ Ⅲ Ⅳ
第8页/共10页
学科网(北京)股份有限公司实验
一段时间后,
现象 一段时间后,铜片无明显现象 铜片表面产生
锈蚀
(1)铜生锈属于________。
A. 化学变化 B. 物理变化
(2)有同学认为实验Ⅰ可省略,理由是________________。
(3)实验Ⅲ中氧化钙的作用是________________。
(4)在虚框中完善实验Ⅳ的设计。
(5)根据上述实验的结论,为铜暖手炉防锈提出一条建议________________。
九、制备碳酸钙(10分)
27. 以工业废渣(含 、CaO和 )为原料,按下图所示的方案制备 。
【资料】 难溶于水,且不与稀盐酸发生反应
(1)该工业废渣是________。
A. 混合物 B. 纯净物
(2)氧化钙与稀盐酸的反应为 ,其中物质X的化学式为________。
(3)若省略步骤Ⅰ中的过滤操作,产生的影响是________________。
(4)滤液a中的氯化钙与加入的碳酸钠会发生复分解反应,写出该反应的化学方程式________________。
(5)测出滤液c的pH为9,它显________。
A. 酸性 B. 中性 C. 碱性
第9页/共10页
学科网(北京)股份有限公司(6)若向滤液c中滴加澄清石灰水,观察到的现象为________________。
(7)工业废渣的质量为 ,制得 的质量为 ,忽略上述方案中物质的损耗,能否确定 和
的大小关系?若能,则写出两者的大小关系;若不能,则写出理由。
第10页/共10页
学科网(北京)股份有限公司