文档内容
奉贤区 2019~2020 学年第一学期教学质量调研试卷
九年级理化(化学部分)
2020.1
考生注意:1. 本试卷满分60分,理化合卷用时100分钟;
2. 答案必须填写在答题卡上。
可能用到的相对原子质量:H–1 C–12 O–16
一、单项选择题(本题共 20 分)
27. 元素“Al”的名称是
A. 氯 B. 银 C. 铝 D. 汞
28. 由原子直接构成的物质是
A. 金刚石 B. 氯化钠 C. 氧气 D. 水
29. 石灰乳属于
A. 悬浊液 B. 乳浊液 C. 溶液 D. 纯净物
30. 不属于绿色能源的是
A. 氢能 B. 风能 C. 地热能 D. 石油
31. 物质名称和化学式书写都正确的是
A. 氧化镁MgO B. 氦气He
2 2
C. 氢氧化钾KOH D. 碳酸钠NaCO
3
32. 下列属于可回收垃圾的是
A. 废温度计 B. 废电池 C. 废药品 D. 废金属
33. 属于氧化物的是
A. O B. H SO C. P O D. Ca(HCO )
2 2 4 2 5 3 2
34. 用来表示“物质的量”的是
A. mol B. n C. M D. g/mol
35. 笑气(NO)是人类最早应用于医疗的麻醉剂之一,其中氮元素的化合价为
2
A. +1 B. +2 C. +4 D. –3
36. 下列物质排放到空气中,不会产生大气污染的是
A. 二氧化硫 B. 二氧化碳 C. 二氧化氮 D. 可吸入颗粒物
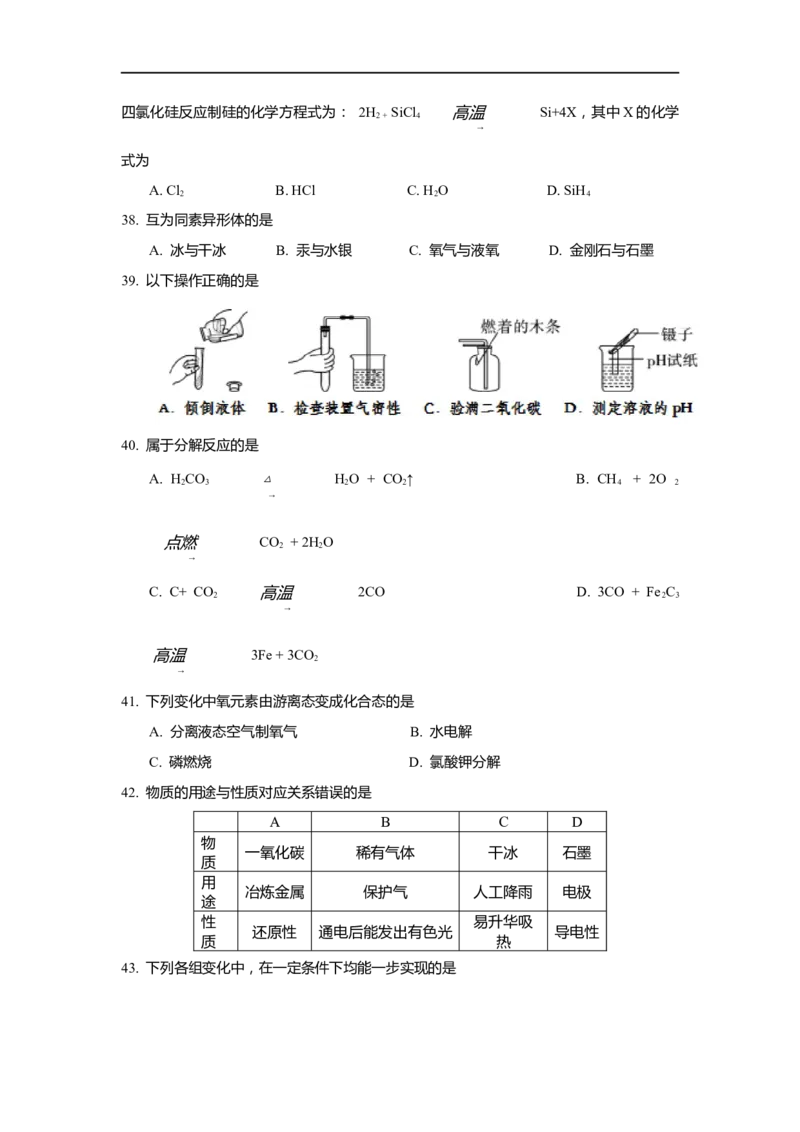
37. 华为开创了“中国芯”时代。“中国芯”的主要材料是髙纯度的单质硅,髙温下氢气
与四氯化硅反应制硅的化学方程式为: 2H SiCl 高温 Si+4X,其中X的化学
2 + 4
→
式为
A. Cl B. HCl C. H O D. SiH
2 2 4
38. 互为同素异形体的是
A. 冰与干冰 B. 汞与水银 C. 氧气与液氧 D. 金刚石与石墨
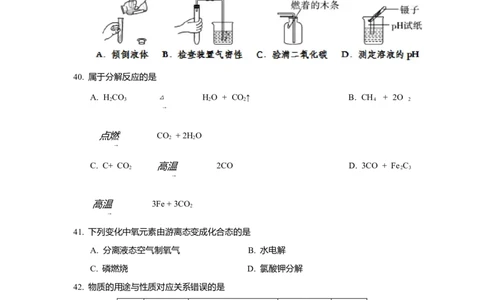
39. 以下操作正确的是
40. 属于分解反应的是
A. H CO △ HO + CO ↑ B. CH + 2O
2 3 2 2 4 2
→
点燃 CO + 2H O
2 2
→
C. C+ CO 高温 2CO D. 3CO + Fe C
2 2 3
→
高温 3Fe + 3CO
2
→
41. 下列变化中氧元素由游离态变成化合态的是
A. 分离液态空气制氧气 B. 水电解
C. 磷燃烧 D. 氯酸钾分解
42. 物质的用途与性质对应关系错误的是
A B C D
物
一氧化碳 稀有气体 干冰 石墨
质
用
冶炼金属 保护气 人工降雨 电极
途
性 易升华吸
还原性 通电后能发出有色光 导电性
质 热
43. 下列各组变化中,在一定条件下均能一步实现的是A. ① B. ② C. ①②都不可以 D. ①②都可以
44. 在一定温度下,将少量生石灰放入一定量的饱和石灰水中,搅拌并冷却到原来温度,
下列说法正确的是
A. 溶剂质量不变 B. 溶质质量不变
C. 溶液质量不变 D. 溶质质量分数不变
45. 只含一种分子的物质一定是
A. 单质 B. 纯净物 C. 混合物 D. 化合物
46. lmol物质充分燃烧,产生的二氧化碳最多的是
A. CH COCH B. CHCHOH C. CH OH D. CH
3 3 3 2 3 4
七、填空题 (共21分)
47. 化学与人类生活息息相关。
① 空气中能供给呼吸的气体是____________。
② 冰箱中放入活性炭除异味,利用了活性炭的____________性。
③ 打开汽水瓶盖,有气泡冒出,说明气体溶解度随压强减小而____________。
④ 近期流感肆虑,“达菲”是目前治疗H1N1流感病毒的良药。生产“达菲”的主要
原料是莽草酸(化学式:C H O)。C H O 由____________种元索组成,lmol C H O 中约
7 10 5 7 10 5 7 10 5
含有____________个H原子。
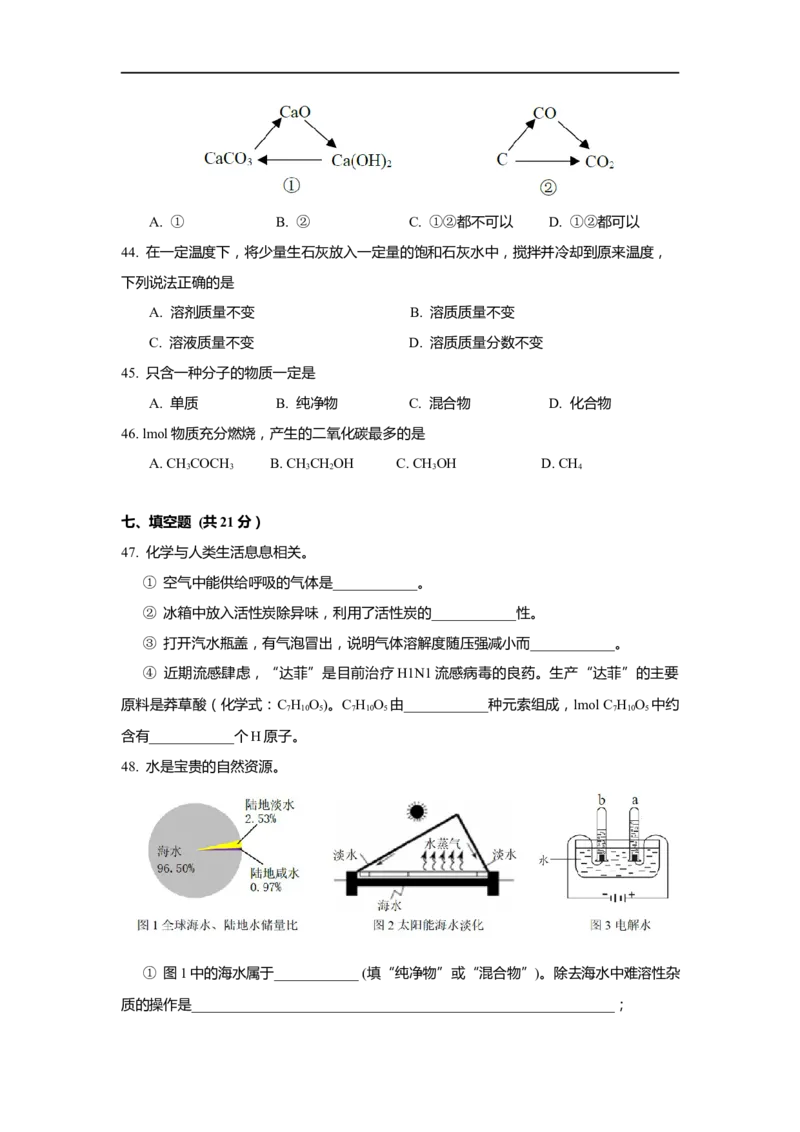
48. 水是宝贵的自然资源。
① 图1中的海水属于____________ (填“纯净物”或“混合物”)。除去海水中难溶性杂
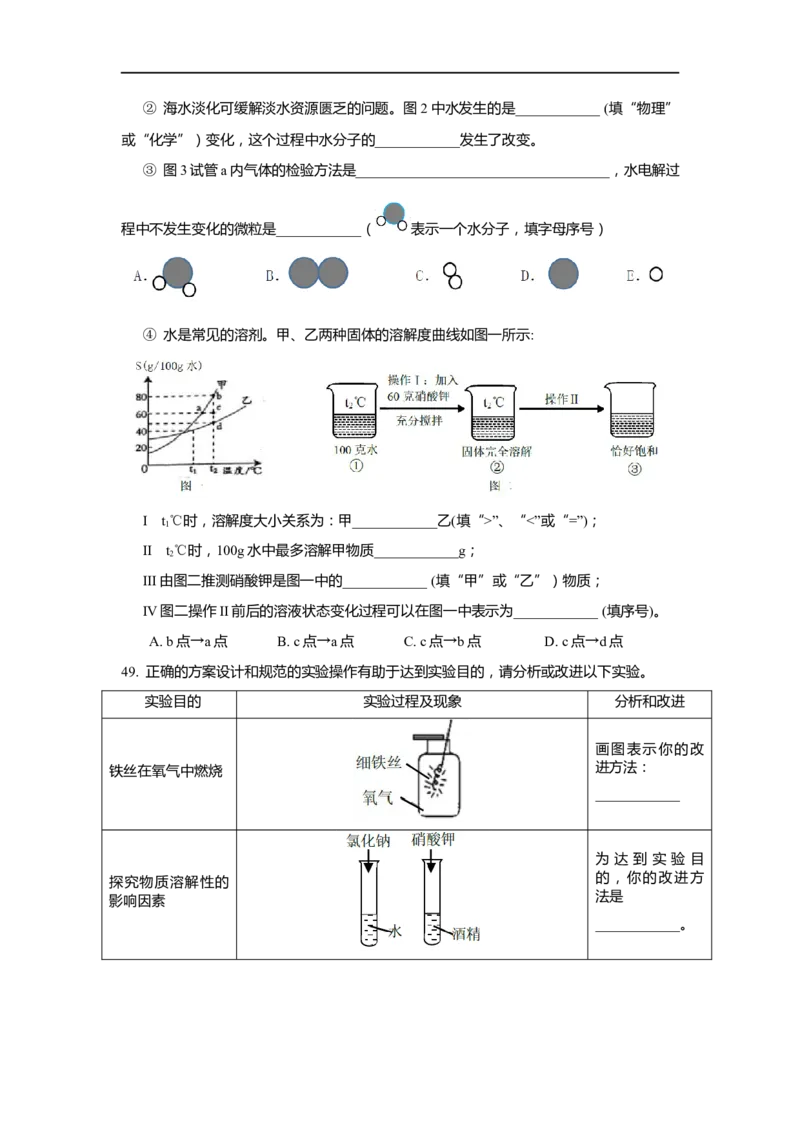
质的操作是____________________________________________________________;② 海水淡化可缓解淡水资源匮乏的问题。图2中水发生的是____________ (填“物理”
或“化学”)变化,这个过程中水分子的____________发生了改变。
③ 图3试管a内气体的检验方法是____________________________________,水电解过
程中不发生变化的微粒是____________( 表示一个水分子,填字母序号)
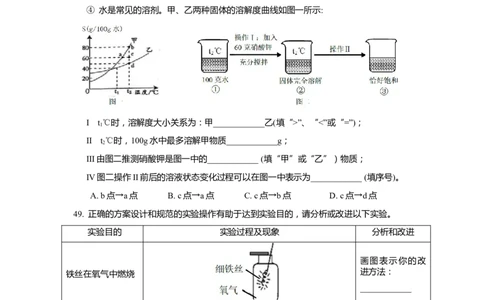
④ 水是常见的溶剂。甲、乙两种固体的溶解度曲线如图一所示:
I t ℃时,溶解度大小关系为:甲____________乙(填“>”、“<”或“=”);
1
II t ℃时,100g水中最多溶解甲物质____________g;
2
III由图二推测硝酸钾是图一中的____________ (填“甲”或“乙”)物质;
IV图二操作II前后的溶液状态变化过程可以在图一中表示为____________ (填序号)。
A. b点→a点 B. c点→a点 C. c点→b点 D. c点→d点
49. 正确的方案设计和规范的实验操作有助于达到实验目的,请分析或改进以下实验。
实验目的 实验过程及现象 分析和改进
画图表示你的改
铁丝在氧气中燃烧 进方法:
____________
为 达 到 实 验 目
的,你的改进方
探究物质溶解性的
法是
影响因素
____________。该实验不能达到
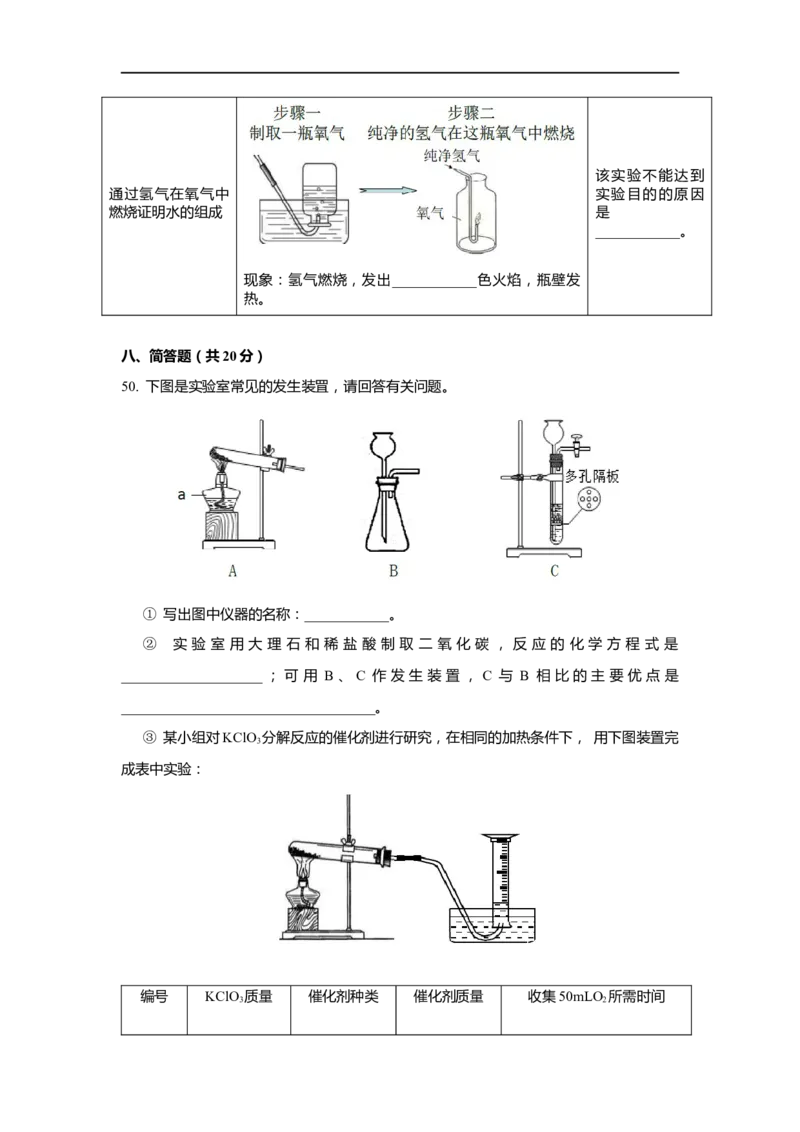
通过氢气在氧气中 实验目的的原因
燃烧证明水的组成 是
____________。
现象:氢气燃烧,发出____________色火焰,瓶壁发
热。
八、简答题(共20分)
50. 下图是实验室常见的发生装罝,请回答有关问题。
① 写出图中仪器的名称:____________。
② 实 验 室 用 大 理 石 和 稀 盐 酸 制 取 二 氧 化 碳 , 反 应 的 化 学 方 程 式 是
____________________ ; 可 用 B 、 C 作 发 生 装 置 , C 与 B 相 比 的 主 要 优 点 是
____________________________________。
③ 某小组对KClO 分解反应的催化剂进行研究,在相同的加热条件下, 用下图装置完
3
成表中实验:
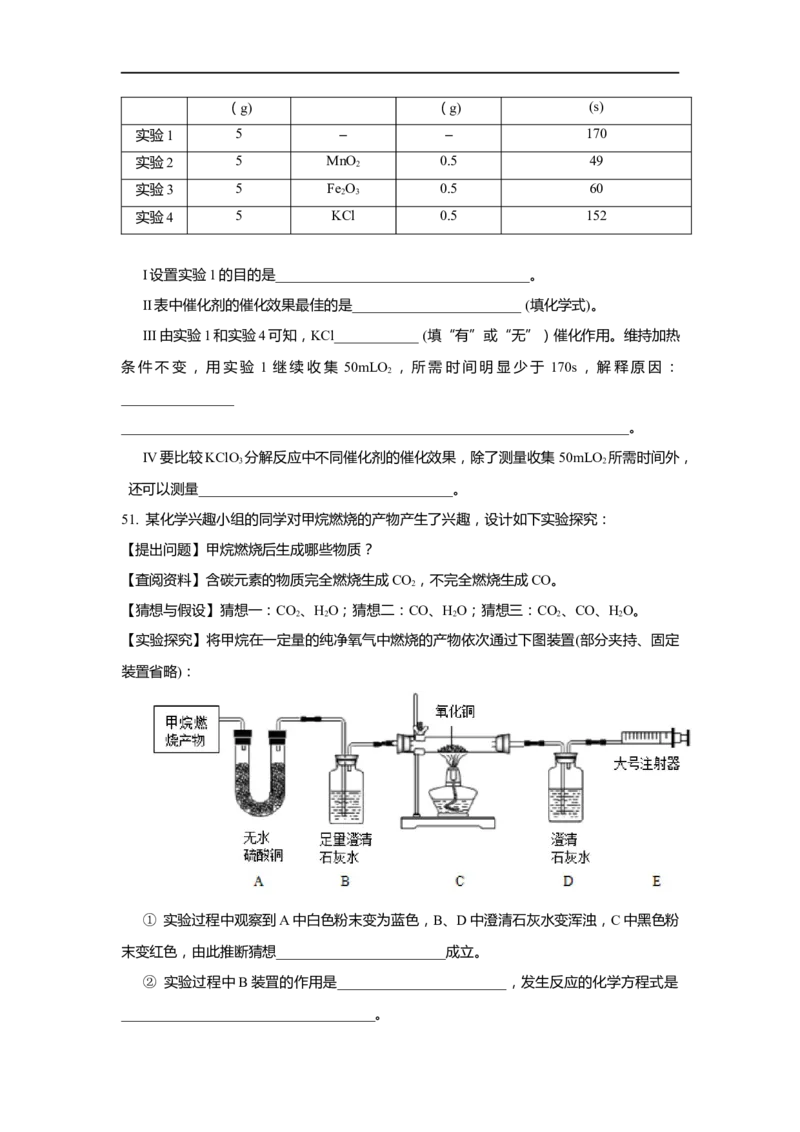
编号 KClO 质量 催化剂种类 催化剂质量 收集50mLO 所需时间
3 2(g) (g) (s)
实验1 5 – – 170
实验2 5 MnO
2
0.5 49
实验3 5 Fe
2
O
3
0.5 60
实验4 5 KCl 0.5 152
I设置实验1的目的是____________________________________。
II表中催化剂的催化效果最佳的是________________________ (填化学式)。
III由实验1和实验4可知,KCl____________ (填“有”或“无”)催化作用。维持加热
条件不变,用实验 1 继续收集 50mLO ,所需时间明显少于 170s,解释原因:
2
________________
________________________________________________________________________。
IV要比较KClO 分解反应中不同催化剂的催化效果,除了测量收集50mLO 所需时间外,
3 2
还可以测量____________________________________。
51. 某化学兴趣小组的同学对甲烷燃烧的产物产生了兴趣,设计如下实验探究:
【提出问题】甲烷燃烧后生成哪些物质?
【査阅资料】含碳元素的物质完全燃烧生成CO,不完全燃烧生成CO。
2
【猜想与假设】猜想一:CO、HO;猜想二:CO、HO;猜想三:CO、CO、HO。
2 2 2 2 2
【实验探究】将甲烷在一定量的纯净氧气中燃烧的产物依次通过下图装置(部分夹持、固定
装置省略):
① 实验过程中观察到A中白色粉末变为蓝色,B、D中澄清石灰水变浑浊,C中黑色粉
末变红色,由此推断猜想________________________成立。
② 实验过程中B装罝的作用是________________________,发生反应的化学方程式是
____________________________________。③ C装置中发生反应的化学方程式是____________________________________。
④ E 处 的 大 号 注 射 器 , 可 以 引 导 气 体 流 向 , 其 另 一 个 主 要 作 用 是
_____________________。
⑤ 实验过程中用纯净O 而不用空气的原因是____________________________________。
2
【 反 思 与 交 流 】 燃 气 热 水 器 必 须 安 装 在 浴 室 外 非 密 闭 空 间 的 原 因 是
______________________。
52. 某同学用右图装置测定过氧化氢溶液中溶质的质量分数。
① 若反应生成 3.2 克氧气,则参加反应的过氧化氢的物质的量为
____________ (利用化学方程式列式计算)。
② 老师评价利用上述方法测定的过氧化氧溶液中溶质质量分数通常偏大,试分析原因
________________________________________________________________________。