文档内容
化学部分
相对原子质量:H-1 C-12 O-16 Cl-35.5 K-39 Ca-40
五、选择题(共20分)
第21-34题,每题均只有1个正确选项,每题1分。
1. 空气中能支持燃烧的气体是
A. O B. N C. He D. CO
2 2 2
【答案】A
【解析】
【详解】空气中含有氧气,且氧气能够支持燃烧,氧气具有助燃性,故选A。
2. 硅是制成光伏电池的半导体材料,硅的元素符号是
A. Se B. S C. Si D. Al
【答案】C
【解析】
【详解】A、Se是硒元素的元素符号。故A错误;
B、S是硫元素的元素符号。故B错误;
C、Si是硅元素的元素符号。故C正确;
D、Al是铝元素的元素符号。故D错误。
故选:C。
3. 属于溶液的是
A. 蒸馏水 B. 矿泉水 C. 泥沙水 D. 油水
【答案】B
【解析】
【详解】A、溶液是具有均一性、稳定性的混合物,蒸馏水属于纯净物,不属于溶液,溶液必须属于混合
物,故A错误;
B、矿泉水中含有可溶性物质,是均一、稳定的混合物,属于溶液,故B正确;
C、泥沙水是不溶性的小颗粒分散到液体中形成的,不均一、不稳定,属于悬浊液,故C错误;
D、油水不均一、不稳定,属于乳浊液,故D错误。
故选B 。
4. 属于化学变化的是
A. 蜡烛熔化 B. 白磷自燃 C. 酒精挥发 D. 干冰升华
【答案】B【解析】
【分析】化学变化有其他物质生成;物理变化没有其他物质生成。
【详解】A.蜡烛熔化的过程中没有其他物质生成,致使蜡烛的状态发生了变化,属于物理变化;
B.白磷燃烧的过程中生成了五氧化二磷,属于化学变化;
C.酒精挥发的过程中没有其他物质生成,属于物理变化;
D.干冰升华的过程中没有其他物质生成,属于物理变化;
故选B。
【点睛】
5. 下图A、B、C、D四点表示对应选项中浴液的pH,其中不合理的是
A. 盐酸 B. 碳酸溶液 C. 食盐水 D. 石灰水
【答案】C
【解析】
【详解】A、盐酸呈酸性且酸性较强,pH<7且比较小,故A正确;
B、碳酸溶液呈酸性且酸性较弱,pH<7且接近7,故B正确;
C、食盐水呈中性,pH=7,故C错误;
D、石灰水呈碱性,pH>7,故D正确;
故选C。
6. 在氧气中燃烧,产生白色固体的是
A. 木炭 B. 红磷 C. 硫粉 D. 铁丝
【答案】B
【解析】
【详解】A 、木炭在氧气中燃烧生成二氧化碳气体,没有固体,故A错误;
B、红磷在氧气中燃烧生成白烟(固体)五氧化二磷,故B正确;
C、硫在氧气中燃烧生成二氧化硫气体,没有固体,故C错误;
D、铁在氧气中燃烧生成黑色固体四氧化三铁,不是白色,故D错误;
故选B。
7. 互为同素异形体的一组物质是
A. 水和冰 B. 水银和汞 C. 石墨和碳-60 D. 氧气和液氧
【答案】C
【解析】【详解】同素异形体为由同种元素组成的不同种单质
A、水和冰是同种物质的不同种物态,且水属于化合物,不是同素异形体,故A错误;
B、水银和汞是同种单质的不同称呼,不是同素异形体,故B错误;
C、石墨和C 都是由碳元素组成的不同单质,是同素异形体,故C正确;
60
D、氧气和液氧是同种单质的不同物态,不是同素异形体,故D错误;
故选C。
8. 下列物质中不含原子团的是
A. 氯化钠:NaCl B. 硝酸银:AgNO
3
C. 硫酸钡:BaSO D. 氢氧化钾:KOH
4
【答案】A
【解析】
【分析】
【详解】A、氯化钠中含钠离子和氯离子,不含原子团,故选项符合题意;
B、硝酸银中含银离子和硝酸根离子,含原子团,故选项不符合题意;
C、硫酸钡中含钡离子和硫酸根离子,含原子团,故选项不符合题意;
D、氢氧化钾中含钾离子和氢氧根离子,含原子团,故选项不符合题意;
故选A。
【点睛】
9. 关于CO和CO 的描述错误的是
2
A. 元素种类相同 B. 都 是无色气体
.
C 分子结构不同 D. 都难溶于水
【答案】D
【解析】
【分析】
【详解】A、两种气体都是由碳元素和氧元素组成的,此选项表述正确;
B、两种气体都是无色气体,此选项表述正确;
C、两种物质的分子结构不同,1个一氧化碳分子是由1个碳原子和1个氧原子构成的,1个二氧化碳分子
是由1个碳原子和2个氧原子构成的,此选项表述正确;
D、一氧化碳难溶于水,二氧化碳能溶于水,此选项表述不正确。
故选D。
【点睛】
10. 物质的用途利用其化学性质的是A. 生石灰做干燥剂 B. 石墨做电极
C. 稀有气体制霓虹灯 D. 干冰做制冷剂
【答案】A
【解析】
【详解】A、生石灰作干燥剂时因为生石灰能够和水发生反应,属于化学性质,故A正确;
B、石墨做电极是因为石墨具有导电性,导电性为物理性质,故B错误;
C、稀有气体做霓虹灯是因为稀有气体在电流作用下发光,是物理性质,故C错误;
D、干冰做制冷剂是因为干冰升华过程吸热,属于物理性质,故D错误;
故选A。
11. 使燃料充分燃烧的下列措施中不合理的是
A. 固体燃料粉碎 B. 液体燃料喷成雾状
C. 增加空气用量 D. 增加燃料用量
【答案】D
【解析】
【分析】
【详解】A:固体燃料粉碎可以增大可燃物与氧气的接触面积。使燃料充分燃烧。合理。
B:液体燃料喷成雾状可以增大可燃物与氧气的接触面积。使燃料充分燃烧。合理。
C:增加空气用量就是增大可燃物与氧气的接触面积。使燃料充分燃烧。合理。
D:增加燃料用量相当于减少可燃物与氧气的接触面积。使燃料不能充分燃烧。不合理。
综上所述:选择D。
【点睛】
12. 关于水分子的说法正确的是
A. 水分子是由氢原子和氧原子构成的 B. 水变成冰后,水分子是静止的
C. 水变成水蒸气后,水分子的体积变大了 D. 水分子可以保持水的物理性质
【答案】A
【解析】
【分析】
【详解】A、水分子是由氢原子和氧原子构成的,此选项表述正确;
B、水变成冰后,水分子也在不断运动,只是运动速度慢了,此选项表述不正确;
C、水变成水蒸气后,水分子的体积没变,水分子之间的间隔变大了,此选项表述不正确;
D、水分子能保持水的化学性质,但不能保持水的物理性质,此选项表述不正确。
故选A 。
【点睛】13. 关于物质的量描述错误的是
A. 表示一定数目微粒的集合体 B. 国际单位制7个基本物理量之一
C. 1mol物质的质量就是该物质的式量 D. 1mol物质约含6.02×1023个微粒
【答案】C
【解析】
【详解】A 、物质的量表示一定数目微粒的集合体,描述无误,故A正确;
B、国际单位制7个基本物理量包括质量、长度、时间、电流强度、发光强度、温度、物质的量,物质的
量是其中之一,故B正确;
C、1mol物质的质量单位为“g”,物质的式量表述的是相对分子质量或相对原子质量,单位为“1”,二者
意义不同,只是在数值上大小相等,故C错误;
D、1mol物质约含6.02×1023个微粒,描述无误,故D正确;
故选C。
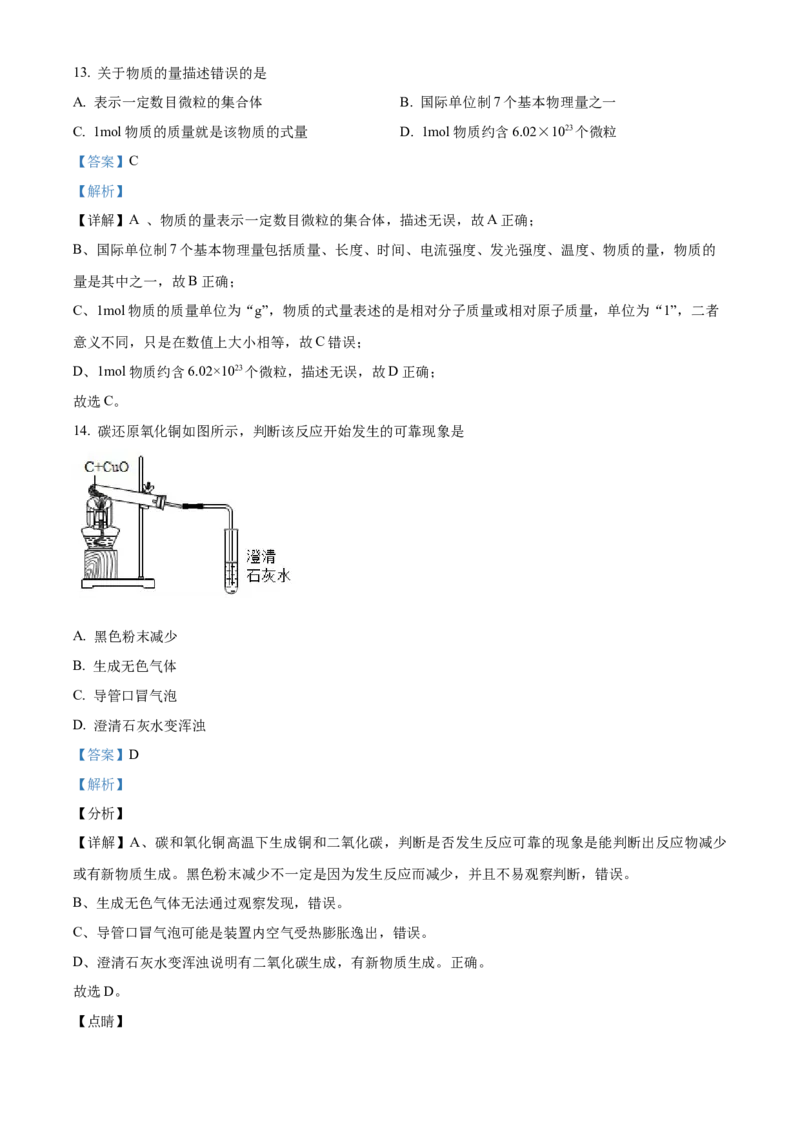
14. 碳还原氧化铜如图所示,判断该反应开始发生的可靠现象是
A. 黑色粉末减少
B. 生成无色气体
C. 导管口冒气泡
D. 澄清石灰水变浑浊
【答案】D
【解析】
【分析】
【详解】A、碳和氧化铜高温下生成铜和二氧化碳,判断是否发生反应可靠的现象是能判断出反应物减少
或有新物质生成。黑色粉末减少不一定是因为发生反应而减少,并且不易观察判断,错误。
B、生成无色气体无法通过观察发现,错误。
C、导管口冒气泡可能是装置内空气受热膨胀逸出,错误。
D、澄清石灰水变浑浊说明有二氧化碳生成,有新物质生成。正确。
故选D。
【点睛】第35~37题,每题均有1-2个正确选项,每题2分选对1个得1分,多选成错选得0分。
15. 关于物质组成的说法正确的是
A. 单质中至少含一种元素 B. 化合物中至少含两种元素
C. 氧化物中只含两种元素 D. 混合物中至少含两种元素
【答案】BC
【解析】
【详解】A、单质为只含有一种元素的纯净物,故A错误;
B、化合物为有两种及两种以上的元素组成的纯净物,故B正确;
C、氧化物为只含两种元素且其中一种为氧元素的化合物,故C正确;
D、混合物中可能含一种元素,也可能含有多种元素,如氧气和臭氧的混合物种只含一种元素。故D错误;
故选BC。
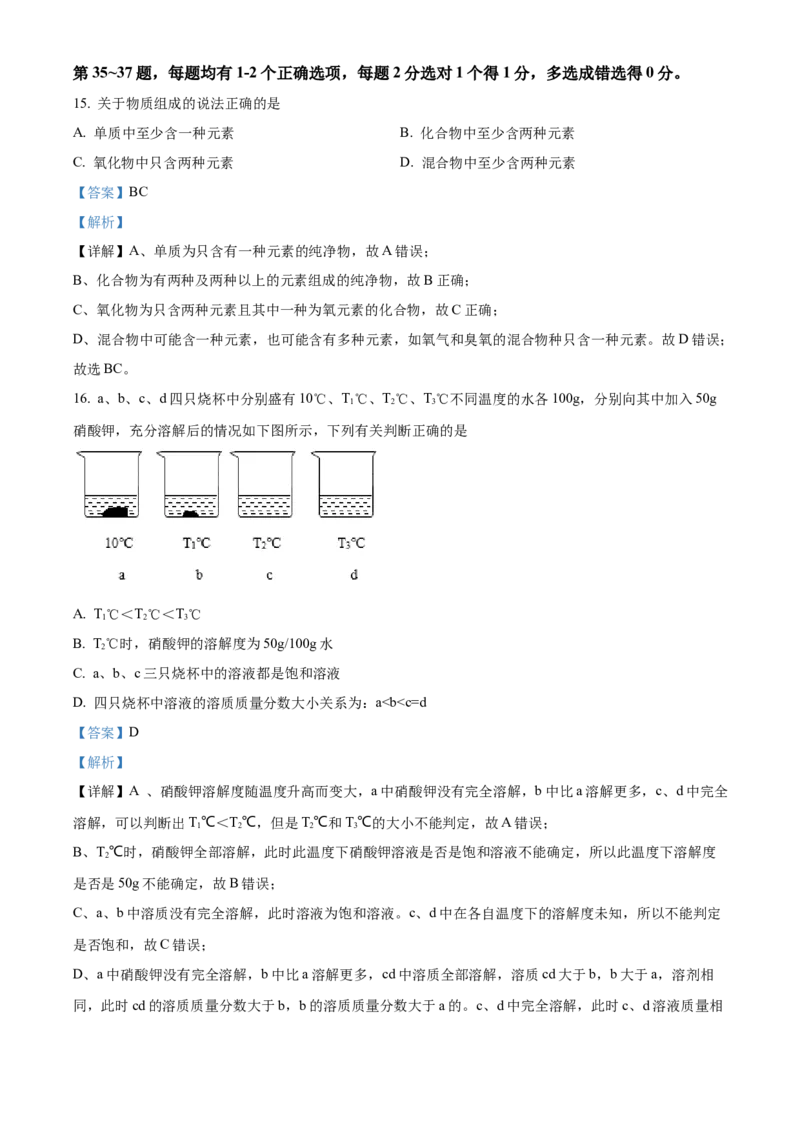
16. a、b、c、d四只烧杯中分别盛有10℃、T℃、T℃、T℃不同温度的水各100g,分别向其中加入50g
1 2 3
硝酸钾,充分溶解后的情况如下图所示,下列有关判断正确的是
A. T℃<T℃<T℃
1 2 3
B. T℃时,硝酸钾的溶解度为50g/100g水
2
C. a、b、c三只烧杯中的溶液都是饱和溶液
D. 四只烧杯中溶液的溶质质量分数大小关系为:a”“=”或“<”);
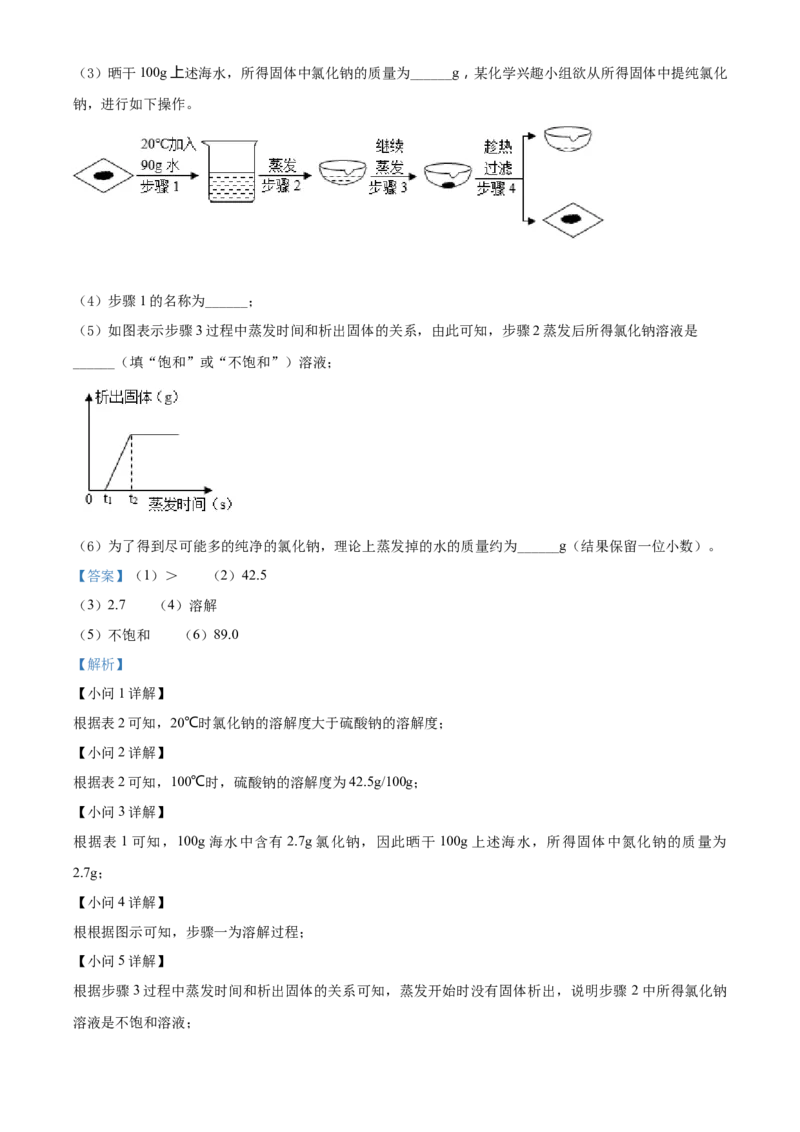
(2)100℃时,硫酸钠的溶解度为______g/100g水;(3)晒干100g上述海水,所得固体中氯化钠的质量为______g,某化学兴趣小组欲从所得固体中提纯氯化
钠,进行如下操作。
(4)步骤1的名称为______;
(5)如图表示步骤3过程中蒸发时间和析出固体的关系,由此可知,步骤2蒸发后所得氯化钠溶液是
______(填“饱和”或“不饱和”)溶液;
(6)为了得到尽可能多的纯净的氯化钠,理论上蒸发掉的水的质量约为______g(结果保留一位小数)。
【答案】(1)> (2)42.5
(3)2.7 (4)溶解
(5)不饱和 (6)89.0
【解析】
【小问1详解】
根据表2可知,20℃时氯化钠的溶解度大于硫酸钠的溶解度;
【小问2详解】
根据表2可知,100℃时,硫酸钠的溶解度为42.5g/100g;
【小问3详解】
根据表1可知,100g海水中含有 2.7g氯化钠,因此晒干 100g上述海水,所得固体中氮化钠的质量为
2.7g;
【小问4详解】
根根据图示可知,步骤一为溶解过程;
【小问5详解】
根据步骤3过程中蒸发时间和析出固体的关系可知,蒸发开始时没有固体析出,说明步骤 2中所得氯化钠
溶液是不饱和溶液;【小问6详解】
需要提纯的固体混合物中含有2.7g氯化钠和0.2g硫酸钠,水的质量为90g,在20℃恒温蒸发水分时,硫酸
钠的溶解度小于氯化钠,为了得到尽可能多的纯净的氯化钠,当水分蒸发至硫酸钠达到饱和状态时,停止
蒸发操作,0.2g硫酸钠溶解达到饱和状态所需要的的水的质量为: ,因此理论上蒸发
掉的水的质量约为:90g-1.0g=89.0g。
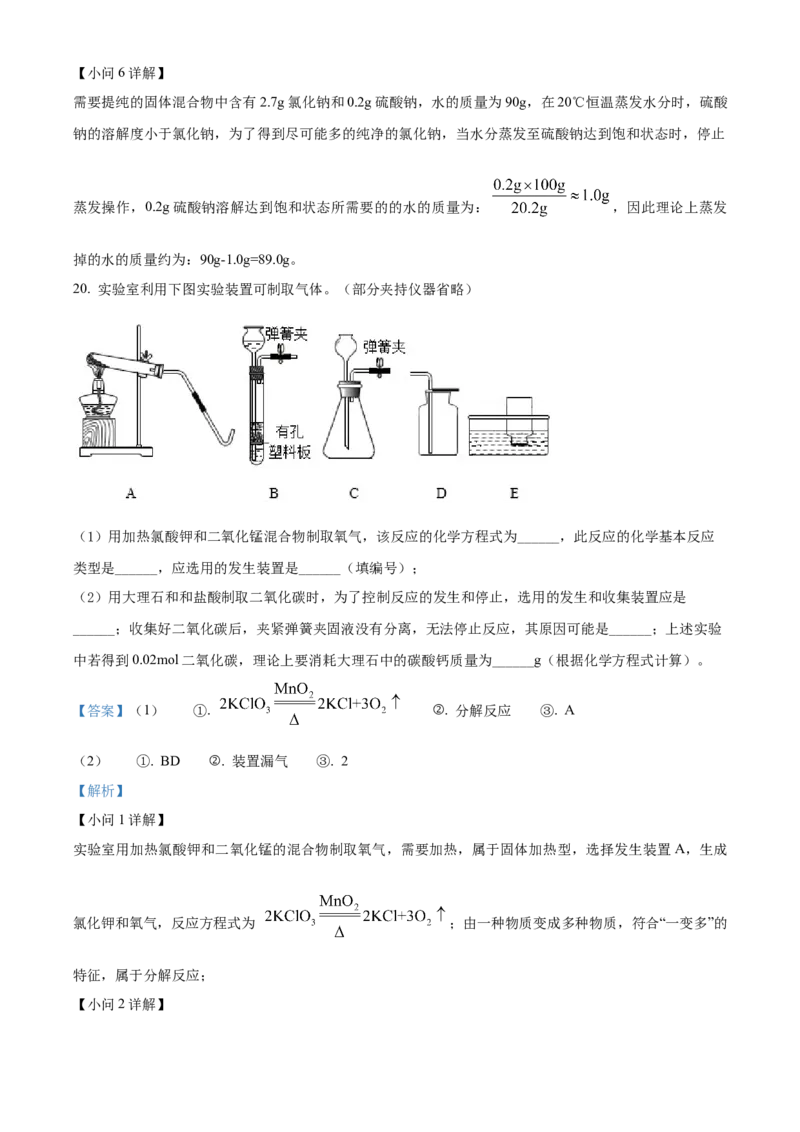
20. 实验室利用下图实验装置可制取气体。(部分夹持仪器省略)
(1)用加热氯酸钾和二氧化锰混合物制取氧气,该反应的化学方程式为______,此反应的化学基本反应
类型是______,应选用的发生装置是______(填编号);
(2)用大理石和和盐酸制取二氧化碳时,为了控制反应的发生和停止,选用的发生和收集装置应是
______;收集好二氧化碳后,夹紧弹簧夹固液没有分离,无法停止反应,其原因可能是______;上述实验
中若得到0.02mol二氧化碳,理论上要消耗大理石中的碳酸钙质量为______g(根据化学方程式计算)。
【答案】(1) ①. ②. 分解反应 ③. A
(2) ①. BD ②. 装置漏气 ③. 2
【解析】
【小问1详解】
实验室用加热氯酸钾和二氧化锰的混合物制取氧气,需要加热,属于固体加热型,选择发生装置A,生成
氯化钾和氧气,反应方程式为 ;由一种物质变成多种物质,符合“一变多”的
特征,属于分解反应;
【小问2详解】用大理石和和盐酸制取二氧化碳属于固液常温型,B装置中装有有孔塑料隔板和弹簧夹可以通过弹簧夹的
开闭控制反应的发生和停止,大理石放在多孔塑料板上与稀盐酸接触反应,当弹簧夹关闭,内部气体增多,
压强增大,液体被压入长颈漏斗,固液分离,反应停止,打开弹簧夹,气体输出,压强减小,液体流入试
管,固液接触,反应发生;二氧化碳易溶于水,密度比空气大,收集二氧化碳可选用向上排空气法,选用
装置D。收集好二氧化碳后,夹紧弹簧夹固液没有分离,无法停止反应,其原因可能是装置漏气;
解:二氧化碳的质量=0.02mol×44g/mol=0.88g。设若得到0.02mol二氧化碳,理论上要消耗大理石中的碳酸
钙质量为
=2g
答:若得到0.02mol二氧化碳,理论上要消耗大理石中的碳酸钙质量2g;
21. 水煤气是一种气态燃料,工业上用水蒸气(HO)通过炽热的焦层(C)所得气体即为水煤气。某化学
2
兴趣小组同学欲探究水煤气的成分,开展如下活动:
【提出问题】水煤气 的成分是什么?
【作出猜想】猜想Ⅰ:CO和H;猜想Ⅱ:CO 和H;猜想Ⅲ:CO、CO 和H
2 2 2 2 2
猜想依据是:______。
经过讨论,小组同学认为水煤气中一定还含有水蒸气。
【查阅资料】H 的化学性质与CO相似,也能与氧化铜反应,产物为铜和水;
2
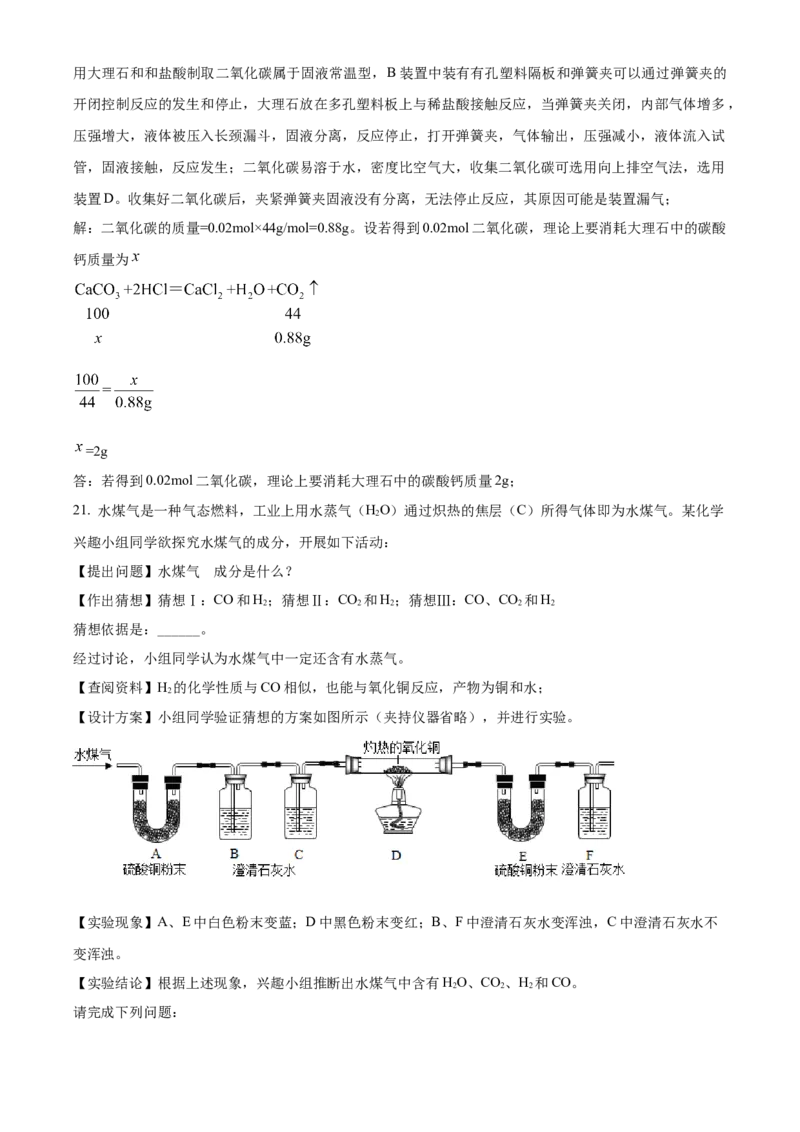
【设计方案】小组同学验证猜想的方案如图所示(夹持仪器省略),并进行实验。
【实验现象】A、E中白色粉末变蓝;D中黑色粉末变红;B、F中澄清石灰水变浑浊,C中澄清石灰水不
变浑浊。
【实验结论】根据上述现象,兴趣小组推断出水煤气中含有HO、CO、H 和CO。
2 2 2
请完成下列问题:①装置A中反应的化学方程式为______;
②推断出水煤气中含有CO的依据是______;
③装置C的作用是______;
【实验评价】该兴趣小组设计的实验方案存在问题,你的改进措施是______。
【 答 案 】 ① . 根 据 质 量 守 恒 定 律 , 化 学 反 应 前 后 元 素 种 类 不 变 ② .
③. D中黑色粉末变红,C中澄清石灰水不变浑浊,F中澄清石灰水变
浑浊 ④. 检验装置B是否把气体中的二氧化碳除尽 ⑤. 在装置C、D之间加装气体干燥装置;在装
置末端放一点燃的酒精灯,处理尾气中的一氧化碳
【解析】
【详解】猜想依据:根据质量守恒定律,化学反应前后元素种类不变,所应物中含有碳、氢、氧三种元素,
所以作出题中三种猜想。
实验结论:①A中为硫酸铜粉末,由白色变蓝色,硫酸铜粉末与水结合形成蓝色的硫酸铜晶体,反应的化
学方程式为: 。
②一氧化碳和氢气都有有还原性,氢气还原氧化铜生成铜和水,一氧化碳还原氧化铜生成铜和二氧化碳;
D中粉末变红说明气体中有一氧化碳和氢气中的一种或两种,又观察到E中白色粉末变蓝,说明有水生成,
从而说明水煤气中含有氢气,观察到C中澄清石灰水不变浑浊,F中澄清石灰水变浑浊,说明有二氧化碳
生成,从而说明水煤气中含有一氧化碳,故答案填:D中黑色粉末变红,C中澄清石灰水不变浑浊F中澄
清石灰水变浑浊。
③装置B的作用是检验并除去二氧化碳,装置C作用应该是检验装置B是否把气体中的二氧化碳除尽。
实验评价:由于气体通过了B、C两装,气体由溶液中逸出,会带出一部分水蒸气,带出的水蒸气也会使
E中的硫酸铜粉末变蓝,会干扰水煤气中是否有氢气的检验,所以应在C、D两装置间加装一个气体干燥
装置,可以用万用瓶内装浓硫酸,;
因为水煤气中含有一氧化碳,实验过程中未反应的一氧化碳逸出会污染空气,所以要在装置末端加装置尾
气处理装置,防止空气污染,如在装置末端放一点燃的酒精灯,处理尾气中的一氧化碳。