文档内容
杨浦区 2019~2020 学年第一学期教学质量调研试卷
九年级理化(化学部分)
2019.12
可能用到的相对原子质量:H-1 He-4 C-12 N-14 O-16 S-32 Ca-40
Cu-64
一、单项选择题(本题共 24 分)
1.属于化学变化的是
A. 木炭燃烧 B. 酒精挥发 C. 矿石粉碎 D. 铁丝弯
曲
2.氢元素的符号是
A. He B. H C. H2 D. 2H
3.澄清石灰水属于
A. 溶液 B. 纯净物 C. 乳浊液 D. 悬浊液
4. 空气成分中,体积分数最大的是( )
A. 氮气 B. 二氧化碳 C. 氧气 D. 稀有气
体
5.保持水化学性质的微粒是
A. 氢原子 B. 氧分子 C. 水分子 D. 水原子
6.活性炭能净水,主要是因为它具有
A. 还原性 B. 吸附性 C. 稳定性 D. 可燃性
7.能使气体物质溶解度增大的操作是
A. 增加溶剂 B. 振荡溶液 C. 增大压强 D. 升高温
度
8.如图所示的实验操作正确的是( )
A. 倾倒液体B. 加热液体
C. 量取液体
D. 吸取液体
9.关于分子、原子说法正确的是
A. 分子可分,原子不可再分 B. 分子的质量大于原子
C. 温度越高,分子运动速率越快 D. 温度升高,分子体积增大
10.关于“胆矾”说法错误的是
A. 颜色:蓝色 B. 类别:化合物
C. 化学式:CuSO ∙5H O D. 作用:检验水
4 2
11.化学方程式与事实相符且正确的是
A. 4Fe+3O 2Fe O B. CuO+C Cu+CO↑
2 2 3
C. CuSO +2NaOH=Na SO +Cu(OH) ↓ D. CO +Ca(OH) =CaCO +H O
4 2 4 2 2 2 3 2
12.城市污水经深度净化处理后的水统称“中水”,因为水质介于自来水(上水)与排入管
道的污水(下水)之间,故名为“中水”,说法正确的是
A. “中水”是一种饮用水
B. 利用“中水”有利于节约水资源
C. “中水”中水分子的构成与蒸馏水中水分子的构成不同
D. 将生活污水净化处理成“中水”的过程中要过滤、吸附和蒸馏
13.2019 年锂电池的研究荣获了诺贝尔化学奖,“锂-空气”电池是锂电池的一种,它在无水电解质中反应的原理:2Li+O LiO,说法错误的是
2 2 2
A. 充电时,反应为分解反应 B. 充电时,氧元素由游离态变为化
合态
C. 放电时,反应为化合反应 D. 放电时,发生 是的氧化反应
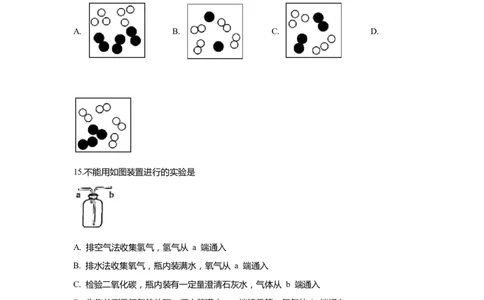
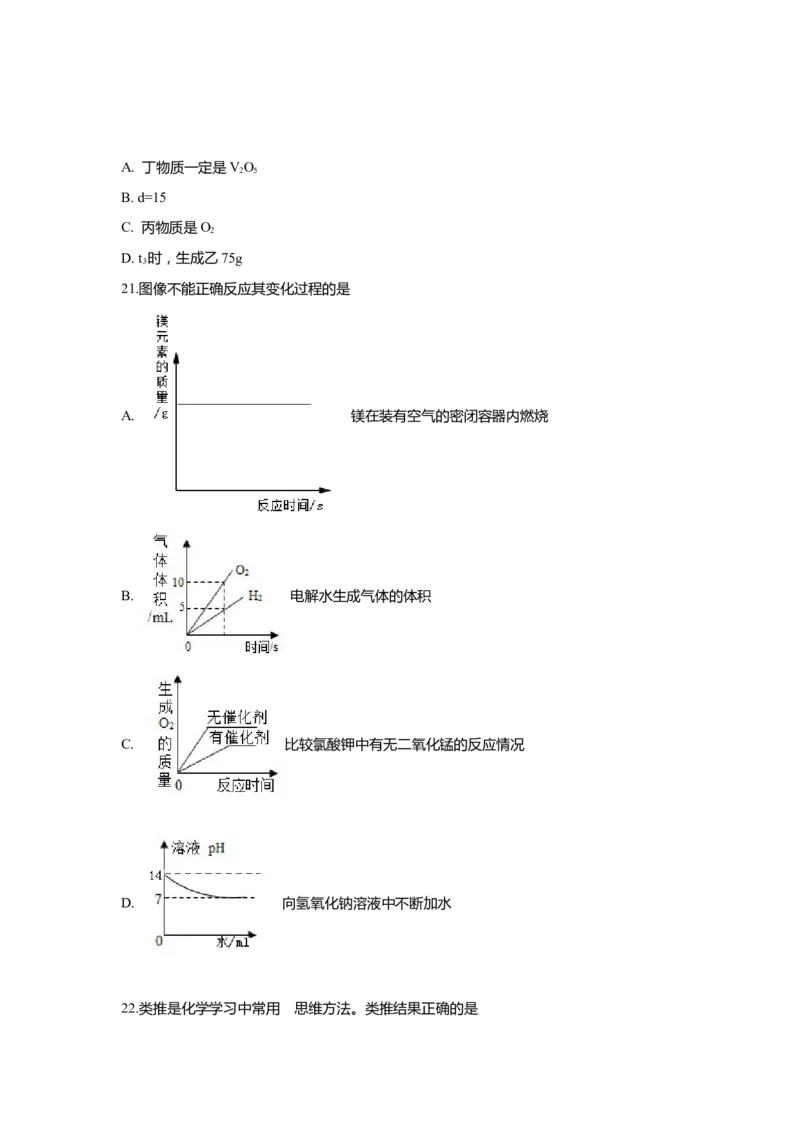
14.下图白球代表氢原子,黑球代表氦原子,表示等质量氢气与氦气 的混合气体是
A. B. C. D.
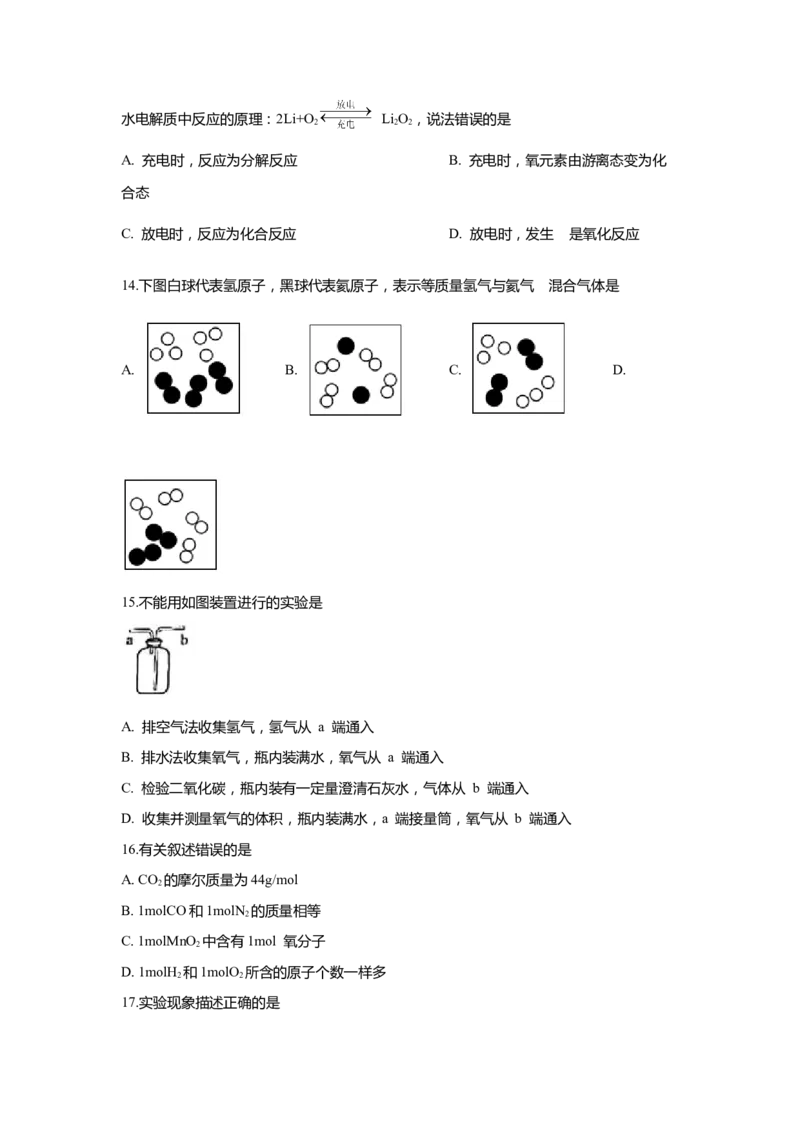
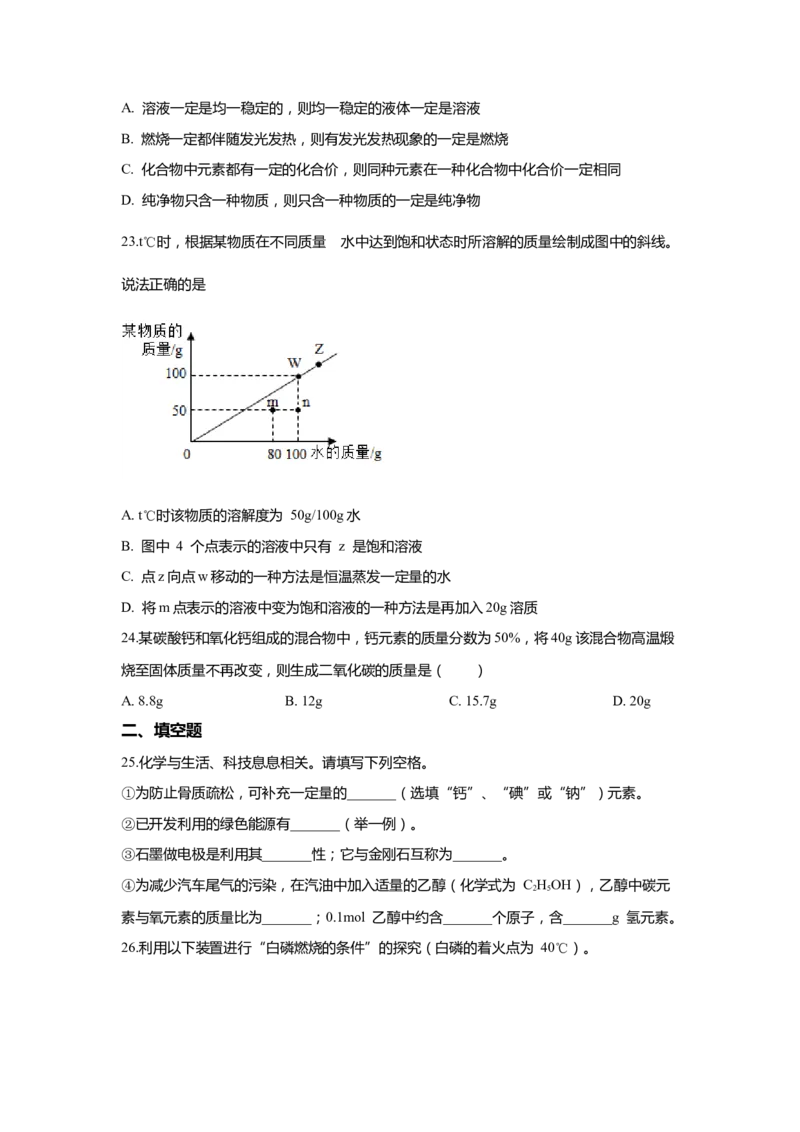
15.不能用如图装置进行的实验是
A. 排空气法收集氢气,氢气从 a 端通入
B. 排水法收集氧气,瓶内装满水,氧气从 a 端通入
C. 检验二氧化碳,瓶内装有一定量澄清石灰水,气体从 b 端通入
D. 收集并测量氧气的体积,瓶内装满水,a 端接量筒,氧气从 b 端通入
16.有关叙述错误的是
A. CO 的摩尔质量为44g/mol
2
B. 1molCO和1molN 的质量相等
2
C. 1molMnO 中含有1mol 氧分子
2
D. 1molH 和1molO 所含的原子个数一样多
2 2
17.实验现象描述正确的是A. 在空气中点燃镁条,发出耀眼的白光,生成白色氧化镁
B. 将红热的铁丝放在空气中,剧烈燃烧,火星四射,生成黑色固体
C. 硫在氧气中燃烧产生明亮的蓝紫色火焰,生成无色无味的气体
D. 木炭在氧气中燃烧,发出白光,放出热量,产生能使澄清石灰石变浑浊的气体
18.推理错误的是
选项 化学反应 影响化学反应的因素
A 镁能与二氧化碳反应,铁不能与二氧化碳反应 反应物的性质
通常木炭充分燃烧生成二氧化碳,不充分燃烧生成一氧化
B 反应温度
碳
C 硫在氧气中比在空气中燃烧更剧烈 反应物的浓度
D 加热氯酸钾反应速率较慢,加入二氧化锰后速度加快 催化剂
A. A B. B C. C D. D
19.说法正确的是
A. 含有一种元素的纯净物是单质
B. 由不同种元素组成的物质是化合物
C. 物质与氧气发生反应时都需要点燃
D. 能生成多种物质的反应是分解反应
20.工业中合成SO 的反应:2SO +O 2SO 。一定条件下,在一密闭容器内投入 SO 、
3 2 2 3 2
O、SO 、VO 四种物质,在不同时刻测得各物质的质量(单位为 g)如下表所示。说法
2 3 2 5
错误的是
甲 乙 丙 丁
t1 100 5 80 5
t2 60 55 a b
t3 40 c d 5A. 丁物质一定是VO
2 5
B. d=15
C. 丙物质是O
2
D. t 时,生成乙75g
3
21.图像不能正确反应其变化过程的是
A. 镁在装有空气的密闭容器内燃烧
B. 电解水生成气体的体积
C. 比较氯酸钾中有无二氧化锰的反应情况
D. 向氢氧化钠溶液中不断加水
22.类推是化学学习中常用 的思维方法。类推结果正确的是A. 溶液一定是均一稳定的,则均一稳定的液体一定是溶液
B. 燃烧一定都伴随发光发热,则有发光发热现象的一定是燃烧
C. 化合物中元素都有一定的化合价,则同种元素在一种化合物中化合价一定相同
D. 纯净物只含一种物质,则只含一种物质的一定是纯净物
23.t℃时,根据某物质在不同质量 的水中达到饱和状态时所溶解的质量绘制成图中的斜线。
说法正确的是
A. t℃时该物质的溶解度为 50g/100g水
B. 图中 4 个点表示的溶液中只有 z 是饱和溶液
C. 点z向点w移动的一种方法是恒温蒸发一定量的水
D. 将m点表示的溶液中变为饱和溶液的一种方法是再加入20g溶质
24.某碳酸钙和氧化钙组成的混合物中,钙元素的质量分数为50%,将40g该混合物高温煅
烧至固体质量不再改变,则生成二氧化碳的质量是( )
A. 8.8g B. 12g C. 15.7g D. 20g
二、填空题
25.化学与生活、科技息息相关。请填写下列空格。
①为防止骨质疏松,可补充一定量的_______(选填“钙”、“碘”或“钠”)元素。
②已开发利用的绿色能源有_______(举一例)。
③石墨做电极是利用其_______性;它与金刚石互称为_______。
④为减少汽车尾气的污染,在汽油中加入适量的乙醇(化学式为 C HOH),乙醇中碳元
2 5
素与氧元素的质量比为_______;0.1mol 乙醇中约含_______个原子,含_______g 氢元素。
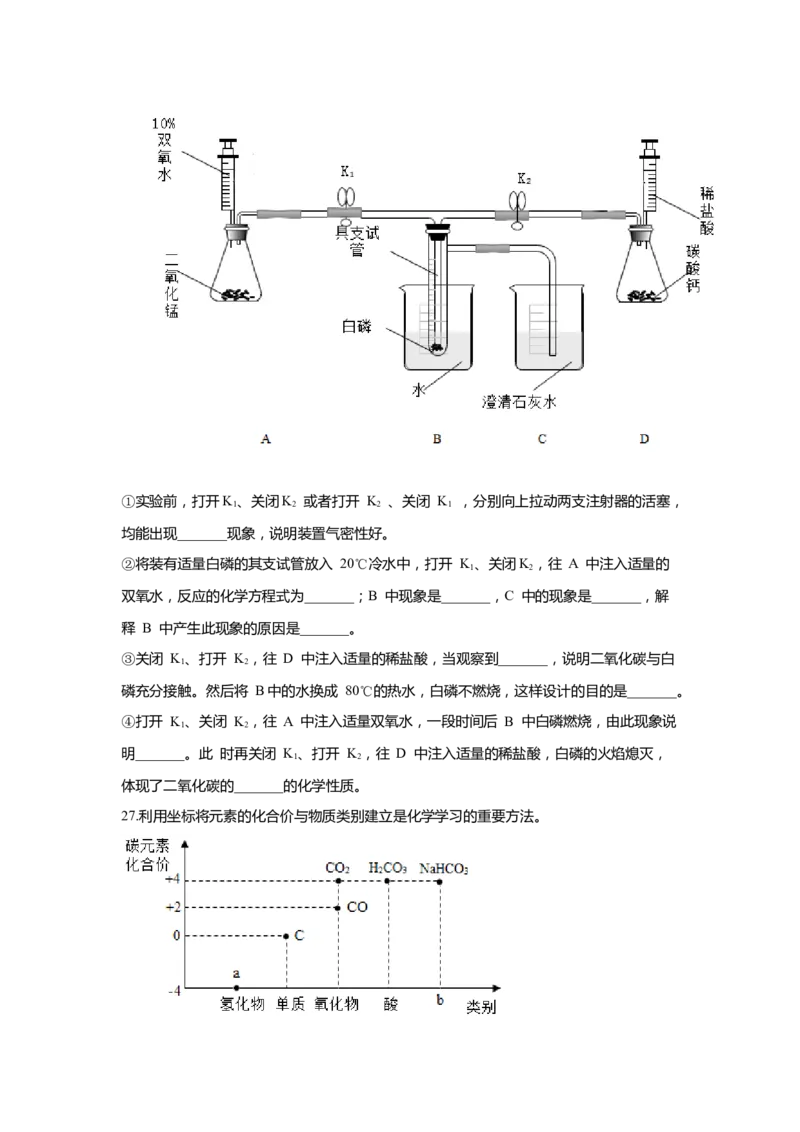
26.利用以下装置进行“白磷燃烧的条件”的探究(白磷的着火点为 40℃)。①实验前,打开K、关闭K 或者打开 K 、关闭 K ,分别向上拉动两支注射器的活塞,
1 2 2 1
均能出现_______现象,说明装置气密性好。
②将装有适量白磷的其支试管放入 20℃冷水中,打开 K、关闭K,往 A 中注入适量的
1 2
双氧水,反应的化学方程式为_______;B 中现象是_______,C 中的现象是_______,解
释 B 中产生此现象的原因是_______。
③关闭 K、打开 K,往 D 中注入适量的稀盐酸,当观察到_______,说明二氧化碳与白
1 2
磷充分接触。然后将 B中的水换成 80℃的热水,白磷不燃烧,这样设计的目的是_______。
④打开 K、关闭 K,往 A 中注入适量双氧水,一段时间后 B 中白磷燃烧,由此现象说
1 2
明_______。此 时再关闭 K、打开 K,往 D 中注入适量的稀盐酸,白磷的火焰熄灭,
1 2
体现了二氧化碳的_______的化学性质。
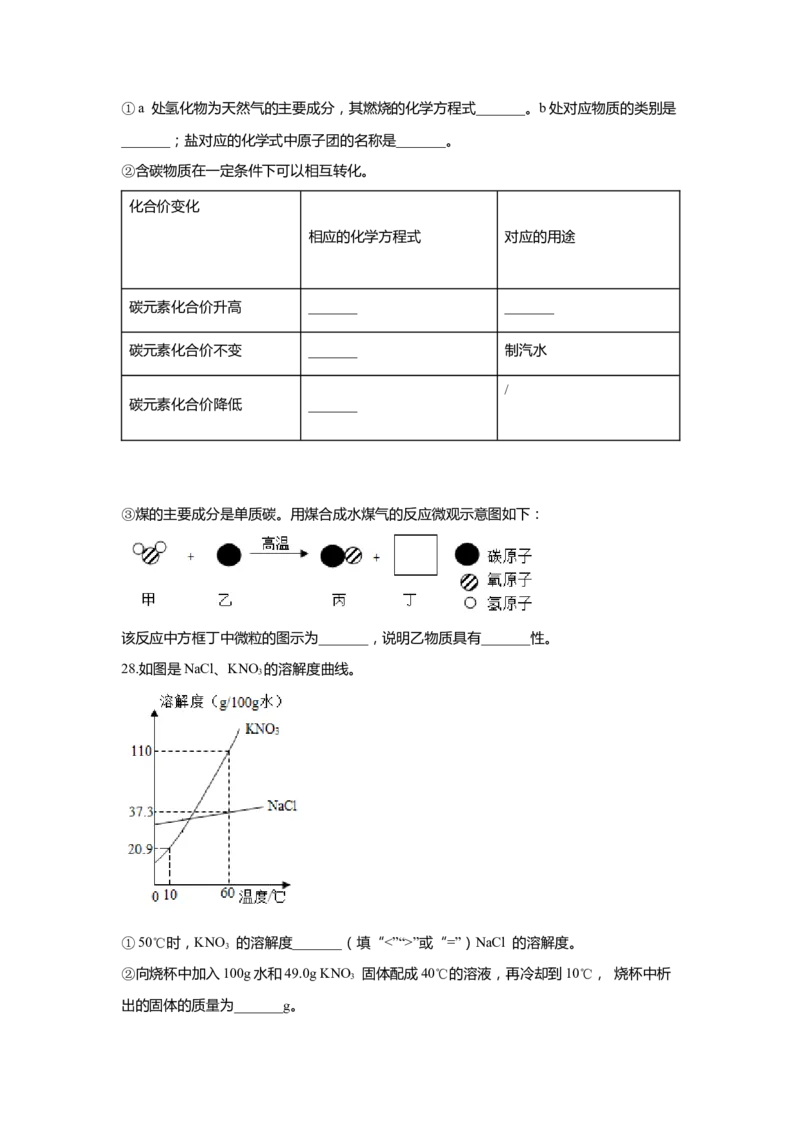
27.利用坐标将元素的化合价与物质类别建立是化学学习的重要方法。①a 处氢化物为天然气的主要成分,其燃烧的化学方程式_______。b处对应物质的类别是
_______;盐对应的化学式中原子团的名称是_______。
②含碳物质在一定条件下可以相互转化。
化合价变化
相应的化学方程式 对应的用途
碳元素化合价升高 _______ _______
碳元素化合价不变 _______ 制汽水
/
碳元素化合价降低 _______
③煤的主要成分是单质碳。用煤合成水煤气的反应微观示意图如下:
该反应中方框丁中微粒的图示为_______,说明乙物质具有_______性。
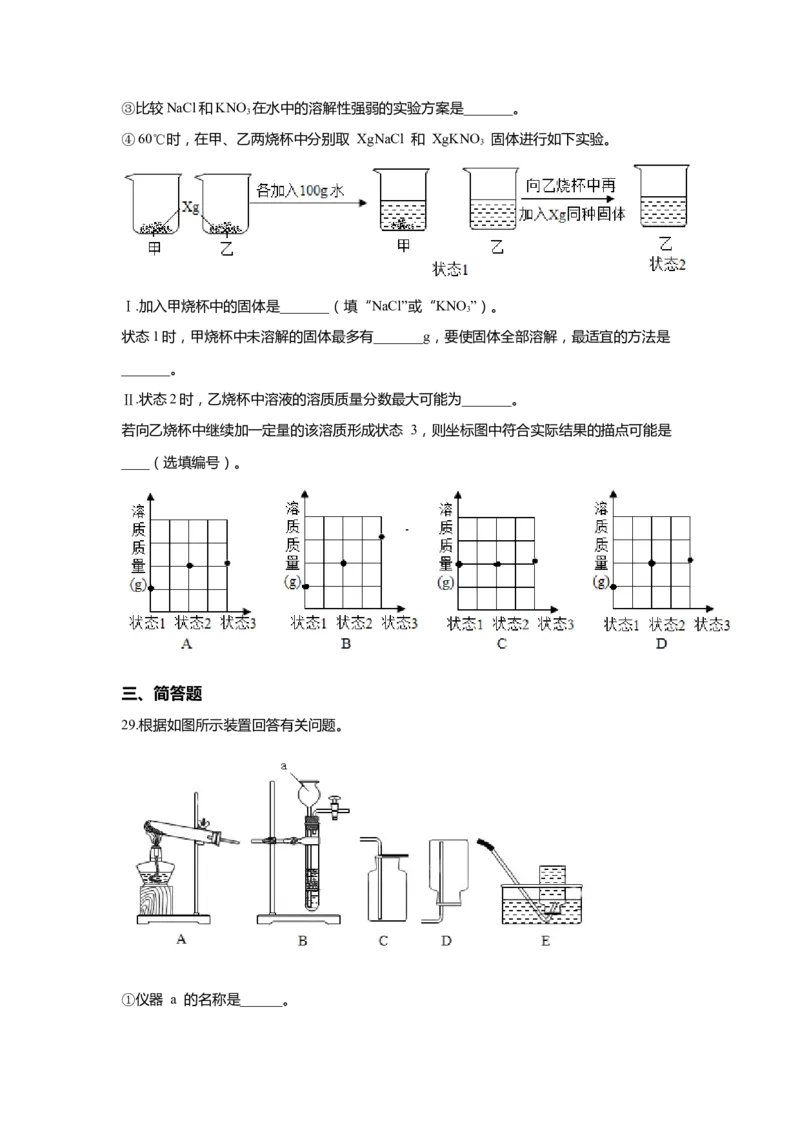
28.如图是NaCl、KNO 的溶解度曲线。
3
①50℃时,KNO 的溶解度_______(填“<”“>”或“=”)NaCl 的溶解度。
3
②向烧杯中加入100g水和49.0g KNO 固体配成40℃的溶液,再冷却到10℃, 烧杯中析
3
出的固体的质量为_______g。③比较NaCl和KNO 在水中的溶解性强弱的实验方案是_______。
3
④60℃时,在甲、乙两烧杯中分别取 XgNaCl 和 XgKNO 固体进行如下实验。
3
Ⅰ.加入甲烧杯中的固体是_______(填“NaCl”或“KNO”)。
3
状态1时,甲烧杯中未溶解的固体最多有_______g,要使固体全部溶解,最适宜的方法是
_______。
Ⅱ.状态2时,乙烧杯中溶液的溶质质量分数最大可能为_______。
若向乙烧杯中继续加一定量的该溶质形成状态 3,则坐标图中符合实际结果的描点可能是
____(选填编号)。
三、简答题
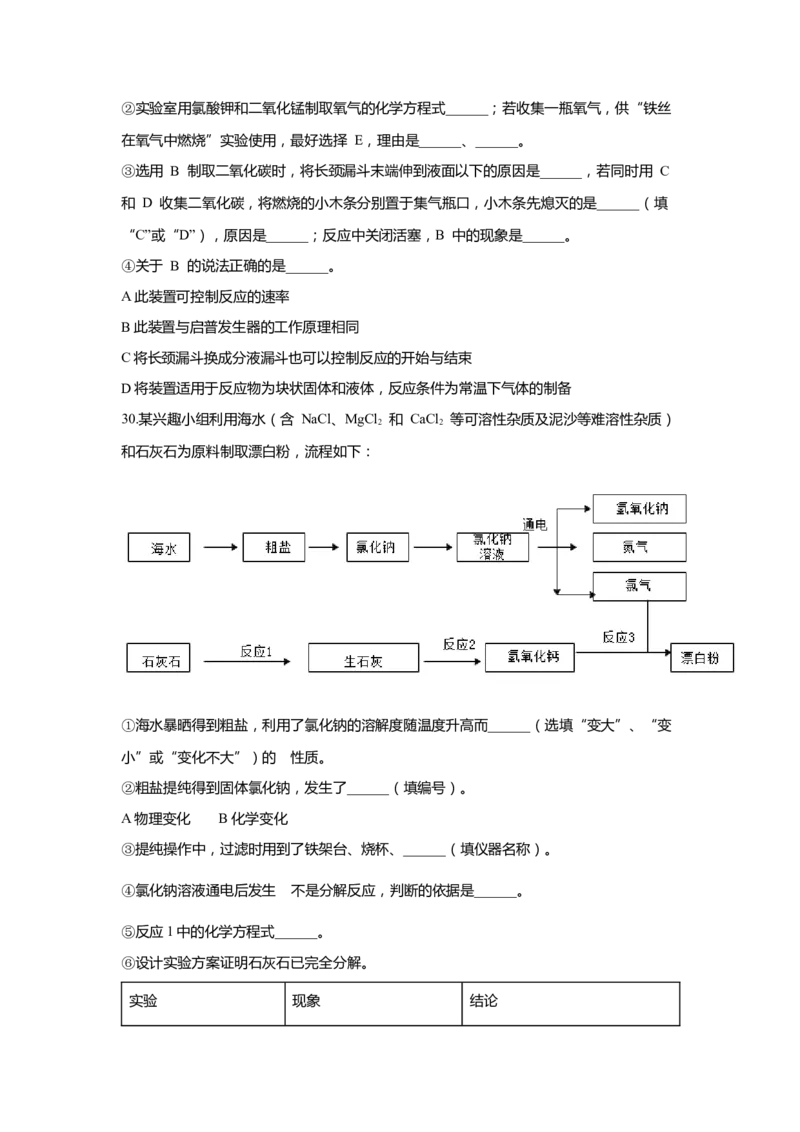
29.根据如图所示装置回答有关问题。
①仪器 a 的名称是______。②实验室用氯酸钾和二氧化锰制取氧气的化学方程式______;若收集一瓶氧气,供“铁丝
在氧气中燃烧”实验使用,最好选择 E,理由是______、______。
③选用 B 制取二氧化碳时,将长颈漏斗末端伸到液面以下的原因是______,若同时用 C
和 D 收集二氧化碳,将燃烧的小木条分别置于集气瓶口,小木条先熄灭的是______(填
“C”或“D”),原因是______;反应中关闭活塞,B 中的现象是______。
④关于 B 的说法正确的是______。
A此装置可控制反应的速率
B此装置与启普发生器的工作原理相同
C将长颈漏斗换成分液漏斗也可以控制反应的开始与结束
D将装置适用于反应物为块状固体和液体,反应条件为常温下气体的制备
30.某兴趣小组利用海水(含 NaCl、MgCl 和 CaCl 等可溶性杂质及泥沙等难溶性杂质)
2 2
和石灰石为原料制取漂白粉,流程如下:
①海水暴晒得到粗盐,利用了氯化钠的溶解度随温度升高而______(选填“变大”、“变
小”或“变化不大”)的 性质。
②粗盐提纯得到固体氯化钠,发生了______(填编号)。
A物理变化 B化学变化
③提纯操作中,过滤时用到了铁架台、烧杯、______(填仪器名称)。
④氯化钠溶液通电后发生 不的是分解反应,判断的依据是______。
⑤反应1中的化学方程式______。
⑥设计实验方案证明石灰石已完全分解。
实验 现象 结论______ ________
石灰石已完全分解
⑦实际工业生产中,反应3化学方程式:2Ca(OH) +2Cl=CaCl +Ca(ClO) +2X,X 的化学式
2 2 2 2
为______,Ca(ClO) 中氯元素的化合价为______,反应物氢氧化钙最好用______(填“饱
2
和石灰水”或“石灰乳”)并不断搅拌。
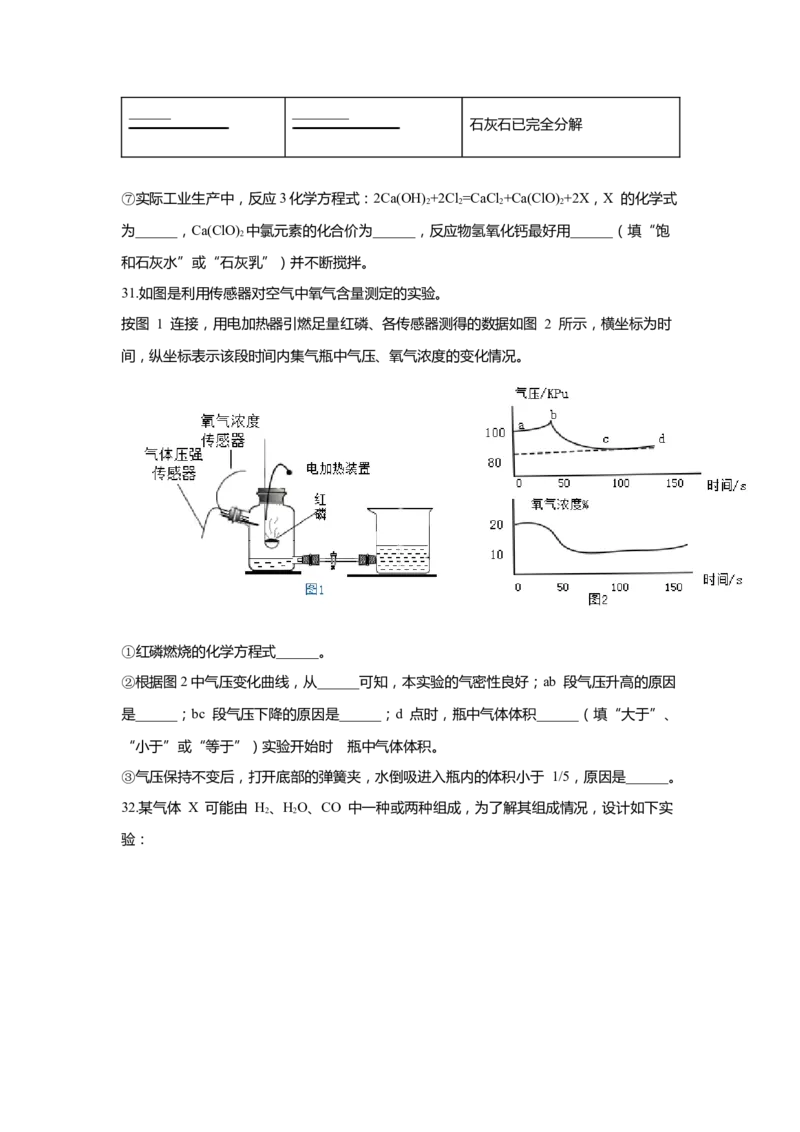
31.如图是利用传感器对空气中氧气含量测定的实验。
按图 1 连接,用电加热器引燃足量红磷、各传感器测得的数据如图 2 所示,横坐标为时
间,纵坐标表示该段时间内集气瓶中气压、氧气浓度的变化情况。
①红磷燃烧的化学方程式______。
②根据图2中气压变化曲线,从______可知,本实验的气密性良好;ab 段气压升高的原因
是______;bc 段气压下降的原因是______;d 点时,瓶中气体体积______(填“大于”、
“小于”或“等于”)实验开始时 瓶中气体体积。
③气压保持不变后,打开底部的弹簧夹,水倒吸进入瓶内的体积小于 1/5,原因是______。
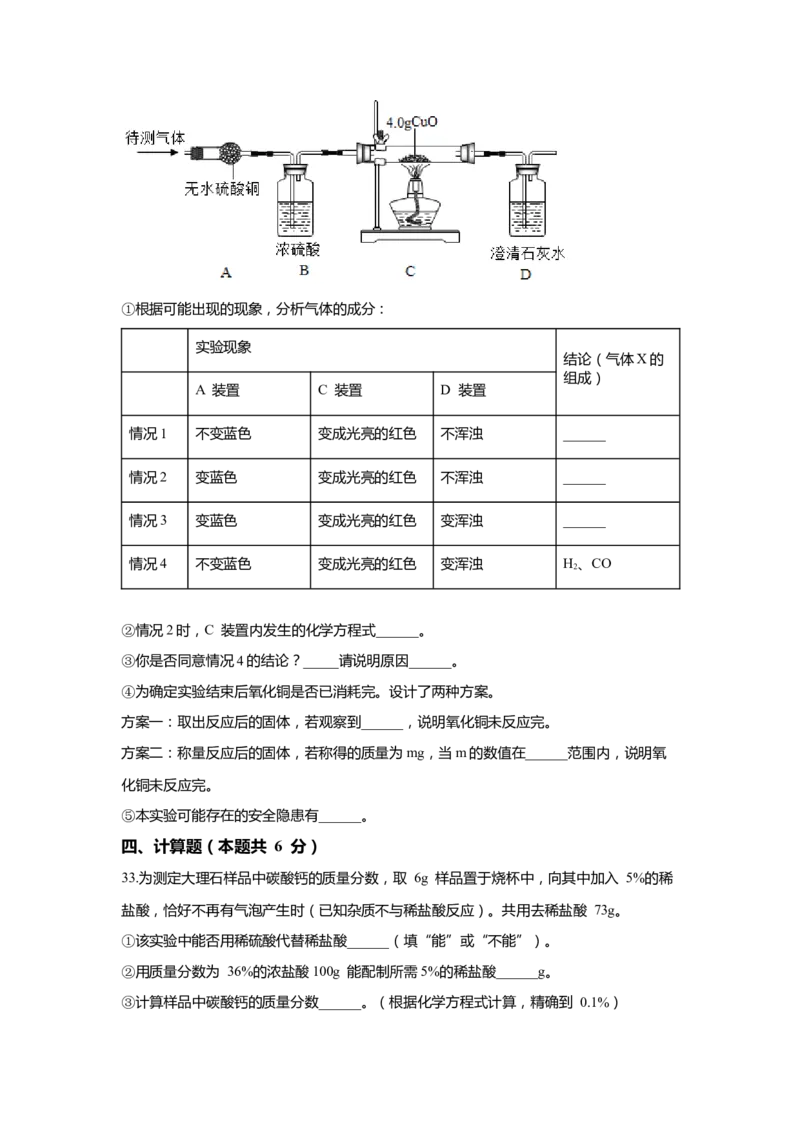
32.某气体 X 可能由 H、HO、CO 中一种或两种组成,为了解其组成情况,设计如下实
2 2
验:①根据可能出现的现象,分析气体的成分:
实验现象
结论(气体X的
组成)
A 装置 C 装置 D 装置
情况1 不变蓝色 变成光亮的红色 不浑浊 ______
情况2 变蓝色 变成光亮的红色 不浑浊 ______
情况3 变蓝色 变成光亮的红色 变浑浊 ______
情况4 不变蓝色 变成光亮的红色 变浑浊 H、CO
2
②情况2时,C 装置内发生的化学方程式______。
③你是否同意情况4的结论?_____请说明原因______。
④为确定实验结束后氧化铜是否已消耗完。设计了两种方案。
方案一:取出反应后的固体,若观察到______,说明氧化铜未反应完。
方案二:称量反应后的固体,若称得的质量为mg,当m的数值在______范围内,说明氧
化铜未反应完。
⑤本实验可能存在的安全隐患有______。
四、计算题(本题共 6 分)
33.为测定大理石样品中碳酸钙的质量分数,取 6g 样品置于烧杯中,向其中加入 5%的稀
盐酸,恰好不再有气泡产生时(已知杂质不与稀盐酸反应)。共用去稀盐酸 73g。
①该实验中能否用稀硫酸代替稀盐酸______(填“能”或“不能”)。
②用质量分数为 36%的浓盐酸100g 能配制所需5%的稀盐酸______g。
③计算样品中碳酸钙的质量分数______。(根据化学方程式计算,精确到 0.1%)