文档内容
长宁区 2021~2022 学年第一学期教学质量调研试卷
九年级理化(化学部分)答案解析版
相对原子质量:H-1 O-16 C-12
五、选择题(共 20 分)21~34 题每题均只有 1 个正确选项
1. 不能改善空气质量的措施是
A. 推广清洁能源 B. 汽车尾气净化 C. 控制工地扬尘 D. 使用空气香薰
【答案】D
【解析】
【分析】
【详解】A、推广清洁能源,可以减少化石燃料的使用,减少污染物的排放,保护环境,不符合题意;
B、汽车尾气净化,可以减少污染物的排放,保护环境,不符合题意;
C、控制工地扬尘,可以减少可吸入颗粒物的排放,保护环境,不符合题意;
D、使用空气香薰,不能改善空气质量,反而空气香薰中的有毒物质会污染环境,符合题意。
故选D。
2. 氢元素符号书写正确的是
A. N B. Ne C. H D. He
【答案】C
【解析】
【分析】根据元素符号的书写方法,第一个字母要大写,第二个字母要小写。
【详解】A、N为氮元素符号,选项不符合题意;
B、Ne为氖元素符号,选项不符合题意;
C、H为氢元素符号,选项符合题意;
D、He为氦元素符号,选项不符合题意。
故选C。
3. 空气中含量最多的成分是
A. 氧气 B. 氮气 C. 氖气 D. 二氧化碳
【答案】B
【解析】
【分析】【详解】空气中含量最多的成分是氮气,约占空气体积的78%。
故选B。
4. SO 中硫元素的化合价是
2
A. +1 B. +2 C. +3 D. +4
【答案】D
【解析】
【详解】SO 中氧元素化合价为-2价,设硫元素化合价为x,根据化合物中正负化合价代数为0,则有x+
2
(-2)×2=0,得x=+4价,故选D。
5. 属于碳的化学性质的是
A. 还原性 B. 导电性 C. 导热性 D. 吸附性
【答案】A
【解析】
【分析】
【详解】物质在化学变化中表现出来的性质属化学性质,如可燃性、还原性、氧化性等,导电性、导热性、
吸附性,不需要发生化学变化就能体现的性质,属于物理性质,故选:A。
【点睛】
6. 自来水生产中,能起到杀菌消毒作用的试剂是
A. 活性炭 B. 氯气 C. 砂石 D. 明矾
【答案】B
【解析】
的
【详解】A、活性炭具有吸附作用,可以吸附水中 色素和异味,没有杀菌消毒作用,不符合题意;
B、氯气与水反应生成的次氯酸具有强氧化性,能杀灭微生物,有杀菌消毒作用,符合题意;
C、自来水生产过程中砂石起到过滤作用,没有杀菌消毒的作用,不符合题意;
D、明矾溶于水生成的胶状物,对悬浮于水中的不溶物有吸附作用,能使不溶物沉降,没有杀菌消毒作用,
不符合题意。
故选:B。
7. NaCO 中原子团的名称是
2 3
A. 三氧化碳 B. 碳酸 C. 碳酸根 D. 碳氧根
【答案】C
【解析】【详解】NaCO 中原子团的名称碳酸根,故选C。
2 3
8. 属于分解反应的是
A. 煅烧大理石 B. 硫的燃烧
C. 向生石灰中滴加水 D. 加热木炭与氧化铜的混合物
【答案】A
【解析】
【分析】
【详解】A、煅烧大理石是碳酸钙高温煅烧生成氧化钙和二氧化碳,该反应符合“一变多”的特点,属于
分解反应,符合题意;
B、硫燃烧生成二氧化硫,该反应符合“多变一”的特点,属于化合反应,不符合题意;
C、向生石灰中滴加水,氧化钙和水反应生成氢氧化钙,该反应符合“多变一”的特点,属于化合反应,
不符合题意;
D、加热木炭与氧化铜的混合物,木炭和氧化铜在高温条件下反应生成铜和二氧化碳,该反应符合“一种
单质与一种化合物反应生成另一种单质和另一种化合物”的反应,属于置换反应,不符合题意。
故选A。
9. 一定能增大二氧化碳在水中溶解度的操作是
A. 边升温边加压 B. 边降温边加压
C. 边升温边减压 D. 边降温边减压
【答案】B
【解析】
【详解】A、对气体来说压强越大溶解度越大,温度越高溶解度越小,故选项操作不正确;
B、加压会使二氧化碳溶解度增大,降温也会使其溶解度增大,故选项操作正确;
C、升温和减压都会使二氧化碳的溶解度变小,故选项操作不正确;
D、降温会使其溶解度增大,减压会使二氧化碳的溶解度变小,故选项操作不正确。
故选B。
10. 室温下,将 pH 为 12 的澄清石灰水敞口放置一段时间后,溶液的 pH 变化可能是
A. 变小为 10 B. 变小为 2 C. 基本不变 D. 变大为 13
【答案】A
【解析】
【详解】澄清石灰水敞口放置一段时间,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,溶液的碱性减弱,
pH将变小,但pH不会小于7,故选A。11. 为了使酒精充分燃烧,做法错误的是
A. 用纯氧替代空气 B. 使用固体酒精
C. 将酒精加热为酒精蒸气 D. 将酒精喷成雾状
【答案】B
【解析】
【分析】
【详解】A、用纯氧代替氧气,增加了氧气的量,能够使酒精充分燃烧,故选项正确;
的
B、使用固体酒精减少了氧气与酒精 接触面积,不利于酒精的充分燃烧,故选项错误;
C、酒精加热为酒精蒸气,使酒精与氧气接触面积增大,有利于酒精充分燃烧,故选项正确;
D、酒精喷成雾状,使酒精与氧气接触面积增大,有利于酒精充分燃烧,故选项正确。
故选B。
12. 由一种分子构成的物质不可能是
A. 单质 B. 化合物 C. 混合物 D. 氧化物
【答案】C
【解析】
【
分析】
【详解】A、单质是由一种元素组成的纯净物,可能是分子或原子构成,故选项不符合题意;
B、化合物是由多种元素组成的,可能是由分子或原子或离子构成,故选项不符合题意;
C、由一种分子构成的一定是纯净物,不可能是混合物,故选项符合题意;
D、氧化物可能有一种分子构成,如二氧化碳等,故选项不符合题意。
故选C。
13. 关于实验室制取氧气的操作,描述正确的是
A. 分别取等量的氯酸钾和二氧化锰,依次加入到试管底部并混合均匀
B. 由上至下,从右向左组装仪器
C. 集气瓶装满水,倒放在水槽中,并将导管伸入集气瓶中
D. 反应停止后,先将导管从水槽中取出,再熄灭酒精灯
【答案】D
【解析】
【详解】A、分别取等量的氯酸钾和二氧化锰,先将两者混合均匀后,再加入到试管底部,故选项描述不正确;
B、组装仪器顺序要从下到上,从左到右,实验完毕撤装置时正好相反,应从右到左,从上到下,故选项
描述不正确;
C、集气瓶装满水,倒放在水槽中,等到气泡连续均匀冒出时,才能将导管伸入集气瓶中,故选项描述不
正确;
D、反应停止后,先将导管从水槽中取出,再熄灭酒精灯,防止水倒吸,炸裂试管,故选项描述正确。
故选D。
14. 关于相对原子质量说法正确的是
A. 相对原子质量的单位是 kg
B. 相对原子质量是一个比值,单位是 g
C. 某原子的相对原子质量在数值上是该原子的实际质量的 12 倍
D. 相对原子质量越大,原子的实际质量也越大
【答案】D
【解析】
【分析】
【详解】A、相对原子质量是一个比值,单位为“1”,不是kg,不符合题意;
B、相对原子质量是一个比值,单位为“1”,不是g,不符合题意;
C、某种原子的相对原子量就等于该原子的实际质量与一种C-12原子的实际质量的1/12相比所得到的比值,
不符合题意;
D、原子的实际质量与相对原子质量呈正比,相对原子质量越大,原子的实际质量也越大,符合题意。
故选D。
35~37 每题均有 1~2 个正确选项
15. 对金刚石和石墨描述正确的是
A. 碳元素都以游离态存在
B. 碳元素都以化合态存在
C. 化学性质相同是由于碳原子排列结构相似
D. 物理性质不同是由于碳原子排列结构不同
【答案】AD
【解析】
【详解】A、金刚石和石墨都是碳元素的单质,碳元素都以游离态存在,故选项描述正确;
B、由A分析可知,碳元素都以游离态存在,故选项描述不正确;C、金刚石和石墨化学性质相同是由于碳原子的原子结构相同,故选项描述不正确;
D、金刚石和石墨物理性质不同是由于碳原子的排列方式不同,故选项描述正确。
故选AD。
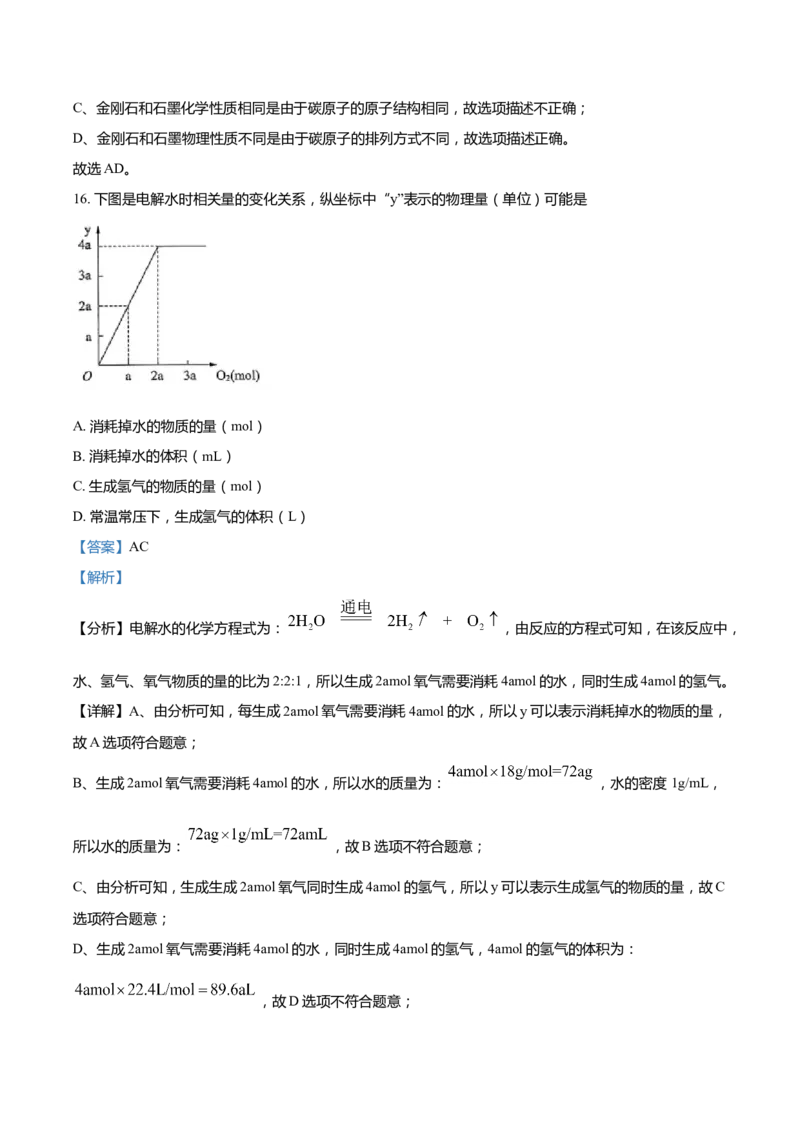
16. 下图是电解水时相关量的变化关系,纵坐标中“y”表示的物理量(单位)可能是
A. 消耗掉水的物质的量(mol)
B. 消耗掉水的体积(mL)
C. 生成氢气的物质的量(mol)
D. 常温常压下,生成氢气的体积(L)
【答案】AC
【解析】
【分析】电解水的化学方程式为: ,由反应的方程式可知,在该反应中,
水、氢气、氧气物质的量的比为2:2:1,所以生成2amol氧气需要消耗4amol的水,同时生成4amol的氢气。
【详解】A、由分析可知,每生成2amol氧气需要消耗4amol的水,所以y可以表示消耗掉水的物质的量,
故A选项符合题意;
B、生成2amol氧气需要消耗4amol的水,所以水的质量为: ,水的密度 1g/mL,
所以水的质量为: ,故B选项不符合题意;
C、由分析可知,生成生成2amol氧气同时生成4amol的氢气,所以y可以表示生成氢气的物质的量,故C
选项符合题意;
D、生成2amol氧气需要消耗4amol的水,同时生成4amol的氢气,4amol的氢气的体积为:
,故D选项不符合题意;故选AC。
17. 实验室二氧化锰中可能含有炭粉,若直接与大量氯酸钾加热,炭粉在大量氧气中燃烧,引起爆炸,上
述反应的化学方程式可能是
A. 8KClO+MnO+12C 8KCl+12CO ↑+MnO
3 2 2 2
B. 8KClO+2C 8KCl+2CO↑+11O ↑
3 2
C. 8KClO+C 8KCl+CO ↑+11O ↑
3 2 2
D. 8KClO+15C 8KCl+9CO ↑+6CO↑
3 2
【答案】C
【解析】
【分析】
【详解】氯酸钾在二氧化锰的催化下受热分解生成氯化钾和氧气,碳在充足的氧气中燃烧生成二氧化碳,
氧气过量,故该反应可能是氯酸钾和碳在加热的条件下反应生成氯化钾、二氧化碳和氧气,即:
。
故选C。
六、简答题
18. 我国科学家首次在实验室实现了二氧化碳到淀粉的从头合成;
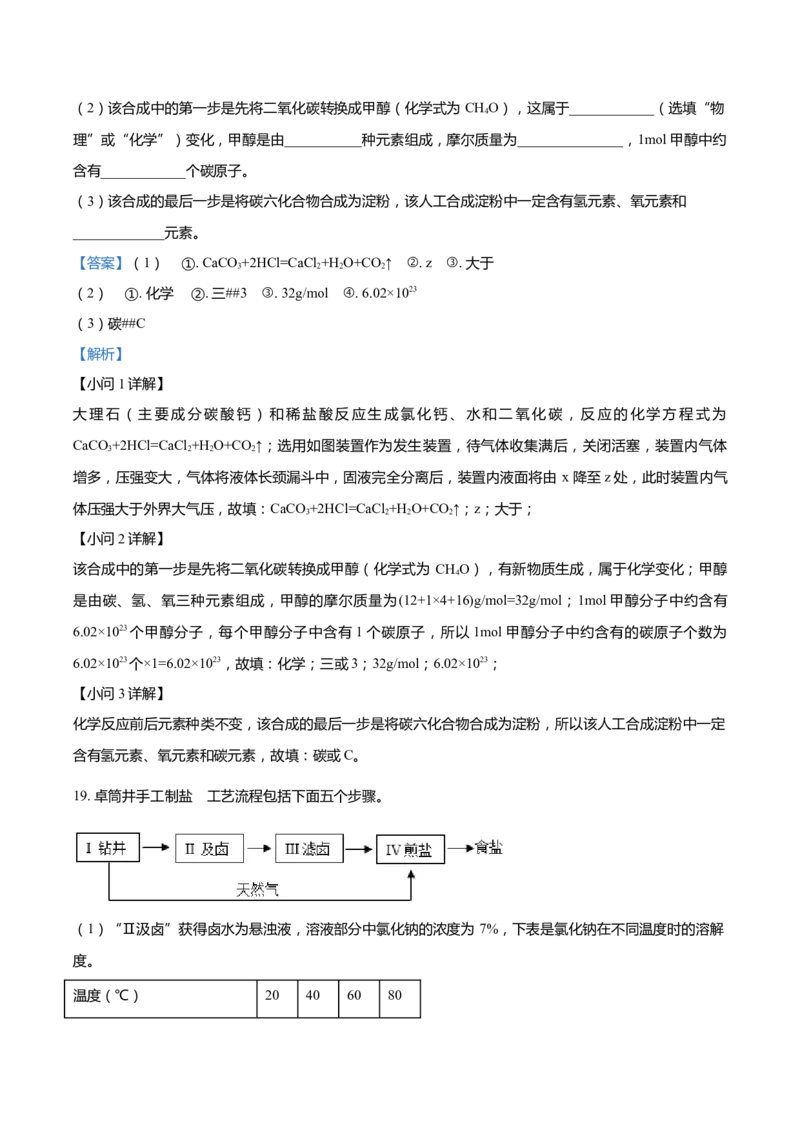
(1)实验室常用块状大理石与稀盐酸制备二氧化碳,该反应的化学方程式是_____________。选用如图装
置作为发生装置,待气体收集满后,关闭活塞,装置内液面将由 x 降至_____________处(选填“y”或
“z”),此时装置内气体压强_____________外界大气压(选填“大于”、“等于”或“小于”)。(2)该合成中的第一步是先将二氧化碳转换成甲醇(化学式为 CHO),这属于____________(选填“物
4
理”或“化学”)变化,甲醇是由___________种元素组成,摩尔质量为_______________,1mol 甲醇中约
含有____________个碳原子。
(3)该合成的最后一步是将碳六化合物合成为淀粉,该人工合成淀粉中一定含有氢元素、氧元素和
_____________元素。
【答案】(1) ①. CaCO +2HCl=CaCl +H O+CO↑ ②. z ③. 大于
3 2 2 2
(2) ①. 化学 ②. 三##3 ③. 32g/mol ④. 6.02×1023
(3)碳##C
【解析】
【小问1详解】
大理石(主要成分碳酸钙)和稀盐酸反应生成氯化钙、水和二氧化碳,反应的化学方程式为
CaCO +2HCl=CaCl +H O+CO↑;选用如图装置作为发生装置,待气体收集满后,关闭活塞,装置内气体
3 2 2 2
增多,压强变大,气体将液体长颈漏斗中,固液完全分离后,装置内液面将由 x 降至z处,此时装置内气
体压强大于外界大气压,故填:CaCO +2HCl=CaCl +H O+CO↑;z;大于;
3 2 2 2
【小问2详解】
该合成中的第一步是先将二氧化碳转换成甲醇(化学式为 CHO),有新物质生成,属于化学变化;甲醇
4
是由碳、氢、氧三种元素组成,甲醇的摩尔质量为(12+1×4+16)g/mol=32g/mol;1mol甲醇分子中约含有
6.02×1023个甲醇分子,每个甲醇分子中含有1个碳原子,所以1mol甲醇分子中约含有的碳原子个数为
6.02×1023个×1=6.02×1023,故填:化学;三或3;32g/mol;6.02×1023;
【小问3详解】
化学反应前后元素种类不变,该合成的最后一步是将碳六化合物合成为淀粉,所以该人工合成淀粉中一定
含有氢元素、氧元素和碳元素,故填:碳或C。
的
19. 卓筒井手工制盐 工艺流程包括下面五个步骤。
(1)“Ⅱ汲卤”获得卤水为悬浊液,溶液部分中氯化钠的浓度为 7%,下表是氯化钠在不同温度时的溶解
度。
温度(℃) 20 40 60 80氯化钠的溶解度(g/100g
36.0 36.6 37.3 38.4
水)
根据表中数据可得出:20℃时,氯化钠溶解度为____________,该卤水的溶液部分是氯化钠的
______________(选填“饱和”或“不饱和”)溶液。
(2)“Ⅲ滤卤”与实验操作过滤的原理一样,其目的是为了分离溶液和____________。
(3)“Ⅳ煎盐”用井中产生的天然气作为燃料,加热滴水除去其中的溶剂,CH 燃烧的化学方程式是
4
___________,该步骤和实验操作_______________(选填“降温结晶”或“蒸发结晶”)的原理相似。
(4)当地人利用工具将卤水在室外风吹日晒一段时间后,浓度可提高至 17%,该步骤称为“晒卤”,应
位于步骤_______________(选填“Ⅱ”、“Ⅲ”或“Ⅳ”)之后,请比较卓筒井手工制盐中“晒卤”和
“煎盐”,两者的原理有何相似之处和不同之处________________。
【答案】(1) ①. 36.0g ②. 不饱和 (2)难溶性杂质
(3) ①.
②. 蒸发结晶
(4) ①. Ⅱ ②. 均利用了蒸发浓缩的原理,但是“晒卤”只是提高了浓度,“煎盐”还利用了结晶原
理
【解析】
【分析】
【小问1详解】
由表可知,20℃时,氯化钠溶解度为36.0g;
20℃时,氯化钠饱和溶液的溶质质量分数为: ,故该卤水的溶液部分
是氯化钠的不饱和溶液;
【
小问2详解】
“Ⅲ滤卤”与实验操作过滤的原理一样,其目的是为了分离溶液和难溶性杂质;
【小问3详解】
甲烷燃烧生成二氧化碳和水,该反应的化学方程式为: ;
天然气燃烧放出热量,加热除去溶剂,该步骤和实验操作蒸发结晶的原理相似;【小问4详解】
“晒卤”是除去卤水中的溶剂,可将卤水的浓度提高至 17%,“晒卤”应位于步骤Ⅱ后,这样可以缩短
“滤卤”和“煎盐”的时间,节约时间和能耗,降低成本;
“晒卤”和“煎盐”均利用了蒸发浓缩的原理,但是“晒卤”只是提高了浓度,“煎盐”还利用了结晶原
理。
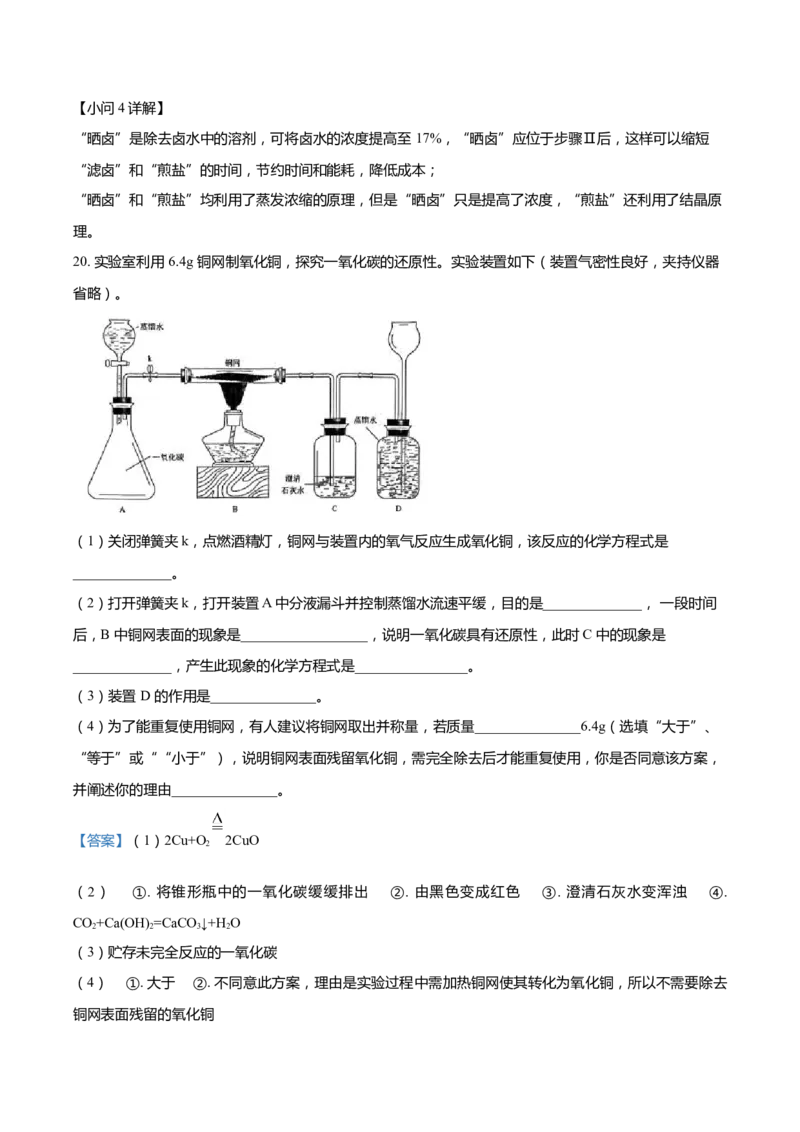
20. 实验室利用 6.4g 铜网制氧化铜,探究一氧化碳的还原性。实验装置如下(装置气密性良好,夹持仪器
省略)。
(1)关闭弹簧夹k,点燃酒精灯,铜网与装置内的氧气反应生成氧化铜,该反应的化学方程式是
______________。
(2)打开弹簧夹k,打开装置A 中分液漏斗并控制蒸馏水流速平缓,目的是______________, 一段时间
后,B 中铜网表面的现象是__________________,说明一氧化碳具有还原性,此时C 中的现象是
______________,产生此现象的化学方程式是________________。
(3)装置 D 的作用是_______________。
(4)为了能重复使用铜网,有人建议将铜网取出并称量,若质量_______________6.4g(选填“大于”、
“等于”或““小于”),说明铜网表面残留氧化铜,需完全除去后才能重复使用,你是否同意该方案,
并阐述你的理由_______________。
【答案】(1)2Cu+O 2CuO
2
(2) ①. 将锥形瓶中的一氧化碳缓缓排出 ②. 由黑色变成红色 ③. 澄清石灰水变浑浊 ④.
CO+Ca(OH) =CaCO ↓+H O
2 2 3 2
(3)贮存未完全反应的一氧化碳
(4) ①. 大于 ②. 不同意此方案,理由是实验过程中需加热铜网使其转化为氧化铜,所以不需要除去
铜网表面残留的氧化铜【解析】
【小问1详解】
关闭弹簧夹 k,点燃酒精灯,铜与氧气在加热的条件下生成氧化铜,反应的化学方程式为 2Cu+O
2
2CuO,故填:2Cu+O 2CuO;
2
【小问2详解】
打开弹簧夹k,打开装置A 中分液漏斗并控制蒸馏水流速平缓,目的是将锥形瓶中的一氧化碳缓缓排出;
B中一氧化碳与氧化铜在加热的条件下生成铜和二氧化碳,一段时间后可观察到铜网表面由黑色变成红色,
二氧化碳能使澄清石灰水变浑浊,二氧化碳与氢氧化钙反应生成碳酸钙沉淀和水,所以可观察到C 中的现
象是澄清石灰水变浑浊,反应的化学方程式为CO+Ca(OH) =CaCO ↓+H O,故填:将锥形瓶中的一氧化碳
2 2 3 2
缓缓排出;由黑色变成红色;澄清石灰水变浑浊;CO+Ca(OH) =CaCO ↓+H O;
2 2 3 2
【小问3详解】
一氧化碳难溶于水,所以装置 D 的作用是贮存未完全反应的一氧化碳,故填:贮存未完全反应的一氧化碳;
【小问4详解】
根据化学方程式2Cu+O 2CuO可知,每128份质量的铜完全反应生成160份质量的氧化铜,所以将铜网
2
取出并称量,若质量大于6.4g,说明铜网表面残留氧化铜,但此方案不合理,理由是实验过程中需加热铜
网使其转化为氧化铜,所以不需要除去铜网表面残留的氧化铜,故填:大于;不同意此方案,理由是实验
过程中需加热铜网使其转化为氧化铜,所以不需要除去铜网表面残留的氧化铜。
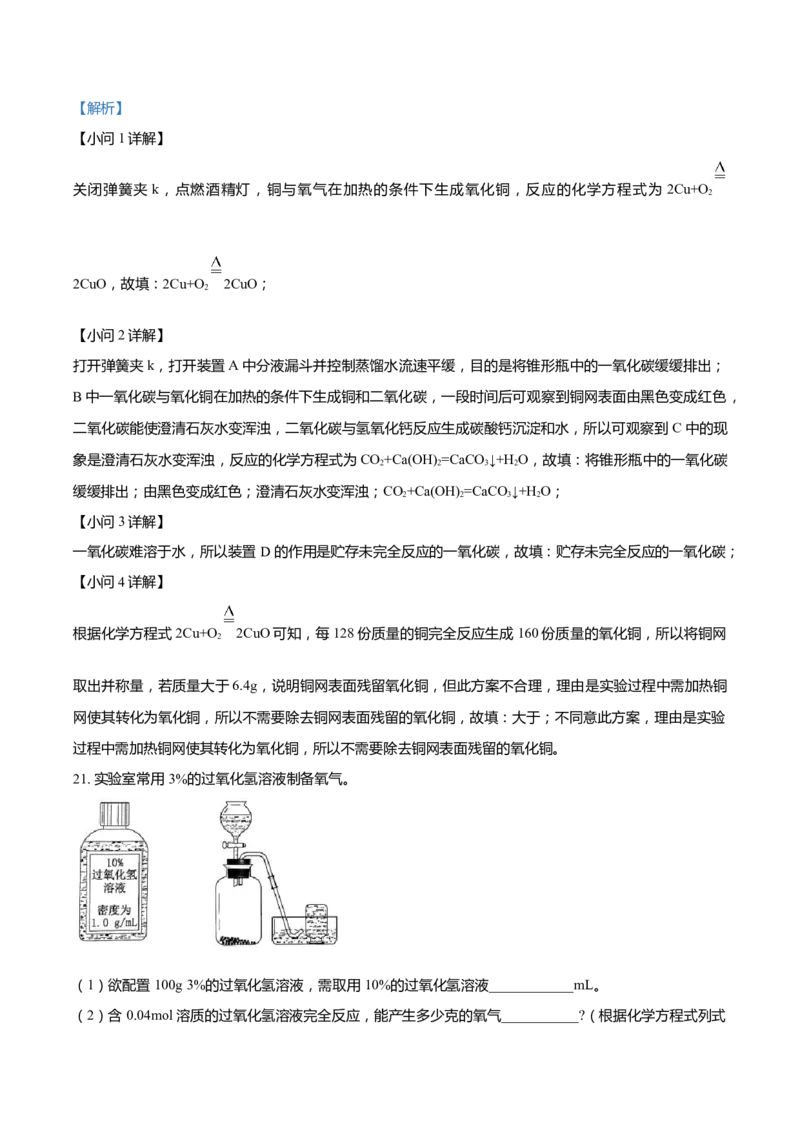
21. 实验室常用 3%的过氧化氢溶液制备氧气。
(1)欲配置 100g 3%的过氧化氢溶液,需取用 10%的过氧化氢溶液____________mL。
(2)含 0.04mol 溶质的过氧化氢溶液完全反应,能产生多少克的氧气___________?(根据化学方程式列式计算)
(3)反应结束后,发生装置内剩余气体的主要成分为氧气,请设计实验方案,收集该剩余气体
______________。
【答案】(1)解:设需取用10%的过氧化氢溶液的质量为x
100g×3%=10%x,x=30g,即30mL
(2)过氧化氢溶液中溶质质量为:0.04mol×34g/mol=1.36g
设能产生氧气的质量为y
y=0.64g
答:能产生氧气的质量为0.64g
(3)通过分液漏斗向装置内加水,将氧气排出,然后利用右边装置利用排水法收集
【解析】
【分析】
【小问1详解】
见答案;
【小问2详解】
见答案;
【小问3详解】
氧气不易溶于水,要想收集氧气,可通过分液漏斗向装置内加水,将氧气排出,然后利用右边装置利用排
水法收集。